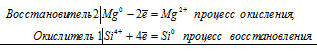Степень окисления кремния. Применение кремниевых соединений
Решение задач на составление уравнений окислительно-восстановительных реакций кремниевых соединений
Задание 387
Какую степень окисления может проявлять кремний в своих соединениях? Составьте уравнения реакций, которые надо провести для осуществления следующих превращений:
МgSi → SiH4 → SiO2 → K2SiO3 → Н2SiO3
При каком превращении происходит окислительно-восстановительная реакция?
Решение:
Для кремния в своих соединениях характерна степень окисления +4.
Уравнения реакций следующих превращений:
б) Окислительно-восстановительной реакцией является реакция силана с водой.
Здесь кремний увеличивает свою степень окисления от -4 до +4, т. е. проявляет свойство восстановителя, а водород уменьшает свою степень окисления от +1 до 0, т. е. Проявляет свойство окислителя;
Задание 388
Какое применение находит кремний? Составьте уравнения реакций, которые надо провести для осуществления следующих превращений: SiO2 → Si → K2SiO3 → Н2SiO3
Окислительно-восстановительные реакции напишите на основании электронных уравнений.
Решение:
а) Применение кремниевых соединений
Кремний в больших количествах используется для получения динамной и трансформаторной стали, которые применяются для изготовления трансформаторов, электромоторов и генераторов. В химическом машиностроении применяют кремниевый чугун (15-17% Si), обладающий кислотоупорными свойствами. Ферросилиций служит добавкой в сталь при её выплавке, для удаления из неё кислорода (образуется SiO2, который уходит в шлак).
Особо чистый кремний применяют для изготовления полупроводниковых устройств (интегральные схемы, солнечные батареи и др.). Кварц используется для изготовления кварцевого стекла, выдерживающего нагревание до 1200 0 С и пропускающего ультрафиолетовое излучение. Изделие из кварца не растрескивается, даже если его нагреть до красного каления и, затем, опустить в холодную воду, благодаря ничтожно малому коэффициенту термического расширения.
Кристаллический кварц обладает пьезоэлектрическими свойствами. Широко используются кварцевые ультразвуковые вибраторы и эталоны частоты.
Огромное применение имеет стекло. Из него изготавливают стеклянные изделия, оконное стекло, посуду, строительные материалы, стекловолокно, стеклоткань и др. изделия.
Из кремния изготавливают ситаллы – материалы, обладающие химической стойкостью и высокой механической прочностью. Их изготавливают из металлургического шлака.
Цемент, керамика, огнеупоры, кирпичи, фаянс, фарфор, асбоцемент представляют собой материалы, содержащие оксид кремния.
Силикат натрия применяют для огнезащитного покрытия деревянных изделий, в производстве силикатных материалов. Фторокремниевую кислоту используют качестве дезинфицирующего средства.
Муллит – соединение в системе Al2O3 — SiO2, устойчивое при высоких температурах.
Цеолиты используют в качестве селективных адсорбентов при очистке и осушке газов (природный газ) и органических жидкостей (углеводороды).
SiH4 и SiCl4 используют для получения кремнийорганических соединений, из которых получают каучукоgодобные материалы, выдерживающие длительное нагревание до 250 0 С и сохраняющие эластичность даже при -60 0 С, клей, огнеупорные лаки и эмали, водоотталкивающие вещества для пропитки тканей, силиконовые смазки, протезные пластмассы, электроизоляционные материалы.
б) Уравнения реакций, которые надо провести для осуществления следующих превращений:
1) SiO2 + 2Mg = Si + 2MgO
2Mg 0 + Si 4+ = 2Mg 2+ + Si 0
SiO2 + 2Mg = Si + 2MgO
В данной реакции магний увеличивает свою степень окисления от 0 до +2, т. е. проявляет свойства восстановителя, а кремний уменьшает свою степень окисления от +4 до 0, т. е. проявляет свойства окислителя.
Si 0 + 4H + = Si 4+ + 2H2 0
В данной реакции кремний увеличивает свою степень окисления от 0 до +4, т. е. проявляет свойства восстановителя, а водород уменьшает свою степень окисления от + до 0, т. е. проявляет свойства окислителя.
В данной реакции кремний не изменяет свою степень окисления — реакция не является окислительно-восстановительной.
Вариант 4
Вопросы:
1. Дайте сравнительную характеристику оксида углерода(II) и оксида углерода(IV). Укажите сходство и различие в физических и химических свойствах. Ответ подтвердите необходимыми уравнениями реакций.
2. В трех пронумерованных пробирках находятся растворы сульфата калия, силиката натрия и карбоната натрия. Как при помощи одного вещества определить содержимое каждой пробирки? Напишите уравнения соответствующих реакций.
3. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
4. К 60 г 10%-ного раствора соды NaHCO3 прилили избыток раствора соляной кислоты. Рассчитайте объем выделившегося углекислого газа (н. у.). (Ответ: 1,6 л.)
Ответы и решения:
1. Физические свойства
Газ, без цвета, без запаха, с примесями, имеет характерный запах, ядовит, легче воздуха
Газ, без цвета, без запаха, малорастворим в воде, тяжелее воздуха
2. Химические свойства
2. Содержимое каждой пробирки можно определить при помощи раствора

задача №4
к главе «Тема IV. Подгруппа углерода. Работа 5. Итоговая по теме IV».
Помогите, пожалуйста, написать уравнения реакций si sio2 ksio3 h2sio3?
Химия | 5 — 9 классы
Помогите, пожалуйста, написать уравнения реакций si sio2 ksio3 h2sio3.
Si + O2 = SiO2SiO2 + 2KOH = K2SiO3 + H2OK2SiO3 + 2HCl = 2KCl + H2SiO3.
Уравнения реакций, позволяющих осуществить следующие превращения : SiO(2)→Si→SiO(2)→Na(2)SiO(3)→H(2)SiO(3)→SiO(2)?
Уравнения реакций, позволяющих осуществить следующие превращения : SiO(2)→Si→SiO(2)→Na(2)SiO(3)→H(2)SiO(3)→SiO(2).
K SiO Zn SO4 MgCO3 PbO Cu составить уравнения возможных реакций с фосфорной кислотой?
K SiO Zn SO4 MgCO3 PbO Cu составить уравнения возможных реакций с фосфорной кислотой.
Помогите написать уравнение реакции хлорирования бензола и уравнение реакции дегидратации этилового спирта?
Помогите написать уравнение реакции хлорирования бензола и уравнение реакции дегидратации этилового спирта?
Помогите пожалуйса надо выбрать какие реакции пойдут и написать уравнение Cl2O7 + CaO SiO + O2 SeO3 + H2O Co2 + O2 Br2O5 + NaOH TeO + K2O?
Помогите пожалуйса надо выбрать какие реакции пойдут и написать уравнение Cl2O7 + CaO SiO + O2 SeO3 + H2O Co2 + O2 Br2O5 + NaOH TeO + K2O.
Закончите уравнение реакции, напишите их в ионной форме, назовите вещества CaO + SiO ² Индекс 2 внизу?
Закончите уравнение реакции, напишите их в ионной форме, назовите вещества CaO + SiO ² Индекс 2 внизу.
Помогите пожалуйста написать уравнения реакций?
Помогите пожалуйста написать уравнения реакций.
Нужно написать уравнение реакции, помогите пожалуйста?
Нужно написать уравнение реакции, помогите пожалуйста.
Помогите решить уравнение ZnS + SiO₂ =?
Помогите решить уравнение ZnS + SiO₂ =.
Уравнение Na₂SiO₃ + 2HCl = 2NaCl + H₂SiO₃ относится к реакции :а) разложения б)обмена в)окислительно — восстановительной г)нейтрализации?
Уравнение Na₂SiO₃ + 2HCl = 2NaCl + H₂SiO₃ относится к реакции :
а) разложения б)обмена в)окислительно — восстановительной г)нейтрализации.
Составьте в молекулярной форме уравнение реакции, которому соответствует следущее ионное уравнение Ba² + SiO₃²⁻ = BaSiO3?
Составьте в молекулярной форме уравнение реакции, которому соответствует следущее ионное уравнение Ba² + SiO₃²⁻ = BaSiO3.
Написать уравнение реакции цезия с кислородом ?
Написать уравнение реакции цезия с кислородом ?
На этой странице сайта, в категории Химия размещен ответ на вопрос Помогите, пожалуйста, написать уравнения реакций si sio2 ksio3 h2sio3?. По уровню сложности вопрос рассчитан на учащихся 5 — 9 классов. Чтобы получить дополнительную информацию по интересующей теме, воспользуйтесь автоматическим поиском в этой же категории, чтобы ознакомиться с ответами на похожие вопросы. В верхней части страницы расположена кнопка, с помощью которой можно сформулировать новый вопрос, который наиболее полно отвечает критериям поиска. Удобный интерфейс позволяет обсудить интересующую тему с посетителями в комментариях.
24. Сходство в том , что на внешнем электронном уровне у атомов одинаковое число электронов 25. Периодически повторяется строение внешнего электронного слоя атома.
Правила определения степеней окисления. 1. В простом веществе степень окисления атомов равна 0 N20, Cl20, H20, Ne0, Fe0, Cu0, O30, P40 2. Степень окисления более электроотрицательного атома обозначают со знаком «−», а менее электроотрицательного – ..
M + 2HCl = MCl2 + H2↑ n(M) = 1. 2 / Mr n(HCl) = 3. 65 / 36. 5 = 0. 1 моль 2n(M) = n(HCl) = 0. 1 / 2 = 0. 05моль 1, 2г / Mr = 0. 05 Mr = 1. 2г / 0. 05моль = 24г / моль(Mg — магний).
Экстракция — это когда подходящим растворителем извлекают вещество из раствора или какой — то смеси, потому что это вещество растворяется в таком растворителе (самые элементарные примеры это запаривание чая, разные спиртовые настойки лекарственных тр..
Вода и глюкоза : являются органическими веществами.
3 вода неорганическое соединение.
Mg(OH)2 + 2Hl = MgCl2 + 2H2O.
Я не уверен , но можно попробовать решетом.
У обоих атомов углерода тип гибридизации — sp3, потому что в соединении нет двойных или тройных связей, двойная связать — sp2, тройная — sp.
http://5terka.com/node/11477
http://himia.my-dict.ru/q/2857242_pomogite-pozalujsta-napisat-uravnenia-reakcij-si/