Как называется сплав алюминия с медью? Производство сплавов металлов на основе меди и алюминия

Одним из самых распространенных металлов на Земле считается алюминий. Его еще называют «летающим металлом». Несмотря на то, что в природе он не встречается в чистом виде, его можно найти во многих минералах. А самый распространенный сплав, который используется для производства множества деталей и конструкций, – это дюралюминий (дюраль).
Его изобрел немецкий ученый Альфред Вильм, который работал на заводе Dürener Metallwerke AG (город Дюрен). Он определил, что сплав алюминия с медью обладает намного более лучшими характеристиками, чем сам металл в чистом виде.
Группа высокопрочных сплавов
На самом деле дюралюминий – это целая группа сплавов, в которых основным компонентом является алюминий, а его легирующими элементами – медь, цинк, марганец, магний. Но в целом их характеристика определяется не только составом, но и способом термообработки. В 1903 году впервые было обнаружено, что в процессе старения сплав алюминия с медью становится еще более прочным и твердым.
Как выяснилось позже, это объясняется тем, что когда после закалки металл находится несколько дней при комнатной температуре, его перенасыщенный твердый раствор распадается, а это, в свою очередь, сопровождается упрочнением материала.
Процесс старения и возврат к предыдущему состоянию
Как уже было сказано ранее, старение металла – важный процесс, который обуславливается структурными превращениями, вызывающими изменения физических и механических свойств. Оно может быть естественным и искусственным. В первом случае сплав выдерживают несколько суток при комнатной температуре.
При искусственном старении время обработки сокращается, но при этом увеличивается температура. Для того чтобы вернуть сплав к предыдущему состоянию, его необходимо на несколько секунд нагреть до 270 градусов и затем быстро остудить.
Производство алюминия
Для того чтобы изготовить сплав алюминия с медью, необходимо высокотехнологичное оборудование и, конечно же, сам металл. Его добывают из бокситов. Это горная порода, которую необходимо измельчить, добавить в неё воду и обработать паром под большим давлением. Таким образом из глинозема отделяют кремний. Затем густую массу помещают в специальную ванну с расправленным криолитом. Содержимое нагревают до 950 °С и через него пропускают электрический ток в 400 кА.
Это позволяет разорвать связь между атомами кислорода и алюминия. В результате последний оседает на дно в качестве жидкого металла. Так из жидкого алюминия делают отливки. Теперь металл полностью готов к механической обработке. Однако для того чтобы повысить его прочность, необходимо в него добавить легирующие элементы и таким образом получить высококачественный сплав алюминия с медью.
Производство дюрали
В общей сложности все алюминиевые сплавы делятся на две группы: литейные и деформированные. Процесс их производства зависит именно от того, какой вид должен получиться в конечном итоге. Кроме того, способ изготовления также зависит и от требуемых характеристик.
Для производства дюраля алюминиевые слитки расплавляют в электрической печи. Интересно, что это один из немногих металлов, который можно переводить из твердого состояния в жидкое и наоборот множество раз. Это не повлияет на его характеристики. В расплавленный алюминий по очереди добавляют медь и другие легирующие элементы, такие как марганец, железо, магний. Очень важно соблюдать процентное соотношение: 93% алюминия, 5% меди, остальные 2% приходятся на другие легирующие элементы.
Закалка и отжиг дюраля
Обязательным для такого сплава является процесс закалки. Время выдержки для небольших деталей составляет всего несколько минут, а температура — около 500 °С. Сразу после процедуры дюраль получается мягким и вязким. Он легко поддается деформации и обработке. Спустя некоторое время сплав твердеет и его механические свойства повышаются. Если превысить порог температуры, происходит окисление и материал теряет свои характеристики. После закалки его необходимо медленно остудить в прохладной воде.
Итак, вы уже знаете, как называется сплав алюминия с медью. Он нередко поддается деформации: холодному прокату, вытяжке, ковке. При этом возникает так называемая нагартовка. Это процесс, в ходе которого в структуре металла происходит передвижение и размножение дислокаций. В итоге сам сплав меняет свою структуру, становится более твердым и прочным. При этом снижается его пластичность и ударная вязкость. Для того чтобы деформации проходили более легко и нагартовка не разрушала металл, используют отжиг. Для этого сплав нагревают до 350 °С и затем остужают на воздухе.
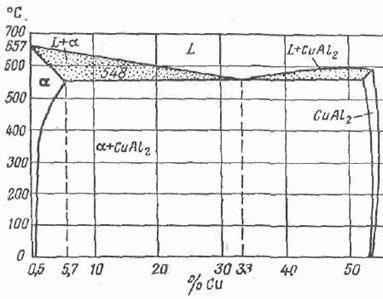
Диаграмма состояния сплава (алюминий и медь)
Для того чтобы наиболее четко описать взаимодействие компонентов дюраля в твердом и жидком состоянии, а также объяснить характер изменения свойств сплава, используют диаграмму состояний.
Из неё видно, что наибольшая растворимость Cu в сплаве с алюминием наблюдается при температуре 548 °С и при этом она составляет 5,7 %. При повышении температуры она будет увеличиваться, а при понижении – уменьшаться. Минимальная растворимость (0,5 %) будет наблюдаться при комнатной температуре. Если же дюраль закалить выше 400 °С, он станет твердым однородным раствором – α.
Во время данного процесса будет происходить распад твердого раствора. Очень необычно ведёт себя сплав алюминия и меди, формула которого — CuAl2. Процесс сопровождается выделением избыточной фазы А1. Такой распад протекает в течение длительного времени. Это и есть то естественное старение, о котором мы уже ранее упоминали.
Свойства сплава
Легирование металла теми или иными элементами позволяет повысить его характеристики. Вы запомнили, как называется сплав алюминия с медью? Какими же свойствами он обладает?
Сам по себе алюминий очень легкий, мягкий и совершенно непрочный. Он растворим в слабо концентрированных щелочах и кислотах. Добавив к алюминию медь и магний, можно получить уже достаточно прочный сплав. Его эксплуатационные параметры достаточно легко улучшить – просто нужно оставить его полежать при комнатной температуре. Так, эффект старения увеличивает прочность дюраля, о чём мы говорили выше.
Сам по себе алюминий достаточно легкий. Незначительный процент меди не утяжеляет сплав. Еще одна положительная характеристика – это возможность многократно переплавлять сплав. При этом он не будет терять своих свойств. Единственное, что необходимо, так это после отливки дать ему «отдохнуть» пару суток.
Недостатком дюралюминия является его низкая коррозионная стойкость. Поэтому чаще всего такой материал покрывают чистым слоем алюминия или же красят лаками и красками.
Алюминиевые сплавы и их применение
Впервые дюраль был использован для изготовления дирижаблей. Легкость и прочность этого материала позволила создать отличный летательный аппарат. Для этого применялась марка Д16т. В настоящее время сплавы с алюминием, цинком, медью и другими легирующими элементами широко используются в космонавтике, авиации и иных областях машиностроения.
Так, например, использование дюралюминия при изготовлении авто может значительно снизить его вес и стоимость, но при этом оно будет достаточно прочным.
В общем, можно отметить, что ассортимент данного сплава достаточно широк: трубы, проволоки, листы, ленты, прутки и литые детали разных форм. Одной из самых востребованных и распространенных марок по-прежнему считается Д16т. Маленькая буква «т» в конце маркировки означает, что сплав закаленный и естественно состарился. Он используется:
- В конструкциях космических аппаратов, морских судов и самолетов.
- Для изготовления различных деталей для станков и машин.
- Для изготовления уличных табличек, дорожных знаков.
Название сплава алюминия и меди должен знать каждый. Дюраль используется и в нефтяной промышленности. Так, специальные трубы, изготовленные из него, могут обеспечить эксплуатацию скважины в течение 6-7 лет.
Как называется сплав алюминия и меди, запомнить легко. Итак, мы рассказали, каким свойствами он обладает и где применяется. Он с легкостью может заменить стальной прокат, в особенности если необходимо сделать конструкцию маловесной.
Алюминий. Химия алюминия и его соединений
Бинарные соединения алюминия
Алюминий
Положение в периодической системе химических элементов
Алюминий расположен в главной подгруппе III группы (или в 13 группе в современной форме ПСХЭ) и в третьем периоде периодической системы химических элементов Д.И. Менделеева.
Электронное строение алюминия и свойства
Электронная конфигурация алюминия в основном состоянии :
+13Al 1s 2 2s 2 2p 6 3s 2 3p 1 1s 



Электронная конфигурация алюминия в возбужденном состоянии :
+13Al * 1s 2 2s 2 2p 6 3s 1 3p 2 1s 



Алюминий проявляет парамагнитные свойства. Алюминий на воздухе быстро образует прочные оксидные плёнки, защищающие поверхность от дальнейшего взаимодействия, поэтому устойчив к коррозии.
Физические свойства
Алюминий – лёгкий металл серебристо-белого цвета, легко поддающийся формовке, литью, механической обработке. Обладает высокой тепло- и электропроводностью.
Температура плавления 660 о С, температура кипения 1450 о С, плотность алюминия 2,7 г/см 3 .
Алюминий — один из наиболее ценных цветных металлов для вторичной переработки. На протяжении последних лет, цена на лом алюминия в пунктах приема непреклонно растет. По ссылке можно узнать о том, как сдать лом алюминия.
Нахождение в природе
Алюминий — самый распространенный металл в природе, и 3-й по распространенности среди всех элементов (после кислорода и кремния). Содержание в земной коре — около 8%.
В природе алюминий встречается в виде соединений:
Корунд Al2O3. Красный корунд называют рубином, синий корунд называют сапфиром.
Способы получения
Алюминий образует прочную химическую связь с кислородом. Поэтому традиционные способы получения алюминия восстановлением из оксида протекают требуют больших затрат энергии. Для промышленного получения алюминия используют процесс Холла-Эру. Для понижения температуры плавления оксид алюминия растворяют в расплавленном криолите (при температуре 960-970 о С) Na3AlF6, а затем подвергают электролизу с углеродными электродами. При растворении в расплаве криолита оксид алюминия распадается на ионы:
На катоде происходит восстановление ионов алюминия:
Катод: Al 3+ +3e → Al 0
На аноде происходит окисление алюминат-ионов:
Суммарное уравнение электролиза расплава оксида алюминия:
Лабораторный способ получения алюминия заключается в восстановлении алюминия из безводного хлорида алюминия металлическим калием:
AlCl3 + 3K → Al + 3KCl
Качественные реакции
Качественная реакция на ионы алюминия — взаимодействие избытка солей алюминия с щелочами . При этом образуется белый аморфный осадок гидроксида алюминия.
Например , хлорид алюминия взаимодействует с гидроксидом натрия:
AlCl3 + 3NaOH → Al(OH)3 + 3NaCl
При дальнейшем добавлении щелочи амфотерный гидроксид алюминия растворяется с образованием тетрагидроксоалюмината:
Обратите внимание , если мы поместим соль алюминия в избыток раствора щелочи, то белый осадок гидроксида алюминия не образуется, т.к. в избытке щелочи соединения алюминия сразу переходят в комплекс:
AlCl3 + 4NaOH = Na[Al(OH)4] + 3NaCl
Соли алюминия можно обнаружить с помощью водного раствора аммиака. При взаимодействии растворимых солей алюминия с водным раствором аммиака также в ыпадает полупрозрачный студенистый осадок гидроксида алюминия.
AlCl3 + 3NH3·H2O = Al(OH)3 ↓ + 3NH4Cl
Al 3+ + 3NH3·H2O = Al(OH)3 ↓ + 3NH4 +
Видеоопыт взаимодействия раствора хлорида алюминия с раствором аммиака можно посмотреть здесь.
Химические свойства
1. Алюминий – сильный восстановитель . Поэтому он реагирует со многими неметаллами .
1.1. Алюминий реагируют с галогенами с образованием галогенидов:
1.2. Алюминий реагирует с серой с образованием сульфидов:
1.3. Алюминий реагируют с фосфором . При этом образуются бинарные соединения — фосфиды:
Al + P → AlP
1.4. С азотом алюминий реагирует при нагревании до 1000 о С с образованием нитрида:
2Al + N2 → 2AlN
1.5. Алюминий реагирует с углеродом с образованием карбида алюминия:
1.6. Алюминий взаимодействует с кислородом с образованием оксида:
Видеоопыт взаимодействия алюминия с кислородом воздуха (горение алюминия на воздухе) можно посмотреть здесь.
2. Алюминий взаимодействует со сложными веществами:
2.1. Реагирует ли алюминий с водой? Ответ на этот вопрос вы без труда найдете, если покопаетесь немного в своей памяти. Наверняка хотя бы раз в жизни вы встречались с алюминиевыми кастрюлями или алюминиевыми столовыми приборами. Такой вопрос я любил задавать студентам на экзаменах. Что самое удивительное, ответы я получал разные — у кого-то алюминий таки реагировал с водой. И очень, очень многие сдавались после вопроса: «Может быть, алюминий реагирует с водой при нагревании?» При нагревании алюминий реагировал с водой уже у половины респондентов))
Тем не менее, несложно понять, что алюминий все-таки с водой в обычных условиях (да и при нагревании) не взаимодействует. И мы уже упоминали, почему: из-за образования оксидной пленки . А вот если алюминий очистить от оксидной пленки (например, амальгамировать), то он будет взаимодействовать с водой очень активно с образованием гидроксида алюминия и водорода:
2Al 0 + 6 H2 + O → 2 Al +3 ( OH)3 + 3 H2 0
Амальгаму алюминия можно получить, выдержав кусочки алюминия в растворе хлорида ртути ( II ):
3HgCl2 + 2Al → 2AlCl3 + 3Hg
Видеоопыт взаимодействия амальгамы алюминия с водой можно посмотреть здесь.
2.2. Алюминий взаимодействуют с минеральными кислотами (с соляной, фосфорной и разбавленной серной кислотой). При этом образуются соль и водород.
Например , алюминий бурно реагирует с соляной кислотой :
2Al + 6HCl = 2AlCl3 + 3H2↑
2.3. При обычных условиях алюминий не реагирует с концентрированной серной кислотой из-за пассивации – образования плотной оксидной пленки. При нагревании реакция идет, образуются оксид серы (IV), сульфат алюминия и вода:
2.4. Алюминий не реагирует с концентрированной азотной кислотой также из-за пассивации.
С разбавленной азотной кислотой алюминий реагирует с образованием молекулярного азота:
При взаимодействии алюминия в виде порошка с очень разбавленной азотной кислотой может образоваться нитрат аммония:
2.5. Алюминий – амфотерный металл, поэтому он взаимодействует с щелочами . При взаимодействии алюминия с раствором щелочи образуется тетрагидроксоалюминат и водород:
2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2 ↑
Видеоопыт взаимодействия алюминия со щелочью и водой можно посмотреть здесь.
Алюминий реагирует с расплавом щелочи с образованием алюмината и водорода:
2Al + 6NaOH → 2Na3AlO3 + 3H2 ↑
Эту же реакцию можно записать в другом виде (в ЕГЭ рекомендую записывать реакцию именно в таком виде):
2Al + 6NaOH → 2NaAlO2 + 3H2↑ + 2Na2O
2.6. Алюминий восстанавливает менее активные металлы из оксидов . Процесс восстановления металлов из оксидов называется алюмотермия .
Например , алюминий вытесняет медь из оксида меди (II). Реакция очень экзотермическая:
2Al + 3CuO → 3Cu + Al2O3
Еще пример : алюминий восстанавливает железо из железной окалины, оксида железа (II, III):
Восстановительные свойства алюминия также проявляются при взаимодействии его с сильными окислителями: пероксидом натрия, нитратами и нитритами в щелочной среде, перманганатами, соединениями хрома (VI):
Сплав алюминия и меди массой 2 г обработали раствором гидроксида натрия, с массовой долей щёлочи 40 % (ρ=1,4 г/мл). Не растворившийся
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,299
- гуманитарные 33,630
- юридические 17,900
- школьный раздел 607,256
- разное 16,836
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
http://chemege.ru/aluminium/
http://www.soloby.ru/959953/%D0%B0%D0%BB%D1%8E%D0%BC%D0%B8%D0%BD%D0%B8%D1%8F-%D0%BE%D0%B1%D1%80%D0%B0%D0%B1%D0%BE%D1%82%D0%B0%D0%BB%D0%B8-%D1%80%D0%B0%D1%81%D1%82%D0%B2%D0%BE%D1%80%D0%BE%D0%BC-%D0%B3%D0%B8%D0%B4%D1%80%D0%BE%D0%BA%D1%81%D0%B8%D0%B4%D0%B0-%D1%80%D0%B0%D1%81%D1%82%D0%B2%D0%BE%D1%80%D0%B8%D0%B2%D1%88%D0%B8%D0%B9%D1%81%D1%8F