Нитрат стронция: способы получения и химические свойства
Нитрат стронция Sr(NO3)2 — соль металла стронция и азотной кислоты. Белый, при плавлении разлагается. Хорошо растворяется в воде (гидролиза нет).
Относительная молекулярная масса Mr = 211,63; относительная плотность для тв. и ж. состояния d = 2,99; tпл = 570º C (разлагается).
Способ получения
1. Нитрат стронция можно путем взаимодействия стронция и разбавленной азотной кислоты, образуется нитрат стронция, оксид азота (I) и вода:
если стронций будет взаимодействовать с очень разбавленной азотной кислотой , то образуются нитрат стронция, нитрат аммония и вода:
2. В результате взаимодействия сульфида стронция и концентрированной азотной кислоты образуется нитрат стронция, сера, оксид азота (IV) и вода:
3. Карбонат стронция вступает в взаимодействие с концентрированной азотной кислотой с образованием нитрата стронция, воды и углекислого газа:
Качественная реакция
Качественная реакция на нитрат стронция — взаимодействие с медью при нагревании в присутствии концентрированной кислоты:
1. При взаимодействии с серной кислотой и медью, нитрат стронция образует сульфат стронция, нитрат меди, бурый газ оксид азота и воду:
Химические свойства
1. Hитрат стронция разлагается при температуре 450 — 500º С с образованием нитрита стронция и кислорода:
а если температуре поднимется выше 570 о С, то на выходе реакции будут образовываться оксид стронция, оксид азота (IV) и кислород:
2. Нитрат стронция реагирует с простыми веществами :
2.1. Нитрат стронция вступает в реакцию с атомным водородом (цинком и в присутствии соляной кислоты). В результате реакции образуется нитрат стронция, хлорид цинка и вода :
3. Возможны реакции между нитратом стронция и сложными веществами :
Нитрат стронция вступает в реакцию с основаниями :
В результате реакции между насыщенным нитратом стронция и насыщенным гидроксидом натрия при комнатной температуре образуется гидроксид стронция и нитрат натрия:
Азотная кислота
Азотная кислота является одной из самых сильных минеральных кислот, в концентрированном виде выделяет пары желтого цвета с резким запахом. За исключением золота и платины растворяет все металлы.
Применяют азотную кислоту для получения красителей, удобрений, органических нитропродуктов, серной и фосфорной кислот. В результате ожога азотной кислотой образуется сухой струп желто-зеленого цвета.
В промышленности азотную кислоту получают в результате окисления аммиака на платино-родиевых катализаторах.
Чистая азотная кислота впервые была получена действием на селитру концентрированной серной кислоты:
Является одноосновной сильной кислотой, вступает в реакции с основными оксидами, основаниями. С солями реагирует при условии выпадения осадка, выделения газа или образования слабого электролита.
При нагревании азотная кислота распадается. На свету (hv) также происходит подобная реакция, поэтому азотную кислоту следует хранить в темном месте.
Реакции с неметаллами
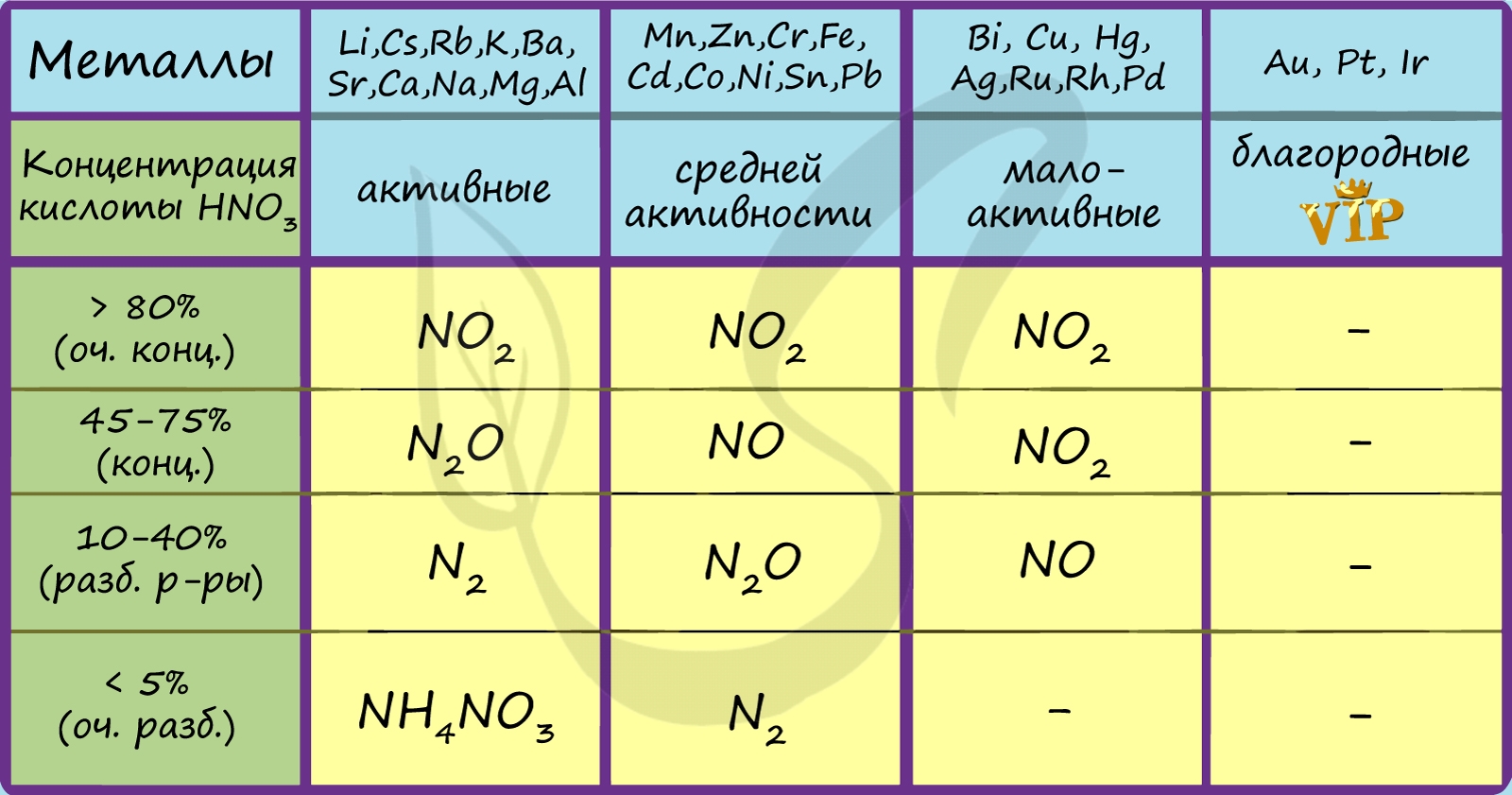
Азотная кислота способна окислить все неметаллы, при этом, если кислота концентрированная, азот обычно восстанавливается до NO2, если разбавленная — до NO.
В любой концентрации азотная кислота проявляет свойства окислителя, при этом азот восстанавливается до степени окисления от +5 до -3. На какой именно степени окисления остановится азот, зависит от активности металла и концентрации азотной кислоты.
Для малоактивных металлов (стоящих в ряду напряжений после водорода) реакция с концентрированной азотной кислотой происходит с образованием нитрата и преимущественно NO2.
С разбавленной азотной кислотой газообразным продуктом преимущественно является NO.
В реакциях с металлами, стоящими левее водорода в ряду напряжений, возможны самые разные газообразные (и не газообразные) продукты: бурый газ NO2, NO, N2O, атмосферный газ N2, NH4NO3.
Помните о закономерности: чем более разбавлена кислота и активен металл, тем сильнее восстанавливается азот. Ниже представлены реакции цинка с азотной кислотой в различных концентрациях.
Посмотрите на таблицу ниже, в которой также отражены изученные нами закономерности.
Концентрированная холодная азотная кислота пассивирует хром, железо, алюминий, никель, свинец и бериллий. Это происходит за счет оксидной пленки, которой покрыты данные металлы.
Al + HNO3(конц.) ⇸ (реакция не идет)
При нагревании или амальгамировании (покрытие ртутью) перечисленных металлов реакция с азотной кислотой идет, так как оксидная пленка на поверхности металлов разрушается.
Соли азотной кислоты — нитраты NO3 —
Получают нитраты в ходе реакции азотной кислоты с металлами, их оксидами и основаниями.
В реакциях с оксидами и основаниями газообразный продукт обычно не выделяется.
Нитрат аммония получают реакция аммиака с азотной кислотой.
Обратите внимание на следующую закономерность: концентрированная азотная кислота, как правило, окисляет железо и хром до +3. Разбавленная кислота — до +2.
- Реакции с металлами, основаниями и кислотами
Как и для всех солей, из нитратов можно вытеснить металл другим более активным. Соли реагируют с основаниями и кислотами, если в результате реакции выпадает осадок, выделяется газ или образуется слабый электролит (вода).
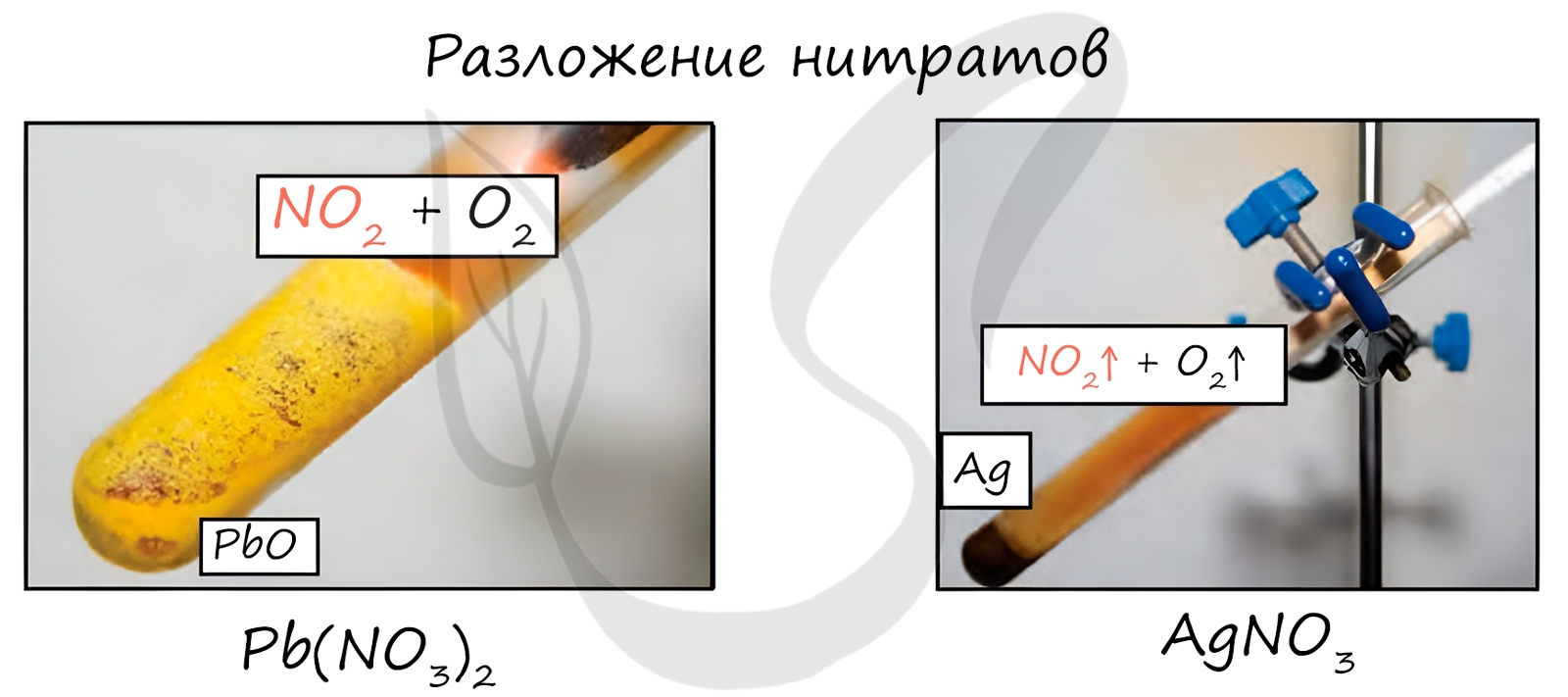
Нитраты разлагаются в зависимости от активности металла, входящего в их состав.
© Беллевич Юрий Сергеевич 2018-2022
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Sr oh 2 hno3 уравнение
I. Строение молекулы

Опытным путём доказано, что в молекуле азотной кислоты между двумя атомами кислорода и атомом азота две химические связи абсолютно одинаковые – полуторные связи. Степень окисления азота +5, а валентность равна IV.
II. Физические свойства
Азотная кислота HNO3 в чистом виде — бесцветная жидкость с резким удушливым запахом, неограниченно растворимая в воде; t°пл.= -41°C; t°кип.= 82,6°С, r = 1,52 г/см 3 . В небольших количествах она образуется при грозовых разрядах и присутствует в дождевой воде.
Под действием света азотная кислота частично разлагается с выделением NО2 и за cчет этого приобретает светло-бурый цвет:
N2 + O2 грозовые эл . разряды → 2NO
Азотная кислота высокой концентрации выделяет на воздухе газы, которые в закрытой бутылке обнаруживаются в виде коричневых паров (оксиды азота). Эти газы очень ядовиты, так что нужно остерегаться их вдыхания. Азотная кислота окисляет многие органические вещества. Бумага и ткани разрушаются вследствие окисления образующих эти материалы веществ. Концентрированная азотная кислота вызывает сильные ожоги при длительном контакте и пожелтение кожи на несколько дней при кратком контакте. Пожелтение кожи свидетельствует о разрушении белка и выделении серы (качественная реакция на концентрированную азотную кислоту – жёлтое окрашивание из-за выделения элементной серы при действии кислоты на белок – ксантопротеиновая реакция). То есть – это ожог кожи. Чтобы предотвратить ожог, следует работать с концентрированной азотной кислотой в резиновых перчатках.
III. Получение
1. Лабораторный способ
2. Промышленный способ
a) Окисление аммиака на платиновом катализаторе до NO
4NH3 + 5O2 → 4NO + 6H2O (условия: катализатор – Pt, t = 500˚С)
б) Окисление кислородом воздуха NO до NO2
в) Поглощение NO2 водой в присутствии избытка кислорода
или 3NO2 + H2O ↔ 2HNO3+NO (без избытка кислорода)
IV. Химические свойства
Для азотной кислоты характерны свойства: общие с другими кислотами и специфические.
1. Химические свойства общие с другими кислотами
1. Очень сильная кислота.
Диссоциирует в водном растворе практически нацело:
2. Реагирует с основными оксидами
3. Реагирует с основаниями
H + + NO3 — + Na + + OH — → Na + + NO3 — + H2O
4. Реагирует с солями, вытесняет слабые кислоты из их солей
2. Специфические свойства азотной кислоты
Азотная кислота — сильный окислитель
N +5 → N +4 → N +2 → N +1 → N o → N -3
N +5 + 8e — →N -3 окислитель, восстанавливается.
1. Разлагается на свету и при нагревании
Образуется бурый газ
2. При взаимодействии с металлами никогда не выделяется водород
HNO3 + Me = соль + H2O + Х
http://studarium.ru/article/170
http://kardaeva.ru/89-dlya-uchenika/9-klass/209-azotnaya-kislota