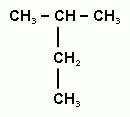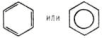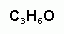11. Третичным спиртом является
1) 2-метилпропанол-1 3) 3-метилпентанол-2
2) 2-метилбутанол-1 4) 2-метилпентанол-2
12. Одноатомным спиртом является вещество, формула которого
1) CH2ОН-CH2ОН 3) C6H5ОН
2) СН3-СНОН-CH2ОН 4) C6H5СН2ОН
13. В молекуле метанола между атомами существуют связи
1) только ковалентные полярные
2) ковалентные полярные и неполярные
3) ковалентные полярные и ионные
4) ковалентные полярные и водородная
14. В результате реакции гидратации алкена нельзя получить спирт, формула которого
1) СН3 ─ СНОН ─ СН3 3) CH3 ─ CH2 ─ ОН
2) СН3 ─ СНОН ─ СН2 ─ СН3 4) CH3 ─ ОН
15. Коэффициент перед формулой кислорода в уравнении реакции горения этанола равен
1) 1 2) 2 3) 3 4) 4
16. Сумма коэффициентов в уравнении реакции горения метанола равна
1) 5 2) 7 3) 9 4) 11
17. Продуктом внутримолекулярной дегидратации этилового спирта является
1) уксусная кислота 3) этаналь
2) диэтиловый эфир 4) этен
18. Продуктом межмолекулярной дегидратации этилового спирта является
1) этаналь 3) этилацетат
2) диэтиловый эфир 4) этилен
19. С метанолом взаимодействует каждое из двух веществ
1) NaOH и H2SO4 3) Н2 и CuO
2) C2H5OH и HCOOH 4) Cu и CH3COOH
20. Предельные одноатомные спирты можно распознать с помощью
1) оксида меди(II) 3) бромной воды
2) гидроксида меди(II) 4) хлорида железа(III)
Тестирование по теме «предельные одноатомные спирты»
Тестирование по теме «Предельные одноатомные спирты» предназначено для проверки уровня усвоения материала по теме. Проводится на заключительном уроке по данной теме в 10 классе.
Тестирование состоит из 10 вопросов.
Вопросы 1-8 базового уровня сложности, оцениваются в 1 балл;
вопрос 9 повышенного уровня сложности, оценивается в 2 балла;
вопрос 10 высокого уровня сложности, оценивается в 3 балла.
Итого 13 баллов.
Просмотр содержимого документа
«Тестирование по теме «предельные одноатомные спирты»»
ТЕСТИРОВАНИЕ ПО ТЕМЕ
«ПРЕДЕЛЬНЫЕ ОДНОАТОМНЫЕ СПИРТЫ»
ОГАОУ «Академия футбола «Энергомаш»
Тестирование по теме «Предельные одноатомные спирты» предназначено для проверки уровня усвоения материала по теме. Проводится на заключительном уроке по данной теме в 10 классе.
Тестирование состоит из 10 вопросов.
Вопросы 1-8 базового уровня сложности, оцениваются в 1 балл;
вопрос 9 повышенного уровня сложности, оценивается в 2 балла;
вопрос 10 высокого уровня сложности, оценивается в 3 балла.
Итого 13 баллов.
Таблица перевода баллов в оценку.
Инструкция по выполнению тестирования
Внимательно читайте вопросы и предполагаемые ответы, выполняйте задания по порядку, ответы к вопросам 1-8 записывайте в виде одной буквы, к вопросу 9 ответ оформите в виде последовательности букв, к вопросу 10 запишите полное решение.
1. Первый представитель ряда алканолов называется:
а) бутанолом; б) пропанолом; в) метанолом; г) этанолом.
2. Общая формула предельных одноатомных спиртов:
3. Вещество состава С2Н5ОН называют:
в) этиловым спиртом;
4. Агрегатное состояние первых трёх представителей предельных одноатомных спиртов:
а) жидкое; б) газообразное; в) твёрдое; г) смешанное.
5. Самым ядовитым предельным одноатомным спиртом, вызывающим слепоту или смерть является:
а) пропанол; б) этанол;
в) этиловый спирт; г) метанол.
6. Наиболее древний способ получения этанола – это:
а) взаимодействием этилена с водой;
б) сбраживание сахаристых веществ;
в) гидролиз хлорэтана;
г) каталитическим восстановление уксусного альдегида.
7. Вещество, для которого характерна реакция гидратации, приводящая к образованию этилового спирта, это:
а) 1; б) 4; в) 2; г) 3.
8. Сумма коэффициентов в уравнении реакции горения этилового спирта равна:
а) 12; б)11; в) 13; г) 9.
9. Для этанола характерно:
а) наличие σ- и π- связей в молекуле;
б) взаимодействие с оксидом меди (II);
в) взаимодействие с натрием;
г) реакция гидрирования;
10. Решите задачу.
Предельный одноатомный спирт обработали металлическим натрием. В результате реакции получили вещество массой 20,5 г и выделился газ объёмом 2,8 л (н.у.). Определите молекулярную формулу спирта.
Найти формулу спирта.
Содержание верного ответа и указания по оцениванию
(допускаются иные формулировки ответа, не искажающие его смысла)
n(вещества)=m/M, где М – молярная масса вещества
Полученное значение n=3 подставим в общую формулу спирта СnH2n+1ОН:
Ответ правильный и полный, включает все названные выше
Правильно записаны два элемента ответа
Правильно записан один элемент ответа
Все элементы ответа записаны неверно
Максимальный балл 3
Список использованной литературы
1. Рудзитис, Г. Е. Химия: неорган. химия [Текст]: учеб. для 8 кл. общеобразоват. учреждений / Г. Е. Рудзитис, Ф. Г. Фельдман. – 12-е изд., испр. – М.: Просвещение, 2008. – 176 с. : ил. – ISBN 978-5-09-019859-2.
Контрольно-измерительные материалы
Просмотр содержимого документа
«Контрольно-измерительные материалы»
Контрольная работа №1: “Углеводороды”
Задания к контрольной работе:
Для вопросов 1-7 выберите вариант ответа (верный — только один ответ из четырех). Каждый правильный ответ: 1 балл, максимально 7 баллов.
Для вопросов 5-7 объясните выбор ответа, записав или уравнение реакции; или определение. Назовите вещества по систематической номенклатуре или составьте их структурную формулу. Каждый правильный дополнительный ответ: 1 балл, максимально 3 балла.
Решите задачу 8, запишите ход решения. Оценивается каждый элемент решения, максимально: 3 балла.
12-13 баллов – оценка “5”, 10-11 баллов – оценка “4”, 7-9 баллов – оценка “3”, менее 7 баллов – оценка “2”.
1 Общей формуле алкенов соответствует:
2 Молекулы алкадиенов содержат:
а) только 
б) одну 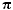
в) две 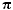
г) бензольное кольцо
а) летучая жидкость, применяется при сварке металлов
б) вязкая жидкость, применяется для получения резины
в) взрывоопасный газ, применяется при сварке металлов
г) газ, применяется для получения резины
4 Вещество, формула которого
5 Изомером циклобутана является:
6 В схеме превращений 3 С2Н2 ———— Х неизвестным веществом Х является:
7 Сумма коэффициентов в реакции горения этана равна:
8 Массовая доля углерода в углеводороде составляет 81,82%, относительная плотность паров этого вещества по кислороду равна 1,375. Найти молекулярную формулу улеводорода. Написать его название и структурную формулу.
Ответы и критерии оценивания к Варианту 1
1 Ответы на вопросы с выбором ответа:
2 Ответы на дополнительный вопрос (для вопросов 5-7):
Содержание возможного ответа
Структурная формула циклобутана или бутена
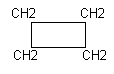
Структурная формула бензола:
Уравнение реакции горения этана:
3 Решение задачи:
Содержание верного ответа и указания по оцениванию (возможен другой тип решения)
Рассчитана относительная молекулярная масса вещества:
Рассчитано молярное соотношение атомов и выведена молекулярная формула:
44х0,8182/12 : 44х0,1818/1 = 3 : 8
Дано название составлена структурная формула вещества:
Ответ правильный и полный, включает все вышеназванные элементы
Правильно записаны первый и второй элементы ответов
Правильно записан только первый элемент ответа
Все элементы ответа записаны неверно (в первом элементе допущена ошибка, повлекшая за собой неправильное решение)
Максимальное число баллов: 7+3+3=13 баллов.
1 Общей формуле алканов соответствует:
2 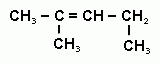
б) 4 — метилпентен-3
в) 2 -метилпентен-2
г) 2,2-диметилбутен -3
3 Для алкинов не характерны реакции
4 Природный каучук – это изомер:
5 При гидратации вещества бутен-1 образуется:
г) бутин и водород
6 Гомологом этилена является:
7 В схеме превращений С2Н4 +Сl2→ Х неизвестным веществом Х является:
8 Массовая доля углерода в углеводороде составляет 85,7%, относительная плотность паров этого вещества по водороду равна 42. Найти молекулярную формулу улеводорода. Написать его название и структурную формулу.
1 Вещество, формула которого С4H6 относится к классу:
а) бесцветный, легко сжижающийся газ
б) бесцветная жидкость, нерастворим в воде, ядовит
в) жидкость, растворим в воде, с неприятным запахом
г) желто-зеленый газ, ядовит
3 
б) 3- метилпентен-3
5 При дегидрировании этана образуется:
в) этановая кислота
6 Сумма коэффициентов в реакции горения ацетилена равна:
7 Число изомеров вещества бутан:
8 Массовая доля водорода в углеводороде составляет 20,0%, относительная плотность паров этого вещества по воздуху равна 1,034. Найти молекулярную формулу улеводорода. Написать его название и структурную формулу
1 Вещество, формула которого СН2=СН –СН =СН2 называется
2 Общей формуле алкинов соответствует:
3 Вещество, формула которого СН3– СН2–СН3 является гомологом:
а) жидкость, нерастворим в воде
б) жидкость, растворим в воде
в) газ, нерастворим в воде
г) газ, растворим в воде
5 В схеме превращений С3Н6 +Н2О → Х неизвестным веществом Х является:
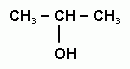
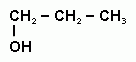
6 Бензол нельзя получить:
а) дегидрированием циклоалканов
б) дегидрированием алканов
в) полимеризацией этилена
г) тримеризацией ацетилена
7 Сумма коэффициентов в реакции горения циклобутана равна:
8 Массовая доля углерода в углеводороде 92,3%. Относительная плотность паров этого вещества по водороду равна 39. Найти молекулярную формулу углеводорода. Написать его название и структурную формулу.
1 Общая формула алкадиенов:
2 Вещество, формула которого
3 Обязательное условие реакции хлорирования алканов:
а) газообразное агрегатное состояние продуктов реакции
в) низкая температура
г) жидкое агрегатное состояние продуктов реакции
а) бесцветный газ, без запаха;
б) бесцветная жидкость, с резким запахом;
в) бесцветная жидкость, без запаха
г) бесцветный газ, с резким запахом.
5 Изомером бутадиена является:
неизвестными веществами Х и Y являются:
а) этилен и вода
б) этен и водород
в) углекислый газ и вода
г) ацетилен и водород
7 При гидратации ацетилена (в присутствии HdSO4 — реакция Кучерова) образуется
в) уксусный альдегид
г) уксусная кислота
8 Массовая доля углерода в углеводороде 82,75%. Относительная плотность паров этого вещества по воздуху равна 2. Найти молекулярную формулу углеводорода. Написать его название и структурную формулу.
1 Вещество, формула которого С4H8 относится к классу:
2 Молекулы алкинов содержат:
а) только одинарные связи
б) одну двойную связь
в) две двойные связи
г) одну тройную связь
3 Вещество, формула которого
а) бесцветный, легко сжижающийся газ
б) бесцветная жидкость
в) огнеопасная жидкость, с неприятным запахом
г) желто-зеленый газ, ядовит
5 При гидрировании бензола получают
6 Число всех изомеров вещества бутен
неизвестным веществом Х является
8 Массовая доля углерода в углеводороде составляет 83,3%, относительная плотность паров этого вещества по водороду равна 36. Найти молекулярную формулу улеводорода. Написать его название и структурную формулу.
Ответы к заданиям 1-8: Варианты 2-6
КАРБОНОВЫЕ КИСЛОТЫ. СЛОЖНЫЕ ЭФИРЫ. ЖИРЫ.
1. Соотнесите термины, используемые для классификации кислот:
Признак классификации: 1) число карбоксильных групп
2) природа углеродного скелета
Тип кислоты: а) предельная, б) одноосновная, в) ароматическая, г) непредельная, д) двухосновная
2. Формула стеариновой кислоты
а) 3-метилбутановая б) 2-метилбутановая в) 3-метилбутеновая г) 3,3-диметилпропановая
4. Соотнесите названия и формулы:
Тривиальное название: систематическое название: формула:
I) уксусная 1) пропеновая а) СН2=СН-СООН
II) муравьиная 2) гексановая б) НООС-СООН
IV) акриловая 4) этандиовая г) СН3-СН2-СН2-СООН
V) щавелевая 5) метановая д) СН3-СООН
VI) капроновая 6) бутановая е) НСООН
5. Какие признаки, верно, отражают физические свойства уксусной кислоты: 1) при комнатной температуре бесцветная жидкость, 2) газообразное вещество, 3) не имеет запаха, 4) имеет характерный запах, 5) плохо растворима в воде, 6) неограниченно растворима в воде, 7) слабый электролит, 8) сильный электролит?
а) 1,4,6,7 б) 2,4,5,6,7 в) 1,3,6,8 г) 1,4,5,7
6. Относительная молекулярная масса предельной одноосновной карбоновой кислоты равна 256. число атомов углерода в этой кислоте равно:
а) 15 б) 16 в) 17 г) 18
Назовите эту кислоту.
7. Какой из металлов реагирует с уксусной кислотой с максимальной скоростью?
а) железо б) олово в) цинк г) кальций
Напишите уравнение реакции.
8. Суммы коэффициентов в молекулярном, полном и сокращенном ионных уравнениях реакции муравьиной кислоты с карбонатом натрия соответственно равны:
а) 7,11,7 б) 7,13,7 в) 5,9,5 г) 7,11,5
9. Взаимодействие пропионовой кислоты с этиловым спиртом называется реакцией:
а) гидратации б) этерификации в) гидрирования г) нейтрализации
Напишите уравнение реакции
10. Дана цепочка превращений
Напишите уравнения реакций.
11. Укажите формулу сложного эфира:
12. Соотнесите: вещество: 1) сложный эфир 2) воск 3) жир 4) мыло
название реакции: а) омыление б) гидролиз в) этерификации г) гидрирование
14. В состав природных жиров не входит кислота:
а) щавелевая б) стеариновая в) масляная г) олеиновая
15. С какими из перечисленных веществ в соответствующих условиях реагирует уксусная кислота: 1) медь, 2) оксид кальция, 3) оксид серы (IV), 4) метанол, 5) хлор, 6) этаналь, 7) фенолятнатрия?
а) 2,4,5,7 б) 1,2,5,6 в) 2,3,4,5 г) 4,5,6
Напишите уравнения реакций.
КАРБОНОВЫЕ КИСЛОТЫ. СЛОЖНЫЕ ЭФИРЫ. ЖИРЫ.
Тип кислоты: формула:
1) предельная а) СН3-СН=СН-СООН б)
2. Пальмитиновая кислота имеет формулу:
а) 2-дихлорбутановая б) 2,2-дихлорбутановая в) 1,1- дихлорпропановая г) 3-дихлорбутановая
4. Соотнесите названия и формулы:
Тривиальное название: систематическое название: формула:
I) муравьиная 1) пропановая а) НООС-СН2 –СН2 – СООН
III) янтарная 3) метановая в) СН3-СООН
IV) валериановая 4) бутандиовая г) НСООН
V) уксусная 5) гексановая д) СН3-СН2 -СООН
5. Относительная молекулярная масса предельной одноосновной карбоновой кислоты равна 284. число атомов углерода в этой кислоте равно:
а) 15 б) 16 в) 17 г) 18
Назовите эту кислоту.
6. С каким из веществ муравьиная кислота вступает в реакцию замещения:
Напишите уравнение реакции.
7. Суммы коэффициентов в молекулярном, полном и сокращенном ионных уравнениях реакции уксусной кислоты с гидроксидом меди (II) соответственно равны:
а) 6,8,8 б) 4,10,4 в) 6,9,7 г) 6,8,4
8. Реакцией этерификации называется взаимодействие кислоты:
а) со щелочью б) со спиртом в) с галогенами г) с металлами
9. Дана цепочка превращений: НС СН …1 …2 …3 …4
Укажите формулы веществ 1 – 4:
10. Какие признаки, верно, отражают физические свойства уксусной кислоты: 1) при комнатной температуре бесцветная жидкость, 2) газообразное вещество, 3) не имеет запаха, 4) имеет характерный запах, 5) плохо растворима в воде, 6) неограниченно растворима в воде, 7) слабый электролит, 8) сильный электролит?
а) 1,4,6,7 б) 2,4,5,6,7 в) 1,3,6,8 г) 1,4,5,7
11. С какими из перечисленных веществ в соответствующих условиях реагирует уксусная кислота: 1) медь, 2) оксид кальция, 3) оксид серы (IV), 4) метанол, 5) хлор, 6) этаналь, 7) фенолятнатрия?
а) 2,4,5,7 б) 1,2,5,6 в) 2,3,4,5 г) 4,5,6
Напишите уравнения реакций.
12. Укажите формулу сложного эфира:
13.Соотнесите: группа веществ: 1) воски 2) жиры 3) мыла 4) сложные эфиры
а) сложные эфиры глицерина и высших карбоновых кислот
б) сложные эфиры высших карбоновых кислот и высших спиртов
в) натриевые и калиевые соли высших карбоновых кислот
г) производные карбоновых кислот, в которых атом водорода карбоксильной группы замещен на углеводородный радикал.
исходные вещества: название реакции:
СН –О-СО-С17Н35 + 3КОН в) этерификации
Напишите уравнения реакций.
15. Какое из веществ выпадает из общего ряда?
а) триолеат глицерина б) тринитрат глицерина в) тристеарат глицерина г) трипальмитат глицерина
При выполнении заданий этой части в бланке ответов № 1 под номером выполняемого вами задания (А1–А30) поставьте знак « × » в клеточку, номер которой соответствует номеру выбранного вами ответа.
А1. Молекулярная формула клетчатки
А2. Какой связью соединены остатки двух моносахаридов в молекуле дисахарида
А3. Для моносахаридов характерны свойства
1. Хорошая растворимость в воде
2. Высокие температуры плавления
А4. К восстанавливающим дисахаридам не относится
А5. Заболевание сахарным диабетом вызвано повышением содержанием в крови
А6. Чем можно отличить глюкозу от фруктозы
1. Хлоридом железа (III)
2. Раскаленной медной проволокой
3. Бромной водой
4. Реакцией серебряного зеркала
А7. Из указанных углеводов не окисляется аммиачным раствором оксида серебра
Ответом к заданиям этой части (В1–В2) является набор цифр или число, которые следует записать в бланк ответов № 1 справа от номера соответствующего задания, начиная с первой клеточки. Каждую цифру и запятую в записи десятичной дроби пишите в отдельной клеточке в соответствии с приведенными в бланке образцами.
В заданиях В2 на установление соответствия запишите в таблицу цифры выбранных вами ответов под соответствующими буквами, а затем получившуюся последовательность цифр перенесите в бланк ответов № 1 без пробелов и других символов. (Цифры в ответе могут повторяться.)
В1. Вещества Х в схемах превращений соответственно являются
А. С6Н12О6 дрожжи Х + СО2
Б. С6Н12О6 + Н2 Ni Х
В. (С6Н10О5)n + 3n НNO3 H2SO4 3nН2O + H2SO4
Г. С6Н12О6 ферменты Х + СО2 + Н2
2. Триацетат целлюлоза
3. Масляная кислота
4. Тринитрат целлюлозы
6. Этиловый спирт
В2. Соотнесите реакцию и ее характерный признак.
1. Сахароза + Cu(OH)2 А. Фиолетовое окрашивание крахмала
2. Крахмал + I2 Б. Блестящий налет на стенках
3. Глюкоза [Ag(NH3)2]OH(t°) В. Комплексное соединение синего цвета
Не забудьте перенести все ответы в бланк ответов № 1.
Для записи ответов к заданиям этой части (С1) используйте бланк ответов № 2. Запишите сначала номер задания (С1), а затем полное решение. Ответы записывайте четко и разборчиво.
С1. Найдите массу футболки из триацетатного волокна, образовавшегося из 243г целлюлозы.
Инструкция по проверке и оценке работ учащихся по химии
Задание с выбором ответа считается выполненным верно, если учащийся указал код правильного ответа. Во всех остальных случаях (выбран другой ответ; выбрано два или больше ответов, среди которых может быть и правильный; ответ на вопрос отсутствует) задание считается невыполненным.
http://kopilkaurokov.ru/himiya/testi/tiestirovaniie_po_tiemie_priediel_nyie_odnoatomnyie_spirty
http://multiurok.ru/index.php/files/kontrolno-izmeritelnye-materialy-44.html