Алгоритмы решения задач
Алгоритм – конечная последовательность точно
сформулированных правил решения типовых задач.
М.С.Пак
Алгоритмы способствуют лучшему запоминанию и систематизации информации, развивают химический интеллект, «машинное» и творческое мышление при решении сложных задач.
В основе алгоритмов (см. также № 26/2001) – метод пропорции, для наглядности последний сопровождается химическими уравнениями, схемами реакций, графическим решением, что помогает лучше понимать задание.
При объяснении решений задач используются алгоритмы, что очень важно и для письменного экзамена по химии.
Помните! Задачи решают в единой системе измерения.
Алгоритм 1.
Метод суммарного уравнения параллельных реакций
Алгоритм можно использовать, когда в условии задачи есть слова «такое же количество» («такая же масса»).
1. Написать, что дано и что необходимо найти.
2. Написать схемы параллельных реакций, расставить коэффициенты.
3. Написать суммарное уравнение:
– только химические формулы задействованных веществ с соответствующими коэффициентами;
– коэффициенты перед одинаковыми химическими формулами суммируются.
Пример * . Некоторое количество углеводорода состава CnH2n–2 дает с избытком хлора 21,0 г тетрахлорида. То же количество углеводорода с избытком брома дает 38,8 г тетрабромида. Напишите молекулярную формулу всех его возможных изомеров.
* Здесь и далее использованы примеры из книги «Задачи по химии» Г.П.Хомченко и школьных олимпиад по химии.
а) п. 1.
Найти: химическая формула – ?
б) п. 2.
в) п. 3.
Найдем индекс n:
Алгоритм 2.
Насыщенные растворы
1. Записать, что дано и что необходимо найти.
2. Составить первую пропорцию, используя определение коэффициента растворимости Краств.
3. Составить вторую пропорцию, исходя из первой и данных задачи:
Решить пропорцию относительно х.
Записать ответ.
При решении обратных задач составляется такая же схема.
Для газов растворимость понижается при нагревании.
Растворимость (коэффициент растворимости Kраств) – количество вещества (в г), которое может раствориться в 100 г растворителя при определенной температуре, образуя насыщенный раствор.
Пример 1. Коэффициент растворимости соли при температуре 50 °С равен 40 г, при температуре 10 °С составляет 15 г. Определите массу осадка, полученного при охлаждении насыщенного при температуре 50 °С раствора массой 70 г до температуры 10 °С.
а) п. 1.
Дано:
Kраств(соли) при t = 50 °С – 40 г,
Kраств(соли) при t = 10 °С – 15 г,
m(насыщ. р-ра) при t = 50 °С – 70 г.
б) п. 2.
в) п. 3.
Ответ. m(осадка) при охлаждении равна 12,5 г.
Пример 2. При н. у. в воде массой 100 г растворяется хлороводород объемом 50,5 л. При температуре 50 °С и нормальном давлении коэффициент растворимости хлороводорода равен 59,6 г. Насыщенный при температуре 0 °С раствор HCl массой 40 г нагрели до температуры 50 °С. Определите массу полученного раствора.
а) п. 1.
Дано:
V(HCl) = 50,5 л (н. у.),
Kраств(HCl) = 59,6 г (50 °С, 1 атм),
m(насыщ. р-ра) = 40 г (0 °С).
б) п. 2.
в) п. 3.
5 г HCl улетучится при нагревании.
Ответ. m(полученного р-ра HCl) = 40 – 5 = 35 г.
Пример 3. В воде массой 100 г растворяется при температуре 30 °С бромид аммония массой 81,8 г. При охлаждении насыщенного при температуре 30 °С раствора NH4Br массой 300 г до температуры 0 °С выпадает в осадок соль массой 36,8 г. Определите, какая масса бромида аммония может быть растворена в воде массой 100 г при t = 0 °С.
а) п. 1.
Дано:
Kраств = 81,8 г (30 °С),
m(насыщ. р-ра) = 300 г (30 °С),
m(осадка) = 36,8 г (0 °С).
б) п. 2.
Ответ. K’раств(0 °С) = 59,5 г.
Алгоритм 3.
Расстановка коэффициентов методом полуреакций
(электронно-ионный баланс)
1. В уравнении окислительно-восстановительной реакции определить элементы, которые меняют степень окисления.
2. Составить электронно-ионный баланс с учетом среды:
– малодиссоциирующие вещества, недиссоциирующие вещества на ионы не расписывают;
– в кислой среде в реакции могут участвовать Н + и Н2О;
– в щелочной среде – ОН – и Н2О;
– в нейтральной среде – Н2О, Н + и ОН – .
3. Записать сокращенное ионное уравнение согласно электронно-ионному балансу:
– суммировать процессы окисления и восстановления с учетом равенства электронов в этих процессах;
– сократить справа и слева в химическом уравнении одинаковые ионы, молекулы.
4. Записать уравнение в молекулярной форме по ионному уравнению, дописать формулы веществ, которые в электронно-ионном балансе не были задействованы.
5. Проверить коэффициенты в молекулярном уравнении.
Составление уравнений окислительно-восстановительных реакций
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
Составление уравнений окислительно-восстановительных реакций.
Для составления уравнений окислительно-восстановительных реакций и определения коэффициентов применяют два метода: метод электронного баланса и ионно-электронный метод (метод полуреакций).
Метод электронного баланса является более простым и учитывает изменение степени окисления элементов в реакциях. Ионно-электронный метод учитывает характер химической связи в молекуле и наличие тех ионов, которые в действительности существуют в растворе, например, MnO4 – , SO4 2- , Cr2O7 2- . При реакциях окисления-восстановления электроны не берутся откуда-то со стороны, а только переходят от одних атомов или ионов к другим, поэтому число электронов, принятых окислителем, равно числу электронов, отданных восстановителем. При составлении уравнений окислительно-восстановительных реакций для того, чтобы правильно написать продукты реакции, необходимо знать свойства реагирующих веществ.
8.3.1.Метод электронного баланса.
Подбор коэффициентов в реакции методом электронного баланса осуществляется по следующей схеме:
1) Составить схему реакции
Разбавленная азотная кислота с а) неактивными металлами (Cu), б) неметаллами (P, As, S) и в) производными этих неметаллов (AsH3, PH3, As2S3) образует оксид азота (II), понижая свою степень окисления:
Атом элемента в своей высшей положительной степени окисления является окислителем, следовательно, окислитель
Атом фосфора проявляет восстановительные свойства в данной реакции, отдавая электроны с последнего энергетического уровня и повышая свою степень окисления до +5.
Следовательно, молекулярное уравнение реакции имеет следующий вид:
2) Определить величину и знак степени окисления элементов до реакции и после реакции.
3) Составить электронный баланс
4) Подставить найденные коэффициенты в уравнение реакции.
5) Подсчитать количество атомов водорода в правой и левой части равенства и уравнять их за счет добавления молекул воды в ту часть равенства, где их недостаточно.
6) Подсчитать количество атомов кислорода.
При правильно написанном и решенном уравнении количество атомов кислорода в правой и левой части равенства совпадает.
Пример 1. Написать уравнение окислительно-восстановительной реакции, подобрав коэффициенты к нему: FeSO4 + KMnO4 + H2SO4→ Fe2(SO4)3 + + MnSO4 + K2SO4 + H2O. Определяем степень окисления элементов до реакции и после реакции.
Составляем уравнения электронного баланса
Подставляем найденные коэффициенты в уравнение реакции. Подсчитываем количество групп в правой части уравнения (15+2+1=18), добавляем в левую часть равенства недостающие -группы в виде коэффициента при H2SO4. уравниваем число атомов водорода в правой и левой части равенства.
Правильность написанного уравнения проверяем по числу атомов кислорода в правой и левой части равенства.
8.3.2. Ионно-электронный метод.
При составлении электронно-ионных уравнений следует исходить не из изменения степени окисления элементов в реагирующих веществах, а нужно учитывать действительно существующие ионы в водном растворе с точки зрения теории электролитической диссоциации. Например, если реакция происходит с участием перманганата калия, то в реакции окислителем будут ионы MnO4 – , а не ионы Mn 7+ , так как перманганат калия в водном растворе диссоциирует KMnO4↔K + +MnO4 – . При этом вещества неионного характера и недиссоциирующие изображаются в электронных уравнениях в виде молекул: NH3, CO, NO2, SiO2, P.
В окислительно-восстановительных реакциях могут получаться различные продукты реакции в зависимости от характера среды – кислой, щелочной, нейтральной. Для таких реакций в молекулярной схеме необходимо указывать окислитель, восстановитель и вещество, характеризующее реакцию среды (кислоту, щелочь, воду). В этом случае в ионном уравнении необходимо руководствоваться правилами стяжения, указывать ионы, характеризующие реакцию среды: H + , OH – , H2O. Правила стяжения сводятся к следующему:
1. В кислой среде избыток ионов O +2 образует с ионами H + молекулы воды:
2. В нейтральной или щелочной среде избыток ионов O 2- образует с молекулами воды гидроксид – ионы:
3. В щелочной среде недостаток ионов O 2– компенсируется двумя ионами OH – , одновременно образуется одна молекула воды:
| Реакция среды | Избыток ионов О 2– | Недостаток ионов О 2– |
| окислитель | восстановитель | |
| Кислая | Н + Н2О | Н2O 2Н + |
| изб. O 2– + 2H + = Н2О | Н2О 2Н + + O 2– | |
| Нейтральная | H2O OH – | Н2O 2Н + |
| изб. О 2– + Н2О 2OН – | Н2О 2Н + + О 2– | |
| Щелочная | Н2O ОН – | 2OН – Н2О |
| изб. О 2– + Н2O 2OН – | 2OН – Н2О + О 2– |
Разберем на конкретных примерах.
Пример 1. Составить уравнение реакции, которая протекает при пропускании сероводорода Н2S через подкисленный раствор перманганата калия КМnO4
При протекании реакции малиновая окраска исчезает и раствор мутнеет. Опыт показывает, что помутнение раствора происходит в результате образования элементарной серы из сероводорода:
В этой схеме число атомов одинаково в левой и правой частях. Для уравнивания зарядов надо от левой части схемы отнять два электрона, после чего можно стрелку заменить на знак равенства:
Эта первая полуреакция — процесс окисления восстановителя H2S.
Обесцвечивание раствора связано с переходом иона МnО – 4 (он имеет малиновую окраску) в ион Mn 2+ (почти бесцветный и лишь при большой концентрации имеет розоватую окраску), что можно выразить схемой
Опыт показывает, что в кислом растворе кислород, входящий в состав ионов MnO – 4, вместе с ионами водорода в конечном итоге образует воду. Поэтому процесс перехода записываем так:
Чтобы стрелку заменить на знак равенства, надо уравнять и заряды. Поскольку исходные вещества имеют семь положительных зарядов (7+), а конечные – два положительных (2+), то для выполнения условия сохранения зарядов надо к левой части схемы прибавить пять электронов:
MnO – 4 + 8H + +5e – = Mn 2+ +4H2О
Это вторая полуреакция – процесс восстановления окислителя – иона MnO – 4.
Для составления общего (суммарного) уравнения реакции надо уравнение полуреакций почленно суммировать, предварительно уравнять число отданных и полученных электронов. В этом случае по правилам нахождения наименьшего кратного определяют соответствующие множители, на которые умножаются равенства полуреакций. Сокращенно запись проводится так:
Сократив на 10 Н + , окончательно получим
Проверяем правильность составленного ионного уравнения. В примере число атомов кислорода в левой части 8, в правой 8; число зарядов в левой части (2-) + (6+) == 4+, в правой 2(2+) = 4+. Уравнение составлено правильно.
Методом полуреакций составляется ионное уравнение реакции. Чтобы от ионного уравнения перейти к молекулярному, поступаем так: в левой части ионного уравнения к каждому аниону подбираем соответствующий катион, а к каждому катиону — анион. Затем такие же ионы в таком же количестве записываем и в правую часть уравнения, после чего ионы объединяем в молекулы:
Пример 2. Реакция среды кислая
1. Составить схему реакции
Из опытных данных знаем, что окислителем является КМnO4. Ион MnO4 – восстанавливается в кислой среде до Мn 2+ (фиолетово-малиновая окраска иона MnO4 – становится бесцветной, переходя в Мn 2+ – ион), следовательно, ион SO3 2 – будет являться восстановителем, переходя в ион SO4 2- .
2. Составить электронно-ионные уравнения
а) для окислителя
Из ионной схемы видно, что, ион MnO4 – – превращается в ион Мn 2+ , при этом освобождаются ионы О 2- , которые по правилу стяжения в кислой среде связываются ионами Н + , образуя молекулы Н2O.
б) для восстановителя
Из ионной схемы видно, что ион SO3 2- превращается в ион SO4 2- . Для этого превращения необходимо добавить ион О 2- , который берется из молекулы H2O (реакция протекает в водной среде), при этом освобождаются два иона Н+.
3. Подсчитать число зарядов в правой и левой части равенства, добавляя или уменьшая необходимое число электронов. Алгебраическая сумма зарядов в обеих частях равенства должна быть одинакова.
MnO4 – + 8H + + 5ē = Mn 2+ + 4H2O
4. Найти основные коэффициенты, т. е. коэффициенты при окислителе и восстановителе:
5. Написать суммарное электронно-ионное уравнение, учитывая найденные коэффициенты:
6. Сократить в левой и правой части уравнения 10 Н + и 5Н2O. Получается ионное уравнение:
7. По ионному уравнению составить молекулярное уравнение реакции:
8. Число ионов и атомов каждого элемента в правой и левой части равенства, должно быть равно.
Пример 3. Реакция среды щелочная.
1. Составить схему реакции
Окислителем в данной реакции является молекула брома, следовательно, восстановителем будет являться метахромит калия, а именно ион СrO2 – .
2. Составить электронно-ионное уравнение
а) для окислителя
б) для восстановителя
Из ионной схемы видно, что ион CrO2 – превращается в ион СгО4 2– . Каждый недостающий ион О 2– берется по правилу стяжения из двух гидроксильных ионов (среда щелочная ОН – ), при этом одновременно образуется одна молекула воды.
3. Подсчитать число зарядов в правой и левой части равенства. Найти коэффициенты при окислителе и восстановителе.
4. Написать суммарное уравнение, учитывая найденные коэффициенты:
5. По ионному уравнению составить молекулярное уравнение реакции.
6. Число атомов и ионов каждого элемента в правой и левой части уравнения должно быть равно.
Пример 4. Реакция среды нейтральная.
1. Составить схему реакции
Окислителем является КМnO4, так как ион элемента в своей высшей степени окисления не способен более отдавать электроны (Мn +7 ). Восстановителем является сульфит калия K2SO3.
2. Составить электронно-ионное уравнение
а) для окислителя
В нейтральной среде избыток ионов кислорода стягивается с молекулами воды, образуя гидроксид-ионы.
б) для восстановителя
Из ионной схемы видно, что ион SО3 2- превращается в ион SO4 2- , для этого необходимо добавить один ион О 2- , который берется из молекулы Н2O (реакция протекает в водной среде). При этом освобождаются два иона Н + .
3. Подсчитать число зарядов в правой и левой части равенства. Найти коэффициенты при окислителе и восстановителе.
4.Написать электронно-ионное уравнение, учитывая найденные коэффициенты:
Сокращаем левую и правую часть равенства на 6Н20. Получаем окончательное ионное уравнение.
5. По ионному уравнению составить молекулярное уравнение реакции.
6. Число атомов и ионов каждого элемента в правой и левей части уравнения должно быть равно.
Пример 5. Исходя из степени окисления (п) азота, серы и марганца в соединениях NН3, HNO2, HNO3, H2S, Н2SO3, Н2SО4, MnO2 и КМnO4, определите, какие из них могут быть только восстановителями, только окислителями и какие проявляют как окислительные, так и восстановительные свойства.
Решение. Степень окисления азота в указанных соединениях соответственно равна: -3 (низшая), +3 (промежуточная), +5 (высшая); n(S), соответственно, равна: -2 (низшая), +4 (промежуточная), +6 (высшая); n(Мn), соответственно, равна: + 4 (промежуточная), +7 (высшая). Отсюда: NН3, H2S — только восстановители; HNO3, H2SO4, КMnО4 — только окислители; НNО2, Н2SО3, MnO2 — окислители и восстановители.
Пример 6. Могут ли происходить окислительно-восстановительные реакции между следующими веществами: a) H2S и HI; б) H2S и Н2SО3; в) Н2SО3 и НС1O4?
а) Степень окисления в Н2S n(S) = -2; в HI n(I) = -1. Так как и сера и иод находятся в своей низшей степени окисления, то оба вещества проявляют только восстановительные свойства и взаимодействовать друг с другом не могут;
б) в H2S n(S) = -2 (низшая), в H2SO3 n(S) = +4 (промежуточная).
Следовательно, взаимодействие этих веществ возможно, причем, Н2SО3 является окислителем;
в) в Н2SO3 n(s) = +4 (промежуточная); в НС1O4 n(Сl) = +7 (высшая). Взятые вещества могут взаимодействовать, Н2SО3 в этом случае будет проявлять восстановительные свойства.
Пример 7. Составьте уравнения окислительно-восстановительной реакции, идущей по схеме:
Решение. Если в условии задачи даны как исходные вещества, так и продукты их взаимодействия, то написание уравнения реакции сводится, как правило, к нахождению и расстановке коэффициентов. Коэффициенты определяют методом электронного баланса с помощью электронных уравнений. Вычисляем, как изменяют степень окисления восстановитель и окислитель, и отражаем это в электронных уравнениях:
Общее число электронов, отданных восстановителем, должно быть равно числу электронов, которые присоединяет окислитель. Общее наименьшее кратное для отданных и принятых электронов 10. Разделив это число на 5, получаем коэффициент 2 для окислителя и продукта его восстановления, а при делении 10 на 2 получаем коэффициент 5 для восстановителя и продукта его окисления. Коэффициент перед веществами, атомы которых не меняют свою степень окисления, находят подбором. Уравнение реакции будет иметь вид:
Пример 8. Составьте уравнение реакции взаимодействия цинка с концентрированной серной кислотой, учитывая максимальное восстановление последней.
Решение. Цинк, как любой металл, проявляет только восстановительные свойства. В концентрированной серной кислоте окислительная функция принадлежит сере (+6). Максимальное восстановление серы означает, что она приобретает минимальную степень окисления. Минимальная степень окисления серы как p-элемента VIA-группы равна -2. Цинк как металл IIВ-группы имеет постоянную степень окисления +2. Отражаем сказанное в электронных уравнениях:
Составляем уравнение реакции:
Перед H2SO4 стоит коэффициент 5, а не 1, ибо четыре молекулы H2SO4 идут на связывание четырех ионов Zn 2+ .
Стехиометрия реакций и материальные расчеты
Читайте также:
|
| В = | -1 |
| -2 | |
| -1 | -1 |
| -1 |
Оказывается, что ранг стехиометрической матрицы равен числу независимых реакций. Ранг представленной матрицы равен 2.
Одновременно с числом независимых реакций определяют равное ему число так называемых ключевых веществ, по которым можно полностью охарактеризовать материальный баланс системы. В простой реакции ключевое вещество только одно (например, циклогексен из предыдущего примера). В сложных системах выбор независимых реакций и ключевых веществ взаимосвязан и определяется тем, чтобы в каждой независимой реакции участвовало хотя бы одно ключевое вещество и в то же время выбранные ключевые вещества участвовали бы только в одной или в некотором минимуме независимых реакций. Так, для дегидратации этанола выгодно выбрать в качестве независимых реакций 1 и 2, а в качестве ключевых веществ — этилен и диэтиловый эфир. Выбор ключевых веществ зависит также от простоты и точности их аналитического определения.
После анализа сложной системы превращений, выбора независимых реакций и ключевых веществ легко провести ее материальный расчет. Для каждой из независимых реакций по аналогии с выражением [2.3] можно записать уравнения полноты реакции
где индекс i соответствует веществу, а индекс j — реакции. Тогда, имея в виду, что каждое из веществ может участвовать в нескольких реакциях (Δni=ΣΔnij), получим:

Зная начальные условия и ni (или Fi) для ключевых веществ, находим вначале по уравнениям [2.5] полноту реакций nj или Fj и затем полный состав реакционной массы. Отметим, что при обратимых реакциях с единственным независимым превращением и одним ключевым веществом справедливы уравнения баланса, выведенные ранее для простых реакций, в том числе соотношения, иллюстрированные на рис. 2.2.
При дегидратации этанола его начальный мольный поток Fc2h5он,0 = 1000 кмоль/ч,
Рассчитать материальный баланс процесса.
При независимых реакциях 1 и 2 (см. ранее) имеем:
Fc2h5он = 1000 – 1*300 – 2*200 = 300 кмоль/ч
Fh2O = 0 + 1*300 + 1*200 = 500 кмоль/ч
На основе этого расчета составляется таблица материального баланса, в которой сопоставляются взятые и полученные количества веществ. Например, для предыдущего расчета получим:
| Наименование компонента | Подано | Получено | ||
| кмоль/ч | кг/ч | кмоль/ч | кг/ч | |
| Этанол | 1 000,0 | 46 000 | 300,0 | 13 800 |
| Этилен | 0,0 | 0,0 | 300,0 | 8 400 |
| Диэтиловый эфир | 0,0 | 0,0 | 200,0 | 14 800 |
| Вода | 0,0 | 0,0 | 500,0 | 9 000 |
| Итого: | 1 000,0 | 46 000 | 1 300,0 | 46 000 |
При балансовых опытах или подведении фактического материального баланса установки обычно наблюдается небольшое расхождение между суммами взятых и полученных веществ. Это объясняется неточностью анализов и неучтенными потерями. Материальные расчеты удобно проводить по независимым суммарным реакциям образования ключевых веществ из исходных реагентов. В рассмотренном выше примере они совпадают с соответствующими простыми реакциями, но в других случаях
бывает не так. Например, при этилировании бензола протекают следующие простые реакции:
Стехиометрический анализ показывает, что из шести простых
реакций две являются независимыми. Столько же имеется и ключевых веществ, за которые можно принять два вещества — этилбензол и диэтилбензол. Суммарные реакции их образования из исходных реагентов таковы:
Одна из них совпадает с соответствующей простой реакцией, а
другая не совпадает и имеет иные стехиометрические коэффициенты, которые обозначим v′i. Выведенное ранее уравнение баланса [2.5] для сложных реакций применимо и для суммарных реакций. Поэтому дальнейший расчет при заданных начальных условиях и Fi (ni) для ключевых веществ проводится аналогично.
Уравнение [2.5] для суммарных реакций образования ключевых веществ служит для составления баланса по исходным реагентам, который часто необходим при исследовании или расчете процесса. Когда каждое из ключевых веществ образуется только по одной суммарной реакции, имеем:
Например, для разбираемого процесса этилирования бензола получим:
Безразмерные характеристики материального баланса реакций.
Как уже было сказано выше, в химии и химической технологии большое значение имеют безразмерные характеристики материального баланса – степень конверсии (степень превращения), селективность и выход.
Степень конверсии(степень превращения, конверсия) – доля прореагировавшего исходного реагента относительно его начального количества. Степень превращения реагента показывает, насколько полно в химико-технологическом процессе используется исходное сырье.
Конверсия реагента A

В примере дегидратации этанола степень его конверсии составляет:
ХROH = (1000 – 300):1000 = 0,70 или 70,0%
Чаще всего в химической реакции участвует не один, а два реагента (или даже больше). При этом обычно степень конверсии определяют по основному реагенту А, но она может быть рассчитана по каждому реагенту, причем в общем случае не обязательно получаются равные результаты.
Степени превращения реагентов A и B, участвующих в реакции (I):

Необходимо помнить, что конверсия – это доля первоначального количества реагента, т. е. пределы изменения Хi определяются соотношением 
Если один из реагентов (например, реагент В) взят в избытке, то всегда
ХВ
Дата добавления: 2015-04-20 ; просмотров: 73 | Нарушение авторских прав
http://farmf.ru/lekcii/sostavlenie-uravnenij-okislitelno-vosstanovitelnyh-reaktsij/
http://lektsii.net/3-76495.html








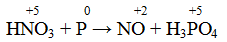
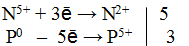
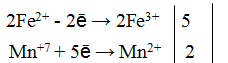
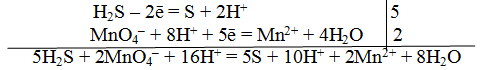
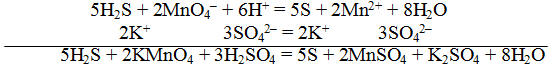
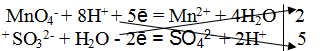
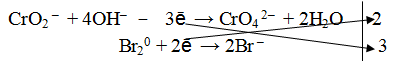
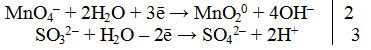
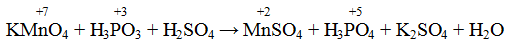
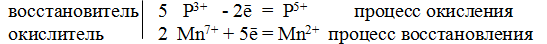
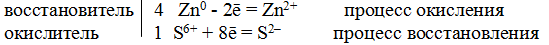
 или
или  [2.1]
[2.1] моль(кмоль)/в ед. времени[2.2]
моль(кмоль)/в ед. времени[2.2]
 [2.3]
[2.3] [2.4]
[2.4] = 12 моль,
= 12 моль,  =
=  = 0 и
= 0 и 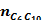 = 3 моль.
= 3 моль.
 = 0 + 2·3 = 6 моль
= 0 + 2·3 = 6 моль = 0 + 1·3 = 3 моль
= 0 + 1·3 = 3 моль













