Глюкоза крайне важна для энергетики клеток
Глюкоза – это субстрат для получения энергии
Энергетика любой клетки нашего организма основана на окислении глюкозы. Окисление глюкозы происходит по двум направлениям:
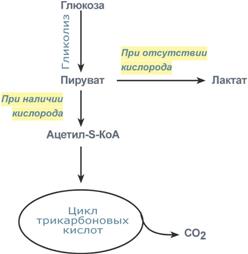 Пути метаболизма пирувата в присут- |
- Окисление с образованием пентоз: рибозы, рибулозы, ксилулозы. Этот путь называется пентозофосфатный шунт и не связан с получением энергии
- Окисление с получением энергии.
Второй путь, т.е. тот по которому глюкоза окисляется для получения энергии, называется гликолиз (греч. glykos — сладкий и греч. lysis — растворение). Конечным продуктом гликолиза является пировиноградная кислота (пируват).
В зависимости от дальнейшей судьбы пирувата различают аэробное и анаэробное окисление глюкозы. Целью обоих типов окисления является получение АТФ .
В аэробном процессе пировиноградная кислота превращается в ацетил-SКоА (реакции ПВК-дегидрогеназы) и далее сгорает в реакциях цикла трикарбоновых кислот до СО2 (реакции ЦТК).
Общее уравнение аэробного окисления глюкозы:
В анаэробном процессе пировиноградная кислота восстанавливается до молочной кислоты (лактата). Лактат является метаболическим тупиком и далее ни во что не превращается, единственная возможность утилизовать лактат – это окислить его обратно в пируват. В микробиологии анаэробный гликолиз называют молочнокислым брожением.
Суммарное уравнение анаэробного гликолиза имеет вид:
Глюкоза – это источник оксалоацетата
После того как пируват синтезировался, он необязательно превращается в ацетил-SКоА или молочную кислоту. Существенное значение имеет его способность карбоксилироваться в оксалоацетат , особенно эта реакция активна в печени. Наличие избытка оксалоацетата «подталкивает» реакции цикла трикарбоновых кислот (доступность субстрата), ускоряет связывание ацетильной группы, ее окисление и производство энергии.
При голодании отсутствие глюкозы в клетках и активация глюконеогенеза в гепатоцитах, ухудшение окисления глюкозы до пирувата при сахарном диабете влечет за собой недостаточное количество оксалоацетата. Это сопровождается гипоэнергетическим состоянием клетки и активацией синтеза кетоновых тел в печени.
Процесс гликолиза его реакции, аэробный и анаэробный (Таблица, схема)
Гликолиз — процесс окисления глюкозы, при котором из одной молекулы глюкозы образуются две молекулы пировиноградной кислоты, не является мембранозависимым процессом. Он происходит в цитоплазме. Однако ферменты гликолиза связаны со структурами цитоскелета. Суть гликолиза состоит в том, что молекула глюкозы (C6H12O6) без участия кислорода распадается на две молекулы пировиноградной кислоты (СН3СОСООН). При этом окисление идет за счет отщепления от молекулы глюкозы четырех атомов водорода, связывающихся со сложным органическим веществом НАД с получением двух молекул НАД•Н. Выделяющаяся при этом энергия запасается (40% от общего количества) в виде макроэргических связей двух молекул АТФ. 60% энергии выделяется в виде тепла. При последующем окислении НАД•Н получается еще 6 молекул АТФ. Таким образом, полный энергетический выход гликолиза в анаэробных условиях составляет 8 молекул АТФ.
Аэробный процесс гликолиза (10 реакций), уравнение (с образованием пирувата):
Анаэробный процесс гликолиза (11 реакций), уравнение (с образованием лактата):
Схема процесса гликолиза и его реакции
На схеме в рамках обозначены исходные субстраты и конечные продукты гликолиза, цифрами в скобках — число молекул.
ATP (АТФ) — это аденозинтрифосфорная кислота, универсальный источник энергии
ADP (АДФ) — это аденозиндифосфат, нуклеотид, участвует в энергетическом обмене
NAD (НАД) — никотинамидадениндинуклеотидфосфата
NADH (НАД•Н) — востановленная форма NAD
Таблица процесс гликолиза его реакции
Для распада и частичного окисления молекулы глюкозы требуется протекание 11 сложных последовательных реакций.
Ферменты, Активаторы, ингибиторы
Подготовительная стадия гликолиза
Стадия активации глюкозы проходит в 5 реакций, в ходе которых 1 молекула гексозы (глюкозы) расщепляется на 2 молекулы триоз-глицеральдегидфосфата
1. Необратимая реакция фосфорилирования глюкозы
Процесс гликолиза начинается с фосфорилирования глюкозы за счет АТФ — первая реакция. Это первая пусковая реакция гликолиза. Ее результатом является глюкозо-6-фосфат, имеющий отрицательный заряд. В гликолизе может участвовать не только глюкоза, но и другие гексозы (фруктоза), но в результате фосфорилирования и активации все равно образуется глюкозо-6-фосфат.
Ингибиторы: глюкозо-6-Ф, фосфоенолпируват.
2. Обратимая реакция изомеризации глюкозо-6-фосфата
Во второй реакции происходит изомеризация (внутримолекулярные перестройки) глюкозо-6-фосфата во фруктозо-6-фосфат.
3. Необратимая реакция фосфорилирования фруктозо-6-фосфата (ключевая стадия гликолиза)
В третьей реакции происходит фосфорилирование (присоединение остатка ортофосфорной кислоты) фруктозо-6-фосфата с образованием фруктозо-1,6-дифосфата. При этом затрачивается еще одна молекула АТФ (уже вторая) — это вторая пусковая реакция гликолиза. Она идет в присутствии Mg2 + и является необратимой, так как сопровождается масштабным уменьшением свободной энергии.
Ингибиторы: АТФ, цитрат, НАДН.
4. Обратимая реакция дихотомического расщепления фруктозо-1,6-дифосфата
В четвертой реакции гликолиза происходит расщепление фруктозо-1,6-дифосфата на две молекулы глицеральдегид-3-фосфата.
5. Обратимая реакция изомеризации дигидроксиацетона-3-фосфат в глицеральдегид-3-фосфат
В пятой реакции происходит изомеризация полученных триозофосфатов. На этом заканчивается первая стадия гликолиза.
Стадия генерации АТФ
Проходит в 6 реакций (или 5), в ходе которых энергия окислительных реакций трансформируется в химическую энергию АТФ (субстратное фосфорилирование).
6. Окисление глицеральдегид-3-фосфата до 1,3-дифосфоглицерата (реакция гликолитической оксиредукции)
В шестой реакции происходит окисление альдегидной группы до карбоксильной. Выделившийся Н+ акцептируется NAD, который восстанавливается до NADH. Освобождающаяся энергия затрачивается для образования высокоэнергетической связи 1,3-бифосфоглицерата (1,3-бифосфоглицериновая кислота).
7. Субстратное фосфорилирование АДФ (7)
В седьмой реакции фосфорильная группа 1,3-бифосфоглицерата переносится на ADP, в результате чего образуется АТР (напоминаем, что следует иметь в виду две параллельные цепи реакций, с участием двух молекул триоз, образовавшихся из одной молекулы гексозы, следовательно, синтезируется не одна, а две молекулы АТР).
8. Реакция изомеризации 3-фосфоглицерата в 2-фосфоглицерат
В восьмой реакции гликолиза происходит перенос фосфатной группы с третьего атома углерода на второй. В результате образуется 2-фосфоглицерат (2-фосфоглицериновая кислота).
9. Реакция енолизации
Девятая реакция сопровождается внутримолекулярными окислительно-восстановительными процессами, в результате которых образуется фосфоенолпируват (фосфоенолпировиноградная кислота) с высокоэнергетической связью во втором атоме углерода и отщепляется молекула воды
10. Реакция субстратного фосфорилирования
В ходе десятой реакции фосфорильная группа переносится на ADP. При этом синтезируется АТР и пируват (пировиноградная кислота). Эта реакция также необратима, поскольку высокоэкзергонична.
11. Реакция обратимого восстановления пировиноградной кислоты до молочной кислоты (в анаэробных условиях)
Если после гликолиза следует аэробное расщепление, пируват мигрирует в матрикс митохондрий, где, взаимодействуя с коэнзимом-А, участвует в образовании ацетил-СоА. В анаэробных условиях пируват при участии NADH восстанавливается до лактата (молочной кислоты), который при этом является конечным продуктом гликолиза. Затем в аэробных условиях лактат может обратно превратиться в пируват и окислиться в митохондриях.
_______________
Источник информации:
1. Биология для поступающих в вузы / Г.Л. Билич, В.А. Крыжановский. — 2008.
2. Биология в таблицах и схемах / Спб. — 2004.
3. Биохимия в схемах и таблицах / И. В. Семак — Минск — 2011.
Полное окисление глюкозы. Энергетический баланс полного окисления глюкозы
Окисление глюкозы до СО2 и Н2О (аэробный распад). Аэробный распад глюкозы можно выразить суммарным уравнением:
С6Н12О6 + 6 О2 → 6 СО2 + Н2О + 2820 кДж/моль.
Этот процесс включает несколько стадий (рис. 7-33).
Аэробный гликолиз — процесс окисления глюкозы с образованием двух молекул пирувата;
Общий путь катаболизма, включающий превращение пирувата в ацетил-КоА и его дальнейшее окисление в цитратом цикле;
ЦПЭ на кислород, сопряжённая с реакциями дегидрирования, происходящими в процессе распада глюкозы.
Гликолиз — это катаболический путь обмена веществ в цитоплазме; он, по-видимому, протекает почти во всех организмах и клетках независимо от того, живут они в аэробных или анаэробных условиях. Баланс гликолиза простой: в аэробных условиях молекула глюкозы деградирует до двух молекул пирувата. Кроме того, образуются по две молекулы АТФ и НАДН + H + (аэробный гликолиз). В анаэробных условиях пируват претерпевает дальнейшие превращения, обеспечивая при этом регенерацию НАД + (см. с. 148). При этом образуются продукты брожения, такие, как лактат или этанол (анаэробный гликолиз). В этих условиях гликолиз является единственным способом получения энергии для синтеза АТФ из АДФ и неорганического фосфата.
Рис. 7-33. Аэробный распад глюкозы. 1-10- реакции аэробного гликолиза; 11 — малат-аспартатный челночный механизм транспорта водорода в митохондрии; 2 (в кружке) — стехиометрический коэффициент.
Выход АТФ при аэробном распаде глюкозы до конечных продуктов
В результате гликолиза образуется пируват, который далее окисляется до СО2 и Н2О в ОПК, описанном в разделе 6. Теперь можно оценить энергетическую эффективность гликолиза и ОПК, которые вместе составляют процесс аэробного распада глюкозы до конечных продуктов (табл. 7-4).
Таким образом, выход АТФ при окислении 1 моль глюкозы до СО2 и Н2О составляет 38 моль АТФ.
В процессе аэробного распада глюкозы происходят 6 реакций дегидрирования. Одна из них протекает в гликолизе и 5 в ОПК (см. раздел 6). Субстраты для специфических NAD-зависимых дегидрогеназ: глицеральдегид-3-фосфат, жируват, изоцитрат, α-кетоглутарат, малат. Одна реакция дегидрирования в цитратном цикле под действием сукцинатдегидрогеназы происходит с участием кофермента FAD. Общее количество АТФ, синтезированное путём окислительного фофорилирования, составляет 17 моль АТФ на 1 моль глицеральдегидфосфата. К этому необходимо прибавить 3 моль АТФ, синтезированных путём субстратного фосфорилирования (две реакции в гликолизе и одна в цитратном цикле).
Учитывая, что глюкоза распадается на 2 фос-фотриозы и что стехиометрический коэффициент дальнейших превращений равен 2, полученную величину надо умножить на 2, а из результата вычесть 2 моль АТФ, использованные на первом этапе гликолиза.


Основное физиологическое назначение катаболизма глюкозы заключается в использовании энергии, освобождающейся в этом процессе для синтеза АТФ.
Энергия, выделяющаяся в процессе полного распада глюкозы до СО2 и Н2О, составляет 2880 кДж/моль.
3.Механизм реакции трансаминирования. Все трансаминазы (как и декарбоксилазы аминокислот) содержат один и тот же кофермент – пиридоксальфосфат. Для реакцийтрансаминирования характерен общий механизм. Специфичность трансаминаз обеспечивается белковым компонентом. Ферменты трансаминирования катализируют перенос NH2-группы не на α-кетокислоту, а сначала на кофермент пиридоксаль-фосфат. Образовавшееся промежуточное соединение (шиффово основание) подвергается внутримолекулярным превращениям (лабилизация α-водо-родного атома, перераспределение энергии связи), приводящим к освобождению α-кетокислоты и пиридоксаминфосфата; последний на второй стадии реакции реагирует с любой другой α-кетокислотой, что через те же стадии образования промежуточных соединений (идущих в обратном направлении) приводит к синтезу новойаминокислоты и освобождению пиридоксальфосфата. Опуская промежуточные стадии образования шиф-фовых оснований, обе стадии реакции трансаминирования можно представить в виде общей схемы:
В связи с тем что во всех пиридоксалевых ферментах (включая транс-аминазы) карбонильная группа кофермента (—СНО) оказалась связанной с ε-аминогруппой лизина белковой части, в классический механизм реакции трансаминирования А.Е. Браунштейн и Э. Снелл внесли следующее дополнение. Оказалось, что взаимодействие между субстратом, т.е. L-амино-кислотой (на рисунке – аспартат), и пиридоксальфосфатомпроисходит не путем конденсации с выделением молекулы воды, а путем реакции замещения, при которой NH2-группа субстрата вытесняет ε-NН2-группу лизина в молекуле ферментного белка, что приводит к формированию пиридоксальфосфатного комплекса.
Существование представленного механизма реакции трансаминирова-ния доказано разнообразными методами, включая методы спектрального анализа по идентификации промежуточных альдиминных и кетиминных производных пиридоксальфосфата.
http://infotables.ru/biologiya/81-biokhimiya/1048-glikoliz
http://lektsii.org/8-71082.html













