Основное уравнение МКТ газов. Температура
Модель идеального газа считается самой простейшей относительно основных положений МКТ. Кинетическая модель идеального газа молекул говорит о том, что при взаимодействии между собой, шарики рассматриваются в качестве идеально упругих. Суммарный объем всех молекул достаточно мал по сравнению с объемом сосуда, в котором находится данный газ. Модель необходима для описания его поведения при различных давлениях и температурах.
Цель молекулярно-кинетической теории – установка связи между макроскопическими и макроскопическими параметрами.
После соударения молекул между собой и стенками сосуда происходит изменение направления движения и времени между интервалами столкновений. Модель идеального газа основывается на законах механики Ньютона, то тесть столкновения соответствуют закону упругого удара.
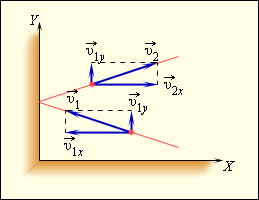
Чтобы определить давление газа на стенку сосуда, учитывается модель идеального газа. Исходя из этого, происходит возникновение сил, которые подчиняются 3 закону Ньютона. Отсюда получим, что проекция скорости υ x перпендикулярна относительно стенки, а знак меняется на противоположный. Проекция υ y параллельна и постоянна. Это показано на рисунке 3 . 2 . 1 .
Рисунок 3 . 2 . 1 . Упругое столкновение молекулы со стенкой.
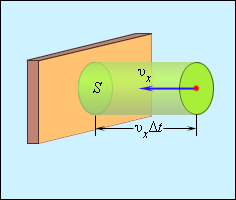
Отсюда следует, что изменение импульса можно записать в виде 2 m 0 υ x с массой молекулы, равной m 0 . Необходимо выделить площадь S , как показано на рисунке 3 . 2 . 2 . По прошествии времени Δ t с S поверхностью столкнутся молекулы с проекциями скорости υ x , которая направлена в сторону стены, и основанием цилиндра S с высотой υ x Δ t .
Рисунок 3 . 2 . 2 . Определение числа столкновений молекул с поверхностью S .
Если за единицу объема брать сосуд с n -ым количеством молекул, тогда их число в объеме цилиндра нужно обозначить, как n S υ x Δ t . Очевидно, что происходит столкновение только половины имеющихся молекул. Тогда количество ударов о S за время Δ t равняется 1 2 n S v x ∆ t .
При столкновении происходит изменение импульса 2 m 0 υ x . Тогда формула n m 0 v x 2 S ∆ t говорит о полном его изменении за определенный промежуток времени. Исходя из закона механики, изменение импульса всех молекул записывается как F Δ t . Силой F обозначается средняя сила, которая действует на молекулы. Но 3 закон Ньютона говорит о том, что аналогичная сила по модулю оказывает действие на поверхность S . Данное утверждение можно зафиксировать F ∆ t = n m 0 v x 2 S ∆ t .
Далее для упрощения следует разделить равенство на выражение S Δ t . Формула примет вид p = F S = n m 0 v x 2 со значением р , обозначаемым в качестве давления газа на стенку сосуда.
Все молекулы, находящиеся в сосуде на единицу объема, имеют разные проекции скоростей на ось О х . При столкновениях прослеживалось статистическое их распределение по скоростям, причем с разными направлениями векторов их скоростей.
Распределением Максвелла называют распределение молекул газа по модулю скоростей.
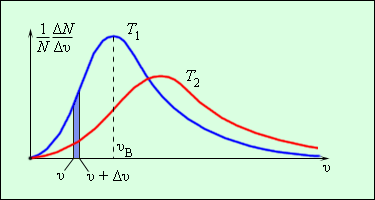
Еще в 1860 г Дж. Максвелл вывел закон распределения молекул газа по скоростям, основываясь на основных положениях молекулярно-кинетической теории молекулы. Рисунок 3 . 2 . 3 . наглядно показывает распределения молекул по скоростям с помощью кривых. На оси О х располагается модуль скорости, а на О у – количество молекул, находящихся на интервале от υ до υ + Δ υ . На рисунке 3 . 2 . 3 . данное значение выделено в виде столбика.
Рисунок 3 . 2 . 3 . Распределение молекул по скоростям. T 2 > T 1 .
Характерные параметры распределения Максвелла – это вероятная скорость υ в ,которая соответствует кривой распределения, и среднеквадратичная скорость υ к в = υ 2 → , где υ 2 → обозначающие среднее значение квадрата скорости.
Если растет температура, тогда максимум кривой будет смещен в сторону больших скоростей, то есть υ в и υ к в увеличатся.
Распределение Максвелла
Для записи формулы давления газа необходимо предположить, что все молекулы разделены на n 1 , n 2 , n 3 группы с проекциями υ x 1 , υ x 2 , υ x 3 . Иначе говоря, записываем ∑ i n i = n . Можно зафиксировать, как n i m 0 v x i 2 . Тогда суммарное давление примет вид p = m 0 ∑ i n i v x i 2 .
Данная сумма является суммой квадратов проекций υ x всех n молекул на единичном объеме газа. При делении выражения на n получим среднее значение квадратичной скорости проекции υ x . Запишем в виде 1 n ∑ n i υ x i 2 = v x 2 → i .
Другая интерпретация формулы давления газа p = n m 0 v x 2 → . Все направления векторов различные, потому среднее значение квадратов проекций на координатные оси равняется v x 2 → = v y 2 → = v z 2 → = 1 3 v 2 → .
Формула для среднего давления газа на стенку сосуда обозначим, как p = p → = 1 3 n m 0 v 2 → = 2 3 n m 0 v 2 → 2 = 2 3 n E k → .
Из уравнения видна связь между р и m 0 и количеством молекул n , средней квадратичной скоростью v 2 → и средней кинетической энергией E k → молекул. Такое уравнение получило название уравнения молекулярно-кинетической уравнения теории газов.
Отсюда следует, что давление газа – это две трети средней кинетической энергии, которое имеется в единице объема. Основное уравнение молекулярно-кинетической теории газов или строения вещества содержит произведение количества молекул n на E k → . Предположительно сосуд имеет газ неизменного объема V , тогда n = N V = c o n s t ( N — число молекул в сосуде). Изменение давления происходит пропорционально изменению кинетической энергии.
Физика. Температура
Температура связана с понятием теплового равновесия. При контакте тела обмениваются энергией, которая передается и получает название количества теплоты.
Тепловым равновесием называют состояние системы тел, которые находятся в тепловом контакте с теплопередачей и с постоянными макроскопическими параметрами.
Температура — физический параметр, который находится в тепловом равновесии. Введение понятия температуры идет из нулевого закона термодинамики.
Температура измеряется с помощью термометра. Для его создания выбирается термометрическое вещество и величину, которая его характеризует. Разные конструкции подразумевают отличия в их свойствах.
Каждый термометр должен быть откалиброван. Использование природных систем с неизменной температурой необходимо для хорошего теплообмена. Температура плавления льда равняется 0 градусов Цельсия, а точка кипения воды – 100 градусов. Одно маленькое деление из шкалы равняется 1 градусу. Существует обозначение замерзания воды по Фаренгейту, то есть 32 ° F . Получаем, что формула примет вид T F = 9 5 T C + 32 или T C = 5 9 ( T F — 32 ) .
На рисунке 3 . 2 . 4 . изображен газовый термометр, который чаще всего заполняют разряженным гелием, воздухом с неизменным объемом, обозначаемым V = c o n s t , и давлением р . Из опыта видно, что возрастание давления идет с повышением температуры по Цельсию.
Рисунок 3 . 2 . 4 . Газовый термометр с постоянным объемом.
Температура кипения газов при давлении
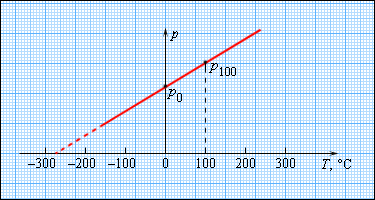
Чтобы произвести калибровку газового термометра, следует выполнить измерение состояния молекул при 0 и 100 градусах. Для этого мы наносим точки p 0 и p 100 на график, после чего проводим прямую линию, как изображено на рисунке 3 . 2 . 5 . Получившийся калибровочный график способен определить температуру с разными значениями давления. При низких температурах возможно нахождение ее «гипотетической». Из опыта видно, что на свойства газа не влияет температура в — 273 , 15 ° С . При понижении температур газ переходит в жидкое или твердое состояние, поэтому получение охлажденного газа невозможно.
Рисунок 3 . 2 . 5 . Зависимость давления газа от температуры при V = c o n s t .
В 1848 году У. Кельвин предлагает использовать точку нулевого давления газа для составления шкалы. Отличие от измерений температуры в Цельсиях в том, что нулевая точка сдвинута на T К = T С + 273 , 15 .
По системе С И температура измеряется по Кельвину и обозначается К . Тогда комнатная температура запишется T С = 20 ° С , а по Кельвину – T К = 293 , 15 К .
Температура кипения газов. Шкала Кельвина
Температурная шкала Кельвина считается абсолютной. Она наиболее приемлема для обозначения физических теорий.
Шкала Кельвина может быть не привязана двумя фиксированными точками, а именно: точка плавления льда и кипения воды с нормальным атмосферным давлением.
Нулевое давление называется абсолютным нулем температуры.
Шкала Кельвина имеет точку, в которой лед, вода и пар будут находиться в тепловом равновесии. Для калибровки других термометров применяют газовые, так как для практики они не подходят в виду своих больших размеров. Отсюда следует, что давление разреженного газа в сосуде постоянного объема V изменяется прямо пропорционально его абсолютной температуре, то есть p
T . Из опыта видно, что неизменный объем V и температура давления T прямо пропорциональны количеству вещества в сосуде к его объему: p
υ V = N N A V = n N A
n , где N принимает обозначение числа молекул в сосуде, а N А – постоянная Авогадро, n = N V – концентрации молекул.
После объединения соотношений получим, что запись примет вид p = n k T , где k считается универсальной постоянной величиной для всех газов, иначе говоря, постоянная Больцмана. Этот ученый являлся одним из создателей опытного обоснования основных положений молекулярно-кинетической теории. Ее обозначение в системе С И k = 1 , 38 ċ 10 – 23 Д ж / К .
При сравнении соотношения p = n k T с уравнением МКТ газов, получим E K → .
Средняя кинетическая энергия беспорядочного движения молекул газа прямо пропорциональна абсолютной температуре.
Температура является мерой для кинетической энергии молекул, которая не зависит от ее величины. Броуновская частица из жидкости и газа обладает аналогичной средней кинетической энергией, как и другая отдельная молекула. Это суждение верно для разномассовых молекул, находящихся в одном сосуде. Состояние равновесия говорит о том, что на них действуют одинаковые средние кинетические энергии, которые определяются температурой смеси. Запись давления смеси газов запишется как сумма парциальных давлений каждого из них: p = p 1 + p 2 + p 3 + … = ( n 1 + n 2 + n 3 + … ) k T .
Отсюда видно, что n 1 , n 2 , n 3 , … является концентрацией молекул газов в смеси. Выражение относят к молекулярно-кинетической теории, установленной Дальтоном: давление в смеси химически невзаимодействующих газов равняется сумме их парциальных давлений.
Основное уравнение молекулярно-кинетической теории (Ерюткин Е.С.)
Этот видеоурок доступен по абонементу
У вас уже есть абонемент? Войти
Как уже было сказано ранее, начиная с этого урока, мы приступаем к изучению только газов. На прошлом уроке мы дали представление о способах количественного описания некой порции вещества. Сейчас же мы начнём описывать газ со стороны его качественных характеристик (микро- и макропараметров). Мы сформулируем понятие об идеальном газе, опишем его параметры и введём соотношение, связывающее эти параметры (основное уравнение МКТ).
Идеальный газ. Температура. Основное уравнение молекулярно — кинетической теории.
Понятие идеального газа как физической идеализации.
Из трех агрегатных состояний, в которых может находиться вещество, наиболее простым для изучения является газообразное. Поэтому изучение свойств веществ мы начинаем именно с свойств газов. В разреженного газа расстояние между молекулами во много раз превышает их размеры. В этом случае взаимодействие между молекулами очень мала и кинетическая энергия движения молекул значительно превышает потенциальную энергию их взаимодействия. Молекулы газа можно рассматривать как маленькие твердые шарики. Вместо реального газа мы будем рассматривать его физическую модель, пренебрегая сложными силами взаимодействия между молекулами и облегчая тем самым изучения свойств газов. Эта модель называется идеальным газом.
Идеальный газ — это газ, взаимодействием между молекулами в котором можно пренебречь.
Газ можно считать идеальным, если:
- отсутствуют силы межмолекулярного взаимодействия, то есть молекулы НЕ привлекаются и не отталкиваются;
- взаимодействие между молекулами происходит только во время их ударяння и является упругой;
- молекулы газа не имеют объема и считаются материальными точками.
Следует помнить, что в физической модели учитывают те свойства реальной системы, учет которых необходимо для объяснения закономерностей поведения системы, исследуются.
Условия, при которых реальные газы можно считать идеальными
Газами, свойства которых близки к свойствам идеального газа, реальные газы, находящиеся под низким давлением имеют высокую температуру. Например, воздух при нормальных условиях (105 Па и 0 ° С) можно приближенно считать идеальным газом.
Вопросы на которые стоит ответить самому себе:
- Почему газы при высокой температуре можно считать идеальными? (Чем выше температура газа, тем больше вследствие теплового движения молекул расстояние между ними по сравнению с размерами, а следовательно, газ ближе к идеальному.
- Почему при высоком давлении свойства реальных газов отличаются от свойств идеального? (При высоком давлении молекулы газов размещаются на расстояниях, которые примерно равны диаметрам самих молекул: для этого их уже нельзя считать материальными точками, следовательно, такой газ нельзя считать идеален.)
Тепловое равновесие и температура как термодинамический параметр идеального газа.
Состояние газа описывают с помощью определенных величин, называют параметрами состояния. различают:
- микропараметры, то есть характеристики собственно молекул — размеры, массу, скорость, импульс, энергию;
- макропараметры, то есть параметры газа как физического тела в целом, — температура, давление, объем.
Со словом «температура» вы знакомы с раннего детства. Теперь ознакомимся с температурой как параметром.
Следовательно, температура характеризует состояние теплового равновесия: все тела находятся в тепловом равновесии, имеют одинаковую температуру.
Тепловое равновесие — это состояние, при котором все макроскопические параметры остаются сколь угодно долго неизменными. Состояние теплового равновесия определяется для изолированной системы, то есть только для тел, которые взаимодействуют только между собой и не взаимодействуют с другими телами.
Следовательно, температура характеризует внутреннее состояние изолированной системы тел, находящихся в состоянии теплового равновесия. Чем быстрее движутся молекулы в теле, тем сильнее есть ощущение тепла во время соприкосновения с ним. Большая скорость движения молекул соответствует большей кинетической энергии. Согласно по величине температуры можно составить представление о кинетической энергии молекул.
Во всех частях системы, находящейся в тепловом равновесии, температура одинакова.
В молекулярно-кинетической теории температура —
это величина, обусловленная средней кинетической энергией частиц, из которых состоит система:
де 
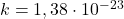
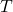
Температура — это мера кинетической энергии теплового движения молекул.
Температура является скалярной величиной, в СИ измеряется в градусах Кельвина.
Основное уравнение молекулярно-кинетической теории (МКТ) выражет зависимость давление газа (

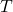
Закон Авогадро: в равных объемах газа при одинаковой температуре и давлении содержится одинаковое количество молекул:
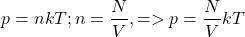
Концентрация (
http://interneturok.ru/lesson/physics/10-klass/osnovy-molekulyarno-kineticheskoy-teorii/osnovnoe-uravnenie-molekulyarno-kineticheskoy-teorii-2
http://repetitor.org.ua/idealnyiy-gaz-temperatura-osnovnoe-uravnenie-molekulyarno-kineticheskoy-teorii