Нитраты: разложение и свойства
Соли азотной кислоты — нитраты
Нитраты металлов — это твердые кристаллические вещества. Большинство очень хорошо растворимы в воде.
1. Нитраты термически неустойчивы , причем все они разлагаются на кислород и соединение, характер которого зависит от положения металла (входящего в состав соли) в ряду напряжений металлов:
- Нитраты щелочных и щелочноземельных металлов ( до Mg в электрохимическом ряду ) разлагаются до нитрита и кислорода.
Например , разложение нитрата натрия:
Исключение – литий .
Видеоопыт разложения нитрата калия можно посмотреть здесь.
- Нитраты тяжелых металлов ( от Mg до Cu, включая магний и медь ) и литий разлагаются до оксида металла, оксида азота (IV) и кислорода:
Например , разложение нитрата меди (II):
- Нитраты малоактивных металлов ( правее Cu ) – разлагаются до металла, оксида азота (IV) и кислорода.
Например , нитрат серебра:
Исключения:
Нитрат железа (II) разлагается до оксида железа (III):
Нитрат марганца (II) разлагается до оксида марганца (IV):
2. Водные растворы не обладают окислительно-восстановительными свойствами, расплавы – сильные окислители .
Например , смесь 75% KNO3, 15% C и 10% S называют «черным порохом»:
Нитрат железа (II)
| Нитрат железа (II) | |
|---|---|
 | |
| Систематическое наименование | Нитрат железа (II) |
| Хим. формула | FeN2O6 |
| Рац. формула | Fe(NO3)2 |
| Состояние | твёрдое |
| Молярная масса | |
| Температура | |
| • плавления | (гексагидрат) 60,5°C |
| Рег. номер CAS | 14013-86-6 |
| PubChem | 9815404 |
| SMILES | |
| RTECS | NO7175000 |
| ChemSpider | 7991154 и 32867051 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Нитрат железа (II) — соль азотной кислоты и двухвалентного железа.
Содержание
Физические свойства
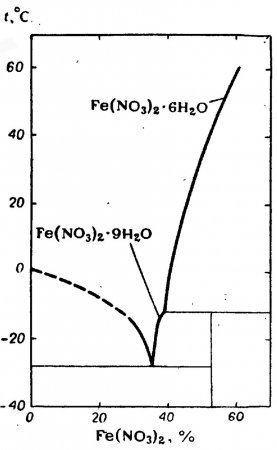
Нитрат железа (II) существует в основном в виде кристаллогидратов Fe(NO3)2·6H2O и Fe(NO3)2·9H2O.
Гексагидрат нитрата железа (II) Fe(NO3)2·6H2O — светло-зелёные кристаллы с ромбической кристаллической решеткой. Хорошо растворяется в воде, причем растворимость растёт вместе с повышением температуры. В равновесии с насыщенным водным раствором существует в интервале от -12 до 60,5 °C и концентрации раствора в пределах 39-69,5%. При более низких температурах и концентрациях растворов устойчив нонагидрат нитрата железа (II) Fe(NO3)2·9H2O.
График растворимости представлен на рисунке.
| Состояние | Температура, °С | Концентрация, % |
| Лед+Fe(NO3)2·9H2O | -28 | (35) |
| Fe(NO3)2·9H2O+Fe(NO3)2·6H2O | (39) | |
| Fe(NO3)2·6H2O | 60,5 | 62,5 |
Безводный нитрат железа (II) и его кристаллогидраты неустойчивы, поэтому легко окисляются на воздухе.
Получение
Нитрат железа (II) образуется при растворении железа в разбавленной азотной кислоте на холоде:
В чистом состоянии его лучше получать обменной реакцией сульфата железа (II) с нитратом свинца (II):
Химические свойства
Проявляет восстановительные свойства. Гидролиз практически не проявляется.
- Водный раствор нитрата железа (II) разлагается при кипячении с образованием основного нитрата железа (III):
4 Fe(NO3)2 + O2 + 2H2O → t 4Fe(OH)(NO3)2
- Реагирует с щелочами с образованием гидроксида железа (II):
Fe(NO3)2 + 2NaOH → Fe(OH)2↓ + 2NaNO3
- С растворимыми карбонатами дает белый карбонат железа (II):
Fe(NO3)2 + K2CO3 → FeCO3↓ + 2KNO3
- Восстанавливается до металлического железа при действии более активного металла
Fe(NO3)2 + Mg → Fe + Mg(NO3)2
- Взаимодействует с гексацианоферратом (III) калия (красной кровяной солью) с образованием тёмно-синего осадка гексацианоферрата (II) железа (III)-калия (берлинская лазурь):
Fe(NO3)2 + K3[Fe(CN)6] → KFe[Fe(CN)6]↓ + 2KNO3
- При термическом разложении образуется оксид железа (III), а не оксид железа (II):
4 Fe(NO3)2 → t 2Fe2O3 + 8NO2↑ + O2↑
Реакция термического разложения гексагидрата нитрата железа (II)
Реакция термического разложения гексагидрата нитрата железа (II)
Уравнение реакции термического разложения гексагидрата нитрата железа (II):
Реакция термического разложения гексагидрата нитрата железа (II).
В результате реакции образуются оксид железа (III), оксид азота (IV), кислород и вода.
Реакция протекает при условии: при температуре 600-700 °C.
Формула поиска по сайту: 4[Fe(NO3)2·6H2O] → 2Fe2O3 + 8NO2 + O2 + 24H2O.
Реакция взаимодействия скандия и хлороводорода
Реакция взаимодействия вольфрама и кислорода
Реакция взаимодействия оксида лития и воды
Выбрать язык
Популярные записи
Предупреждение.
Все химические реакции и вся информация на сайте предназначены для использования исключительно в учебных целях — только для решения письменных, учебных задач. Мы не несем ответственность за проведение вами химических реакций.
Химические реакции и информация на сайте
не предназначены для проведения химических и лабораторных опытов и работ.
http://chem.ru/nitrat-zheleza-ii.html
http://chemicalstudy.ru/reaktsiya-termicheskogo-razlozheniya-geksagidrata-nitrata-zheleza-ii/