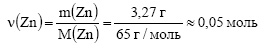При сгорании 3,27 г цинка выделилось 174 кДж. Вычислите теплоту образования оксида цинка (тепловой эффект).
Решение:
Молярная масса цинка равна 65 г/моль. Вычислим количество вещества цинка:
По уравнению реакции из 2 моль цинка образуется 2 моль оксида цинка, значит из 0,05 моль цинка образуется 0,05 моль оксида цинка. Теплотой образования называется количество теплоты, выделяющееся при образовании 1 моль вещества. При образовании 0,05 моль выделилось 174 кДж тепла. Пусть при образовании 1 моль выделится х кДж тепла. Составим пропорцию:
Ответ: теплота образования оксида цинка равна 3480 кДж.

задача №1
к главе «Глава IV. Химические реакции».
Please wait.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 6e31b1650cda6b39 • Your IP : 85.95.188.35 • Performance & security by Cloudflare
При сжигании 13 г цинка выделилось 69, 6 кДж теплоты, Составьте термохимические уравнение этой реакции,?
Химия | 10 — 11 классы
При сжигании 13 г цинка выделилось 69, 6 кДж теплоты, Составьте термохимические уравнение этой реакции,.
Zn(к) + О2(г) = ZnO(к) + 69.
При сжигании 11 г ацетальдегида выделилось 298, 11 кДж теплоты?
При сжигании 11 г ацетальдегида выделилось 298, 11 кДж теплоты.
Составьте термохимическое уравнение этой реакции.
При сгорании 32г метана CH4 выделилось 1604 кДж Теплоты?
При сгорании 32г метана CH4 выделилось 1604 кДж Теплоты.
Составьте термохимическое уравнение реакции горения метана.
При сжигании 6, 5 г цинка выделилась теплота, равная 34?
При сжигании 6, 5 г цинка выделилась теплота, равная 34.
Составьте термохимическое уравнение этой реакции.
При сжигании 6, 08 г магния выделилось 152, 5 кДж тепла?
При сжигании 6, 08 г магния выделилось 152, 5 кДж тепла.
Составьте термохимическое уравнение этой реакции.
При сгорании 8г кальция выделилось 127 кДж теплоты?
При сгорании 8г кальция выделилось 127 кДж теплоты.
Составьте термохимическое уравнение реакции.
При сжигании 2 моль фосфора выделяется 1504 кдж теплоты?
При сжигании 2 моль фосфора выделяется 1504 кдж теплоты.
Составьте термохимическое уравнение реакции горения фосфора.
При сжигании 62 г фосфора выделилось 1504 КДж теплоты?
При сжигании 62 г фосфора выделилось 1504 КДж теплоты.
Составьте термохимическое уравнение реакции горения фосфора.
При сжигание 5, 6 л угарного газа выделилось 70, 5 кДЖ теплоты?
При сжигание 5, 6 л угарного газа выделилось 70, 5 кДЖ теплоты.
Вычислите тепловой эффект реакции горения угарного газа и составьте термохимическое уравнение это реакции.
При сжигании 6г этанола выделяется 95, 58 кДж?
При сжигании 6г этанола выделяется 95, 58 кДж.
Составьте термохимическое уравнение реакции.
НУ ПОМОГИТЕ ПОЖАЛУЙСТА?
НУ ПОМОГИТЕ ПОЖАЛУЙСТА!
«! При сжигании 1, 3г цинка в кислороде выделилось 7, 96 кдж теплоты.
Вычеслите тепловой эффект и напишите термохимическое уравнение реакции горения цинка.
Вы находитесь на странице вопроса При сжигании 13 г цинка выделилось 69, 6 кДж теплоты, Составьте термохимические уравнение этой реакции,? из категории Химия. Уровень сложности вопроса рассчитан на учащихся 10 — 11 классов. На странице можно узнать правильный ответ, сверить его со своим вариантом и обсудить возможные версии с другими пользователями сайта посредством обратной связи. Если ответ вызывает сомнения или покажется вам неполным, для проверки найдите ответы на аналогичные вопросы по теме в этой же категории, или создайте новый вопрос, используя ключевые слова: введите вопрос в поисковую строку, нажав кнопку в верхней части страницы.
А но это не точно : ))).
Ответ Ca3 (PO4)2 = 15, 5 г.
Массовая доля Cl (смотрим цифры с запятыми в таблице) = 35. 5 у O = 16 (для хлора всегда берут 35. 5, а для остальных элементов округляют до целых чисел) Затем мы все это складываем Cl2O3 = (35. 5 * 2) + (16 * 3) = 71 + 48 = 119.
Алмаз 1 2 3 4 Л а м а Зонт»’ 2 1 3 4 А л м а з.
Гомолог : C4H6 Изомер : CH2 = C = CH2 (межклассовая ), (пропадиен).
Если 14, 3% — водород, то 100% — 14, 3% = 85, 7% — углерод. Пусть m = 100г Следовательно m(H) = 14. 3г, m(C) = 85, 7г M(H) = 1г / моль, M(C) = 12г / моль n = m / M n(H) = 14, 3 моль, n(C) = 7, 1 моль n(H) : n(C) = 14, 3 : 7. 1 = 2 : 1 Т. Е. форму..
С — просто «це». Хим. элемент — углерод. Fe3O4 — «феррум» три «о» четыре. Хим. элементы : железо, кислород. Na2CO3 — «натрий» два «це» «о» три. Хим. элементы : натрий, углерод, кислород. KNO3 — «калий» «н» «о» три. Хим. элементы : калий, азот.
А) Mg + 2HCl — > MgCl2 + H2 (ОВР) так как изменяется степень окисления Mg(0) + 2H( + )Cl( — ) — > Mg( + 2)Cl2( — ) + H2(0) b) S + O2 — > SO2 (ОВР) S(0) + O2(0) — > S( + 4)O( — 2) c) 2Li + H2 — > 2LiH (ОВР) 2Li(0) + H2(0) — > 2Li( + )H( — ) d) 2H3PO4 ..
2Zn + O₂ = 2ZnO (X1) ZnO + H₂SO₄ = ZnSO₄ + H₂O ZnSO₄ + 2KOH = K₂SO₄ + Zn(OH)₂ (X2) Zn(OH)₂ + 2KOH (t) = K₂ZnO₂ + 2H₂O K₂ZnO₂ + 4HCl = 2KCl(p — p) + ZnCl₂(p — p) + 2H₂O ZnCl₂ + Na₂CO₃ = 2NaCl + ZnCO₃↓ (отфильтровать) KCl + Na₂CO₃≠ ZnCO₃↓ + 2HCl = ZnCl..
Физические : превращение воды в лёд — важно, например, для обитателей водоемов, превращение в пар — круговорот воды в природе. Плавление металлов — изготовление посуды, ювелирных изделий, в конце концов оловянных солдатиков. Химические : гашение из..
http://gomolog.ru/reshebniki/11-klass/rudzitis-i-feldman-2019/12/zadanie-9.html
http://himia.my-dict.ru/q/1897225_pri-sziganii-13-g-cinka-vydelilos/