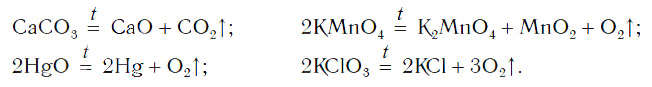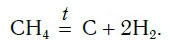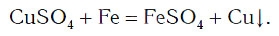Урок 13. Типы химических реакций
В уроке 13 «Типы химических реакций» из курса «Химия для чайников» мы узнаем о типах химических реакций; подробно рассмотрим каждый тип и научимся их различать.
Мир химических реакций весьма разнообразен. Самые различные химические реакции постоянно происходят в природе, осуществляются человеком. Можно ли классифицировать химические реакции? Что положить в основу их классификации? Сущность всякой химической реакции состоит в превращении веществ: разрушаются исходные вещества и образуются продукты реакций, меняется число и состав исходных веществ и продуктов реакции. Характер этих изменений и положен в основу классификации химических реакций.
Реакции соединения
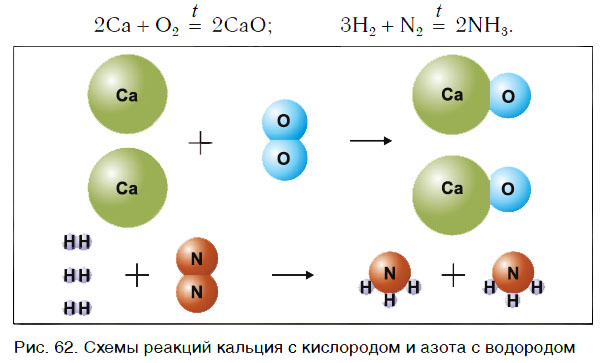
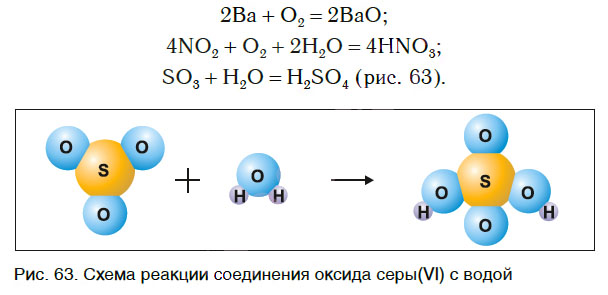
Рассмотрим уравнения следующих реакций (рис. 62):
Чем сходны данные реакции между собой? Тем, что в результате взаимодействия двух веществ получается только одно вещество. Такие реакции получили название реакций соединения.
Реакции соединения — это реакции, в результате которых из двух или нескольких веществ образуется одно новое сложное вещество.
В одних случаях из двух простых веществ получается одно сложное, в других — соединяются два и более простых или сложных веществ:
Реакции разложения
Рассмотрим уравнения следующих реакций:
Можно заметить, что из одного сложного вещества получается два или более новых веществ. Это реакции разложения. В них могут образовываться как простые, так и сложные вещества.
Реакции разложения — это реакции, в результате которых из одного сложного вещества образуется несколько новых веществ.
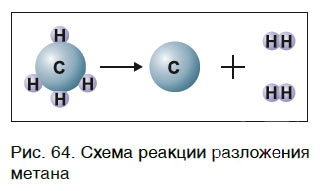
Для начала реакции разложения обычно необходимо нагреть исходные вещества. Например, негашеную известь CaO в промышленности получают нагреванием известняка CaCO3, реакция разложения происходит при температуре около 1000 °С. К такому типу реакций относится и реакция разложения метана CH4 (рис. 64) — составной части природного газа:
Реакции замещения
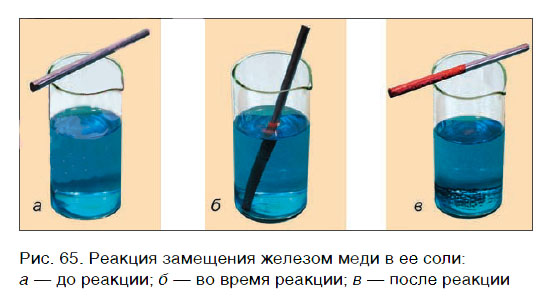
А могут ли взаимодействовать между собой два вещества: одно простое и одно сложное? Проверим это на опыте. В раствор медного купороса опустим небольшой кусочек железа — кнопку, гвоздь, канцелярскую скрепку с хорошо очищенной поверхностью. Через 2—3 мин извлечем железо из раствора и увидим, что на его поверхности образовался темно-красный налет меди. В химическую реакцию вступили простое (Fe) и сложное (CuSO4) вещества, и образовались новое простое (Cu) и новое сложное (FeSO4) вещества:
Из опыта и уравнения химической реакции хорошо видно, что атомы железа заместили атомы меди в сложном веществе (рис. 65). Такие химические реакции относятся к реакциям замещения.
Реакции замещения — это реакции, в результате которых атомы простого вещества замещают атомы одного из элементов в сложном веществе.
Для протекания таких реакций необходимо соблюдать некоторые особые условия. Не все простые вещества обязательно должны взаимодействовать со сложными веществами. В дальнейшем при изучении химии вы познакомитесь с этими условиями, а также с другими типами химических реакций.
Краткие выводы урока:
- Реакции соединения — это реакции, в результате которых из двух или нескольких веществ образуется одно новое сложное вещество.
- Реакции разложения — это реакции, в результате которых из одного сложного вещества образуется несколько новых веществ.
- Реакции замещения — это реакции, в которых атомы простого вещества замещают атомы одного из элементов в сложном веществе.
Надеюсь урок 13 «Типы химических реакций» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии. Если вопросов нет, то переходите к следующему уроку.
Урок 8 Бесплатно Химическая реакция- уравнение и типы
Начало
Продолжим изучение химической реакции как одной из основ химической науки.
Ведь полноценное понимание этой темы нужно для дальнейшего изучения химии, и в то же время это сделает вас образованнее не только в научном плане, но и в бытовом!
Уравнение химической реакции
Вся информация о протекающей химической реакции (исходные вещества, продукты реакции, условия протекания, тепловой эффект) на письме фиксируется в виде уравнения реакции.
Уравнение можно записать для любой реакции. Для этого нужно знать состав молекул исходных веществ и продуктов.
Всё это записывается в виде химических формул.
Всё происходит как в математике: в левой части записываются формулы исходных веществ, а в правой – формулы продуктов.
Только вместо знака «равно» чаще всего ставят стрелку: она показывает, что реакция идёт именно в этом направлении.
У меня есть дополнительная информация к этой части урока!
В некоторых случаях возможно протекание реакции при одних и тех же условиях в обоих направлениях. В таком случае обычно ставят две стрелки в обе стороны, но также и допустимо ставить знак «равно».
В некоторых случаях (когда это требуется) указывают условия протекания реакции и тепловой эффект реакции.
Условия протекания записывают над стрелкой, а тепловой эффект – в виде количества теплоты в левой части, если реакция эндотермическая, и в правой части, если экзотермическая.
Для примера запишем уравнение реакции водорода с кислородом:
Зигзаг обозначает искру – условие для начала реакции, а «+ Q» – то, что в результате реакции выделяется энергия.
В зависимости от конкретных задач условия протекания и тепловой эффект могут вообще не отмечать или отмечать конкретное числовое значение теплового эффекта.
Если среди продуктов реакции есть газ, около его формулы пишут стрелку вверх.
Например, когда мы капаем на рану перекись водорода, под действием ферментов крови она разлагается с выделением кислорода:
У меня есть дополнительная информация к этой части урока!
Кислород обладает обеззараживающим действием и способствует более быстрой свёртываемости крови!
Перекись водорода может разлагаться не только под воздействием ферментов крови, но и многих других веществ.
Разложение перекиси водорода в присутствии оксида марганца (IV) (Оксид марганца (IV) в химической реакции не участвует).
Если реакция идет в растворе и в результате выпадает осадок, то пишут стрелку вниз.
Садовые деревья весной обрабатывают от паразитов «бордосской жидкостью». Чтобы её приготовить, смешивают растворы извести и медного купороса.
При этом наблюдается выпадение хлопьев, которые состоят сразу из двух нерастворимых веществ: гидроксида меди и сульфата кальция.
Получившийся сульфат кальция, гипс, образует корку, которая будет дольше держаться на стволе дерева, и поэтому такая смесь дольше защищает его от вредителей.
Запишем уравнение этой реакции
Как правильно читать уравнение химической реакции?
В химии принято делать это примерно так: «один моль сульфата меди реагирует с одним молем гидроксида кальция с образованием одного моля гидроксида меди и одного моля сульфата кальция».
То есть коэффициент перед формулой вещества считают количеством вещества в молях, а не количеством молекул.
Ведь в реальной жизни мы наблюдаем реакцию не единичных молекул, а большого объема веществ.
При составлении уравнений химики опираются на два основных закона природы: закона сохранения массы и закона постоянства состава веществ.
Пройти тест и получить оценку можно после входа или регистрации
Уравнения химических реакций

Средняя оценка: 4.3
Всего получено оценок: 982.
Средняя оценка: 4.3
Всего получено оценок: 982.
Запись химического взаимодействия, отражающая количественную и качественную информацию о реакции, называют уравнением химических реакций. Записывается реакция химическими и математическими символами.
Основные правила
Химические реакции предполагают превращение одних веществ (реагентов) в другие (продукты реакции). Это происходит благодаря взаимодействию внешних электронных оболочек веществ. В результате из начальных соединений образуются новые.
Чтобы выразить ход химической реакции графически, используются определённые правила составления и написания химических уравнений.
В левой части пишутся изначальные вещества, которые взаимодействуют между собой, т.е. суммируются. При разложении одного вещества записывается его формула. В правой части записываются полученные в ходе химической реакции вещества. Примеры записанных уравнений с условными обозначениями:
- CuSO4 + 2NaOH → Cu(OH)2↓+ Na2SO4;
- CaCO3 = CaO + CO2↑;
- 2Na2O2 + 2CO2 → 2Na2CO3 + O2↑;
- CH3COONa + H2SO4(конц.) → CH3COOH + NaHSO4;
- 2NaOH + Si + H2O → Na2SiO3 + H2↑.
Коэффициенты перед химическими формулами показывают количество молекул вещества. Единица не ставится, но подразумевается. Например, уравнение Ba + 2H2O → Ba(OH)2 + H2 показывает, что из одной молекулы бария и двух молекул воды получается по одной молекуле гидроксида бария и водорода. Если пересчитать количество водорода, то и справа, и слева получится четыре атома.
Обозначения
Для составления уравнений химических реакций необходимо знать определённые обозначения, показывающие, как протекает реакция. В химических уравнениях используются следующие знаки:
- → – необратимая, прямая реакция (идёт в одну сторону);
- ⇄ или ↔ – реакция обратима (протекает в обе стороны);
- ↑ – выделяется газ;
- ↓ – выпадает осадок;
- hν – освещение;
- t° – температура (может указываться количество градусов);
- Q – тепло;
- Е(тв.) – твёрдое вещество;
- Е(газ) или Е(г) – газообразное вещество;
- Е(конц.) – концентрированное вещество;
- Е(водн.) – водный раствор вещества.
Вместо стрелки (→) может ставиться знак равенства (=), показывающий соблюдение закона сохранения вещества: и слева, и справа количество атомов веществ одинаково. При решении уравнений сначала ставится стрелка. После расчёта коэффициентов и уравнения правой и левой части под стрелкой подводят черту.
Условия реакции (температура, освещение) указываются сверху знака протекания реакции (→,⇄). Также сверху подписываются формулы катализаторов.
Какие бывают уравнения
Химические уравнения классифицируются по разным признакам. Основные способы классификации представлены в таблице.
Признак
Реакции
Описание
Пример
По изменению количества реагентов и конечных веществ
Из простого и сложного вещества образуются новые простые и сложные вещества
Несколько веществ образуют новое вещество
Из одного вещества образуется несколько веществ
Обмен составными частями (ионами)
По выделению тепла
По типу энергетического воздействия
Действие электрического тока
Действие высокой температуры
По агрегатному состоянию
Существует понятие химического равновесия, присущее только обратимым реакциям. Это состояние, при котором скорости прямой и обратной реакции, а также концентрации веществ равны. Такое состояние характеризуется константой химического равновесия.
При внешнем воздействии температуры, давления, света реакция может смещаться в сторону уменьшения или увеличения концентрации определённого вещества. Зависимость константы равновесия от температуры выражается с помощью уравнений изобары и изохоры. Уравнение изотермы отражает зависимость энергии и константы равновесия. Эти уравнения показывают направление протекания реакции.

Что мы узнали?
В уроке химии 8 класса была рассмотрена тема уравнений химических реакций. Составление и написание уравнений отражает ход химической реакции. Существуют определённые обозначения, показывающие состояние веществ и условия протекания реакции. Выделяют несколько видов химических реакций по разным признакам: по количеству вещества, агрегатному состоянию, поглощению энергии, энергетическому воздействию.
http://ladle.ru/education/himia/8class/himicheskaya-reakciya15
http://obrazovaka.ru/himiya/uravneniya-himicheskih-reakciy-8-klass.html