Полисахариды. Крахмал и целлюлоза
Крахмал
1. Физические свойства
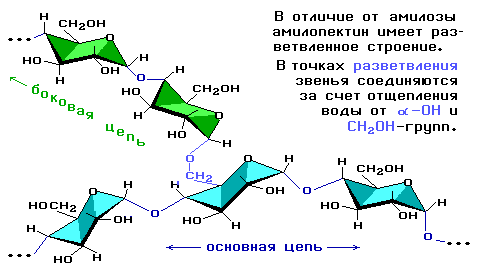
Это белый порошок, нерастворимый в холодной воде и образующий коллоидный раствор (крахмальный клейстер) в горячей воде. Существует в двух формах: амилоза – линейный полимер, растворимый в горячей воде, амилопектин – разветвлённый полимер, не растворимый в воде, лишь набухает.
2. Нахождение в природе
Крахмал – основной источник резервной энергии в растительных клетках – образуется в растениях в процессе фотосинтеза и накапливается в клубнях, корнях, семенах:
Содержится в клубнях картофеля, зёрнах пшеницы, риса, кукурузы.
Гликоген (животный крахмал), образуется в печени и мышцах животных.
Состоит из остатков α — глюкозы.
В состав крахмала входят:
· амилоза (внутренняя часть крахмального зерна) – 10-20%
· амилопектин (оболочка крахмального зерна) – 80-90%
Цепь амилозы включает 200 – 1000 остатков α-глюкозы и имеет неразветвленное строение.
Амилопектин состоит из разветвленных макромолекул, молекулярная масса которых достигает 1 — 6 млн.
Амилоза и амилопектин гидролизуются под действием кислот или ферментов до глюкозы, которая служит непосредственным источником энергии для клеточных реакций, входит в состав крови и тканей, участвует в обменных процессах. Поэтому крахмал – необходимый резервный углевод питания.
Подобно амилопектину построен гликоген (животный крахмал), макромолекулы которого отличаются большей разветвлённостью:
Крахмал широко применяется в различных отраслях промышленности (пищевой, бродильной, фармацевтической, текстильной, бумажной и т.п.).
· Ценный питательный продукт.
· Для накрахмаливания белья.
· В качестве декстринового клея.
5. Химические свойства полисахаридов
Гидролиз протекает ступенчато:
крахмал декстрины мальтоза глюкоза
Охлаждённый крахмальный клейстер + I 2 (раствор) = синее окрашивание, которое исчезает при нагревании.
Макромолекула амилозы представляет собой спираль, каждый виток которой состоит из 6 звеньев α-глюкозы.
При взаимодействии амилозы с йодом в водном растворе молекулы йода входят во внутренний канал спирали, образуя так называемое соединение включения. Это соединение имеет характерный синий цвет. Данная реакция используется в аналитических целях для обнаружения, как крахмала, так и йода (йодкрахмальная проба)
Целлюлоза
Целлюлоза (клетчатка) – растительный полисахарид, являющийся самым распространенным органическим веществом на Земле.
1. Физические свойства
Это вещество белого цвета, без вкуса и запаха, нерастворимое в воде, имеющее волокнистое строение. Растворяется в аммиачном растворе гидроксида меди ( II ) – реактиве Швейцера.
2. Нахождение в природе
Этот биополимер обладает большой механической прочностью и выполняет роль опорного материала растений, образуя стенку растительных клеток. В большом количестве целлюлоза содержится в тканях древесины (40-55%), в волокнах льна (60-85%) и хлопка (95-98%). Основная составная часть оболочки растительных клеток. Образуется в растениях в процессе фотосинтеза.
Древесина состоит на 50% из целлюлозы, а хлопок и лён, конопля практически чистая целлюлоза.
Хитин (аналог целлюлозы) – основной компонент наружного скелета членистоногих и других беспозвоночных, а также в составе клеточных стенок грибов и бактерий.
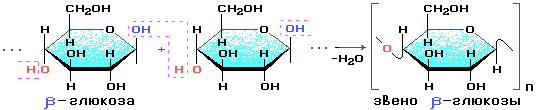
Состоит из остатков β — глюкозы
Получают из древесины
Целлюлоза используется в производстве бумаги, искусственных волокон, пленок, пластмасс, лакокрасочных материалов, бездымного пороха, взрывчатки, твердого ракетного топлива, для получения гидролизного спирта и др.
· Получение ацетатного шёлка – искусственное волокно, оргстекла, негорючей плёнки из ацетилцеллюлозы.
· Получение бездымного пороха из триацетилцеллюлозы (пироксилин).
· Получение коллодия (плотная плёнка для медицины) и целлулоида (изготовление киноленты, игрушек) из диацетилцеллюлозы.
· Изготовление нитей, канатов, бумаги.
· Получение глюкозы, этилового спирта (для получения каучука)
К важнейшим производным целлюлозы относятся:
— метилцеллюлоза (простые метиловые эфиры целлюлозы) общей формулы
— ацетилцеллюлоза (триацетат целлюлозы) – сложный эфир целлюлозы и уксусной кислоты
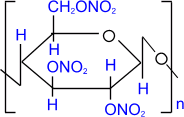
— нитроцеллюлоза (нитраты целлюлозы) – сложные азотнокислые эфиры целлюлозы:
6. Химические свойства
Гидролиз протекает ступенчато :
крахмал декстрины мальтоза глюкоза
Целлюлоза – многоатомный спирт, на элементную ячейку полимера приходятся три гидроксильных группы. В связи с этим, для целлюлозы характерны реакции этерификации (образование сложных эфиров). Наибольшее практическое значение имеют реакции с азотной кислотой и уксусным ангидридом. Целлюлоза не дает реакции «серебряного зеркала».
целлюлоза
тринитрат целлюлозы
Полностью этерифицированная клетчатка известна под названием пироксилин, который после соответствующей обработки превращается в бездымный порох. В зависимости от условий нитрования можно получить динитрат целлюлозы, который в технике называется коллоксилином. Он так же используется при изготовлении пороха и твердых ракетных топлив. Кроме того, на основе коллоксилина изготавливают целлулоид.
2. Взаимодействие с уксусной кислотой:
При взаимодействии целлюлозы с уксусным ангидридом в присутствии уксусной и серной кислот образуется триацетилцеллюлоза.
триацетилцеллюлоза
Триацетилцеллюлоза (или ацетилцеллюлоза) является ценным продуктом для изготовления негорючей кинопленки и ацетатного шелка. Для этого ацетилцеллюлозу растворяют в смеси дихлорметана и этанола и этот раствор продавливают через фильеры в поток теплого воздуха.
Растворитель испаряется и струйки раствора превращаются в тончайшие нити ацетатного шелка.
Говоря о применении целлюлозы, нельзя не сказать о том, что большое количество целлюлозы расходуется для изготовления различной бумаги. Бумага – это тонкий слой волокон клетчатки, проклеенный и спрессованный на специальной бумагоделательной машине.
Углеводы
Теория по теме Углеводы. Краткие конспект по углеводам. Классификация углеводов, химические свойства углеводов, способы получения углеводов. Свойства и получение моносахаридов (глюкоза, фруктоза), олигосахаридов (сахароза и др.), полисахаридов.
| Углеводы (сахара) – органические соединения, имеющие сходное строение, состав большинства которых отражает формула Cx(H2O)y, где x, y ≥ 3. |
Исключение составляет дезоксирибоза, которая имеют формулу С5Н10O4 (на один атом кислорода меньше, чем рибоза).
Классификация углеводов
По числу структурных звеньев
- Моносахариды — содержат одно структурное звено.
- Олигосахариды — содержат от 2 до 10 структурных звеньев (дисахариды, трисахариды и др.).
- Полисахариды — содержат n структурных звеньев.
Некоторые важнейшие углеводы:
| Моносахариды | Дисахариды | Полисахариды |
| Глюкоза С6Н12О6 Дезоксирибоза С5Н10О4 | Сахароза С12Н22О11 Целлобиоза С12Н22О11 | Целлюлоза (С6Н10О5)n Крахмал(С6Н10О5)n |
По числу атомов углерода в молекуле
- Пентозы — содержат 5 атомов углерода.
- Гексозы — содержат 6 атомов углерода.
- И т.д.
По размеру кольца в циклической форме молекулы
- Пиранозы — образуют шестичленное кольцо.
- Фуранозы — содержат пятичленное кольцо.
Химические свойства, общие для всех углеводов
1. Горение
Все углеводы горят до углекислого газа и воды.
| Например, при горении глюкозы образуются вода и углекислый газ |
2. Взаимодействие с концентрированной серной кислотой
Концентрированная серная кислота отнимает воду от углеводов, при этом образуется углерод С («обугливание») и вода.
| Например, при действии концентрированной серной кислоты на глюкозу образуются углерод и вода |
Моносахариды
| Моносахариды – гетерофункциональные соединения, в состав их молекул входит одна карбонильная группа (группа альдегида или кетона) и несколько гидроксильных. |
Моносахариды являются структурными звеньями олигосахаридов и полисахаридов.
Важнейшие моносахариды
| Название и формула | Глюкоза C6H12O6 | Фруктоза C6H12O6 | Рибоза C5H10O5 |
| Структурная формула |  |  |  |
| Классификация |
|
|
|
Глюкоза
Глюкоза – это альдегидоспирт (альдоза).
Она содержит шесть атомов углерода, одну альдегидную и пять гидроксогрупп.
Глюкоза существует в растворах не только в виде линейной, но и циклических формах (альфа и бета), которые являются пиранозными (содержат шесть звеньев):
| α-глюкоза | β-глюкоза |
 |  |
Химические свойства глюкозы
Водный раствор глюкозы
В водном растворе глюкозы существует динамическое равновесие между двумя циклическими формами — α и β и линейной формой:
Качественная реакция на многоатомные спирты: реакция со свежеосажденным гидроксидом меди (II)
При взаимодействии свежеосажденного гидроксида меди (II) с глюкозой (и другими моносахаридами происходит растворение гидроксида с образованием комплекса синего цвета.
Реакции на карбонильную группу — CH=O
Глюкоза проявляет свойства, характерные для альдегидов.
- Реакция «серебряного зеркала»
- Реакция с гидроксидом меди (II) при нагревании. При взаимодействии глюкозы с гидроксидом меди (II) выпадает красно-кирпичный осадок оксида меди (I):
- Окисление бромной водой. При окислении глюкозы бромной водой образуется глюконовая кислота:
- Также глюкозу можно окислить хлором, бертолетовой солью, азотной кислотой.
| Концентрированная азотная кислота окисляет не только альдегидную группу, но и гидроксогруппу на другом конце углеродной цепи. |
- Каталитическое гидрирование. При взаимодействии глюкозы с водородом происходит восстановление карбонильной группы до спиртового гидроксила, образуется шестиатомный спирт – сорбит:
- Брожение глюкозы. Брожение — это биохимический процесс, основанный на окислительно-восстановительных превращениях органических соединений в анаэробных условиях.
Спиртовое брожение. При спиртовом брожении глюкозы образуются спирт и углекислый газ:
Молочнокислое брожение. При молочнокислом брожении глюкозы образуется молочная кислота:
Маслянокислое брожение. При маслянокислом брожении глюкозы образуется масляная кислота (внезапно):
- Образование эфиров глюкозы (характерно для циклической формы глюкозы).
Глюкоза способна образовывать простые и сложные эфиры.
Наиболее легко происходит замещение полуацетального (гликозидного) гидроксила.
Например, α-D-глюкоза взаимодействует с метанолом.
При этом образуется монометиловый эфир глюкозы (α-O-метил-D-глюкозид):
| Простые эфиры глюкозы получили название гликозидов. |
В более жестких условиях (например, с CH3-I) возможно алкилирование и по другим оставшимся гидроксильным группам.
Моносахариды способны образовывать сложные эфиры как с минеральными, так и с карбоновыми кислотами.
| Например, β-D-глюкоза реагирует с уксусным ангидридом в соотношении 1:5 с образованием пентаацетата глюкозы (β-пентаацетил-D-глюкозы): |
Получение глюкозы
Гидролиз крахмала
В присутствии кислот крахмал гидролизуется:
Синтез из формальдегида
Реакция была впервые изучена А.М. Бутлеровым. Синтез проходит в присутствии гидроксида кальция:
Фотосинтез
В растениях углеводы образуются в результате реакции фотосинтеза из CO2 и Н2О:
Фруктоза
| Фруктоза — структурный изомер глюкозы. Это кетоноспирт (кетоза): она тоже может существовать в циклических формах (фуранозы). |
Она содержит шесть атомов углерода, одну кетоновую группу и пять гидроксогрупп.
| Фруктоза | α-D-фруктоза | β-D-фруктоза |
 |  |  |
Фруктоза – кристаллическое вещество, хорошо растворимое в воде, более сладкое, чем глюкоза.
В свободном виде содержится в мёде и фруктах.
Химические свойства фруктозы связаны с наличием кетонной и пяти гидроксильных групп.
При гидрировании фруктозы также получается сорбит.
Дисахариды
| Дисахариды – это углеводы, молекулы которых состоят из двух остатков моносахаридов, соединенных друг с другом за счет взаимодействия гидроксильных групп (двух полуацетальных или одной полуацетальной и одной спиртовой). |
Сахароза (свекловичный или тростниковый сахар) С12Н22О11
Молекула сахарозы состоит из остатков α-глюкозы и β-фруктозы, соединенных друг с другом:
В молекуле сахарозы гликозидный атом углерода глюкозы связан из-за образования кислородного мостика с фруктозой, поэтому сахароза не образует открытую (альдегидную) форму.
| Поэтому сахароза не вступает в реакции альдегидной группы – с аммиачным раствором оксида серебра с гидроксидом меди при нагревании. Такие дисахариды называют невосстанавливающими, т.е. не способными окисляться. |
Сахароза подвергается гидролизу подкисленной водой. При этом образуются глюкоза и фруктоза:
Мальтоза С12Н22О11
Это дисахарид, состоящий из двух остатков α-глюкозы, она является промежуточным веществом при гидролизе крахмала.
| Мальтоза является восстанавливающим дисахаридом (одно из циклических звеньев может раскрываться в альдегидную группу) и вступает в реакции, характерные для альдегидов. |
При гидролизе мальтозы образуется глюкоза.
Полисахариды
| Полисахариды — это природные высокомолекулярные углеводы, макромолекулы которых состоят из остатков моносахаридов. |
Основные представители — крахмал и целлюлоза — построены из остатков одного моносахарида — глюкозы.
Крахмал и целлюлоза имеют одинаковую молекулярную формулу: (C6H10O5)n, но совершенно различные свойства.
Это объясняется особенностями их пространственного строения.
Крахмал состоит из остатков α-глюкозы, а целлюлоза – из β-глюкозы, которые являются пространственными изомерами и отличаются лишь положением одной гидроксильной группы:
Крахмал
Крахмалом называется полисахарид, построенный из остатков циклической α-глюкозы.
В его состав входят:
- амилоза (внутренняя часть крахмального зерна) – 10-20%
- амилопектин (оболочка крахмального зерна) – 80-90%
Цепь амилозы включает 200 — 1000 остатков α-глюкозы (средняя молекулярная масса 160 000) и имеет неразветвленное строение.
Амилопектин имеет разветвленное строение и гораздо большую молекулярную массу, чем амилоза.
Свойства крахмала
- Гидролиз крахмала: при кипячении в кислой среде крахмал последовательно гидролизуется:
- Крахмал не дает реакцию “серебряного зеркала” и не восстанавливает гидроксид меди (II).
- Качественная реакция на крахмал: синее окрашивание с раствором йода.
Целлюлоза
Целлюлоза (клетчатка) – наиболее распространенный растительный полисахарид. Цепи целлюлозы построены из остатков β-глюкозы и имеют линейное строение.
Свойства целлюлозы
- Образование сложных эфиров с азотной и уксусной кислотами.
Нитрование целлюлозы.
Так как в звене целлюлозы содержится 3 гидроксильные группы, то при нитровании целлюлозы избытком азотной кислоты возможно образование тринитрата целлюлозы, взрывчатого вещества пироксилина:
Ацилирование целлюлозы.
При действии на целлюлозу уксусного ангидрида (упрощённо-уксусной кислоты) происходит реакция этерификации, при этом возможно участие в реакции 1, 2 и 3 групп ОН.
Получается ацетат целлюлозы – ацетатное волокно.
- Гидролиз целлюлозы.
Целлюлоза, подобно крахмалу, в кислой среде может гидролизоваться, в результате тоже получается глюкоза. Но процесс идёт гораздо труднее.
Урок химии по теме «Полисахариды». 10-й класс
Разделы: Химия
Класс: 10
Цели урока. Рассмотреть важнейшие полисахариды: крахмал и целлюлозу в сравнении их строения, свойств, применения и значения в природе.
Оборудование: медиапроектор, экран, ПК; крахмал и крахмальный клейстер, йодная настойка, пипетка, пробирки. У учащихся на каждой парте: вата, лупа, держатель, спички, пипетка, йодная настойка.
1. Организационный момент.
2. Проверка домашнего задания.
2.1 Что такое углеводы?
2.2 Что такое моносахариды? Приведите примеры.
2.3 Назовите формулу глюкозы.
2.4 Какие вещества относят к дисахаридам? Почему?
2.5 Назовите формулу сахарозы.
Углеводы. Химический диктант.
- Вещество при обычных условиях твердое, кристаллическое, сладкое.
- Хорошо растворяется в воде.
- Получают в промышленности гидролизом природного сырья.
- Получают в промышленности искусственно.
- Реагирует с аммиачным раствором оксида серебра.
- Реагирует со свежеприготовленным гидроксидом меди в щелочной среде.
- “Осветляет” известковое молоко.
- Может образовывать сложные эфиры.
- Может подвергаться гидролизу.
- Применяется в производстве зеркал.
- Используется в качестве пищевого продукта.
- Используется как лекарственный препарат.
- Свойства вещества проявляется при хлебопечении.
- Используется в производстве карамели.
Проверка диктанта, типичные ошибки.
Понятие о полисахаридах.
Ежедневно сталкиваясь со множеством бытовых предметов, продуктов питания, природных объектов, продуктов промышленного производства, мы не задумываемся о том, что все вокруг есть и индивидуальные химические вещества или совокупность этих веществ. Любое вещество обладает собственной структурой и свойствами. Человек с момента своего появления на Земле употреблял растительную пищу, содержащую крахмал, использовал для своих нужд древесину и другие растительные объекты, состоящие главным образом из другого природного полисахарида — целлюлозы. Затем научился выделять и перерабатывать природные полимеры, получая из них ценные вещества, материалы, продукты: бумагу и ткани, муку и патоку, спирт и древесный уголь. И только в начале XIX в. стало возможным изучение химического состава природных высокомолекулярных веществ, строения их молекул. В этой области были сделаны важнейшие открытия.
Некоторые углеводы представляют собой природные полимеры, состоящие из многих сотен и даже тысяч моносахаридных звеньев, входящих в состав одной макромолекулы. Поэтому такие вещества получили название полисахариды. Наиболее важными среди полисахаридов являются крахмал и целлюлоза. Оба они образуются в растительных клетках из глюкозы, основного продукта процесса фотосинтеза.
Наша задача сегодня – рассмотреть физические и химические свойства крахмала и целлюлозы, сравнить их состав и строение.
Таблица на доске (по мере определения характеристик, учитель записывает их на доске). Учащиеся, отвечают на вопросы – заполняют таблицу, проводят опыты.
| Крахмал. | Целлюлоза. | |
| Нахождение в природе(из личного опыта). | Картофель (20%), пшеница, кукуруза (70%), рис (80%). | Древесина, лен, конопля (60%), хлопок (98%). |
| Физические свойства (Э1). | Белый порошок, хрустит при трении – невысокая механическая прочность, нерастворим в холодной воде, частично растворим в воде горячей. | Белое волокнистое вещество, имеет высокую механическую прочность, нерастворимо в горячей и холодной воде, хорошо впитывает воду. |
| Состав. | (С6Н10О5)n | (С6Н10О5)n |
| Строение. | Состоит из остатков – глюкозы. Амилоза – линейная спираль, амилопектин имеет разветвленную структуру. | Состоит из остатков β –г люкозы. Линейные молекулы, образующие волокна за счет водородные связей. |
| Химические свойства. | См Э2 | |
| Биологическая роль. | Запасной питательный материал, источник углеводов (глюкозы). | Стенки клеток, питательное вещество животных. |
| Применение. | Пищевая – глюкоза, патока, спирт. Медицина – мази, присыпки, лекарственные препараты для лечения заболеваний ЖКТ. Текстильная – крахмаление белья (защитная пленка, препятствующая загрязнению). | Древесина – опилки (глюкоза, спирт), бумага, искусственное волокно (вискоза, ацетатное). Текстильная – хлопок, лен (нити, ткани). Нитрование – фотопленка, нитролаки, бездымный. порох |
Эксперимент 1 (Э 1)
- Цвет, внешний вид, форма.
- Механическая прочность. Скрутите клочок ваты в жгут и попробуйте разорвать его (волокно). Разотрите пальцами комок крахмала. Что напоминает услышанный звук? Что вы можете сказать о механической прочности этих веществ?
- Растворимость в воде (холодной, горячей). (Растворить в холодной воде, нагреть.)
На предыдущих уроках мы говорили о составе полисахаридов. Давайте вспомним, какой состав имеют крахмал и целлюлоза. Почему же имея одинаковый состав, эти вещества обладают столь разными свойствами? (имеют разное строение).
Давайте разберемся со строением полисахаридов. Почему эти вещества называются полисахаридами? Из остатков какого моносахарида они состоят? Какие формы глюкозы вы знаете? Какие будут участвовать в образовании полисахаридов? Вспомните, чем отличаются друг от друга -глюкоза и β-глюкоза? (Положение гидроксогруппы у первого атома углерода.)
Слайд 1, слайд 2.
Соединяясь в друг с другом в длинные цепочки остатки глюкозы образуют длинные молекулы, которые в пространстве ведут себя по-разному. Таблица. Например, молекулы целлюлозы, образованные остатками β-глюкозы, образуют линейные цепочки. Между соседними гидроксогруппами образуются водородные связи (напомнить), благодаря которым и формируются волокна. Именно водородные связи обуславливают высокую механическую прочность целлюлозы и ее нерастворимость в воде. Крахмал представляет собой смесь двух полисахаридов – амилозы и амилопектина. Они оба образованы остатками -глюкозы, но амилоза получена при участии 1 и 4 атомов углерода (получается линейная молекула), а в образовании амилопектина участвуют 1 и 6 атомы углерода и образуется разветвленная древовидная структура.
Химические свойства. Эксперимент 2.
Разное строение приводит и к разным свойствам.
1. Взаимодействие с йодом. Рассмотрим специфическое свойство крахмала – взаимодействие с йодом. В пробирку поместите 30 капель крахмального клейстера и 30 капель воды. Добавьте 2 капли спиртовой настойки йода. Что наблюдаете?
Таблица. Молекула амилазы свернута в спираль, внутри которой имеется канал. Именно в этом канале располагаются молекулы йода и удерживаются за счет притяжения и образования слабых связей между йодом и крахмалом. Нагрейте пробирку с раствором. Что наблюдаете? Окраска исчезает, потому что разрушаются связи. После охлаждения связи восстанавливаются, окраска появится вновь.
2. Горение (окисление).
Горение ваты (занимательный опыт).
Оборудование: фарфоровая чашка, перманганат калия (крист.), серная кислота (конц.), хлопковая вата.
Ход работы: в фарфоровую чашку поместите 2–3 г. кристаллического перманганата калия, добавьте пипеткой концентрированную серную кислоту – получается полужидкая кашица. В чашку бросьте кусочек ваты. Что наблюдаете?
Будет ли гореть крахмал?
Подожгите комочек крахмала. Сравните скорость горения этих веществ.
Окисление бумаги серной кислотой. На листе бумаги написать концентрированной серной кислотой любое слово и прогреть на пламени. Обугливание.
3. Гидролиз. Что это за процесс ? как его проводят? Назовите условия. Запишите уравнение реакции.
Целлюлоза → глюкоза (в одну стадию).
Крахмал → декстрины → мальтоза → глюкоза (процесс находит применение в хлебопечении).
4. Этерификация. Что это такое? С чем? С какими кислотами?
Запишите уравнение реакции взаимодействия целлюлозы с азотной и уксусной кислотами.
5. Растворение целлюлозы. Мы говорили, что целлюлоза не растворима в воде. Ее можно растворить в реактиве Швейцера.
Применение. (См. таблицу.)
- Опишите цвет, внешний вид, форму.
- Определите механическую прочность. Скрутите клочок ваты в жгут и попробуйте разорвать его (волокно). Разотрите пальцами комок крахмала. Что напоминает услышанный звук? Что вы можете сказать о механической прочности этих веществ?
- Растворимость в воде (холодной, горячей). (Растворить в холодной воде, нагреть.)
- Подожгите комочек крахмала. Сравните скорость горения этих веществ.
http://chemege.ru/uglevody/
http://urok.1sept.ru/articles/647679