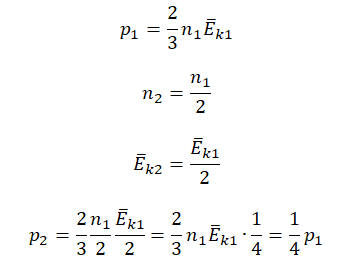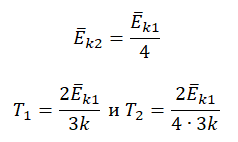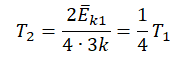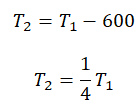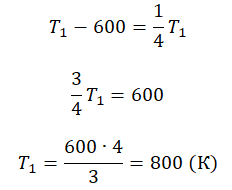Основное уравнение молекулярно-кинетической теории (Ерюткин Е.С.)
Этот видеоурок доступен по абонементу
У вас уже есть абонемент? Войти
Как уже было сказано ранее, начиная с этого урока, мы приступаем к изучению только газов. На прошлом уроке мы дали представление о способах количественного описания некой порции вещества. Сейчас же мы начнём описывать газ со стороны его качественных характеристик (микро- и макропараметров). Мы сформулируем понятие об идеальном газе, опишем его параметры и введём соотношение, связывающее эти параметры (основное уравнение МКТ).
Основное уравнение МКТ идеального газа
теория по физике 🧲 молекулярная физика, МКТ, газовые законы
Идеальный газ — газ, удовлетворяющий трем условиям:
- Молекулы — материальные точки.
- Потенциальная энергия взаимодействия молекул пренебрежительно мала.
- Столкновения между молекулами являются абсолютно упругими.
Реальный газ с малой плотностью можно считать идеальным газом.
Измерение температуры
Температуру можно измерять по шкале Цельсия и шкале Кельвина. По шкале Цельсия за нуль принимается температура, при которой происходит плавление льда. По шкале Кельвина за нуль принимается абсолютный нуль — температура, при котором давление идеального газа равно нулю, и его объем тоже равен нулю.
Обозначение температуры
- По шкале Цельсия — t. Единица измерения — 1 градус Цельсия (1 o C).
- По шкале Кельвина — T. Единица измерения — 1 Кельвин (1 К).
Цена деления обеих шкал составляет 1 градус. Поэтому изменение температуры в градусах Цельсия равно изменению температуры в Кельвинах:
При решении задач в МКТ используют значения температуры по шкале Кельвина. Если в условиях задачи температура задается в градусах Цельсия, нужно их перевести в Кельвины. Это можно сделать по формуле:
Если особо важна точность, следует использовать более точную формулу:
Пример №1. Температура воды равна o C. Определить температуру воды в Кельвинах.
T = t + 273 = 2 + 273 = 275 (К)
Основное уравнение МКТ идеального газа
Давление идеального газа обусловлено беспорядочным движением молекул, которые сталкиваются друг с другом и со стенками сосуда. Основное уравнение МКТ идеального газа связывает давление и другие макропараметры (объем, температуру и массу) с микропараметрами (массой молекул, скоростью молекул и кинетической энергией).
Основное уравнение МКТ
Давление идеального газа пропорционально произведению концентрации молекул на среднюю кинетическую энергию поступательного движения молекулы.
p = 2 3 . . n − E k
p — давление идеального газа, n — концентрация молекул газа, − E k — средняя кинетическая энергия поступательного движения молекул.
Выражая физические величины друг через друга, можно получить следующие способы записи основного уравнения МКТ идеального газа:
p = 1 3 . . m 0 n − v 2
m 0 — масса одной молекулы газа;
n — концентрация молекул газа;
− v 2 — среднее значение квадрата скорости молекул газа.
Среднее значение квадрата скорости не следует путать со среднеквадратичной скоростью v, которая равна корню из среднего значения квадрата скорости:
p = 1 3 . . ρ − v 2
k — постоянная Больцмана (k = 1,38∙10 –3 Дж/кг)
T — температура газа по шкале Кельвина
Пример №2. Во сколько раз уменьшится давление идеального одноатомного газа, если среднюю кинетическую энергию теплового движения молекул и концентрацию уменьшить в 2 раза?
Согласно основному уравнению МКТ идеального газа, давление прямо пропорционально произведению средней кинетической энергии теплового движения молекул и концентрации его молекул. Следовательно, если каждая из этих величин уменьшится в 2 раза, то давление уменьшится в 4 раза:
Следствия из основного уравнения МКТ идеального газа
Через основное уравнение МКТ идеального газа можно выразить скорость движения молекул (частиц газа):
v = √ 3 k T m 0 . . = √ 3 R T M . .
R — универсальная газовая постоянная, равная произведения постоянной Авогадро на постоянную Больцмана:
R = N A k = 8 , 31 Д ж / К · м о л ь
Температура — мера кинетической энергии молекул идеального газа:
Полная энергия поступательного движения молекул газа определяется формулой:
Пример №3. При уменьшении абсолютной температуры на 600 К средняя кинетическая энергия теплового движения молекул неона уменьшилась в 4 раза. Какова начальная температура газа?
Запишем формулу, связывающую температуру со средней кинетической энергией теплового движения молекул, для обоих случаев, с учетом что:
Составим систему уравнений:

Алгоритм решения
Решение
График построен в координатах (V;Ek). Процесс 1–2 представляет собой прямую линию, исходящую из начала координат. Это значит, что при увеличении объема растет средняя кинетическая энергия молекул. Но из основного уравнения МКТ идеального газа следует, что мерой кинетической энергии молекул является температура:
Следовательно, когда кинетическая энергия молекул растет, температура тоже растет.
Запишем уравнение Менделеева — Клапейрона:
Так как количество вещества одинаковое для обоих состояния 1 и 2, запишем:
ν R = p 1 V 1 T 1 . . = p 2 V 2 T 2 . .
Мы уже выяснили, что объем и температура увеличиваются пропорционально. Следовательно, давление в состояниях 1 и 2 равны. Поэтому процесс 1–2 является изобарным, давление во время него не меняется.
Процесс 2–3 имеет график в виде прямой линии, перпендикулярной кинетической энергии. Так как температуры прямо пропорциональна кинетической энергии, она остается постоянной вместе с этой энергией. Следовательно, процесс 2–3 является изотермическим, температура во время него не меняется. Мы видим, что объем при этом процессе уменьшается. Но так как объем и давление — обратно пропорциональные величины, то давление на участке 2–3 увеличивается.
pазбирался: Алиса Никитина | обсудить разбор | оценить
Первоначальное давление газа в сосуде равнялось р1. Увеличив объём сосуда, концентрацию молекул газа уменьшили в 3 раза, и одновременно в 2 раза увеличили среднюю энергию хаотичного движения молекул газа. В результате этого давление р2 газа в сосуде стало равным
Тест 10 класс «Основы молекулярно-кинетической теории»
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
Данный тест можно использовать после изучения тем : «Основные положения МКТ и её опытное подтверждение», «Масса и размеры молекул», «Основное уравнение МКТ идеального газа». Тест составлен для контроля знаний учащихся 10 класса, обучающихся по учебнику «Физика-10» Мякишев, Буховцев ( 2 часа в неделю) с использованием заданий открытого банка заданий ФИПИ.
Тест по теме « Основы молекулярно-кинетической теории »
1. Правильно ли утверждение, что броуновское движение есть результат столкновения частиц, взвешенных в жидкости?
1) утверждение верно 2) утверждение неверно 3) не знаю.
2. Относительная молекулярная масса гелия равна 4. Выразите в кг/моль молярную массу гелия.
1) 0,004 кг/моль 2) 4 кг/моль 3) 4 ∙ 10 -4 кг/моль.
3. Укажите основное уравнение МКТ газов.
1) 


4. Постоянная Авогадро показывает
1) число молекул в веществе 2) число молекул в углероде
3) в одном моле любого вещества содержится разное количество молекул
4) в одном моле любого вещества содержится одинаковое количество молекул
5. Массы молекул очень малы, в молекулярной физике их сравнивают с …
1) 1/13 массы атома углерода 2) 1/13 массы атома водорода
3) 1/12 массы атома водорода 4) 1/12 массы атома углерода
6. Какое количество вещества содержится в 8 граммах водорода?
7. Сколько молекул находится в 32 кг кислорода?
8. Одним из подтверждений положения молекулярно-кинетической теории строения вещества о том, что частицы вещества хаотично движутся, может служить:
A. Возможность испарения жидкости при любой температуре.
Б. Зависимость давления столба жидкости от глубины.
B. Выталкивание из жидкости погруженных в нее тел.
Какие из утверждений правильны?
1) только А 2) только Б 3) только А и Б 4) только Б и В
9. Хаотичность теплового движения молекул газа в небольшом сосуде приводит к тому, что
1) плотность газа одинакова во всех точках занимаемого им сосуда
2) плотность вещества в газообразном состоянии меньше плотности этого вещества в жидком состоянии
3) газ легко сжимается
4) при охлаждении и сжатии газ превращается в жидкость
10.Отвечая на вопрос учителя, Сережа, используя положения МКТ, указал следующие характеристики теплового движения молекул вещества:
A) в веществе каждая молекула движется с присущей ей скоростью, которая не меняется с течением времени;
Б) не бывает резкого изменения по модулю или направлению скорости какой-либо молекулы вещества;
B) среднее число молекул, у которых значение модуля скорости больше 300 м/с, но меньше 350 м/с, не меняется с течением времени;
Г) среднее значение модуля скоростей всех молекул вещества не меняется с течением времени.
Какие из этих признаков Сережа указал правильно (считая, что температура вещества постоянна)?
1) А и Б 2) В и Г 3) А и В 4) Б и Г
11. Давление идеального газа прямо пропорционально
1) средней скорости его молекул
2) среднеквадратичной скорости его молекул
3) среднему квадрату скорости его молекул
4) квадрату средней скорости его молекул
12.Концентрацию молекул одноатомного идеального газа уменьшили в 5 раз. Одновременно в 2 раза увеличили среднюю энергию хаотичного движения молекул газа. Чему равно отношение конечного давления к начальному?
13. Во сколько раз изменится давление идеального газа, если среднюю кинетическую энергию теплового движения молекул газа увеличить в 2 раза и концентрацию молекул газа увеличить в 2 раза?
Тест по теме « Основы молекулярно-кинетической теории »
1. Какое выражение, приведенное ниже, соответствует формуле количества вещества?
1) 



2. Что называют тепловым движением?
1) движение одного тела по поверхности другого
2) беспорядочное движение молекул
3) движение тела в горячей воде
4) броуновское движение
3. Чему равно отношение числа молекул в одном моле кислорода к числу молекул в одном моле азота?
1) 

4. Масса вещества, в количестве одного моля, называется…
1) молекулярная 2) молярная 3) атомная 4) ядерная
5. М (Н 2 О) = 18·10 -3 кг/моль что это за число…
1) молярная масса вещества 2) потенциальная масса вещества
3) атомная масса вещества 4) относительная молекулярная масса вещества
6. Сколько молекул содержится в 1 кг водорода?
7. Какое количество вещества содержится в теле, состоящем из 1,204·10 24 молекул?
8.Чем можно объяснить, что через некоторое время после открытия в комнате флакона с духами их запах ощущается по всему помещению?
1) Диффузией газов
2) Теплопроводностью стенок флакона
3) Духи могут действовать на рецепторы носа на расстоянии
4) Духи в открытом флаконе испускают излучение, улавливаемое рецепторами носа
9. Идеальный газ, находящийся в закрытом сосуде, оказывает давление на его стенки. Это объясняется тем что
1) молекулы прилипают к стенкам сосуда
2) идеальный газ имеет большую плотность
3) молекулы газа передают стенкам энергию
4) молекулы газа передают стенкам импульс
10.В учебнике по физике в одном из абзацев написано: «Молекулы считаются материальными точками, которые хаотически движутся и абсолютно упруго соударяются друг с другом и со стенками сосуда. В промежутках между столкновениями молекулы друг с другом и со стенками сосуда не взаимодействуют». Какая физическая модель описывается в этом абзаце учебника?
1) монокристаллическое твердое тело 2) поликристаллическое твердое тело
3) идеальная жидкость 4) идеальный газ
11.Средняя кинетическая энергия поступательного движения молекул идеального газа прямо пропорциональна
1) среднему квадрату скорости его молекул
2) квадрату средней скорости его молекул
3) средней скорости его молекул
4) среднеквадратичной скорости его молекул
12.Среднюю кинетическую энергию теплового движения молекул разреженного газа уменьшили в 2 раза и концентрацию молекул газа уменьшили в 2 раза. Чему равно отношение конечного давления к начальному?
13.При неизменной концентрации молекул идеального газа средняя квадратичная скорость теплового движения его молекул увеличилась в 4 раза. Во сколько раз изменилось давление газа?
http://spadilo.ru/osnovnoe-uravnenie-mkt-idealnogo-gaza/
http://infourok.ru/test-klass-osnovi-molekulyarnokineticheskoy-teorii-4019081.html