Please wait.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 6e14154d4b153a7d • Your IP : 85.95.188.35 • Performance & security by Cloudflare
Взаимодействие ацетата натрия с серной кислотой?
Химия | 1 — 4 классы
Взаимодействие ацетата натрия с серной кислотой.
2CH₃COONa + H₂SO₄ = Na₂SO₄ + 2CH₃COOH
CH₃COOH⁻ + H⁺ = CH₃COOH.
Вычислите массу ацетата натрия который получится в результате взаимодействия ледяной кислоты с избытком гидроксида натрия?
Вычислите массу ацетата натрия который получится в результате взаимодействия ледяной кислоты с избытком гидроксида натрия.
Взаимодействие ацетата натрия с концентрированым раствором гидрокарбаната натрия?
Взаимодействие ацетата натрия с концентрированым раствором гидрокарбаната натрия.
Метаналь взаимодействует с а)оксидом серебра(1) б)разбавленной серной кислотой в)гидроксидом меди (2) г)ацетатом натрия д)соляной кислотой е)водородом?
Метаналь взаимодействует с а)оксидом серебра(1) б)разбавленной серной кислотой в)гидроксидом меди (2) г)ацетатом натрия д)соляной кислотой е)водородом.
Между какими ионами происходит взаимодействие при смешивании растворов : а)нитрата серебра и хлорида натрия б)карбоната натрия и серной кислоты в)хлорида бария и серной кислоты г)гидроксида натрия и с?
Между какими ионами происходит взаимодействие при смешивании растворов : а)нитрата серебра и хлорида натрия б)карбоната натрия и серной кислоты в)хлорида бария и серной кислоты г)гидроксида натрия и серной кислоты д)гидроксида бария и серной кислоты?
Расчитайте массу ацетата натрия, который был получен в результате взаимодействия 18 г уксусной кислоты с карбонатом натрия?
Расчитайте массу ацетата натрия, который был получен в результате взаимодействия 18 г уксусной кислоты с карбонатом натрия.
К ацетату натрия прилейте несколько капель серной кислоты?
К ацетату натрия прилейте несколько капель серной кислоты.
Запишите уравнение реакции.
Найдите массу ацетата натрия, образующегося при взаимодействии 1, 61 г натрия с уксусной кислотой?
Найдите массу ацетата натрия, образующегося при взаимодействии 1, 61 г натрия с уксусной кислотой.
Окислительно — восстановительные реакции ( на примере взаимодействия натрия с серной кислотой)?
Окислительно — восстановительные реакции ( на примере взаимодействия натрия с серной кислотой).
Нетрат натрия взаимодействует с серной кислотой?
Нетрат натрия взаимодействует с серной кислотой.
Напишите уравнение реакции при взаимодействии натрия и серной кислоты?
Напишите уравнение реакции при взаимодействии натрия и серной кислоты?
На этой странице сайта, в категории Химия размещен ответ на вопрос Взаимодействие ацетата натрия с серной кислотой?. По уровню сложности вопрос рассчитан на учащихся 1 — 4 классов. Чтобы получить дополнительную информацию по интересующей теме, воспользуйтесь автоматическим поиском в этой же категории, чтобы ознакомиться с ответами на похожие вопросы. В верхней части страницы расположена кнопка, с помощью которой можно сформулировать новый вопрос, который наиболее полно отвечает критериям поиска. Удобный интерфейс позволяет обсудить интересующую тему с посетителями в комментариях.
1) СН3 — СН(ОН) — СН(СН3) — С(СН3)(С2Н5) — СН2 — СН3 2) СН3 — СН(ОН) — СН(С2Н5) — СН(СН3) — СН2 — СН2 — СН3 3) СН3 — СН2 — С(СН3)(СН3) — СОН 4) СН3 — СН2 — СН(С2Н5) — СН2 — СН(С2Н5) — СОН 5) СН3 — СН(СН3) — СН(СН3) — С(СН3)(С2Н5) — СН2 — СООН 6) СН3 ..
В 1 моль ортофосфата натрия содержится 69 г натрия, то 23 г его будет содержаться в 1 / 3 моль данного вещества.
Наверное так) удачи ).
Пожалуйста здесь электронный бананс можно ещё электонно — ионный написать.
HBr = H + Br H2SO4 = 2H + SO4 HNO3 = H + NO3 HClO4 = H + CLO4 H3PO4 = 3H + PO4 HMnO4 = H + MnO4 Кислоты диссоциируют на катионы водорода и анионы кислотного остатка. В растворах кислот всегда присутствуют одинаковые ионы водорода — Н( + ).
Так как если бы химию соединили с другими науками о природе, то получилась бы какая — то каша. Каждая наука изучает что — то своё.
1) Оксиды : CaO, CuO, Mn2O7, ZnO, N2O5, SO3, SO2, P2O5, Na2O, B2O3, BeO, CrO3, MnO2, Br2O5, Rb2O, PbO2 2) Основания : Cu(OH)2, LiOH, Be(OH)2, Ca(OH)2, Ba(OH)2, NaOH, KOH, Fe(OH)2, Zn(OH)2 3) Кислоты : HNO3, H2S, HCl, H2SO4, H3PO4, H2SO3, HMnO4, H3AsO..
M (Na3BO3) = (23 * 3) + 11 + (16 * 3) = 128 г \ моль.
Вроде так, но это не точно.
В) он просто не может с ним реагировать так как ничего не случиться.
Ацетат натрия (свойства и применение)
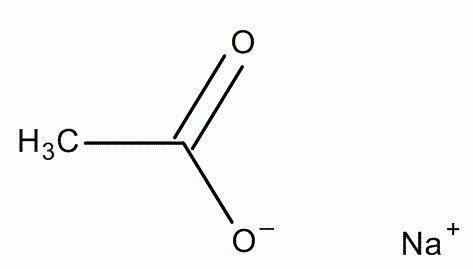
Это химическое вещество многие знают под бытовым названием «горячий лед». На самом деле, ацетат натрия (C2H3O2Na) представляет собой искусственные кристаллы тех солей, которые входят в состав уксусной кислоты. Данное вещество широко распространено в природе. Оно имеется в составе многих клеток растительного и животного происхождения, поэтому ацетат натрия можно обнаружить во многих фруктах и ягодах. Также его образование происходит в ходе бактериальной ферментации, что приводит к его появлению в кисломолочных продуктах.
Свойства химического вещества
Ацетат натрия не без основания назвали «горячим льдом», поскольку в экзотермическом процессе кристаллизации он сильно нагревается. Это вещество имеет кристаллическую структуру. Оно практически бесцветно и имеет слабо выраженный запах уксусной кислоты. Его кристаллы обладают отличительной чертой: в эфире и спирте они очень плохо растворяются, а вот во время взаимодействия с водой они очень быстро превращаются в раствор ацетата натрия. Так, 76 г этого вещества растворяется в 100 мл H2O. Ацетат натрия обладает низким уровнем токсичности и не горюч. Удельная теплота его плавления составляет 264-289 к, а температура разложения: 324 °C. Ацетат натрия, тригидрат которого имеет точку плавления 58 °C, при нагревании до 100 °C в емкости, находящейся к кипятке, растворяется в своей кристаллизационной воде (расплавляется). Таким образом, он преобразуется в раствор. При его охлаждении наблюдается перенасыщение этого вещества в воде. Такой раствор замечательно переохлаждается до температуры 20-24 °C без образования его твердой фазы. После нажатия на металл в емкости происходит образование центра кристаллизации. В процессе роста он заставляет этот раствор преобразовываться в твердую фазу тригидрата натриевого ацетата. Этот процесс сопровождает значительное выделение тепла (264-289 кДж/кг).
Способы получения ацетата натрия
Как сделать ацетат натрия в домашних условиях
Другими словами, получение ацетата в домашних условиях называют «гашением соды». В результате этой химической реакции получается нестойкое соединение, моментально разлагающееся на воду и углекислый газ. Во время выпаривания получившегося раствора образуется кристаллический ацетат натрия. Как правило, для его получения берут соду и кислоту в соотношениях: 84 г гидрокарбоната натрия с 750 г винного уксуса (8%) или с 86 г уксусной эссенции (70%). В последнем случае выпаривание не понадобится. В результате реакции получается около 80 г ацетата натрия.
Другие названия ацетата натрия
Чаще всего для обозначения данного вещества используют такие его синонимы: натриевая соль уксусной кислоты, натриевый ацетат, натрия этаноат.
Применение ацетата натрия в качестве пищевой добавки
Данное вещество применяют в различных отраслях. Так, в пищевой промышленности его используют в качестве консерванта под обозначением Е262. На сегодняшний день производство некоторых продуктов питания без него не обходится. Так, ацетат натрия добавляют в муку для защиты хлебобулочных изделий от так называемой «картофельной болезни», вызываемой спорообразующими бактериями Bacillus mesentericus, очень распространенными в природе. При производстве чипсов также используют эту добавку для придания им приятного вкуса и аромата. Е262 добавляют и в овощные консервы, поскольку ее воздействие на продукты смягчает очень острый привкус уксусной кислоты. Многие люди очень настороженно относятся к различного рода пищевым добавкам. На самом деле, Е262 благодаря своей низкой токсичности разрешена к применению во всех европейских странах. В РФ также не устанавливалась максимальная ежедневная доза употребления ацетата натрия.
Использование в медицине
Также не редко использование данного вещества в медицинских целях. Оно имеется в составе многих лекарственных средств. Так, в частности, его можно обнаружить во многих мочегонных препаратах. Ацетаты натрия применяются в качестве ощелачивающих средств при матаболическом ацидозе и гипонатриемии.
Применение вещества в других отраслях
Помимо вышеперечисленных областей применения ацетат натрия используют в текстильной промышленности и строительстве. Данное вещество используется для нейтрализации уже отработанной серной кислоты, попадающей в сточные воды. Ацетат натрия применяют как фоторезист в процессе обработки тканей анилиновыми красителями. Он также используется в процессе дубления кож солями хрома (протравливание). Ацетат натрия во время производства синтетических резин замедляет вулканизацию хлоропрена. Его используют как противоморозную добавку для любых разновидностей бетона при производстве монолитных конструкций. Это вещество применяют в производстве так называемых «химических» обогревателей и грелок. Это обусловлено его способностью нагреваться до довольно высоких температур. Ацетат натрия является основным компонентом широко распространенной смеси под названием «горячий лед». Применяется это вещество и в производстве уксусного ангидрида, мыл, ацетилхлорида, ацетатов меди, винилацетата и других химикатов. Он используется как катализатор поликонденсации и компонент кислотных закрепителей для фотографий. Его применяют для получения электролитов и буферных растворов в гальванотехнике.
Негативные свойства вещества
Хотя ацетат натрия и малотоксичен, чрезмерное его употребление все-таки может нанести заметный ущерб здоровью человека. Так, его не рекомендуют людям, страдающим от таких заболеваний: артериальная гипертензия, вегето-сосудистая дистония, дисбактериоз. Следует значительно ограничить потребление продуктов, содержащих Е262 и тем, у кого наблюдаются проблемы с кишечником, мочевыводящими путями, печенью, желчным пузырем. Это обусловлено тем, что ацетат натрия в кишечники нередко превращается в токсичные нитраты, обладающие канцерогенным действием. Именно поэтому медики предупреждают о том, что чрезмерное потребление продуктов, содержащих Е262, может привести к образованию злокачественных опухолей, отравлениям и возникновению аллергических реакций. Ацетат натрия нельзя применять при производстве детских пищевых продуктов, поэтому наличие на упаковке маркировки Е262 является серьезной причиной отказа от их покупки.
Признаки отравления ацетатом натрия
К ним относятся: головокружение, головная боль, бледность кожи, острые болевые ощущения в животе, нарушение координации, затруднение дыхания, судороги, обмороки.
Взаимодействие ацетата натрия с другими веществами
Сочетание этого химиката с муравьиной кислотой дает аддукты. В результате его соединения с оксидом азота образуется нитрит натрия и уксусный ангидрит. Такие вещества, как ацетат натрия + концентрированная серная кислота, в соединении дают уксусную кислоту.
http://himia.my-dict.ru/q/1935327_vzaimodejstvie-acetata-natria-s-sernoj-kislotoj/
http://www.syl.ru/article/141235/mod_atsetat-natriya-svoystva-i-primenenie