Диффузия газов в твердых телах
Механизм проницаемости газа сквозь твердое тело можно представить как процесс растворения газа в материале со стороны высокого давления, диффузии в направлении убывающей концентрации и последующего выделения газа на стороне низкого давления.
Удельным потоком диффузии газа в твердом теле называется количество газа, диффундирующее в единицу времени через единичную площадку в направлении, перпендикулярном этой площадке.
Уравнения для случая диффузии газов в твердых телах имеют вид:
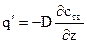
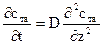
где 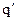
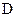
Коэффициент диффузии в твердом теле 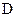
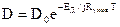
где 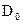
Дата добавления: 2016-02-11 ; просмотров: 1049 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Диффузия в твердых телах, жидкостях и газах: определение, условия
Среди многочисленных явлений в физике процесс диффузии относится к одним из самых простых и понятных. Ведь каждое утро, готовя себе ароматный чай или кофе, человек имеет возможность наблюдать эту реакцию на практике. Давайте узнаем больше об этом процессе и условиях его протекания в разных агрегатных состояниях.
Что такое диффузия
Данным словом именуется проникновение молекул или атомов одного вещества между аналогичными структурными единицами другого. При этом концентрация проникающего соединений выравнивается.
Впервые этот процесс был подробно описан немецким ученым Адольфом Фиком в 1855 г.
Название данного термина было образовано от латинского отглагольного существительного diffusio (взаимодействие, рассеивание, распространение).
Диффузия в жидкости
Рассматриваемый процесс может происходить с веществами во всех трех агрегатных состояниях: газообразном, жидком и твердом. Чтобы отыскать практические примеры этого, стоит просто заглянуть на кухню.
Варящийся на плите борщ – это один из них. Под действием температуры молекулы глюкозинбетанина (вещества, благодаря которому свекла обладает таким насыщенным алым цветом) равномерно реагируют с молекулами воды, придавая ей неповторимый бордовый оттенок. Данный случай — это пример диффузии в жидкостях.
Помимо борща, данный процесс можно увидеть и в стакане чая или кофе. Оба эти напитка имеют столь равномерный насыщенный оттенок благодаря тому, что заварка или частички кофе, растворяясь в воде, равномерно распространяются между ее молекулами, окрашивая ее. На этом же принципе построено действие всех популярных растворимых напитков девяностых: Yupi, Invite, Zuko.
Взаимопроникновение газов
Продолжая дальше искать проявления рассматриваемого процесса на кухне, стоит принюхаться и насладиться приятным ароматом, исходящим от букета свежих цветов на обеденном столе. Почему так происходит?
Атомы и молекулы, переносящие запах, находятся в активном движении и вследствие него перемешиваются с частицами, уже содержащимися в воздухе, и довольно равномерно рассеиваются в объеме помещения.
Это проявление диффузии в газах. Стоит отметить, что само вдыхание воздуха тоже относится к рассматриваемому процессу, как и аппетитный запах свежеприготовленного борща на кухне.
Диффузия в твердых телах
Кухонный стол, на котором стоят цветы, застелен скатертью яркого желтого цвета. Подобный оттенок она получила благодаря способности диффузии проходить в твердых телах.
Сам процесс придания полотну какого-то равномерного оттенка проходит в несколько этапов следующим образом.
- Частички желтого пигмента диффундировали в красильной емкости по направлению к волокнистому материалу.
- Далее они были впитаны внешней поверхностью окрашиваемой ткани.
- Следующим шагом была снова диффузия красителя, но на этот раз уже внутрь волокон полотна.
- В финале ткань зафиксировала частички пигмента, таким образом окрасившись.
Диффундирование газов в металлах
Обычно, говоря об этом процессе, рассматривают взаимодействия веществ в одинаковых агрегатных состояниях. Например, диффузия в твердых телах, твердых веществах. Для доказательства этого явления проводится опыт с двумя прижатыми друг к другу металлическими пластинами (золото и свинец). Взаимопроникновение их молекул происходит довольно долго (один миллиметр за пять лет). Этот процесс используется для изготовления необычных украшений.
Однако диффундировать способны и соединения в разных агрегатных состояниях. К примеру, существует диффузия газов в твердых телах.
В процессе экспериментов было доказано, что подобный процесс протекает в атомарном состоянии. Для его активации, как правило, нужно значительно повышение температуры и давления.
Примером такой газовой диффузии в твердых телах является водородная коррозия. Она проявляется в ситуациях, когда возникшие в процессе какой-нибудь химической реакции атомы водорода (Н2) под действием высоких температур (от 200 до 650 градусов Цельсия) проникают между структурными частицами металла.
Помимо водорода, в твердых телах диффузия кислорода и других газов также способна происходить. Этот незаметный глазу процесс приносит немало вреда, ведь из-за него могут рушиться металлические сооружения.
Диффундирование жидкостей в металлах
Однако не только молекулы газов могут проникать в твердые тела, но и жидкостей. Как и в случае с водородом, чаще всего такой процесс приводит к коррозии (если речь идет о металлах).
Условия ускорения диффузии. Коэффициент диффузии
Разобравшись с тем, в каких веществах может происходить рассматриваемый процесс, стоит узнать об условиях его протекания.
В первую очередь быстрота диффузии зависит от того, в каком агрегатном состоянии пребывают взаимодействующие вещества. Чем больше плотность материала, в котором происходит реакция, тем медленнее ее скорость.
В связи с этим диффузия в жидкостях и газах всегда будет проходить более активно, нежели в твердых телах.
К примеру, если кристаллы перманганата калия KMnO4 (марганцовка) бросить в воду, они в течение нескольких минут придадут ей красивый малиновый цвет. Однако если посыпать кристаллами KMnO4 кусочек льда и положить все это в морозилку, по прошествии нескольких часов перманганат калия так и не сможет полноценно окрасить замороженную Н2О.
Из предыдущего примера можно сделать еще один вывод об условиях диффузии. Помимо агрегатного состояния, на скорость взаимопроникновения частиц влияет также и температура.
Чтобы рассмотреть зависимость от нее рассматриваемого процесса, стоит узнать о таком понятии, как коэффициент диффузии. Так называется количественная характеристика ее скорости.
В большинстве формул она обозначается при помощи большой латинской литеры D и в системе СИ измеряется в квадратных метрах на секунду (м²/с), иногда — в сантиметрах за секунду (см 2 /м).
Коэффициент диффузии равен количеству вещества, рассеивающегося через единицу поверхности на протяжении единицы времени, при условии, что разность плотностей на обеих поверхностях (расположенных на расстоянии равном единице длины) равна единице. Критерии, определяющие D, – это свойства вещества, в котором происходит сам процесс рассеивания частиц, и их тип.
Зависимость коэффициента от температуры можно описать при помощи уравнения Аррениуса: D = D0exp(-E/TR).
В рассмотренной формуле Е – минимальная энергия, необходимая для активации процесса; Т – температура (измеряется по Кельвину, а не Цельсию); R – постоянная газовая, характерная для идеального газа.
Помимо всего вышеперечисленного, на скорость диффузии в твердых телах, жидкости в газах влияет давление и излучение (индукционное или высокочастотное). Кроме того, многое зависит от наличия катализирующего вещества, часто именно оно выступает в роли пускового механизма для начала активного рассеивания частиц.
Уравнение диффузии
Данное явление — частный вид уравнения дифференциального при частных производных.
Его цель — отыскать зависимость концентрации вещества от размеров и координат пространства (в котором оно диффундирует), а также времени. При этом заданный коэффициент характеризует проницаемость среды для реакции.
Чаще всего уравнение диффузии записывают следующим образом: ∂φ (r,t)/∂t = ∇ x [D(φ,r) ∇ φ (r, t)].
В нем φ (t и r) — плотность рассеивающегося вещества в точке r во время t. D (φ, r) — диффузии обобщенный коэффициент при плотности φ в точке r.
∇ — векторный дифференциальный оператор, компоненты которого по координатам относятся к частным производным.
Когда коэффициент диффузии зависим от плотности, уравнение является нелинейным. Когда нет — линейным.
Рассмотрев определение диффузии и особенности данного процесса в разных средах, можно отметить, что он имеет как положительные, так и отрицательные стороны.
Диффузия в газах
Диффузией молекул газа является процесс перемещения частичек вещества, обусловленный беспорядочным движением его молекул. Процесс диффузии осуществляется за счет разности концентрации вещества в разных точках занимаемого объема, результатом диффузии является равномерное распределение вещества по всему предоставленному объему.
Явление диффузии может наблюдаться в жидкостях, газах и твердых телах. Диффузия в газах является самым быстрым процессом, а в твердых телах – самым длительным. Такая разница существует из-за особенностей структуры вещества и свойств его молекул. Обычно явление диффузии рассматривается как проникновение одного вещества в другое, для газов это явление взаимопроникновения.
Явление диффузии в газах
Для любого необратимого процесса характерно воздействие внешних факторов на физическую систему. При таких условиях состояние физической системы выводится из состояния равновесия. Как известно, любая система стремится к равновесию.
Такие явления движения молекул представляют собой необратимый самопроизвольный процесс, сопровождающийся тепловым движением вследствие вывода системы из равновесия. Таким образом формируются потоки диффузии и импульса. Здесь играют роль два свойства импульса: его направление и направление перемещения импульса.
Согласно абсолютным значениям, любой поток будет равнозначен массе вещества, его внутренней энергии (теплопроводности) и его импульсу (вязкости). Глубокий молекулярно-кинетический анализ подобных процессов перемещения очень сложный из-за беспорядочного движения молекул и нарушения состояния физического равновесия. Это способствует отклонению распределения молекул в соответствии со скоростями Максвелла.
Процесс диффузии газов происходит таким образом. Диффузия характеризуется взаимопроникновением и перемешиванием молекул двух или более взаимодействующих физических систем. Самодиффузия происходит при смешивании молекул одного вещества, в газовой смеси диффузия происходит из-за разницы концентраций каждого из газов, составляющих смесь.
Не нашли что искали?
Просто напиши и мы поможем
В процессе диффузии происходит перемещение частиц из точки с большой концентрацией в точку с небольшой. Перемещение массы вещества во процессе диффузии описывается законом Фика:
где \(m\) – масса газа;
\(D\) – коэффициент диффузии;
\(
\(S\) – некоторая площадь, находящаяся перпендикулярно направлению перемещения массы;
\(t\) – время перемещения.
Во время диффузии газов вещество перемещается в сторону уменьшения плотности газа. Согласно молекулярно-кинетической теории, коэффициент диффузии показывает скорость перемещения молекул и определяется следующим выражением:
где \(u\) – среднеарифметическая скорость молекул;
\(λ\) – средняя длина свободного перемещения молекул.
Если ввести понятие вектора плотности тока диффундирующих частиц \( j_D\) , закон Фика примет следующий вид:
где \(n_0\) – концентрация частиц газа.
Процесс перемещения в газах
Необратимые процессы, которые возникают в термодинамических неравномерных системах, называются явлениями перемещения. К ним относятся диффузия (перемещения массы), теплопроводность (перемещение тепла) и вязкость (перемещение импульса).
В процессе повышения температуры диффузия газов значительно ускоряется, а при росте давления наоборот замедляется. При этом диффузия тяжелых молекул происходит медленнее, чем более легких.
Вязкость имеет место во время трения при параллельном движении слоев газа или жидкости с разными по значению скоростями.
В процессе перемещения любого тела в жидкости или газе во время его взаимодействия с молекулами оно передает им импульс. Точно так же и тело получает от молекул импульс противоположного направления. В подобном случае имеет место ускорение газа и замедление тела под действием сил трения. Такая же сила возникает при движении двух соприкасающихся газов, которые распространяются с разной скоростью.
Причиной внутреннего трения газов является перемещение импульса между слоями. Сила трения при этом пропорциональна градиенту скорости согласно закону Ньютона:
где \(n\) – коэффициент динамической вязкости, который зависит от плотности газа.
Этот коэффициент показывает значение импульса, перемещаемого за единицу времени сквозь единицу площади при единичном градиенте скорости. Коэффициент динамической вязкости газов не зависим от давления, но зависим от температуры.
Сложно разобраться самому?
Попробуй обратиться за помощью к преподавателям
Теплопроводность описывает перемещение внутренней энергии между газовыми слоями. При возникновении разницы температур между двумя соседними слоями газа, начинается теплообмен.
Благодаря беспорядочному движению молекул в смежных слоях происходит выравнивание их внутренних энергий. В итоге будет наблюдаться энергетическое перемещение от теплых слоев к менее нагретым. Согласно закону Фурье тепловой поток \(q\) будет пропорционален градиенту температуры и рассчитывается по формуле:
Вакуум и разрежение газов
Разреженный газ – это такой газ, плотность которого на столько мала, что средняя длина перемещения молекул \(λ\) равна линейным размерам сосуда, в котором находится газ. Такое состояние газа является вакуумом.
Различают несколько степеней вакуума:
низкая ( \(λ );
средняя ( \(λ=1\) );
высокая ( \(λ>1\) );
сверхвысокая ( \(λ≫1\) ).
Разреженные и не разреженные газы отличаются своими характеристиками. При откачивании газа из сосуда будет уменьшаться давление, при этом число столкновений молекул за единицу времени будет уменьшаться, следствием чего будет увеличиваться длина перемещения молекул.
Создание вакуума имеет огромное значение в сфере науки и техники. Вакуум применяется в большинстве сегодняшних электронных приборах, комплектующие которых просто невозможно создать без вакуума.
http://fb.ru/article/331939/diffuziya-v-tverdyih-telah-jidkostyah-i-gazah-opredelenie-usloviya
http://spravochnikvs.com/diffuziya_v_gazah








