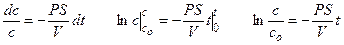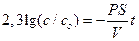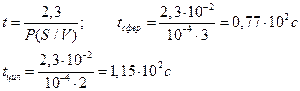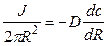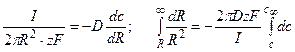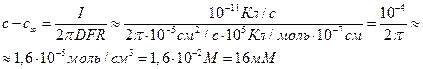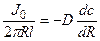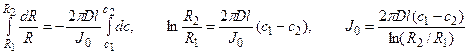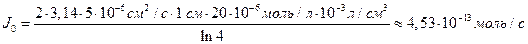Законы Фика | Основы диффузии
Итак, в основе любой теории диффузии (красителей в волокнистых материалах, компонентов в пластических массах, обмена ионов в ионообменных материалах, а также частиц в кристаллических веществах, включающих металлы, полупроводники, оксиды, керамику, стекла и т.д.), лежат законы Фика. Существуют два закона Фика – первый и второй.
Первый закон Фика
Первый закон Фика описывает квазистационарные процессы, когда проницаемая для обменивающихся местами частиц мембрана (пластинка) разделяет две среды (которые могут быть жидкими или газообразными) с существенно постоянными условиями на границах раздела. Эта мембрана может быть инертной по отношению в диффундирующим веществам (например, пористое стекло, разделяющее водные солевые растворы различной концентрации или солевого состава) или активной по отношению к одному или нескольким диффундирующим компонентам (например, палладиевая мембрана, пропускающая через себя водород при высокой температуре из-за специфических процессов сорбции на ее границе и практически не пропускающая другие газы).
Уравнение, описывающее первый закон Фика, имеет следующий вид:
где j – поток вещества через единицу поверхности, D – коэффициент диффузии (в общем случае – коэффициент взаимодиффузии), C — концентрации по толщине мембраны, равная разнице концентраций переносимого вещества по обе стороны мембраны, x — толщина мембраны.
Очевидно, что к обсуждаемым нами процессам образования цинкового покрытия это уравнение неприменимо, поскольку изучаемые нами процессы являются нестационарными.
Второй закон Фика описывает нестационарные процессы, и именно его необходимо применять для описания закономерностей, с которыми имеют дело как металлурги, так и работники других специальностей, соприкасающиеся с проблемами массопереноса в твердых телах.
Рассмотрим его действие на следующем примере. Возьмем два одинаковых образца, имеющих плоскую поверхность и состоящих из металла, который под воздействием нейтронного облучения способен создавать радиоактивные атомы той же природы. Облучим нейтронным потоком один из двух образцов с тем, чтобы создать в нем радиоактивность, соединим плотно по поверхностям облученный и необлученный образцы между собой и для убыстрения процесса будем выдерживать эту композицию при повышенной температуре. Вследствие теплового движения радиоактивные атомы из одной части образца будут диффундировать во вторую его часть, причем этот процесс будет продвинут тем более, чем более высока температура и чем больше время опыта. Затем образцы разъединим, и в каждом образце послойно измерим радиоактивность (технология этого типа эксперимента разработана очень хорошо). В результате эксперимента получаются кривые, изображенные на рис. 7.38, которые соответствующим образом обрабатываются для расчета эффективных коэффициентов диффузии. Концентрация радиоактивных ионов на межфазной границе будет равна половине той, что была в исходном левом образце, а сам процесс диффузии будет описываться уравнением:
Метод обработки таких кривых, как следует из литературы, был предложен физиком по фамилии Матано, и, как правило, называется методом Матано и иногда методом Матано- Больцмана (вероятно, из-за того, что метод возник как результат анализа решений уравнений диффузии, полученных одним из великих физиков теперь уже позапрошлого века Больцманом).
Если поверхность образца контактирует с какой-либо средой в жидкой форме, то на границе раздела концентрация данной среды, как правило, остается постоянной, но на форме фронта в железном образце эта особенность эксперимента при условии постоянства эффективного коэффициента диффузии сказывается достаточно мало (рис.7.39).
Для процесса цинкования необходимо смоделировать именно такую картинку. В этом случае концентрация диффундирующего вещества на границе двух сред является практически постоянной, и диффузия вещества в другую среду будет идти до тех пор, пока не достигнет стационара.
Рис. 7.38. Форма фронта диффузии при контакте двух твердых образцов, в одном из которых (в данном случае слева) методом нейтронного облучения созданы радиоактивные атомы, для двух значений времени эксперимента.
Рис. 7.39. Ожидаемая форма фронта в поглощающей среде при диффузии из среды с постоянной концентрацией на границе.
Второй закон Фика
Уравнение нестационарной диффузии описывается, как было уже сказано, вторым законом Фика, который для диффузии с постоянной концентрацией на границе двух фаз имеет следующий вид:
где n = 2, 1 или 0 – для шара, бесконечного цилиндра и бесконечной пластины.
Для бесконечной пластины уравнение имеет вид:
Ниже приведены соответствующие решения для степени завершения обмена как функции времени при постоянных коэффициентах диффузии:
для шара:
для пластины:
и для бесконечного цилиндра:
μ — корни функции Бесселя нулевого порядка, Bt = π 2 F0
N — степень завершения процесса обмена
F0 = D*t / l 2 — безразмерный параметр, где (D — коэффициент диффузии, t — время, l — линейный параметр)
Эти уравнения показывают, какая доля атомов (от максимально возможной) накапливается в поглощающей части образца.
Анализ показывает, что получаемые кривые, изображенные на рис. 7.39, никоим образом не напоминают типичный фронт сорбции цинка поверхностью железа, картинку которого можно видеть на рис. 7.40. Если верить кривой, полученной на рис. 7.39, наибольшей толщиной должны обладать ζ— и Г1-фазы, а δ-фаза должна иметь промежуточную толщину (о η-фазе мы поговорим несколько позже). Аналогичные результаты (то есть не совпадающие с фронтом, изображенным на рис. 7.39) были получены в значительном количестве исследований, и вот отсюда начинается игра ума.
Одни начинают искать причину в том, что поскольку изучаемое тело имеет кристаллическую структуру, то коэффициенты диффузии в различных направлениях являются различными. Действительно, на монокристаллах в ряде случаев это доказано. Но вот беда: сталь – это поликристаллическое тело, и для процесса цинкования этим вряд ли можно объяснить упомянутые выше экспериментальные закономерности.
Другие ищут причину отклонения от теоретической зависимости в методе Матано в том, что необходимо в уравнении второго закона Фика использовать не градиент концентрации, а градиент химического потенциала. В этом случае уравнение значительно усложняется, и неизвестно, какие результаты – отражающие или не отражающие действительность – будут получены.
Наконец, третьи пошли логически более правильным путем. На самом деле, при диффузии в металле с примесью (сплаве) диффундирует не один вид частиц, а, как минимум, два. Эти два вида частиц диффундируют навстречу друг другу, к тому же обладают различной подвижностью. Если отсчитывать скорость их передвижения от некоторой воображаемой плоскости (рис 7.41), то будет обнаружено, что через некоторое время эксперимента эта плоскость передвинется в сторону той части образца, которая содержит более быстрые частицы (эффект Киркендаля).
Рис. 7.40. Форма фронта, рассчитанная из содержания цинка в каждой из фаз внутри цинкового покрытия.
Рис. 7.41. Сущность эффекта Киркендаля. Пластина из латуни окружена слоем меди, нанесенной электролитически, причем на границе латунного образца предварительно закреплены метки из молибденовой проволоки. В результате выдерживания образца в течение нескольких сотен часов при повышенной температуре метки передвинулась внутрь образца.
Когда анализируют данные по кинетике образования цинк- железного покрытия на образце, исследуются дотошно любые факты, включая тип и структуру образующихся железо-цинковых сплавов, но ни в одной статье до настоящего времени не анализировалась форма фронта цинка в покрытии. Между тем, именно форма фронта говорит о многом, и именно выяснение причин ее образования может стать ключом к количественному описанию скорости образования железо-цинковых слоев.Обратим внимание на следующее. Почти во всех исследованиях в низкотемпературной области (достоверных сведений о форме фронта в высокотемпературной области нами не найдено) образуется форма обрывного фронта, близкая к изображенной на рис. 7.40. Эта форма не сильно зависит от температуры процесса, толщины образующегося покрытия и наличия или отсутствия в образце кремния (фосфора). Между тем имеется очень мало процессов, которые характеризуются такой формой фронта. Одним из таких процессов является процесс горения с быстрым отводом образующихся продуктов горения от поверхности. Для горящего шара, например, процесс горения описывается уравнением:
где R — радиус шара до начала горения, r — радиус координаты горения, D — коэффициент диффузии.
Очевидно, что если мы сделаем плоский образец с защитой боковых поверхностей, то процесс горения будет происходить только на одной из поверхностей без изменения ее реальной площади, то есть скорость уменьшения толщины образца будет пропорциональна времени. Пример такого процесса – «курение сигареты» автоматическим курильщиком с постоянной скоростью просасывания воздуха через образец.
Между тем, в огромном большинстве исследований наблюдается обратноквадратичная зависимость скорости образования слоя (скорости вымывания железа в расплав) от времени, то есть выполняется зависимость:
Однако необходимо тщательно проверить последнее утверждение, прежде чем принимать его за аксиому.
На рис. 7.42 и 7.43 приведены данные по зависимости скорости накопленияжелеза в расплаве от времени при различных температурах. В книге утверждается, что при построении этих данных в координатах получаются прямые линии для всех температур, кроме данных при 510°С, где наблюдается прямолинейная зависимость. Проверим это утверждение.
Рис. 7.42. Зависимость скорости накопления железа в расплаве с течением времени от температуры в высокотемпературной области.
Рис. 7.43. Зависимость скорости накопления железа в расплаве от времени в низкотемпературной области.
Таблица № 7.5. Определение формального порядка реакции методом сравнения с базисной зависимостью для данных по скорости вымывания железа из образца в течение процесса цинкования.
Диффузия ионов и неэлектролитов
Диффузия представляет собой спонтанное движение растворенного вещества в сторону понижения концентрации. Диффузионные законы определяют движение незаряженных веществ в объеме (на любых расстояниях при отсутствии конвекции), перенос ионов в неперемешиваемых слоях у поверхности мембран, а также движение ионов на малых расстояниях.
Формула Стокса–Эйнштейна связывает коэффициент диффузии D с температурой T, вязкостью среды η и радиусом диффундирующих частиц r (k – константа Больцмана). Например, вязкость воды при 20°С составляет ηH2O= 10 –3 Па∙с (1 Па = 1 Н/м 2 ).
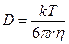
Пользуясь (4.1), можно оценить коэффициент диффузии в воде для малых молекул с радиусом
0,2 нм (10 –5 см 2 /с) или для молекул другого размера. На движение ионов в растворе влияет электрическое поле. Коэффициент диффузии иона зависит от его заряда (z):
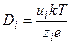
где u – подвижность иона, имеющая размерность м 2 ·с –1 ·В –1 (см 2 ·с –1 ·В –1 ), е – заряд электрона. Например, подвижности ионов K + и Na + равны 7,6·10 –4 и 5,2·10 –4 см 2 ·с –1 ·В –1 , соответственно. Из (4.1) и (4.2) получаем уравнение для расчета подвижности иона по его радиусу и заряду.
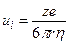
Подвижность численно равна скорости движения ионов (см/с) при напряженности поля 1 В/см.
Законы Фика описывают скорость диффузии вещества, а также пространственное распределение концентрации диффундирующего вещества в различные моменты времени.
Первый закон Фика связывает поток вещества J с коэффициентом диффузии D и градиентом концентрации (dc/dx). Размерность потока – моль∙см –2 ∙с –1 ).
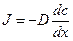
В случае диффузии через тонкую мембрану
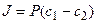
где P=Dg/h – проницаемость, h – толщина мембраны, g – коэффициент распределения вещества между водной и липидной фазами, а 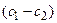
Второй закон Фика описывает направление изменений концентрации вещества во времени (dc/dt) в зависимости от знака второй производной (d 2 c/dx 2 ), определяющей вогнутость или выпуклость профиля концентрации по координате x:
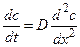
Из (4.6) в частности следует, что в случае одномерной стационарной диффузии (т.е. при dc/dt=0) профиль концентрации линеен: 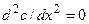
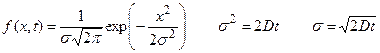
где x – координата, f(x,t) – функция распределения, σ – среднеквадратичное отклонение для нормального распределения вещества относительно исходной точки при x = 0, σ 2 – дисперсия, а t – время. Область, расположенная между координатами ±σ, содержит более 68% от общего количества диффундирующего вещества. Согласно уравнению Эйнштейна, величина σ, обозначаемая также 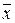
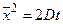
где 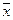
Пример 4.1. После инъекции в клетку некоторого вещества до концентрации co, клетку отмывают средой, не содержащей этого вещества. Какое время инкубации необходимо, чтобы внутренняя концентрация вещества понизилась в 10 раз, если проницаемость мембраны для этого вещества составляет 10 –4 см/с? Решить задачу для клетки сферической формы с диаметром 200 мкм и для цилиндрической клетки с диаметром 200 мкм и длиной 1 см.
Решение: При записи первого закона Фика учтем, что диффузия происходит через тонкую мембрану и, что концентрация во внешнем растворе равна нулю.
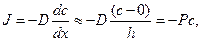
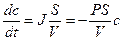
Решение этого дифференциального уравнения описывает кинетику изменения концентрации вещества внутри клетки:
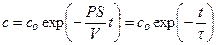
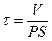
Уравнение решают методом разделения переменных и интегрирования по времени от нуля до t при соответствующем изменении концентрации от co до c.
Для ответа на вопрос задачи удобно перейти к десятичным логарифмам:
Отношение S/V определяется геометрией клетки. Для сферы и цилиндра оно составляет соответственно

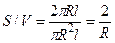
С учетом условия задачи c/co = 0,1 и R = 0,01 см, находим искомое время t:
Аналогичный подход используется для случаев, когда в момент времени t = 0 в наружный раствор добавляют проникающее вещество, которое начинает поступать внутрь клетки, причем наружная концентрация остается постоянной (co = const) из-за большого объема среды по сравнению с объемом клеток. В таком опыте моменту времени t = 0 соответствует внутренняя концентрация с = 0, а произвольному моменту времени t соответствует внутренняя концентрация с. В этом случае интегрирование дифференциального уравнения приводит к следующему решению:
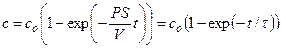
Пример 4.2. Предположим, что через калиевый канал с устьем R = 10 Å протекает ток I силой 10 пА (рис. 4.1.). При этом концентрация К + в устье повышается по сравнению с объемом раствора. Найти концентрацию в области устья канала, если концентрация К + в объеме составляет 10 мМ. При расчете принять, что коэффициент диффузии К + в воде
Решение: На выходе из канала суммарный поток переносимых ионов диффундирует во всех направлениях, ограничиваемых полусферой. Выделим элемент поверхности полусферы и запишем поток через единицу поверхности, пользуясь первым законом Фика.
Суммарный поток вещества J связан с электрическим током I соотношением 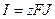
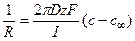
Следовательно, перепад концентрацией между устьем канала и объемом раствора составит
Соответственно, концентрация в устье канала cx составит 26 мМ.
Пример 4.3. Концентрация Са 2+ в питательном растворе на расстоянии 300 мкм от поверхности корня составляет 100 мкМ, а у поверхности корня с диаметром 200 мкм – 80 мкМ. Оценить диффузионный поток Са 2+ к поверхности корня на 1 см его длины (моль·с –1 ), а также поток Са 2+ на единицу поверхности корня (моль·см –2 ·с –1 ) в предположении, что коэффициент диффузии D = 5·10 –6 см 2 /с.
Решение: Обозначим суммарный диффузионный поток для сегмента корня длиной l символом J0. Поток Са 2+ направлен радиально из объема среды к центру корня. Поток через единичный участок цилиндрической поверхности неперемешиваемого слоя на расстоянии R от центра корня составит J0/(2πRl). Запишем уравнение первого закона Фика в радиальных координатах:
Решая уравнение, находим формулу для расчета потока по концентрациям на разном удалении от центра корня (концентрации с1 и с2 для радиальных расстояний R1 и R2).
В расчете на единицу поверхности корня поток составит
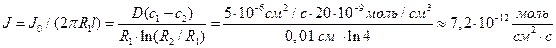
Медфизика Биомембраны. Структура, свойства (стр. 1 )
 | Из за большого объема этот материал размещен на нескольких страницах: 1 2 3 4 5 6 |
Биомембраны. Структура, свойства.
Толщина билипидного слоя и толщина биологической мембраны в целом составляют: 3,5нм и 10нм 8нм и

Жидкостно-мозаичная модель биологической мембраны включает в себя: Белковый слой, полисахариды и поверхностные липиды Липидный монослой и холестерин Липидный бислой Липидный бислой, белки, микрофиламенты
Липидная часть биологической мембраны находится в следующем физиологическом состоянии: жидкокристаллическом твердом кристаллическом твердом аморфном жидком аморфном
Характерное время переноса молекулы фосфолипидов из одного положения равновесия в другое при латеральной и флип-флоп диффузии составляет: 107-108 с; 10-7с 70-80с; 1 час 10-7-10-8 с; 1 час 1-2 часа; 10с
Удельная электрическая ёмкость биологической мембраны 0,005 Ф/м2 0,5⋅10-3 Ф/м2 0,005 Ом/м2 0,5⋅10-3 Ом/м2
Фазовый переход липидного слоя мембран из жидкокристаллического состояния в гель сопровождается: Увеличением толщины мембраны Уменьшением толщины мембраны Толщина мембраны не изменяется Такой переход происходить не может
Основу структуры биологических мембран составляют: aминокислоты двойной слой фосфолипидов углеводы слой белков
Вязкость липидного слоя мембран близка к вязкости: растительного масла этанола ацетона воды
Латеральной диффузией молекул в мембранах называется. . . перескок молекул поперек мембраны – из одного монослоя в другой; вращательное движение молекул; перемещение молекул вдоль плоскости мембраны активный транспорт молекул через мембрану
10. Укажите правильные высказывания:
1) Структурной основой биологической мембраны являются белки.
2) Обязательным структурным компонентом биологических мембран являются соединения, состоящие из полярной «головки» и неполярного «хвоста», например, фосфолипиды.
3) Латеральная диффузия липидов и белков в биомембранах осуществляется значительно быстрее, чем диффузия поперѐк мембраны – из слоя в слой.
4) Латеральная диффузия липидов и белков в биомембранах осуществляется значительно медленнее, чем диффузия поперѐк мембраны – из слоя в слой.
11. Установите соответствие:
1) Плотность потока вещества а) P=Dk/l ;
2) Коэффициент проницаемости б) dc/dx ;
3) Градиент концентрации в) J= — D⋅dc/dx
Транспорт веществ через биологические мембраны
12. Перенос ионов при пассивном и активном транспорте происходит в направлении из области, где




13. Уравнение диффузии неэлектролитов (Фика) записывается:




14. Молекула валиномицина переносит через мембрану:




15. Перенос вещества при облегченной диффузии идет по сравнению с простой диффузией:
с такой же скоростью быстрее в противоположную сторону медленнее
16. Определите плотность потока незаряженных частиц через мембрану, если коэффициент диффузии 10-5см2/с, толщина мембраны 8нм, концентрации вещества с внутренней и с внешней стороны мембраны, соответственно,
Свн=16 ммоль/л, Снар=96 ммоль/л. Коэффициент распределения k=0,2.
2·10-8моль/(м2·с); 2·10-5моль/(м2·с); 0,2 моль/(м2·с); 2 моль/(м2·с).
17. Уравнение Нернста – Планка показывает, что. . .
перенос ионов определяется неравномерностью их распределения (градиентом концентрации) и воздействием электрического поля (градиентом электрического потенциала); главная роль в возникновении потенциала покоя принадлежит ионам калия; потенциал покоя возникает в результате активного транспорта; мембраны обладают избирательной проницаемостью.
18. Плотность потока вещества J имеет размерность:
моль/(м·с); моль/(м3·с); моль/(м2·с); моль/с
19. Коэффициент проницаемости Р вещества через мембрану имеет размерность:
с/м2; м/с; моль/(м2·с); кг/м3
20. Укажите правильные высказывания:
1) Вещество диффундирует через мембрану тем легче, чем меньше его коэффициент распределения.
2) Облегчѐнная диффузия – это перенос ионов специальными молекулами – переносчиками.
3) Облегчѐнной называют диффузию веществ, имеющих высокие значения коэффициента распределения.
4) Диффузия заряженных частиц через мембрану подчиняется уравнению Фика.
5) Диффузия заряженных частиц через мембрану подчиняется уравнению Нернста-Планка.
6) Диффузия незаряженных частиц через мембрану подчиняется уравнению Нернста-Планка.
21. Определите градиент концентрации для ионов калия на мембране, если толщина мембраны 10нм, концентрация [К+]нар=55ммоль/л, [К+]вн=555ммоль/л, коэффициент распределения k=0,1.
5⋅10 9моль/м4 5⋅10-9моль/м4 5⋅10 9моль/м 5⋅109моль/м2
22. Чему равен мебранный потенциал покоя, если концентрация ионов калия внутри клетки 125ммоль/л, снаружи – 2,5 ммоль/л, а толщина мембраны
-98мВ. 98мВ — 98 В 0,098В
23. Чему равна напряженность электрического поля на мембране в состоянии
Чему равен мебранный потенциал покоя, если концентрация ионов калия внутри клетки 400ммоль/л, снаружи – 40 ммоль/л, а толщина мембраны
58мВ. –0,58 В –58 мВ –0,058В
24. Мембранным потенциалом цм называют:
цм = цвн — цнар цм = цнар – цвн цм = цвн + цнар цм = цвн/цнар
25. Диаметр кончика внутриклеточного электрода, используемого для измерения мембранного потенциала:
соизмерим с размером клетки много меньше размеров клетки много больше размеров клетки
26. Какой транспорт ионов создает мембранную разность потенциалов?
активный пассивный мембранная разность потенциалов не связана с транспортом ионов
27. Как соотносятся проницаемости мембраны аксона кальмара для ионов калия и натрия в покое?
Рк:PNa = 1:20 Рк:PNa = 1:0,45 Рк:PNa = 1:0,04
28. Что больше: скорость распространения электрического сигнала vэл. по проводам или скорость распространения нервного импульса vнерв. по мембране аксона?
vэл >> vнерв. vэл vнер
29. Чему равна напряженность электрического поля на мембране в состоянии покоя, если концентрация ионов калия внутри клетки 125ммоль/л, снаружи – 2,5 ммоль/л, а толщина мембраны 8 нм? (RT/F=0,025B)
1,2⋅10-7 В 1,2⋅107 В/м 12⋅107 В/м 120⋅10-7 В/м
30. Чему равна напряженность электрического поля на мембране в состоянии покоя, если концентрация ионов калия внутри клетки 400ммоль/л, снаружи –
40 ммоль/л, а толщина мембраны 8 нм? (RT/F=0,025B)
7,2⋅106 В/м 7,2⋅10-7 В/м 7,2⋅107 В/м 720⋅10-7 В/м
31. Рассчитайте амплитуду потенциала действия, если концентрация калия и натрия внутри клетки возбудимой ткани соответственно: 125ммоль/л,
1,5 ммоль/л, а снаружи 2,5ммоль/л и 25ммоль/л. (RT/F=0,025B)
168мВ. –168мВ –98 мВ 70мВ
32. Оцените величину амплитуды нервного импульса, пользуясь уравнением Нернста для расчета калиевого и натриевого потенциалов, если [К+]нар=10ммоль/л, [К+]вн=400ммоль/л, [Na+]нар=450ммоль/л, [Na+]вн=50ммоль/л; RT/F=0,025В.
147 мВ; — 70 мВ; 0 мВ.
33. Для возникновения трансмембранной разности потенциалов необходимо и достаточно:
наличие избирательной проницаемости и различие концентраций ионов по обе стороны от мембраны; повышенная проницаемость для ионов; наличие избирательной проницаемости и различие концентраций ионов по обе стороны от мембраны различие концентраций ионов по обе стороны от мембраны наличие избирательной проницаемости мембраны.
http://helpiks.org/3-92262.html
http://pandia.ru/text/80/533/6373.php