Составьте уравнения электролитической диссоциации следующих веществ : хлорида натрия, бромоводородной кислоты, иодида кальция?
Химия | 10 — 11 классы
Составьте уравнения электролитической диссоциации следующих веществ : хлорида натрия, бромоводородной кислоты, иодида кальция.
Составьте уравнения электролитической диссоциации сульфата натрия, хлорида цинка, фосфата калия?
Составьте уравнения электролитической диссоциации сульфата натрия, хлорида цинка, фосфата калия.
ПОМОГИТЕ составьте уравнения электролитической диссоциации в водных растворах NaOH, FeCI₂, H₂SO₄ составьте уравнения электролитической диссоциации следующих веществ а)сульфата меди (2) б)хлорида кальц?
ПОМОГИТЕ составьте уравнения электролитической диссоциации в водных растворах NaOH, FeCI₂, H₂SO₄ составьте уравнения электролитической диссоциации следующих веществ а)сульфата меди (2) б)хлорида кальция в)гидроксида натрия составьте уравнение электролитической диссоциации электролитов а)K₂SO₄, CuSO₄, AL₂(SO₄)₃ б)FeCI₃, Fe(NO₃)₃, Fe₂(SO₄)₃.
Составьте уравнение электролитической диссоциации следующих веществ Li2SO3?
Составьте уравнение электролитической диссоциации следующих веществ Li2SO3.
Составьте уравнение электролитической диссоциации следующих веществсульфата меди (2)хлорида кальциягидроксида натрияплизззззззззз помогите?
Составьте уравнение электролитической диссоциации следующих веществ
сульфата меди (2)
Помогите, пожалуйста?
Составьте уравнения электролитической диссоциации следующих веществ :
Хлорида железа (2)
Гидроксида кальция 4.
Написать уравнения диссоциации веществ : карбоната калия, гидроксида кальция, фосфата аммония, бромоводородной кислоты, угольной кислоты, силиката натрия, сульфита натрия?
Написать уравнения диссоциации веществ : карбоната калия, гидроксида кальция, фосфата аммония, бромоводородной кислоты, угольной кислоты, силиката натрия, сульфита натрия.
Составьте уравнения диссоциации следующих электролитов : иодид бария, серная кислота, гидроксид кальция?
Составьте уравнения диссоциации следующих электролитов : иодид бария, серная кислота, гидроксид кальция.
Напишите уравнения электролитической диссоциации следующих веществ : бромида калия, фторида натрия, иодида лития иодоводороднойкислоты?
Напишите уравнения электролитической диссоциации следующих веществ : бромида калия, фторида натрия, иодида лития иодоводороднойкислоты.
Напишите уравнения диссоциации следующих веществ : а) Хлорид цинка ; б) Нитрат кальция ; в) Сульфат натрия ; г) Гидроксид кальция ; д) Бромоводородная кислота?
Напишите уравнения диссоциации следующих веществ : а) Хлорид цинка ; б) Нитрат кальция ; в) Сульфат натрия ; г) Гидроксид кальция ; д) Бромоводородная кислота.
Напишите уравнения электролитической диссоциации следующих веществ хлорида магния карбоната калия нитрат железа III гидроксид натрия азотная кислота?
Напишите уравнения электролитической диссоциации следующих веществ хлорида магния карбоната калия нитрат железа III гидроксид натрия азотная кислота.
На этой странице вы найдете ответ на вопрос Составьте уравнения электролитической диссоциации следующих веществ : хлорида натрия, бромоводородной кислоты, иодида кальция?. Вопрос соответствует категории Химия и уровню подготовки учащихся 10 — 11 классов классов. Если ответ полностью не удовлетворяет критериям поиска, ниже можно ознакомиться с вариантами ответов других посетителей страницы или обсудить с ними интересующую тему. Здесь также можно воспользоваться «умным поиском», который покажет аналогичные вопросы в этой категории. Если ни один из предложенных ответов не подходит, попробуйте самостоятельно сформулировать вопрос иначе, нажав кнопку вверху страницы.
Смеси : — Бензин ; — Кровь ; — Зола. Чистые вещества : — Соль ; — Золото.
Cu(OH)2 = CuO + H2O M(Cu(OH)2) = 98г / моль M(CuO) = 80г / моль n(Cu(OH)2) = 196 / 98 = 2моль nCu(OH)2 : nCuO = 1 : 1 n(CuO) = 2моль m(CuO) = 2 * 80 = 160г CuO + H2 = Cu + H2O n(CuO) = 2моль nCuO : nH2 = 1 : 1 n(H2) = 2моль V(H2) = 2 * 22, 4 = 44, 8л..
Гидроксид меди(основание) азотная кислота (кислоты) оксид фосфора 5 класс оксиды гидроксиды алюминия 3 основание оксид плюмбума (оксид).
То, где есть группа ОН – это основания, или гидрооксиды (меди, алюминия), второе – азотная кислота, третье оксид фосфора, последнее – оксид свинца.
Одна из структурных составляющих стали и чугунаструктурн. Составляющая стали и чугуна.
4H₂S⁺⁶O₄ + P⁻³H₃ = H₃P⁺⁵O₄ + 4H₂O + 4S⁺⁴O₂ S⁺⁶ + 2e = S⁺⁴ 8 4 P⁻³ — 8e = P⁺⁵ 2 1.
Структурная формула во вложении.
1)2Zn + O2 = 2ZnO 2)ZnO + H2SO4 = ZnSO4 + H2O 3) ZnSO4 + 2NaCl = ZnCl2 + Na2SO4 4)ZnCl2 + 2NaOH = Zn(OH)2 + 2NaCl 5)2 NaOH + Zn(OH)2 = Na2ZnO2 + 2H20(Если в растворе — будут другие вещества, а тут именно при сплавлении) Если помог, нажми кнопочку спа..
Во второй реакции написал, что образуется виниловый спирт, не устойчивое соединение, которое потом переходит в этаналь. Но можешь его не писать.
Решение : (А) Al / Al2(SO4)3 / / Fe2(SO4)3 / Fe (К) Уравнение электродных процессов : Al( — ) : Al — 3e = Al(3 + ) Fe( + ) : Fe(3 + ) + 3e = Fe Уравнение реакции : 2Al + Fe2(SO4)3 — — — >Al2(SO4)3 + 2Fe.
Что такое электролитическая диссоциация
Давно известно, что некоторые растворы проводят электрический ток (такие растворы получили название электролитов), а некоторые — не проводят (неэлектролиты).
Кроме электропроводности электролиты и неэлектролиты имеют много других отличий. При одинаковой молярной концентрации электролиты (по сравнению с неэлектролитами) обладают:
- более высокой температурой кипения;
- более низкой температурой замерзания;
- более высоким осмотическим давлением;
- более низким давлением пара растворителя.
Такое большое различие в свойствах растворов ученые объясняют тем фактом, что в электролитах при растворении образуется гораздо большее кол-во частиц, которые еще и обладают зарядом, хотя, в общем, раствор электролита нейтрален.
Впервые теорию электролитической диссоциации (разделения) сформулировал в 1887 г. шведский ученый С. Аррениус, ее основные положения заключались в следующем:
- электролиты, растворяясь в воде, диссоциируют (распадаются) на положительно (катионы) и отрицательно (анионы) заряженные ионы;
- под воздействием внешнего электрического поля катионы в растворе электролита начнут двигаться к катоду (отрицательному электроду), анионы — к аноду (положительному электроду);
- электролитическая диссоциация является обратимым процессом — параллельно с распадом молекул на ионы идет обратный процесс ассоциации (ионы соединяются в молекулы), в результате чего в растворе устанавливается динамическое равновесие.
Через несколько лет, в 1891 г., русский ученый И. Каблуков внес существенные уточнения в теорию Аррениуса, введя понятие сольватации катионов и анионов (формирование химических связей между растворителем и растворяемым веществом).
| Электролитической диссоциацией (ионизацией) называют процесс распада электролитов на ионы в водном растворе (расплаве) |
Ионами называют атомы (группы атомов), которые имеют заряд (положительный — анионы или отрицательный — катионы).
| Растворы электролитов нейтральны потому, что общая сумма зарядов анионов всегда равна общей сумме зарядов катионов |
Механизм электролитической диссоциации
Электролиты бывают двух видов: раствором с ионной связью и раствором с ковалентной связью.
Растворители, в которых протекает процесс диссоциации, обязательно состоят из полярных молекул.
Механизм диссоциации электролитов с ионной и ковалентной связью различен.
Диссоциация хлорида натрия
Хлорид натрия является веществом с ионной связью, в узлах кристаллической решетки NaCl находятся ионы натрия и хлора.
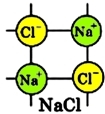
Рис. 1. Кристаллическая решетка хлорида натрия.
При погружении поваренной соли в воду на первой стадии растворения (диссоциации NaCl) полярные молекулы воды под действием электростатического притяжения приклеиваются своей отрицательной стороной к катионам натрия (Na + ), а положительной стороной к анионам хлора (Cl — ):
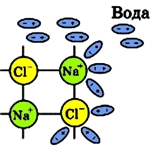
Рис. 2 Притяжение полярных молекул воды к ионам NaCl.
По мере склеивания молекул воды с ионами натрия и хлора происходит ослабление ионных связей Na + с Cl — :
Кристаллическая решетка постепенно разрушается, в результате чего, освободившиеся ионы переходят в раствор, в котором они тут же связываются с молекулами воды — такие ионы называются гидратированными.
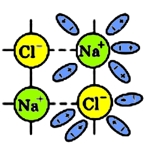
Рис. 3 Ослабление ионных связей хлорида натрия.
Ионные связи хлорида натрия разрываются и гидратированные ионы переходят в раствор:
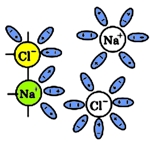
Рис. 4 Переход гидратированных ионов натрия и хлора в раствор.
В водном растворе диссоциация ионных соединений всегда протекает полностью.
Диссоциация хлороводорода
Хлороводород является веществом с ковалентной полярной связью.
Под воздействием молекул воды ковалентные связи поляризуются еще больше и становятся связями ионными, после чего происходит процесс, описанный выше:
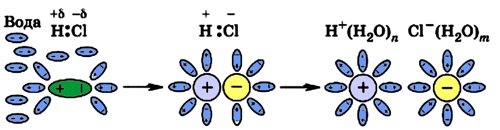
Рис. 5 Диссоциация полярной молекулы HCl.
Из вышесказанного можно сделать вывод, что электролитическая диссоциация возможна в полярных растворителях (вода, этиловый спирт). При диссоциации в первую очередь разрываются наиболее полярные связи (самая большая разность в электроотрицательности атомов, составляющих связь; см. Понятие электроотрицательности).
Растворитель выполняет не только роль разделения катионов и анионов растворяемого вещества, но также замедляет обратный процесс ассоциации ионов в исходную молекулу, поскольку сольватированные (гидратированные) ионы окружены «прилипшими» молекулами растворителя, что мешает сближению (под воздействием кулоновского электростатического притяжения) и воссоединению в молекулу катионов и анионов. Кол-во молекул растворителя, находящихся в гидратной оболочке ионов, зависит от природы ионов, концентрации и температуры раствора.
Одно из главных отличий диссоциации электролитов с полярной связью от диссоциации электролитов с ионной связью заключается в том, что такая диссоциация может быть частичной — это зависит от полярности связей в молекулах электролитов.
Уравнения электролитических диссоциаций записываются следующим образом:
Электролитическая диссоциация протекает за счет энергии, выделяемой в процессе разрушения кристаллической решетки растворяемого вещества во время взаимодейтсвия молекул растворителя с веществом. Следует сказать, что диссоциация может протекать и без растворителя, например, при высокой температуре, когда образуется расплав вещества (энергия для разрушения кристаллической решетки берется из внешнего источника высокой температуры).
ИТОГ : Электролитическая диссоциация — это процесс распада вещества (электролита) на ионы (в растворах под воздействием полярных молекул растворителя; в расплавах — под воздействием высокой температуры).
Свойства ионов
Атомы элементов и их ионы — это далеко не «родственники». По своим физическим и химическим свойствам ионы сильно отличаются от нейтральных атомов, из которых они образовались.
Такие сильные различия между атомами и их ионами объясняются разным электронным строением.
При наличии в растворе нескольких электролитов они диссоциируют в сторону образования: 1) осадков; 2) газов; 3) слабых электролитов.
- пример диссоциации с образованием осадков:
- пример диссоциации с образованием газов:
- пример диссоциации с образованием слабых электролитов:
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
Please wait.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Cloudflare Ray ID: 6e172db05d92163a • Your IP : 85.95.188.35 • Performance & security by Cloudflare
http://prosto-o-slognom.ru/chimia/04_dissotsiatsiya.html
http://gomolog.ru/reshebniki/9-klass/zadachnik-kuznecova-2020/2-2.html









