Внутренняя энергия и работа идеального газа
теория по физике 🧲 термодинамика
Числом степеней свободы механической системы называют количество независимых величин, с помощью которых может быть задано положение системы.
Внутренняя энергия идеального газа представляет собой сумму только кинетической энергии всех молекул, а потенциальной энергией взаимодействия можно пренебречь:
U = ∑ E k 0 = N E k 0 = m N A M . · i k T 2 . . = i 2 . . · m M . . R T = i 2 . . ν R T = i 2 . . p V
i — степень свободы. i = 3 для одноатомного (или идеального) газа, i = 5 для двухатомного газа, i = 6 для трехатомного газа и больше.
Изменение внутренней энергии идеального газа в изопроцессах
| Основная формула | |||||||||||
| Изотермический процесс | |||||||||||
| Изобарное расширение | |||||||||||
| Изохорное увеличение давления | |||||||||||
| Произвольный процесс |
| Изобарное расширение: A ‘ = p ( V 2 − V 1 ) | 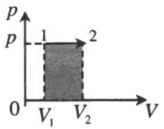 |
| Изобарное сжатие: A ‘ = p ( V 2 − V 1 ) | 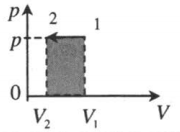 |
| Изохорное охлаждение: | 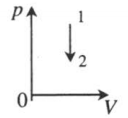 |
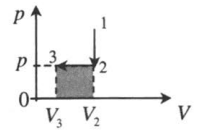 | |
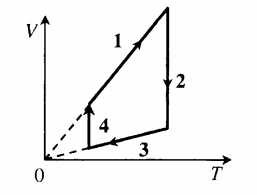
| Замкнутый цикл: 1–2: A ‘ = ( p 1 − p 3 ) ( V 2 − V 1 ) | 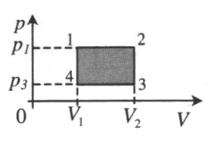 |
| Произвольный процесс: A ‘ = p 1 + p 2 2 . . ( V 2 − V 1 ) | 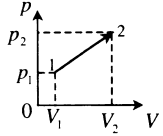 |
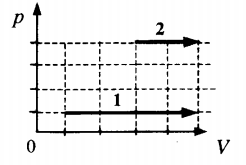
Пример №2. На pV-диаграмме показаны два процесса, проведенные с одним и тем же количеством газообразного неона. Определите отношение работ A2 к A1 в этих процессах.
Неон — идеальный газ. Поэтому мы можем применять формулы, применяемые для нахождения работы идеального газа. Работа равна площади фигуры под графиком. С учетом того, что в обоих случаях изобарное расширение, получим:
A 2 = p ( V 2 − V 1 ) = 4 p ( 5 V − 3 V ) = 4 p 2 V = 8 p V
A 1 = p ( V 2 − V 1 ) = p ( 5 V − V ) = 4 p V
Видно, что работа, совершенная во втором процессе, вдвое больше работы, совершенной газом в первом процессе.
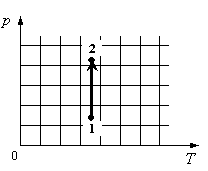
Для каждой величины подберите соответствующий характер изменения:
3) не изменяется
Запишите в таблицу выбранные цифры для каждой физической величины. Цифры в ответе могут повторяться.
Алгоритм решения
- Определить по графику, как меняется давление.
- Определить, как меняется объем.
- Определить, отчего зависит внутренняя энергия газа, и как она меняется в данном процессе.
Решение
На графике идеальный одноатомный газ изотермически сжимают, так как температура остается неизменной, а давление увеличивается. При этом объем должен уменьшаться. Но внутренняя энергия идеального газа определяется его температурой. Так как температура постоянна, внутренняя энергия не изменяется.
pазбирался: Алиса Никитина | обсудить разбор | оценить
Один моль аргона, находящийся в цилиндре при температуре T1=600 K и давлении p1=4⋅10 5 Па, расширяется и одновременно охлаждается так, что его температура при расширении обратно пропорциональна объёму. Конечное давление газа p2=10 5 Па. Какое количество теплоты газ отдал при расширении, если при этом он совершил работу A=2493 Дж?
Вычисление работы расширения идеальных газов в термодинамических процессах
Для многих термодинамических систем единственным видом работы является работа расширения газа, причем многие газы при достаточно низких давлениях и сравнительно высоких температурах приближенно подчиняются законам идеальных газов. Рассмотрим математические соотношения для вычисления работы расширения идеального газа в различных процессах.
При расширении газа совершается работа:
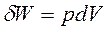
или в интегральной форме
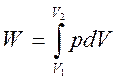
Вычисленная по уравнению (1.6) работа представляет собой максимальную работу, которую совершает газ при протекании процесса в условиях, близких к равновесным (в обратимом процессе).
Для интегрирования уравнения (1.6) необходимо знать зависимость между давлением и объемом газа, то есть уравнение состояния газа. Эта зависимость для идеального газа описывается уравнением состояния Менделеева–Клапейрона:
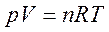
где n – количество моль идеального газа; R – универсальная газовая постоянная, равная 8,314 Дж/(моль·К).
Рассмотрим выражение для максимальной работы расширения идеального газа в пяти процессах: изобарном, изотермическом, изохорном, изобарно-изотермическом и адиабатическом.
1. Изобарный процесс (p=const).
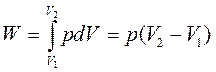
Учитывая, что 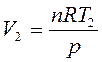
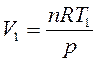
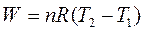
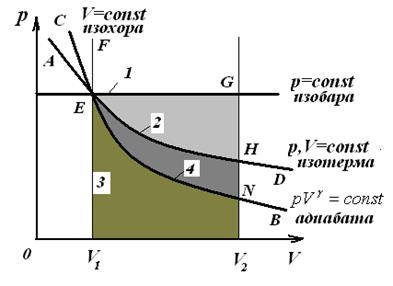
Таким образом, в изобарическом процессе работа расширения совершается при нагревании системы. Графически работу расширения в изобарном процессе можно рассчитать как площадь прямоугольника V1EGV2 (рис.1.1).
2. Изотермический процесс (Т=const).
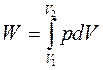
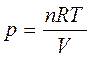
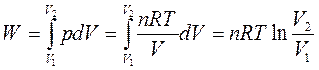
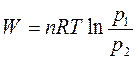
Графически изотермический процесс представляется кривой AD, а работу расширения в этом процессе – площадью V1EНV2 (рис.1.1).
3. Изохорный процесс (V=const).
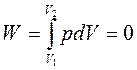
Графически изохорный процесс можно представить прямой V1EF(рис.1.1).
4. Изобарно-изотермический процесс (р, Т=const).
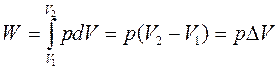
Учитывая, что 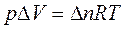
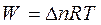
где Δn – изменение количества моль газов в результате реакции.
Таким образом, в изобарно-изотермическом процессе работа расширения совершается за счет изменения числа моль газов–участников реакции. Величина Δn может быть положительной и отрицательной, в зависимости от того увеличивается или уменьшается количество моль газов во время процесса. В системе с неизменным числом моль такой процесс невозможен.
5. Адиабатический процесс (Q = 0).
В адиабатическом процессе одновременно изменяются температура и давление газа. В связи с тем, что газ не получает теплоты извне, то работа адиабатического расширения совершается за счет уменьшения внутренней энергии системы и газ охлаждается:
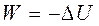
Приращение внутренней энергии зависит от молярной теплоемкости идеального газа при постоянном объеме:
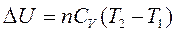
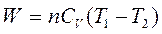
Графически адиабатический процесс представляется кривой СВ, а работу расширения в этом процессе – площадью V1ENV2 (рис.1.1).
Рис.1.1. Работа расширения идеального газа при изменении его объема (от V1 до V2 ) в изобарном (1), изотермическом (2), изохорном (3) и адиабатическом (4) процессах.
Из рис.1.1. следует, что наибольшая работа расширения будет совершаться в изобарном процессе, а наименьшая – в адиабатическом, в изохорном процессе работа расширения равна нулю.
Термохимия. Закон Гесса
Все химические и физико-химические процессы (растворение, кристаллизация, испарение, разбавление растворов и др.) сопровождаются выделением или поглощением тепла. При соблюдении определенных условий теплота процесса называется его тепловым эффектом.
Тепловой эффект химической реакции – это количество теплоты, которое выделяется или поглощается при необратимом протекании процесса, когда единственным видом работы является работа расширения. При этом температуры исходных веществ и продуктов реакции должны оставаться постоянными.
Химические уравнения с указанием тепловых эффектов химических реакций и агрегатного состояния реагирующих веществ называются термохимическими уравнениями.
Примером термохимического уравнения может служить уравнение реакции окисления угля до углекислого газа:
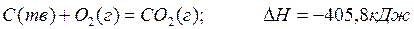
Раздел химической термодинамики, изучающий тепловые эффекты различных физико-химических процессов, называется термохимией.Основным законом термохимии является закон Гесса, который можно рассматривать как следствие первого начала термодинамики.
Закон Гесса – тепловой эффект химической реакции не зависит от пути протекания процесса, а зависит от начального и конечного состояния системы.
Это означает, что если из данных исходных веществ можно получить одни и те же конечные продукты различными путями, то, независимо от вида промежуточных реакций, суммарный тепловой эффект будет одним и тем же.
Блог об энергетике
энергетика простыми словами
Основные термодинамические процессы
Основными процессами в термодинамике являются:
- изохорный, протекающий при постоянном объеме;
- изобарный, протекающий при постоянном давлении;
- изотермический, происходящий при постоянной температуре;
- адиабатный, при котором теплообмен с окружающей средой отсутствует;
- политропный, удовлетворяющий уравнению pv n = const.
Изохорный, изобарный, изотермический и адиабатный процессы являются частными случаями политропного процесса.
При исследовании термодинамических процессов определяют:
- уравнение процесса в p—v иT—s координатах;
- связь между параметрами состояния газа;
- изменение внутренней энергии;
- величину внешней работы;
- количество подведенной теплоты на осуществление процесса или количество отведенной теплоты.
Изохорный процесс

При изохорном процессе выполняется условие v = const.
Из уравнения состояния идеального газа (pv = RT) следует:
т. е. давление газа прямо пропорционально его абсолютной температуре:
Работа расширения в изохорном процессе равна нулю (l = 0), так как объем рабочего тела не меняется (Δv = const).
Количество теплоты, подведенной к рабочему телу в процессе 1-2 при cv = const определяется по формуле:
Т. к.l = 0, то на основании первого закона термодинамики Δu = q, а значит изменение внутренней энергии можно определить по формуле:
Изменение энтропии в изохорном процессе определяется по формуле:
Изобарный процесс
Изобарным называется процесс, протекающий при постоянном давлении p = const. Из уравнения состояния идеального газа слуедует:
т. е. в изобарном процессе объем газа пропорционален его абсолютной температуре.
Работа будет равна:
Количество теплоты при cp = const определяется по формуле:
Изменение энтропии будет равно:
Изотермический процесс
При изотермическом процессе температура рабочего тела остается постоянной T = const, следовательно:
т. е. давление и объем обратно пропорциональны друг другу, так что при изотермическом сжатии давление газа возрастает, а при расширении – снижается.
Работа процесса будет равна:
Так как температура остается неизменной, то и внутренняя энергия идеального газа в изотермическом процессе остается постоянной (Δu = 0) и вся подводимая к рабочему телу теплота полностью превращается в работу расширения:
При изотермическом сжатии от рабочего тела отводится теплота в количестве, равном затраченной на сжатие работе.
Изменение энтропии равно:
Адиабатный процесс
Адиабатным называется процесс изменения состояния газа, который происзодит без теплообмена с окружающей средой. Так как dq = 0, то уравнение первого закона термодинамики для адиабатного процесса будет иметь вид:
В адиабатном процессе работа расширения совершается только за счет расходования внутренней энергии газа, а при сжатии, происходящем за счет действия внешних сил, вся совершаемая ими работа идет на увеличение внутренней энергии газа.
Обозначим теплоемкость в адиабатном процессе через cад, и условие dq = 0 выразим следующим образом:
Это условие говорит о том, что теплоемкость в адиабатном процессе равна нулю (cад = 0).
и уравнение кривой адиабатного процесса (адиабаты) в p, v-диаграмме имеет вид:
В этом выражении k носит название показателя адиабаты (так же ее называют коэффициентом Пуассона).
kвыхлопных газов ДВС = 1,33
Из предыдущих формул следует:
Техническая работа адиабатного процесса (lтехн) равна разности энтальпий начала и конца процесса (i1 – i2).
Адиабатный процесс, происходящий без внутреннего трения в рабочем теле, называется изоэнтропийным. В T, s-диаграмме он изображается вертикальной линией.
Обычно реальные адиабатные процессы протекают при наличии внутреннего трения в рабочем теле, в результате чего всегда выделяется теплота, которая сообщается самому рабочему телу. В таком случае ds > 0, и процесс называется реальным адиабатным процессом.
Политропный процесс
Политропным называется процесс, который описывается уравнением:
Показатель политропы n может принимать любые значения в пределах от -∞ до +∞, но для данного процесса он является постоянной величиной.
Из уравнения политропного процесса и уравнения Клайперона можно получить выражение, устанавливающее связь между p, vи Tв любых двух точках на политропе:
Работа расширения газа в политропном процессе равна:
В случае идеального газа эту формулу можно преобразовать:
Количество подведенной или отведенной в процессе теплоты определяется с помощью первого закона термодинамики:
представляет собой теплоемкость идеального газа в политропном процессе.
При cv, k и n = const cn = const, поэтому политропный процесс иногда определят как процесс с постоянной теплоемкостью.
Политропный процесс имеет обобщающее значение, ибо охватывает всю совокупность основных термодинамических процессов.
Графическое представление политропа в p, v координатах в зависимости от показателя политропа n.
pv 0 = const (n = 0) – изобара;
pv = const (n = 1) – изотерма;
p 0 v = const, p 1/∞ v = const, pv ∞ = const – изохора;
n > 0 – гиперболические кривые,
n По материалам моего конспекта лекций по термодинамике и учебника «Основы энергетики». Автор Г. Ф. Быстрицкий. 2-е изд., испр. и доп. — М. :КНОРУС, 2011. — 352 с.
http://lektsia.com/5×7165.html
http://energoworld.ru/theory/osnovnyie-termodinamicheskie-protsessyi/