Лекция №4
План лекции:
МЕЖФАЗНЫЕ ВЗАИМОДЕЙСТВИЯ МЕЖДУ КОНДЕНСИРОВАННЫМИ ФАЗАМИ
К межфазным взаимодействиям между конденсированными фазами относятся смачивание, растекание и адгезия.
Как правило, адгезия и смачивание сопровождают друг друга. Эти явления широко распространены в природе и в различных отраслях промышленности (нанесение лакокрасочных покрытий, получение материалов на основе связующих и наполнителей — бетон, резина и т. д.)
АДГЕЗИЯ
Адгезия — межфазное взаимодействие, или взаимодействие между приведёнными в контакт поверхностями конденсированных тел разной природы (прилипание). Адгезия обеспечивает между двумя телами соединение определенной прочности, обусловленное межмолекулярными силами.
Адгезия между — ж/ж, ж/т, т/т.
Адгезия — результат стремления системы к уменьшению поверхностной энергии, поэтому это самопроизвольный процесс. Работа адгезии Wa, характеризующая прочность адгезионной связи, определяется работой обратного разрыва адгезионной связи, отнесённой к единице площади:
W s = WаS, где Ws — полная работа адгезии (4.1)
Cоотношение между Wa и s :
Предположим, что имеется контакт между 3 фазами — 1 — газ, 2 -жидкость, 3 — твердое тело, 2, 3 — конденсированные фазы. Введем следующие обозначения поверхностных натяжений:
s 2,3 — поверхностное натяжение на границе раздела двух конденсированных фаз
s 2,1 и s 3,1 — поверхностное натяжение на границе с воздухом
Уравнение Дюпре отражает закон сохранения энергии при адгезии. Из него следует, что работа адгезии тем больше, чем больше поверхностные натяжения исходных компонентов и чем меньше конечное межфазное натяжение.
Уравнение 4.2 справедливо только для изобарно-изотермического процесса в отсутствии электрического и химического взаимодействия между контактирующими телами, его используют только для определения равновесной работы адгезии жидкости.
Равновесную работу адгезии можно сопоставить с равновесной работой когезии. Когезия — определяет связь между молекулами внутри тела и в пределах одной фазы, характеризует прочность конденсированных тел и их способность противодействовать внешнему усилию.
Механизм адгезии
Первая стадия — транспортная, перемещение адгезива (клеящего вещества) к поверхности субстрата (тело, на которое наносят адгезив) и их определенное ориентирование в межфазном слое.
Вторая стадия — взаимодействие адгезива и субстрата, обусловлено различными силами (от ван-дер-ваальсовых до химических).
Завершается процесс адгезии межмолекулярным взаимодействием контактирующих фаз, что соответствует минимальной поверхностной энергии. Различают несколько механизмов (и, соответственно, теорий) в зависимости от природы взаимодействующих тел и условий, при которых происходит адгезия.
1.Механическая адгезия — осуществляется путем затекания в поры и трещины поверхности твердого тела жидкого адгезива., который потом затвердевает, обеспечивая механическое зацепление.
2.Молекулярная (адсорбционная) адгезия — возникает под действием межмолекулярных ван-дер-ваальсовых сил и водородных связей.
3.Электрическая теория — связана с образованием ДЭС на границе раздела между адгезивом и субстратом.
4.Диффузионный механизм — предусматривает взаимное проникновение молекул и атомов в поверхностные слои взаимодействующих фаз.
Чаще всего механизм адгезии является смешанным.
Теоретическая оценка адгезии очень приближённа, т. е., механизм её недостаточно изучен.
СМАЧИВАНИЕ
Смачивание — это поверхностное явление, заключающееся во взаимодействии жидкости с твёрдым или другим жидким телом при наличии контакта трех несмачивающихся фаз, одна из которых воздух.
Степень смачивания количественно характеризуется косинусом краевого угла (угла смачивания) или просто краевым углом (углом смачивания).
Рис.4.2. К выводу уравнения для краевого угла (закон Юнга).
Рис.4.2. иллюстрирует состояние капли жидкости на поверхности твердого тела в условиях равновесия. Поверхностная энергия твердого тела, стремясь уменьшиться, вызывает растяжение капли по поверхности. Эта энергия равна поверхностному натяжению твердого тела на границе с воздухом s 3,1 .Межфазная энергия на границе твердого тела с жидкостью s 2,3 стремится сжать каплю. Растеканию препятствуют когезионные силы, действующие внутри капли. Действие когезионных сил направлено от границы между твердой, жидкой и газообразной фазами по касательной к сферической поверхности капли и равно s 2,1 .Угол q — краевой угол или угол смачивания.
Чем меньше краевой угол , тем лучше смачивание поверхности.
Если cos( q )>0 , то поверхность хорошо смачиваемая, cos( q )
Если разность s 3,1 — s 2,3 в уравнении Дюпре заменить её выражением из закона Юнга, то
Wa/ s 2,1 = 1+ cos( q ) — уравнение Дюпре-Юнга (4.5)
4.3, 4.4, 4.5 — только для идеально гладких тел. На поверхности реальных тел есть поры, трещины, и т. д.
Рассмотрим кинетический катерезис, который замедляет достижение равновесной формы капли.
Рис.4.3.Статические углы натекания и оттекания.
Для реальных тел: равновесный угол смачивания равен полусумме предельных углов натекания и оттекания:
cos( q ) = (cos( q нт ) + сos( q от ))/2 (4.6)
Влияние шероховатости на кривой угол:
k = cos( q ш )/cos( q ) , где к — коэфф. шероховатости
При повышении степени шероховатости смачиваемость улучшается.
РАСТЕКАНИЕ
Капля жидкости, нанесенная на поверхность, может оставаться на ее определенном участке, и система будет находится в равновесии в соответствии с законом Юнга, или же растекаться по поверхности. В обоих случаях система переходит в состояние с минимальной энергией Гиббса.
Из этого соотношения следует, что уменьшение межфазного натяжения s 2,3 (увеличение работы адгезии) и поверхностного натяжения жидкости s 2,1 , способствует растеканию жидкости.
Растекание происходит в том случае, если работа адгезии превышает работу когезии.
Способность жидкости растекаться зависит от когезии наносимых на поверхность жидкостей.
С повышением температуры увеличивается работа адгезии, поэтому нерастекающаяся жидкость с увеличением температуры может начать растекаться.
2.3.2. Смачивание и растекание на границе твердое тело – жидкость – газ
В большинстве случаев жидкость на поверхности твердого тела остается в виде капли, большей или меньшей толщины, контактирующей с твердым телом под определенным углом, который называется краевым углом смачивания и обозначается буквой Q (рис. 1.24). Растекание капли по поверхности прекратится при достижении равновесия, которое без учета сил тяжести может быть описано уравнением Юнга:

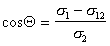
где индексы 1, 2, 3 – обозначают, соответственно, твердую, жидкую и газовую фазы.
Работа адгезии выражается уравнением Дюпре:
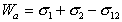
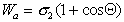
Рис. 1.24. Капля жидкости на поверхности твердого тела (схема)
Работа адгезии при 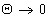
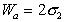
Следует помнить, что определение работы адгезии в реальных системах предполагает равновесие фаз, насыщенных относительно друг друга.
Кроме того, твердая поверхность, по которой происходит растекание жидкости, не свободна. Она обычно покрыта пленкой вещества, адсорбированного из газо-паровой фазы. Эта пленка имеет поверхностное давление p, поэтому
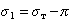
Смачивание неоднородных, пористых или шероховатых поверхностей сопровождается запиранием пузырьков воздуха в неровностях. В результате этого краевые углы смачивания сухой и предварительно увлажненной поверхностей различаются. Такое явление носит название «гистерезис смачивания». Гистерезис смачивания проявляется также при загрязнении поверхности, в результате чего она становится неоднородной при закреплении на ней твердых частиц или жировых пленок. В этом случае поверхность ведет себя как составная.
Шероховатость поверхности учитывается введением коэффициента шероховатости r, представляющего отношение площади поверхности реального тела к площади идеально гладкой поверхности, тогда
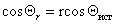
Можно отметить, что если краевой угол смачивания гладкой поверхности, например полимерной пленки, меньше 90 o , то шероховатость (ткань из волокон этого полимера) уменьшает его, если же он больше 90 o , то шероховатость его увеличивает. Для составной поверхности, которая специфична для большинства текстильных материалов, наличие участков различной природы может быть учтено введением коэффициентов x, характеризующих долю поверхности с различными свойствами. Например, если текстильный материал изготовлен из волокон двух видов 1 и 2, то
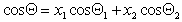
Если переплетение нитей таково, что получается сетчатый или дырчатый материал, то уравнение (2.50) принимает вид
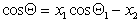
где х2 – доля открытой поверхности.
Как мы обсуждали выше, поверхностное натяжение можно разделить на компоненты дисперсионных и полярных сил, а при нахождении межфазового натяжения для многих жидких границ можно ограничиться лишь дисперсионной составляющей. Такое ограничение позволяет провести обсуждение явления смачивания (по крайней мере, низкоэнергетических поверхностей, к каковым можно отнести подавляющее большинство волокнообразующих полимеров), в рамках теории дисперсионных сил.
Как показал Н. В. Чураев смачивание неполярной жидкостью твердой поверхности возможно, если будет соблюдаться условие смачивания, которое выражается уравнением
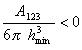
где А123 – составная постоянная Гамакера при взаимодействии жидкости (фаза 2) с твердым телом (фаза 1) на границе с воздухом (фаза 3); hmin — наименьшая толщина пленки, которая фактически соответствует Ван-дер-Ваальсову расстоянию, т.е. hmin = (0,22¸0,24) нм. Например, для воды на поверхности тефлона А123 = -7·10 — 21 Дж.
Учет только дисперсионных сил приводит к уравнению
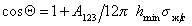
При расчетах углов смачивания твердых поверхностей следует учитывать поверхностное давление пленки, образованной при адсорбции из газо-паровой фазы. Тогда с учетом уравнения (1.2.48), уравнение Юнга (1.2.45) следует записать в виде
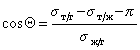
Способ расчета поверхностного давления предложили Бэнгхэм и Разорук:
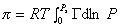
где P – равновесное давление, Г– равновесная адсорбция газа (пара), Ps – давление насыщения.
При больших углах смачивания и слабом взаимодействии жидкости с твердым телом поверхностное давление обычно не учитывают.
Для неполярных жидкостей на низкоэнергетической поверхности твердого тела для работы адгезии было получено выражение
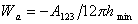
Поэтому уравнение Дюпре (1.2.46) можно записать
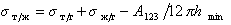
Для дисперсионной составляющей жидкости
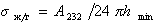
где А232 – постоянная Гамакера взаимодействия жидкости через прослойку газа (пара).
Сочетая уравнения (1.2.47), (1.2.55) и (1.2.56), получаем
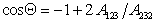
Очевидно, что Q = 0, т.е. при полном смачивании, cosQ = 1, если
Уравнение (1.2.57) позволяет прогнозировать вероятность смачивания (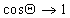
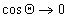
Чаще, однако, прибегают к определению постоянной Гамакера по известному значению межфазового натяжения на границе «твердое тело — газ». Эту характеристику поверхности твердого тела находят при распространении подхода Джирифалько и Гуда, рассмотренного нами выше для границы двух жидкостей, на поверхность раздела «жидкость — твердое тело», уравнения (1.2.23), (1.2.35).
Так приложение уравнения (1.2.34) к уравнению Юнга для случая смачивания неполярной жидкостью поверхности полимерного материала позволяет получить уравнение, известное как уравнение Фоукса, при
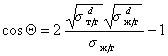
Если жидкости неполярны и 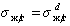
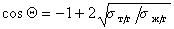
Уравнение (1.2.59) Зисман предложил использовать для определения поверхностного натяжения твердых тел. Очевидно, что при 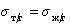
Естественно, что метод Зисмана ограничен некоторыми условиями, в частности, из уравнения (1.2.57) следует, что полное смачивание возможно при дисперсионной неразличимости твердого тела и жидкости, т.е. при А232= А123.
В действительности такого условия никогда невозможно достигнуть хотя бы потому, что если жидкость и твердое тело будут иметь одинаковый химический состав, их постоянные Гамакера будут различаться из-за различий в плотности.
Другое ограничение, связанное с применением метода Зисмана, основано на том, что использовать для измерения краевых углов смачивания следует лишь неполярные жидкости. Наиболее целесообразно применять гомологические ряды жидкостей. При величине поверхностного натяжения жидкостей более 35 мДж/м 2 метод Зисмана уже дает высокую погрешность, так как необходимо учитывать вклад полярных сил, которые в отличие от дисперсионной составляющей могут иметь и отрицательное значение. С другой стороны, приложение для смачивания твердых тел полярными жидкостями уравнения Ву (1.2.36) позволяет рассчитать полярную составляющую поверхностного натяжения жидкости, если для одной из неполярных жидкостей измерить краевой угол смачивания. Для расчета используют уравнение
Рис. 1.25. Зависимость смачивания поверхностей от поверхностного натяжения жидкостей. Материал поверхности: 1- FC-721; 2- ПТФЭ (тефлон); 3 — полиэтилен
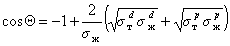
Этот метод позволил разделить величину поверхностного натяжения жидкостей на полярную и дисперсионную компоненты и определить поверхностное натяжение многих волокнообразующих полимеров.
Пример зависимости косинуса угла смачивания поверхности пленок различными жидкостями приведен на рис.1.25. Для описания этих зависимостей Зисман предложил использовать эмпирическое уравнение
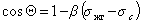
где bэмпирическая постоянная, sс – «критическое» поверхностное натяжение твердого тела, при котором происходит полное смачивание твердого тела жидкостью. Очевидно, что cos Q =1 при условии sжг = sс .
Как мы обсуждали выше, этот критерий в известной мере является условным, хотя и отражает энергетическое состояние поверхности твердого тела.
Реальное значение поверхностного натяжения твердого тела экспериментально определить невозможно, также как и рассчитать его теоретически. В этой связи метод Зисмана нашел широкое применение в практике исследования полимерных материалов, а также полимерных покрытий тканей, используемых в качестве отделочных материалов
Смачивание и растекание жидкостей
Смачивание – это поверхностное явление, заключающееся во
взаимодействии жидкости с твердым или другим жидким телом при наличии одновременного контакта трех несмешивающихся фаз, одна из которых обычно является газом (воздухом).
При нанесении капли жидкости на поверхность твердого тела (или другой жидкости) можно наблюдать разные явления. В одном случае нанесенная жидкость сохраняет форму капли, в другом случае капля растекается по поверхности. Рассмотрим первый случай (рис. 9.10)
 |
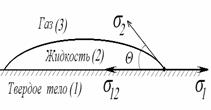
Рис. 9.10 Смачивание жидкостью твердого тела
Линия соприкосновения трех фаз называется периметром смачивания. Угол q называется краевым углом смачивания. Он отсчитывается со стороны жидкости. Поскольку капля находится в состоянии равновесия, действие сил на нее скомпенсировано. Рассмотрим эти силы. Как известно, силы поверхностного натяжения направлены на сокращение площади контакта фаз по касательной к поверхности. На рис. 9.10 эти силы представлены векторами, выходящими из точки соприкосновения всех трех фаз 0.
sТ-Г – стремиться уменьшить площадь контакта твердого тела с газом, поэтому растягивает пленку жидкости по твердому телу.
sТ-Ж – стремится уменьшить площадь контакта твердого тела с жидкостью, поэтому стягивает каплю жидкости в шарик.
sЖ-Г – стремится уменьшить площадь контакта жидкости с газом, поэтому стягивает каплю жидкости в шарик (шарообразная поверхность имеет наименьшую площадь).
Рассмотрим равнодействующую сил, действующих на каплю в точке 0 вдоль поверхности твердого тела. Это силы поверхностного натяжения sТ-Г, sТ-Ж, а также проекция sЖ-Г на выбранную ось

В состоянии равновесия равнодействующая сил равна 0:
Полученное соотношение (9.16) называется законом Юнга.
Краевой угол смачивания q или cosq являются количественной характеристикой смачивания. Чем меньше угол q и соответственно больше cosq, тем лучше смачивается поверхность.
Закон Юнга позволяет выразить cosq через поверхностные межфазные натяжения:

Сочетание уравнения Дюпре (9.15) с законом Юнга (9.16) позволяет выразить работу адгезии Wa через косинус краевого угла смачивания q.
Из уравнения (9.16) выразим разность
Полученную разность подставим в уравнение 9.15
Уравнение (9.18) называют уравнением Дюпре — Юнга. Оно позволя-ет рассчитать работу адгезии, если известно поверхностное натяжение жидкости и краевой угол смачивания. Обе эти величины сравнительно легко определяются экспериментально: q – путем проектирования капли на экран (с помощью несложной установки) и измерения краевого угла на проекции капли. С помощью уравнения Дюпре – Юнга (9.18) легко найти соотношение между работой когезии смачивающей жидкости и работой адгезии между жидкостью и смачиваемым телом.
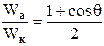
или
С использованием полученных соотношений рассмотрим возможные случаи поведения капли жидкости на твердой поверхности (или на другой жидкости) (табл. 9.4)
Как видно из табл. 9.4 предельным случаем смачивания является растекание жидкости по поверхности, которое наблюдается при нулевом краевом угле смачивания.
Растекание жидкостей по поверхности
Особо остановимся на предельном случае смачивания – растекании жидкости по поверхности, которое наблюдается при q = 0 0 (см. табл. 9.4), когда работа адгезии равна работе когезии (Wa = Wк). Очевидно, что чем больше преобладает работа адгезии над работой когезии, тем лучше будет растекаться жидкость по поверхности. Величина
называется коэффициентом растекания или критерием Гаркинса.
Если f > 0 – жидкость растекается (Wa > Wк)
Если f
Гидрофильность и гидрофобность поверхностей имеет огромное значение в природе, в технологических процессах. Процессами гидрофилизации и гидрофобизации поверхности можно управлять, нанося специальные покрытия (лакокрасочные) или обрабатывая поверхность растворами поверхностно — активных веществ.
В табл. 9.5 приведены значения краевых углов смачивания для некоторых веществ.
Краевые углы смачивания водой некоторых веществ
| Вещество | q | Вещество | q | Вещество | q |
| Кварц | 0 0 | Графит | 55 0 | Парафин | 106 0 |
| Малахит | 17 0 | Тальк | 69 0 | Фторопласт | 108 0 |
Из веществ, приведенных в таблице, гидрофильными свойствами обладают: кварц, малахит, графит, тальк, а гидрофобными – парафин и фторопласт.
Процесс растекания зависит от соотношения работ адгезии и когезии, а те в свою очередь определяются величинами поверхностного натяжения на границе раздела разных фаз.
На основе изложенного можно сделать некоторые общие выводы:
1.Процесс растекания зависит как от s поверхности, по которой происходит растекание, так и от s жидкости, которая растекается.
2.Поверхности, по которым происходит растекание делятся на высокоэнергетические и низкоэнергетические.
Критерии смачивания, несмачивания и
| Несмачивание жидкостью поверхности q > 90 0 (тупой угол) | Смачивание жидкостью поверхности q 0 (острый угол) |
 | |
| предельные случаи | |
| 1) q = 180 0 (полное несмачивание, на практике не встречается) cos180 0 = -1 Wa = 0 | 1) q = 0 0 (полное смачивание, т.е. растекание) cos0 0 = 1 Wa = Wк |
| 2) q = 90 0 (неполное смачивание) cos90 0 = 0 Wa = 1/2Wк | 2) q = 90 0 (неполное смачивание) cos90 0 = 0 Wa = 1/2Wк |
| в общем виде | |
| 90 0 0 -1 0 0 0 2 . s таких поверхностей зависит от твердости и точки плавления веществ (табл. 9.4). Примерами таких веществ служат металлы, оксиды металлов, соли, кварц, стекло, рубин, алмаз. Стремление к понижению свободной поверхностной энергии в таких телах очень велико. Выигрыш в энергии от того, что эта поверхность будет модифицирована за счет адсорбции или просто покрыта другой жидкостью, обычно больше, чем свободная поверхностная энергия большинства органических и неорганических жидкостей на границе их с паром. Поэтому жидкости смачивают высокоэнергетические поверхности и полностью растекаются на них. Например, по поверхности жидкой ртути (s = 475 мДж/м 2 ) растекаются практически все жидкости. Однако, если ртуть загрязнена, то растекание не происходит, вода, например, скатывается в шарики. Это один из приемов проверки чистоты ртути. б) Низкоэнергетические поверхности имеют значение s 2 . Это твердые полимеры, органические соединения, оксиды неметаллов, поверхность воды. Значения s для таких поверхностей соизмеримы с таковыми для органических и неорганических жидкостей. Поэтому в данном случае смачивание и несмачивание будет зависеть от соотношения поверхностных натяжений жидкости и поверхности. Можно отметить, что самые низкоэнергетические поверхности (фторопласты, парафины) не смачиваются большинством жидкостей. 3.Растекающиеся жидкости имеют разное значение поверхностного натяжения. Чем выше значение s, тем выше работа когезии (см. 9.4) и тем хуже растекаются такие жидкости. Чем ниже s, тем меньше работа когезии и тем легче растекаются жидкости. Например, вода, обладающая высоким значением s (72 мДж/м 2 ), плохо растекается по разным поверхностям, в то время как углеводороды (бензин, гексан, бензол, s от 18 до 30), растекаются практически по любым поверхностям. Например, нефть растекается по воде, образуя пятна огромной площади; а вода по нефти не растекается, собирается в капли. Это связано с тем, что sводы > sнефти примерно в 3 раза. Поскольку работы адгезии и когезии определяются величинами поверхностных натяжений на границах раздела фаз, то, изменяя значения s введением различных веществ в жидкость или модифицируя поверхность обработкой различными композициями, можно обеспечить перевод процесса несмачивания в смачивание, а смачивания в растекание и наоборот. Капиллярные явления Капиллярные явления наблюдаются в капиллярах и капиллярно-пористых телах, содержащих жидкость. Капиллярные явления заключаются в поднятии или опускании уровня жидкости в капиллярах по сравнению с уровнем жидкости в сосуде, в который опущены эти капилляры (рис. 9.11 и 9.12). Капиллярное поднятие или опускание жидкостей связано с возникновением кривизны поверхности (выпуклый или вогнутый мениск). В свою очередь появление кривизны поверхности связано с процессами смачивания (q 0 , вогнутый мениск) или несмачивания (q > 90 0 , выпуклый мениск) жидкостями стенок капилляров. Давление в фазах, разделенных искривленной поверхностью, отличается от давления в фазах с плоской поверхностью. Причиной возникновения давления является действие сил поверхностного натяжения, которые стремятся уменьшить площадь поверхности раздела фаз (выпрямить ее), Силы эти направлены вдоль поверхности, а равнодействующая этих сил (sр) будет направлена к центру кривизны поверхности (рис. 9.13) Рис. 9.11. Капиллярное поднятие жидкости r0 – радиус капилляра; r – радиус кривизны поверхности жидкости (мениска); q – краевой угол смачивания, q 0 ; h – высота поднятия жидкости.
Рис. 9.12. Отрицательное капиллярное поднятие жидкости, q > 90 0 Рис. 9. 13. Схема, иллюстрирующая возникновение капиллярного Возникающее дополнительное давление Dр, называемое капил-лярным давлением, в одном случае будет направлено вниз и будет способствовать опусканию уровня жидкости (рис. 9.13,а), в другом случае будет направлено вверх и вызовет поднятие жидкости в капиллярах (рис. 9.13,в). Надо отметить, что капиллярные явления возникают только в капиллярах, радиус которых соизмерим с радиусом кривизны поверхности. В широких трубках такие явления не возникают. Для поверхности, имеющей форму правильной сферы: где Dр – капиллярное давление; s – поверхностное натяжение жидкости; r – радиус кривизны поверхности. Для цилиндрической поверхности (возникающей при опускании двух параллельных пластин в жидкость, когда расстояние между пластинами мало) длиной l и радиусом r: Уравнения (9.21) и (9.22) известны под названием уравнений Лапласа. Из них следует, что, чем выше значение s и меньше радиус кривизны, тем выше возникающее давление. При равновесии лапласовское давление равно гидростатическому давлению столба жидкости высотой h (рис. 9.11 и 9.12) Dр = ± 2s/r = (r – r0)gh, (9.23) где r – плотность жидкости; r0 – плотность насыщенного пара; g – ускорение свободного падения; r – радиус кривизны (мениска). Если выразить радиус кривизны через радиус капилляра и краевой угол смачивания, то получим r0 = r cosq ® Из уравнения 9.23 и 9.24 для высоты капиллярного поднятия h получим выражение Уравнение 9.25 называется формулой Жюрена. Эта формула значительно упрощается для случая, когда краевой угол q близок к 0 0 (если жидкость растекается по поверхности). Такой случай реализуется для воды и углеводородов в стеклянных капиллярах. Тогда получим упрощенное выражение Из этой формулы следует, что чем выше s и меньше радиус капилляра, тем выше капиллярное поднятие. Эта формула используется при определении величины поверхностного натяжения жидкости. Капиллярным поднятием жидкостей объясняется ряд известных явлений и процессов. Пропитка бумаги, тканей обусловлена капиллярным поднятием жидкостей в порах; водонепроницаемость тканей обеспечивает-ся их гидрофобностью и как следствие – отрицательным капиллярным поднятием; подъем воды из почвы по стволам растений происходит благодаря волокнистому строению древесины; капиллярными явлениями обусловлены процессы кровообращения в кровеносных сосудах; процессы адсорбции на мелкопористых сорбентах, которые сопровождаются капиллярной конденсацией. Подъем глубинных вод в грунтах и почвах обеспечивает влагой растительность. Для предотвращения высыхания почвы (испарения воды с поверхности) проводят рыхление (боронование) с целью разрушения капилляров и трещин, по которым поднимается влага. Интересным примером проявления капиллярного давления может служить возникновение капиллярной стягивающей силы между частицами, пластинками при наличии между ними прослойки жидкости с вогнутым мениском (при хорошем смачивании частиц жидкостью). Например, сухой песок – сыпучее вещество. При небольшом увлажнении песок хорошо формуется, т.к. между частицами возникают капиллярные силы, стягивающие частицы. При сильном увлажнении песок расплывается, т.к. между частицами исчезает мениск, частицы со всех сторон окружены жидкостью. Еще один пример капиллярного стягивания – это «прилипание» друг к другу стеклянных пластинок, между которыми находится очень тонкая прослойка воды (одна капля). Такие пластинки очень трудно оторвать друг от друга. источники: http://xumuk.ru/colloidchem/35.html http://lektsia.com/5x38bb.html |


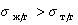
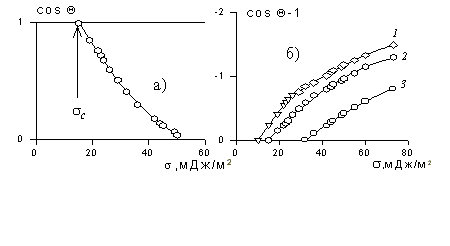





 (9.24)
(9.24) (9.25)
(9.25)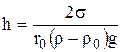 (9.26)
(9.26)