25*. Составьте уравнения электролиза водных растворов следующих веществ: а) Ва(ОН)2, б) SrCl2, в) CuCl2, г) HCl, д) Cr(NO3)3. Анод нерастворимый.
25*. Составьте уравнения электролиза водных растворов следующих веществ: а) Ва(ОН)2, б) SrCl2, в) CuCl2, г) HCl, д) Cr(NO3)3. Анод нерастворимый.

задача №25
к главе «Глава 4. Вещества и их свойства. §18. Металлы».
Выделите её мышкой и нажмите CTRL + ENTER
Большое спасибо всем, кто помогает делать сайт лучше! =)
Нажмите на значок глаза возле рекламного блока, и блоки станут менее заметны. Работает до перезагрузки страницы.
Электролиз растворов и расплавов солей и окислительно-восстановительные реакции (стр. 3 )
 | Из за большого объема этот материал размещен на нескольких страницах: 1 2 3 4 5 6 7 8 |
Электролиз растворов нитрита и сульфита натрия на инертных
электродах без диафрагмы.
В нитрит — и сульфит-ионах атомные частицы N+3 и S+4 занимают промежуточные степени окисления. Поэтому при прохождении постоянного электрического тока через водные растворы нитрита и сульфита натрия можно ожидать окисления на аноде нитрит — и сульфит-ионов и восстановление на катоде молекул воды.
КNO2 (р) = К+ + NO2- , H2O ↔ ОН — + H+
К2SO3 = 2К+ + SO32-, H2O ↔ ОН — + H+

NO2- + 3H2O = H2 + NO3- + 2Н+ + 2ОН —
Так как электролиз ведут без диафрагмы, то имеет место процесс нейтрализации Н+ + ОН — = H2O. Тогда в окончательном виде получим:
КNO2 + H2O = H2 + КNO3
Возможен и другой механизм анодного окисления:
1) вода окисляется по схеме
2H2O − 4ē = О2 + 4Н+
2) затем протекает процесс окисления NO2- кислородом:
Так как нитрит калия в водном растворе подвергается гидролизу по первой ступени, создается щелочная среда, процесс окисления на аноде необходимо записать следующим образом:
NO2- + 2ОН — − 2ē = NO3- + H2O
(недостаток кислорода в левой части восполняют за счет ОН- — ионов, а недостаток водорода в правой части — за счет молекул воды).
С учетом этого составим электродные процессы:

NO2- + H2O = H2 + NO3-
В окончательном молекулярном виде получим то же, что и при рН =7:
КNO2 + H2O = H2 + КNO3
Процесс окисления на аноде при рН > 7 можно представить и так:
1) ОН — — ионы окисляются с образованием кислорода:
4ОН — − 4ē = О2 + 2H2O
2) затем нитрит-ионы окисляются кислородом:
Аналогичным образом можно записать электролиз раствора К2SO3:
катод: 2H2O + 2ē = H2 + 2ОН — 1
К2SO3 + H2O = H2 + К2SO4
Возможный процесс окисления на аноде при рН = 7 можно представить и так:
1) окисление воды:
2H2O − 4ē = О2 + 4Н+
2) сульфит-ионы окисляются кислородом:
2SO32- + О2 = 2SO42-
 В случае щелочной среды имеем:
В случае щелочной среды имеем:
катод: 2H2O + 2ē = H2 + 2ОН — 1
В общем виде: SO32- + H2O = H2 + SO42-
К2SO3 + H2O = H2 + К2SO4
Возможные процессы окисления на аноде при рН > 7:
1) 4ОН — − 4ē = О2 + 2H2O
2) 2SO32- + О2 = 2SO42-

анод: MnO42- − 1ē = MnO4- 2
2K2MnO4 + 2H2O = 2KMnO4 + H2↑ + 2КОН
Электролиз водного раствора гидроксида натрия на инертных
электродах с диафрагмой
На катоде восстанавливаются молекулы воды, а на аноде окисляются гидроксид-ионы:


Вывод. Путем электролиза растворов щелочей можно получать как газообразный водород, так и кислород, электролиз без диафрагмы проводить опасно, из-за возможности образования «гремучей» смеси.
Серная кислота сильна только по первой стадии диссоциации:
По второй стадии диссоциации она считается кислотой средней силы:
В результате этого на электродах идут следующие процессы:

анод: 2HSO4- −2ē = H2S2O8 1
 |
В общем виде: 2HSO4- + 2Н+ = H2↑ + H2S2O8
2H2SO4 = H2↑ + H2S2O8
Электролиз по такой схеме возможен при больших плотностях тока.
1) КHSO4 = К+ + HSO4-

анод: 2HSO4- -2ē = H2S2O8 1
 |
2HSO4- + 2H2O = H2↑ + H2S2O8 + 2OH — или
2КHSO4 + 2H2O = H2↑ + H2S2O8 + 2КOH
3) H2S2O8 + 2КOH = К2S2O8↓ + 2H2O
2КHSO4 = К2S2O8↓ + H2↑
Электролиз по такой схеме возможен при больших плотностях тока.
Электролиз водного раствора соли Cr2(SO4)3 на инертных электродах
Cr2(SO4)3 = 2Сr3+ + 3SO42-

2H2O + 2ē = H2↑ + 2ОН — 4 при рН =7

В общем виде: 2Cr2(SO4)3(p) + 10H2O → 4Cr + 5O2↑ + 4H2↑ + 6H2SO4
Процесс электролиза иногда упрощенно записывают без учета восстановления воды на катоде, так как количество электричество, расходуемое при этом незначительно:
2Cr2(SO4)3(p) + 6H2O → 4Cr + 3O2↑ + 6H2SO4
Если учесть гидролиз соли Cr2(SO4)3 , то на катоде вместо восстановления воды необходимо записывать процесс восстановления ионов водорода, при этом окончательная реакция электролиза не будет отличаться от написанного.
Получение ферратов анодным окислением железа в щелочном

катод: 2H2O + 2ē = H2↑ + 2ОН — 3

В растворе: Fe+6 + 4ОН — = FeО42- + 4Н+
Суммарные электродные процессы:


В окончательном виде: Feo + 2H2O + 2ОН — = FeО42- + 3H2↑
Feo + 2H2O + 2КОН = К2FeО4 малиновый + 3H2↑
Марганец можно получить электролизом раствора MnSO4:
2MnSO4(р) + 2H2O = 2Mn↓катод + O2↑ анод + 2H2SO4
Хром можно получить электролизом раствора Cr2(SO4)3
2Cr2(SO4)3(p) + 6H2O → 4Cr + 3O2↑ + 6H2SO4


2H+ + 2HSO4- = H2↑ + H2S2O6(O2) ,
2) затем идет реакция:
H2S2O6(O2) + 2NH4+ = (NH4)2S2O6(O2)↓ + 2H+,
3) далее проводят гидролиз:
(NH4)2S2O6(O2) + 2H2O = 2NH4HSO4 + H2O2
II. Электролиз расплавов солей
Необходимо помнить, что при плавлении солей и щелочей происходит их электролитическая диссоциация. Если теперь через такой расплав электролита пропустить постоянный электрический ток, катионы перемещаются к катоду и восстанавливаются, а анионы окисляются на аноде.
На катоде катионы металлов восстанавливаются по схеме:
Окисление кислородсодержащих анионов на аноде протекает сложнее, чем бескислородных:
4ОН — − 4ē = О2 + 2Н2О, 2SO42- −4ē = 2SO3 + O2o,
2CO32- −4ē = 2CO2 + O2o, 2NO3- −2ē = 2NO2 + O2o
2SO32- −4ē = 2SO2 + O2o, 2PO43- −4ē = 2PO3- + O2o
Электролизом расплавов соответствующих солей или их гидроксидов получают металлы: щелочные и щелочноземельные, магний, медь, алюминий и др.
Электрохимический способ получения фтора в расплавах:
1) HF + KF, при 70-100 оС;
2) HF в расплаве KH2F3 , при 80-120 оС
3) HF в расплаве KHF2 , при 240-300 оС
Электролизу подвергается во всех случаях HF:
1) в расплаве происходит электролитическая диссоциация и
3HFрасплав ↔ H2F+ + HF2- (автопротолиз) (1)
2) электродные процессы:


2H2F+ + 2HF2- = F2о + H2о + 4HFо
2HF(расплав) = H2 + F2
Электролиз расплава гиидроксида натрия
NaOH(расплав) = Na+ + ОН —


Электролиз
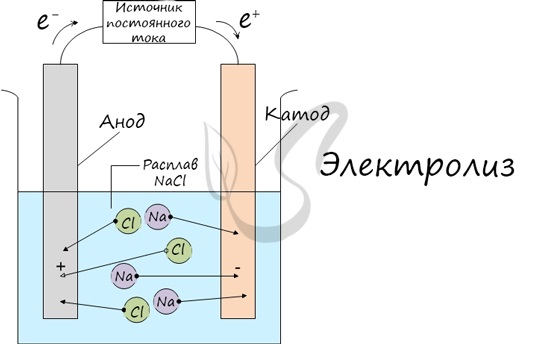
Электролиз (греч. elektron — янтарь + lysis — разложение) — химическая реакция, происходящая при прохождении постоянного тока через электролит. Это разложение веществ на их составные части под действием электрического тока.
Процесс электролиза заключается в перемещении катионов (положительно заряженных ионов) к катоду (заряжен отрицательно), и отрицательно заряженных ионов (анионов) к аноду (заряжен положительно).
Итак, анионы и катионы устремляются соответственно к аноду и катоду. Здесь и происходит химическая реакция. Чтобы успешно решать задания по этой теме и писать реакции, необходимо разделять процессы на катоде и аноде. Именно так и будет построена эта статья.
Катод
К катоду притягиваются катионы — положительно заряженные ионы: Na + , K + , Cu 2+ , Fe 3+ , Ag + и т.д.
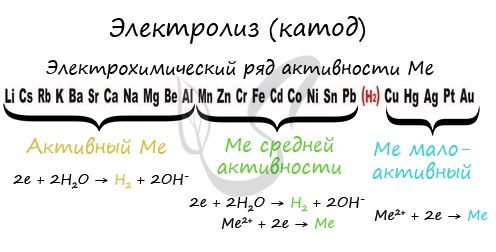
Чтобы установить, какая реакция идет на катоде, прежде всего, нужно определиться с активностью металла: его положением в электрохимическом ряду напряжений металлов.
Если на катоде появился активный металл (Li, Na, K) то вместо него восстанавливаются молекулы воды, из которых выделяется водород. Если металл средней активности (Cr, Fe, Cd) — на катоде выделяется и водород, и сам металл. Малоактивные металлы выделяются на катоде в чистом виде (Cu, Ag).
Замечу, что границей между металлами активными и средней активности в ряду напряжений считается алюминий. При электролизе на катоде металлы до алюминия (включительно!) не восстанавливаются, вместо них восстанавливаются молекулы воды — выделяется водород.
В случае, если на катод поступают ионы водорода — H + (например при электролизе кислот HCl, H2SO4) восстанавливается водород из молекул кислоты: 2H + — 2e = H2
К аноду притягиваются анионы — отрицательно заряженные ионы: SO4 2- , PO4 3- , Cl — , Br — , I — , F — , S 2- , CH3COO — .
При электролизе кислородсодержащих анионов: SO4 2- , PO4 3- — на аноде окисляются не анионы, а молекулы воды, из которых выделяется кислород.
Бескислородные анионы окисляются и выделяют соответствующие галогены. Сульфид-ион при оксилении окислении серу. Исключением является фтор — если он попадает анод, то разряжается молекула воды и выделяется кислород. Фтор — самый электроотрицательный элемент, поэтому и является исключением.
Анионы органических кислот окисляются особым образом: радикал, примыкающий к карбоксильной группе, удваивается, а сама карбоксильная группа (COO) превращается в углекислый газ — CO2.
Примеры решения
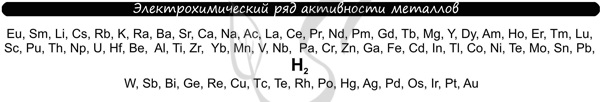
В процессе тренировки вам могут попадаться металлы, которые пропущены в ряду активности. На этапе обучения вы можете пользоваться расширенным рядом активности металлов.
Теперь вы точно будете знать, что выделяется на катоде 😉
Итак, потренируемся. Выясним, что образуется на катоде и аноде при электролизе растворов AgCl, Cu(NO3)2, AlBr3, NaF, FeI2, CH3COOLi.
Иногда в заданиях требуется записать реакцию электролиза. Сообщаю: если вы понимаете, что образуется на катоде, а что на аноде, то написать реакцию не составляет никакого труда. Возьмем, например, электролиз NaCl и запишем реакцию:
NaCl + H2O → H2 + Cl2 + NaOH (обычно в продуктах оставляют именно запись «NaOH», не подвергая его дальнейшему электролизу)
Натрий — активный металл, поэтому на катоде выделяется водород. Анион не содержит кислорода, выделяется галоген — хлор. Мы пишем уравнение, так что не можем заставить натрий испариться бесследно 🙂 Натрий вступает в реакцию с водой, образуется NaOH.
Запишем реакцию электролиза для CuSO4:
Медь относится к малоактивным металлам, поэтому сама в чистом виде выделяется на катоде. Анион кислородсодержащий, поэтому в реакции выделяется кислород. Сульфат-ион никуда не исчезает, он соединяется с водородом воды и превращается в серую кислоту.
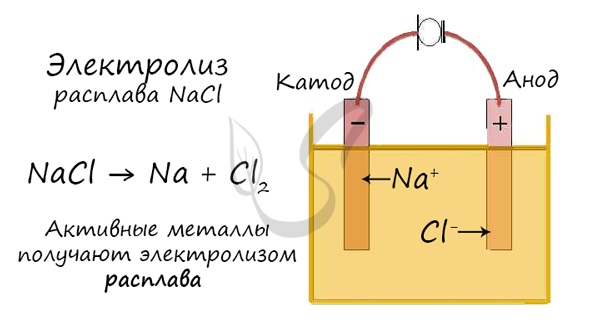
Электролиз расплавов
Все, что мы обсуждали до этого момента, касалось электролиза растворов, где растворителем является вода.
Перед промышленной химией стоит важная задача — получить металлы (вещества) в чистом виде. Малоактивные металлы (Ag, Cu) можно легко получать методом электролиза растворов.
Но как быть с активными металлами: Na, K, Li? Ведь при электролизе их растворов они не выделяются на катоде в чистом виде, вместо них восстанавливаются молекулы воды и выделяется водород. Тут нам как раз пригодятся расплавы, которые не содержат воды.
В безводных расплавах реакции записываются еще проще: вещества распадаются на составные части:
© Беллевич Юрий Сергеевич 2018-2022
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
http://pandia.ru/text/80/271/60083-3.php
http://studarium.ru/article/157


 В случае щелочной среды имеем:
В случае щелочной среды имеем: