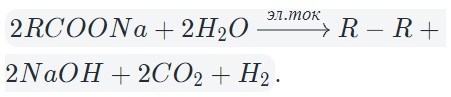Показать, существует ли разница в продуктах электролиза растворов и расплавов солей хлорида титана (II), йодида лития.
| 🎓 Заказ №: 22214 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Показать, существует ли разница в продуктах электролиза растворов и расплавов солей хлорида титана (II), йодида лития.
Решение: Поскольку стандартные электродные потенциалы титана и лития имеют очень низкие значения ( В В Na Na Ti Ti 2,714 ; 1,603 / / 2 ), то при электролизе растворов хлорида титана (II) и йодида лития на катоде происходит восстановление молекул воды. Записываем электронные уравнения при электролизе раствора хлорида титана (II) 2 2 2 A: Cl e Cl K : 2H2О 2e H2 2ОН
Научись сам решать задачи изучив химию на этой странице:
|
Услуги:
|
Готовые задачи по химии которые сегодня купили:




















































Образовательный сайт для студентов и школьников
Копирование материалов сайта возможно только с указанием активной ссылки «www.lfirmal.com» в качестве источника.
© Фирмаль Людмила Анатольевна — официальный сайт преподавателя математического факультета Дальневосточного государственного физико-технического института
Электролиз расплавов и растворов
О чем эта статья:
11 класс, ЕГЭ/ОГЭ
Электролиз — это окислительно-восстановительная реакция, которая протекает на электродах и основана на пропускании электрического тока через раствор или расплав.
Не менее важными участниками электролиза являются электроды: катод и анод. Если вы вдруг забыли, что такое катод и анод в химии, напомним.
Катод — это отрицательно заряженный электрод, который притягивает положительно заряженные ионы (катионы). А анод — это положительно заряженный электрод, который притягивает к себе отрицательно заряженные ионы (анионы). Таким образом, на катоде всегда происходит процесс восстановления, а на аноде всегда происходит процесс окисления.
Электроды бывают растворимые и инертные. Растворимые изготавливаются из металлов, например, меди и подвергаются химическим превращениям в ходе электролиза. А вот инертные или нерастворимые электроды не подвергаются химическим превращениям и остаются в неизменном виде как до реакции, так и после нее. Как правило, такие электроды изготавливают из графита или платины.
Виды электролиза
Различают два вида электролиза:
Электролиз водного раствора.
Прежде чем мы рассмотрим каждый процесс отдельно, давай познакомимся с общими для двух видов процессами на электродах.
Процесс на катоде K (−)
Катион принимает электроны и восстанавливается:
Me +n + ne − → Me 0 (восстановление).
Процесс на аноде A (+)
Анион отдает электроны и окисляется:
неMe −n − ne − → неMe 0 (окисление).
Процессы, протекающие при электролизе в общем случае:
К − : Ме +n + ne − → Ме 0 ;
А + : неМе −n − ne − → неМе 0 .
Суммарное уравнение электролиза:
Электролиз расплава
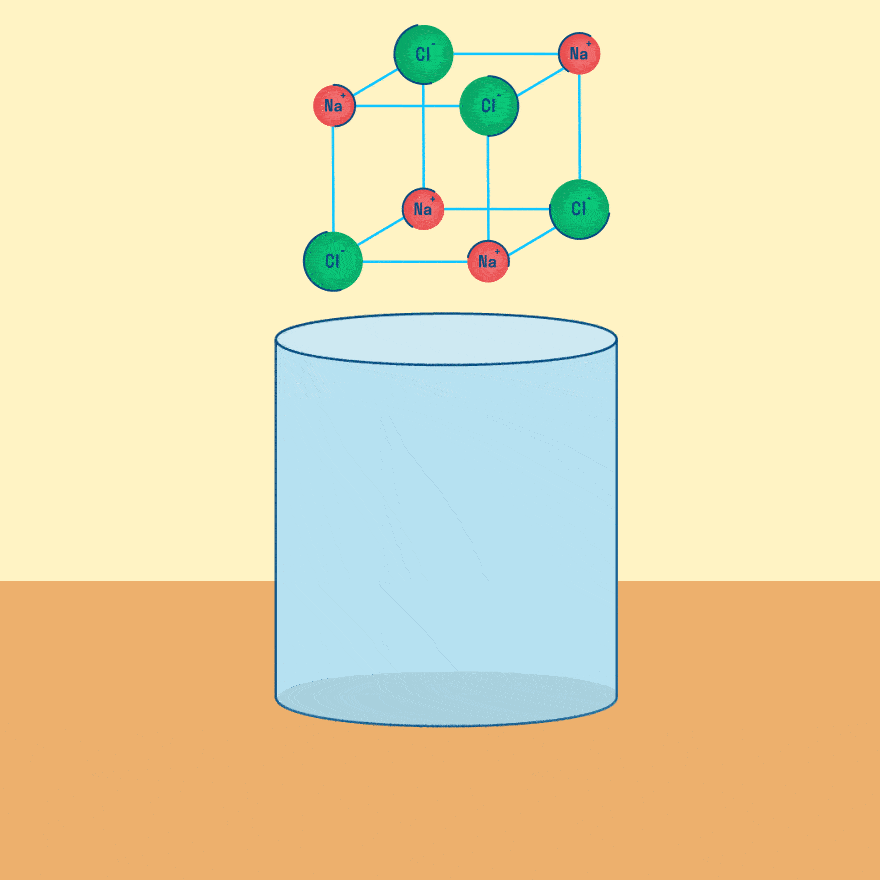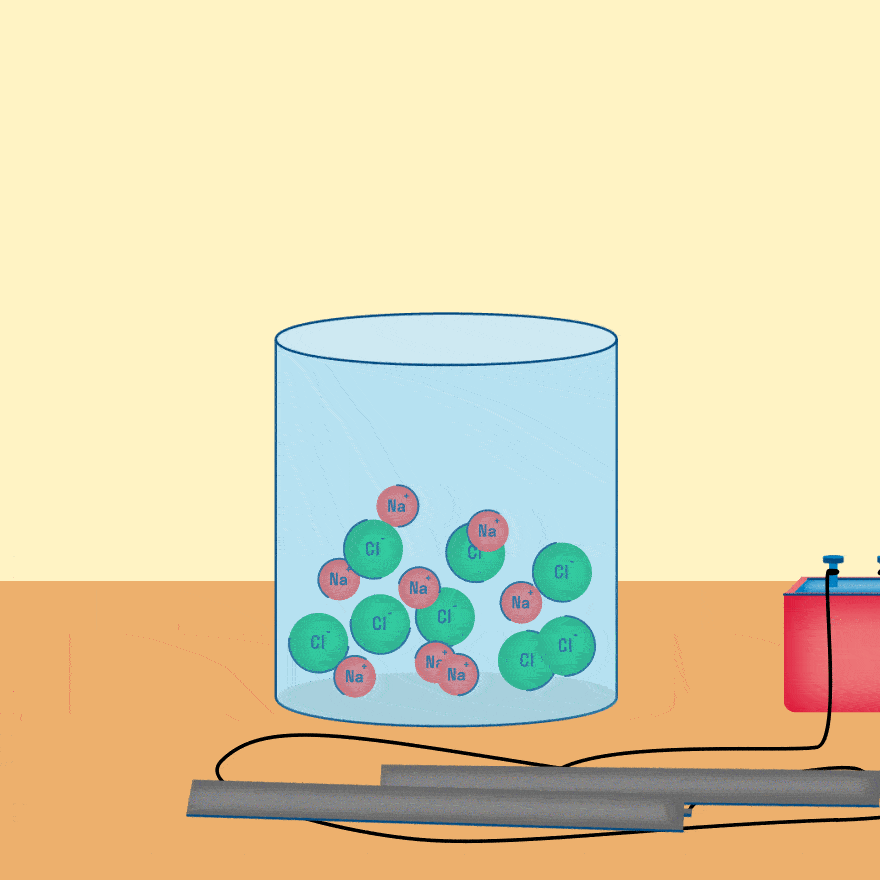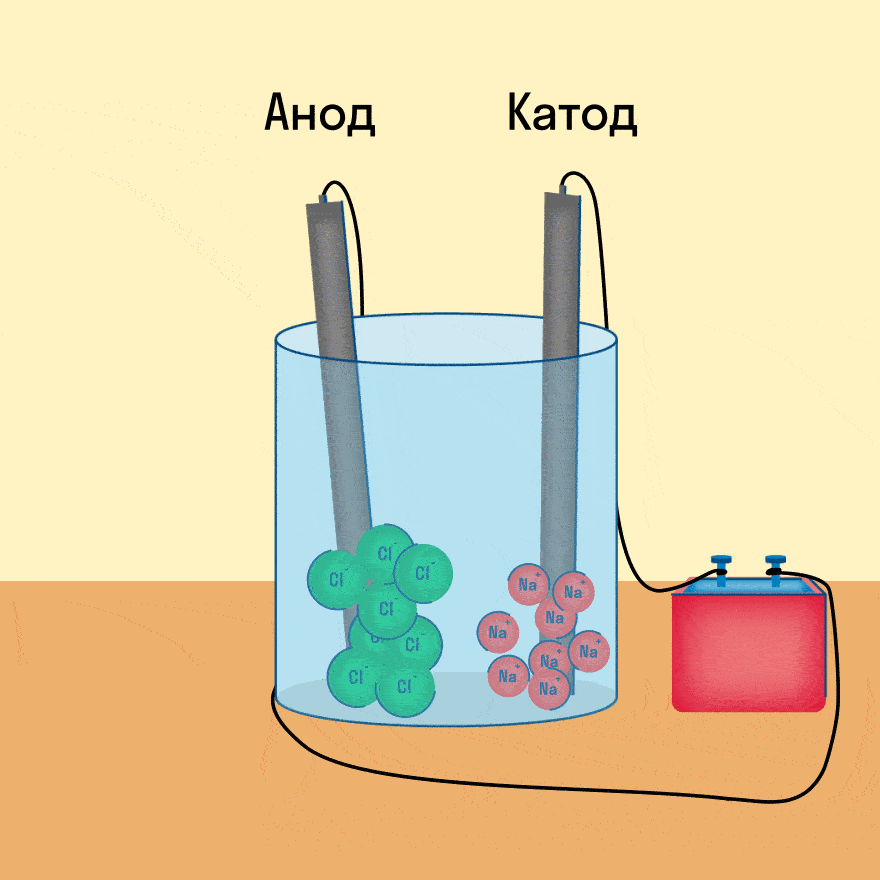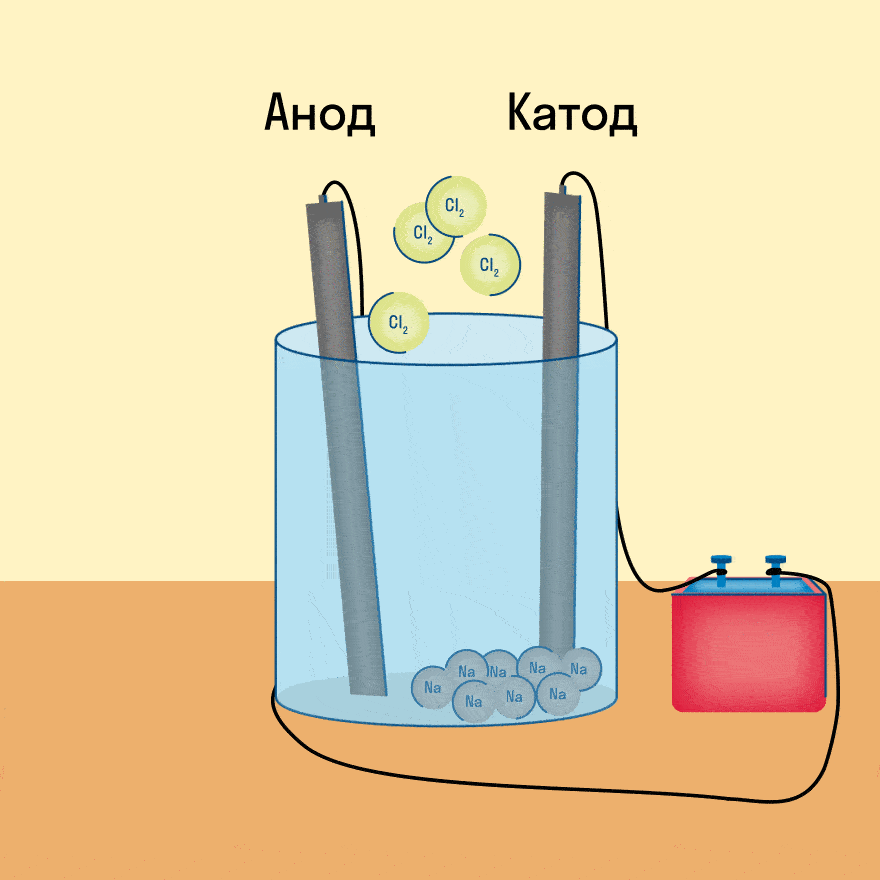
Рассмотрим электролиз расплава пищевой соли — хлорида натрия. При сильном нагревании кристаллический твердый хлорид натрия плавится. Полученный расплав содержит подвижные ионы хлора и натрия, освободившиеся из кристаллической решетки, и проводит электрический ток.
К − : 2Na + + 2e − = 2Na 0
А + : 2Cl − − 2e − = Cl2
Суммарное уравнение электролиза:
При опускании в расплав угольных (инертных) электродов, присоединенных к источнику тока, ионы приобретают направленное движение: катионы движутся к отрицательно заряженному электроду (катоду), анионы — к положительно заряженному электроду (аноду) и отдают электроны.
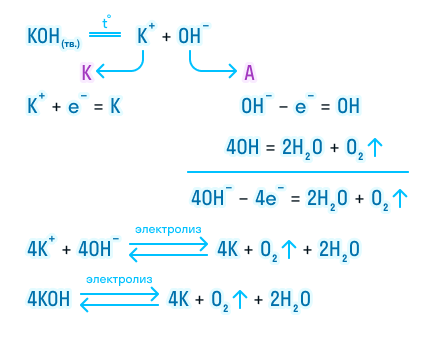
Теперь давайте рассмотрим электролиз расплава гидроксида калия.
На катоде происходит восстановление калия за счет принятия электронов. А на аноде протекает более сложная реакция. Гидроксогруппы отдают свой электрон и становятся нейтральными, но такое состояние для них крайне невыгодно, так как неустойчиво, и они объединяются в группы, чтобы потом разложиться с выделением газообразного кислорода и воды
Итог электролиза расплава — металлический калий на катоде, газообразный кислород и пары воды на аноде.
Электролиз раствора
Основным отличием водного раствора от расплава является присутствие молекул воды и ионов H + и OH — как продуктов диссоциации воды. В связи с этим возле катода и анода скапливаются ионы, которые конкурируют как друг с другом, так и с молекулами воды. Рассмотрим электролиз на примере водного раствора KF:
К − : 4H2O + 4e − = 2H2 0 + 4OH −
Суммарное уравнение электролиза:
Как видно, ни калий, ни фтор не фигурируют в продуктах электролиза. Почему так происходит?
Наиболее активные металлы — сильные восстановители. Калий — как раз такой металл, поэтому обратный процесс восстановления активных металлов из соединений осуществить сложно. При электролизе водных растворов солей активных металлов на катоде протекает восстановление не катионов этих металлов, а воды с образованием водорода.
Разберем порядок восстановления катионов металлов на катоде в зависимости от их активности.
Последовательность разрядки катионов зависит от положения металла в электрохимическом ряду напряжения.
Если у катода накапливаются молекулы воды и катионы металла, который находится в ряду напряжения после водорода, то восстанавливаются ионы металла.
Если у катода накапливаются молекулы воды и катионы металла, который стоит в начале ряда напряжения от лития до алюминия включительно, то восстанавливаются ионы водорода из молекул воды. Катионы металла не восстанавливаются, остаются в растворе.
Если у катода накапливаются молекулы воды и катионы металла, который расположен в ряду напряжения между алюминием и водородом, то восстанавливаются и ионы металла, и частично ионы водорода из молекул воды.
Если в растворе находится смесь катионов разных металлов, то сначала восстанавливаются катионы менее активного металла.
При электролизе раствора кислоты на катоде восстанавливаются катионы водорода до газообразного водорода.
Для удобства мы собрали информацию об электролизе в таблице:
Теперь разберемся, что происходит с анионами в водных растворах при электролизе. Для начала познакомимся с последовательностью восстановления анионов на аноде:
Чем меньше выражена восстановительная активность, тем хуже анионы могут окисляться на аноде. К тому же процесс на аноде зависит от материала анода и от природы аниона.
Если анод инертный или нерастворимый, то на нем протекают следующие реакции:
При электролизе растворов солей бескислородных кислот (кроме фторидов!), на аноде происходит процесс окисления аниона.
При электролизе растворов солей кислородсодержащих кислот и фторидов на аноде выделяется газообразный кислород вследствие окисления молекул воды. Анион при этом не окисляется, оставаясь в растворе.
При электролизе растворов щелочей происходит окисление гидроксид-ионов.
Если анод растворимый, то на нем всегда происходит окисление металла анода — независимо от природы аниона.
Исключением является электролиз солей карбоновых кислот. Таблица выше не описывает происходящее на аноде. Давайте рассмотрим, что же там происходит.
В результате электролиза водных растворов солей щелочных металлов карбоновых кислот происходит образование углеводородов вследствие рекомбинации углеводородных радикалов.
В общем виде электролиз солей карбоновых кислот можно записать так:
На катоде образуется газообразный водород, а на аноде — углекислый газ, углеводород, полученный удвоением радикала. В катодном пространстве накапливается щелочь.
В случае разделения катодного и анодного пространства углекислый газ реагирует со щелочью с образованием гидрокарбоната.
Применение электролиза
А теперь самое главное: зачем вообще нужен электролиз? Рассмотрим применение этого вида ОВР:
С помощью электролиза расплавов природных соединений в металлургической промышленности получают активные металлы (калий, натрий, бериллий, кальций, барий). С помощью электролиза растворов солей — цинк, кадмий, кобальт и другие.
В химической промышленности электролиз используют для получения фтора, хлора, водорода, кислорода, щелочей, бертолетовой соли и других веществ.
Электролиз с растворимым анодом используют для нанесения металлических покрытий (из хрома, золота, никеля, серебра), что предохраняет металлические изделия от коррозии и придает им декоративный вид.
Вопросы для самопроверки
1. Выберите верное продолжение фразы «катод — это. »:
Положительно заряженный электрод, к которому притягиваются положительно заряженные ионы.
Положительно заряженный электрод, к которому притягиваются отрицательно заряженные ионы.
Отрицательно заряженный электрод, к которому притягиваются положительно заряженные ионы.
Отрицательно заряженный электрод, к которому притягиваются отрицательно заряженные ионы.
2. Продолжите фразу «электролиз — это…»:
ОВР с применением тока.
Реакция без изменения степеней окисления с применением тока.
ОВР с применением катализаторов.
3. Как заряжен анион?
Не имеет заряда.
4. Чем отличается электролиз раствора от электролиза расплава?
В расплаве плавится твердое.
Присутствием молекул воды и продуктов ее диссоциации.
5. Если металл стоит в ряду активности металлов между алюминием и водородом, что выделится на катоде?
Металл и водород.
При электролиза водного раствора фторида лития что на аноде выделится?
Уравнение электролиза расплава хлорида титана 2
FOR-DLE.ru — Всё для твоего DLE 😉
Привет, я Стас ! Я занимаюсь так называемой «вёрсткой» шаблонов под DataLife Engine.
На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх.
Раньше я занимался простой вёрсткой одностраничных, новостных и т.п. шаблонов на HTML, Bootstrap. Однажды увидев сайты на DLE решил склеить пару шаблонов и выложить их в интернет. В итоге эта парочка шаблонов набрала неплохую популярность и хорошие отзывы, и я решил создать отдельный проект.
Кроме шаблонов я так же буду выкладывать полезную информацию для DataLife Engin и «статейки» для веб мастеров. Так же данный проект будет очень полезен для новичков и для тех, кто хочет правильно содержать свой сайт на DataLife Engine. Надеюсь моя работа вам понравится и вы поддержите этот проект. Как легко и удобно следить за обновлениями на сайте?
Достаточно просто зарегистрироваться на сайте, и уведомления о каждой новой публикации будут приходить на вашу электронную почту!
Задание 1
Что такое электролиз? Электролиз ― окислительно-восстановительный процесс, протекающий на электродах при пропускании постоянного электрического тока через растворы или расплавы электролитов.
Какие виды электролиза различают? Различают электролиз расплавов электролитов и электролиз растворов электролитов.
Задание 2
Охарактеризуйте практическое применение электролиза.
Основные направления промышленного применения электролиза:
― получение активных металлов (IА- и IIА-групп, а также алюминия) ;
― получение активных неметаллов (галогенов, водорода, кислорода) ;
― гальванопластика ― получение металлических копии с металлического или неметаллического оригинала;
― гальваностегия ― нанесение металлических или декоративных покрытии на изделия (главным образом металлические) ― золочение, серебрение, никелирование, хромирование и др;
― рафинирование ― очистка от посторонних примесей цветных металлов.
Задание 3
Какие металлы и неметаллы ― простые вещества можно получить только с помощью электролиза? Щелочные металлы, поскольку среди простых веществ они являются самыми сильными восстановителями, и неметал фтор, который является самым электроотрицательным элементом, следовательно, в природе не существует веществ способных окислить фторид-анионы F — .
Задание 4
Почему самый распространённый металл в земной коре ― алюминий ― был получен сравнительно поздно? Почему первоначально алюминий стоил дорого? Как удалось удешевить его производство? Алюминий был получен сравнительно поздно из-за невозможности получить его из растворов соли электролизом, из-за того что алюминий ― активный металл, сразу вступал в реакцию с водой, а также невозможностью получить алюминий из расплавов соли, т. к. многие соли алюминия разлагаются при достижении температуры плавления, в виду этого соль алюминия превращалась в оксид алюминия, который имел очень высокую температуру плавления (2044°C).
Впервые алюминий был получен из хлорида алюминия с помощью калия, который был получен с помощью электролиза расплава гидроксида калия.
Задание 5
Сравните процессы гидролиза и электролиза. Гидролиз ― процесс разложения исходных веществ при взаимодействии с водой с образованием новых соединений, не является ОВР. Электролиз ― окислительно-восстановительный процесс, протекающий на электродах при пропускании постоянного электрического тока через растворы или расплавы электролитов.
Задание 6
Назовите продукты электролиза раствора и расплава хлорида цинка; раствора нитрата цинка.
Продукты электролиза раствора и расплава хлорида цинка: цинк и хлор.
Раствор: CuCl2 эл.т. ⟶ Cu + Cl2
Расплав: CuCl2 эл.т. ⟶ Cu + Cl2
Продукты электролиза раствора нитрата цинка: цинк, азотная кислота, кислород.
Раствор: 2Zn(NO3)2 + 2H2O эл.т. ⟶ 2Zn + 4HNO3 + O2
Задание 7
Установите соответствие между солью и продуктом, образующимся на катоде при электролизе водного раствора этой соли.
| Соль | Продукт на катоде |
| А) хлорид аммония Б) нитрат серебра В) бромид стронция Г) сульфат меди (II) | 1) водород 2) серебро 3) медь 4) аммиак 5) стронций 6) кислород |
Ответ: А) 1, 4; Б) 2; В) 1; Г) 3
Задание 8
Установите соответствие между формулой соли и названием продукта, образующегося на инертном аноде при электролизе водного раствора этой соли.
| Формула соли | Название продукта на аноде |
| А) LiCl Б) CuBr2 В) KF Г) NaI | 1) фтор 2) хлор 3) бром 4) иод 5) водород 6) кислород |
Ответ: А) 2; Б) 3; В) 1; Г) 4
Задание 9
Установите соответствие между формулой вещества и уравнением процесса, протекающего на катоде при электролизе водного раствора этого вещества.
| Формула вещества | Уравнение катодного процесса |
| А) HNO3 Б) KOH В) BaCl2 Г) AgNO3 | 1) 2H + +2ē ⟶ H2 2) 2H2O +2ē ⟶ H2 + 2OH — 3) К + -ē ⟶ K 0 4) Ba 2+ +2ē ⟶ Ba 0 5) Ag + +ē ⟶ Ag 0 6) 4OH — -4ē ⟶ O2 + 2H2O |
Ответ: А) 2; Б) 2; В) 2; Г) 5
Задание 10
Какие изделия, используемые в быту, на ваш взгляд, были изготовлены с применением гальванопластики и гальваностегии?
http://skysmart.ru/articles/chemistry/elektroliz-rasplavov-i-rastvorov
http://gdz.cool/h11_gos_2019/1297-h11_gos_2019__15__.html