ДИФФУЗИОННЫЕ, МЕМБРАННЫЕ И ФАЗОВЫЕ ПОТЕНЦИАЛЫ
Для возникновения биопотенциалов решающее значение имеют потенциалы, обусловленные несимметричным, неравномерным распределением ионов. К таким потенциалам могут быть отнесены диффузионные, мембранные и фазовые.
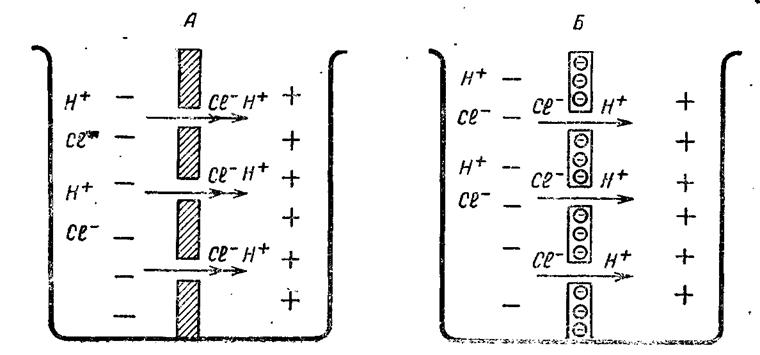
Диффузионные потенциалы возникают на границе раздела двухжидких сред в результате различной подвижности ионов. Допустим, имеется сосуд с раствором соляной кислоты, разделенный пористой перегородкой
(рис. 28, А). Пусть в левой половине сосуда концентрация соляной кислоты будет выше, чем в правой. Тогда ионы водорода и хлора будут диффундировать из левой половины сосуда в правую по градиенту концентрации. Скорости диффузии ионов будут определяться их подвижностями. Подвижность иона водорода равна 315 см 2 Ом -1 * г-экв, а подвижность иона хлора — 65,5. В результате большей подвижности ионы водорода при диффузии будут намного опережать ионы хлора. А так как ионы водорода имеют положительный заряд, а ионы хлора — отрицательный, то в правой половине сосуда возникнет положительный заряд, а в левой — отрицательный.
Возникающая диффузионная разность потенциалов приводит к торможению более «быстрых» ионов и ускорению более «медленных», поскольку силы возникающего электрического поля направлены против сил диффузий. Диффузионная разность потенциалов достигает максимального значения в тот момент, когда скорости диффузии ионов становятся равными. Диффузионная разность потенциалов Е находится из уравнения Гендерсона:

где U— подвижность катиона; V — подвижность аниона; R . — газовая постоянная; Т — абсолютная температура; п — валентность ионов; Р — число Фарадея; а1— актив-
168
Рис. 28. Схема возникновения диффузионного (А) и мембранного (Б)
Стрелки — направление диффузии ионов; кружки — наличие фиксированных
зарядов на мембране.
ность ионов в области, откуда идет диффузия; а2— активность ионов в области, куда идет диффузия.
Под активностью ионов понимают их активную концентрацию. Активность ионов всегда меньше их абсолютной концентрации, что обусловлено взаимодействием ионов друг с другом, а также их взаимодействием с электрически заряженными группами других молекул. Активность выражается произведением коэффициента активности f, определяемым эмпирически, на абсолютную концентрацию С ионов:

Как следует из уравнения (1), диффузионная разность потенциалов зависит от разности в подвижностях катиона и аниона и от отношения активностей ионов в измеряемых участках. Очевидно, что при одинаковой подвижности катионами аниона, а также при отсутствии концентрационного градиента диффузионный потенциал будет равен нулю.
В биологическом объекте наиболее отчетливо диффузионный потенциал может проявляться, вероятно, только при механическом повреждении клеток. Из места повреждения происходит диффузия ионов в неповрежденные участки и возникает диффузионный потенциал, который суммируется при измерении демаркационного потенциала с потенциалом покоя клетки.
Частным видом диффузионного потенциала можно считать мембранный потенциал. Допустим,пористую перегородку в сосуде, которая пропускала и катионы, и анионы, заменили полупроницаемой мембраной, пропускающей только катионы (рис. 28, Б). Такой мембраной может быть мембрана с большой концентрацией фиксированных отрицательных зарядов — катионообменная мембрана. В таком случае подвижность ионов хлора в мембране равна нулю и в правую часть сосуда диффундируют только ионы водорода. Диффузия ионов водорода не будет бесконечным процессом, поскольку они испытывают притяжение к оставшимся по другую сторону мембраны ионам хлора. После установления равновесия между силами диффузии и силами электрического поля на мембране возникает двойной электрический слой и диффузия ионов прекращается. Если V=0, то уравнение (1) превращается в уравнение Нернста, с помощью которого вычисляется мембранная разность потенциалов:
(3)
где обозначения те же, что и в уравнении (1). Как следует из уравнения (3), мембранный потенциал зависит от температуры и от величины концентрационного градиента диффундирующих через мембрану ионов.
Если перейти от натуральных логарифмов к десятичным и подставить в уравнение (3) значения постоянных R и F , то при 20°С получим:
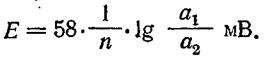
Уравнением (4) обычно пользуются для практических расчетов мембранного потенциала; оно показывает, что при изменении отношения активностей ионов в 10 раз потенциал изменяется на 58 мВ.
В соответствии с современными представлениями, потенциалы покоя, повреждения и действия являются по своей природе мембранными потенциалами.
Так же как и мембранные, известную аналогию с диффузионными потенциалами имеют и фазовые потен циалы. Фазовые потенциалы возникают на границе раздела двух несмешивающихся фаз (например, раствор электролита в воде и какое-либо масло) в результате
различной растворимости катионов и анионов в неводной фазе. Если, например, катионы лучше, чем анионы, растворяются в неводной фазе, то они интенсивнее диффундируют в нее и заряжают ее положительно по отношению к водной фазе.
Поскольку цитоплазма клеток (представляет собой многофазную микрогетерогенную систему, то на поверхностях раздела фаз могут возникать фазовые потенциалы небольшой величины. Величину фазовых потенциалов находят из уравнения (1).
ТЕОРИИ ПРОИСХОЖДЕНИЯ БИОПОТЕНЦИАЛОВ
Хорошо теоретически разработана и подтверждена блестящими экспериментами мембранная теория биопотенциалов. Мембранная теория была выдвинута еще в 1902 г. Бернштейном. Однако только в 50-х годах эта теория была по настоящему развита и экспериментально обоснована Ходжкиным, которому принадлежат основные идеи и теории о роли ионных градиентов в возникновении биопотенциалов и о механизме распределения ионов между клеткой и средой.
Сущность этой теории заключается в том, что потенциал покоя и потенциал действия являются по своей природе мембранными потенциалами, — обусловленными полупроницаемыми свойствами клеточной мембраны и неравномерным распределением ионов между клеткой и
средой, которое поддерживается механизмами активного
переноса, локализованными в самой мембране. Ниже основные представления мембранной теории будут рассмотрены более подробно.
Согласно фазовой теории биопотенциалов (Д. Н. Насонов, В. Я. Александров, А. С. Трошин, 1944), цитоплазма представляет собой единую, несмешивающуюся с водой фазу. Ионы в цитоплазме находятся на 80 — 90% в связанном состоянии (в основном с белками), поэтому в невозбужденных и неповрежденных клетках разность электрических потенциалов отсутствует. При возбуждении или повреждении клеток ионы освобождаются от белковоионных комплексов цитоплазмы и
диффундируют в окружающую среду. За счет диффузии
ионов и возникают потенциалы действия и повреждения.
Однако впоследствии эта теория не получила экспериментального подтверждения. Во-первых, было пока-
зано, что ионы в клетках находятся в свободном состоянии (по крайней мере, их основная часть). Во-вторых, с помощью микроэлектродной техники были зарегистрированы потенциалы клеток в состоянии покоя, которые фазовой теорией не признавались. Кроме того, имеется еще ряд фактических и теоретических возражений против фазовой теории, поэтому в настоящее время в целом она мало кем признается, хотя отдельные ее положения имеют значение для объяснения определенных биоэлектрических явлений.
В последнее время на смену фазовой пришла полиэлектролитная теория, которая объясняет потенциал покоя и потенциал действий свойствами молекул полиэлектролитов в клетке. Полиэлектролитными считаются молекулы с большим количеством фиксированных зарядов, которые обусловлены концевыми и боковыми диссоциирующими группами (СООН и NH2). К полиэлектролитным можно отнести белковые молекулы (см. главу 8). Согласно этой теории, основой цитоплазмы служит комплексный полиэлектролитный гель сетчатой структуры с фиксированными на ней отрицательными зарядами, который способен избирательно накапливать калий в ионном виде. При возбуждении полиэлектролитные структуры временно утрачивают избирательность к ионам калия, что вызывает вначале диффузию натрия в клетку, а затем — калия из клетки в окружающую среду. Диффузия ионов и служит причиной возникновения и исчезновения деполяризации клетки.
Опыты Курелла и других авторов подтверждают, что потенциал покоя существует в нативной клетке, а не возникает в результате повреждения. Однако предполагаемый им механизм поглощений ионов калия клеткой за счет избирательной сорбции полиэлектролитами, а также изменение этой избирательности при возбуждении вызывают сомнения. Возможно, что наличие полиэлектролитов в цитоплазме является одним из факторов, определяющих наличие некоторого количества связанных ионов калия в клетке.
ПОТЕНЦИАЛ ПОКОЯ
Между внутренней и наружной поверхностями клеточной мембраны всегда существует разность электрических потенциалов. Эта разность потенциалов, изме-
ренная в состоянии физиологического покоя клетки, называется потенциалом покоя. Потенциал покоя клетки можно измерить с помощью стеклянного микроэлектрода, введенного непосредственно в цитоплазму; второй электрод приэтом находится во внеклеточной жидкости. Кончик микроэлектрода, имеющего внутри канал, заполненный концентрированным раствором КСl, может иметь диаметр всего в долю микрона. При введении микроэлектрода мембрана клетки охватывает его кончик и ее повреждения практически не происходит. Основные работы по выяснению механизмов возникновения биопотенциалов были выполнены на крупных клетках: гигантских аксонах кальмаров, клетках водоросли Nitella и др. Эти клетки могут иметь диаметр до 1 мм, что очень удобно для исследования.
На основании большого экспериментального материала было установлено, что цитоплазма в состоянии покоя
клеток всегда имеет отрицательный потенциал по отношению к потенциалу межклеточной жидкости. Потенциал покоя у разных клеток имеет величину от 50 до 100 мВ. В табл. 3 приведены значения потенциала покоя для некоторых клеток.
Согласно современным взглядам, причиной возникновения потенциалов клеток как в покое, так и при возбуждении является неравномерное распределение ионов калия и натрия между содержимым клеток и окружающей средой. Как уже указывалось в главе 6, концентрация ионов калия внутри клеток в 20 — 40 раз превышает их содержание в окружающей клетку жидкости-
173
Напротив, концентрация натрия в межклеточной жид-кости в 10 — 20 раз выше, чем внутри клеток. Такое не-равномерное распределение ионов обусловлено активным переносом ионов — работой натрий-калиевого насоса (см. главу 6).
Как было установлено, возникновение ‘потенциала покоя обусловлено в основном наличием концентрацион: ного градиента ионов калия. Эта точка зрения базируется на том, что ионы калия внутри клетки находятся в свободном состоянии, т. е. не связаны с другими ионами и молекулами и могут свободно диффундировать. Исследования Ходжкина и Кейнеса (1953), выполненные с радиоактивным 42 К на гигантских аксонах кальмара, показали, что подвижность и коэффициент диффузии 42 К внутри волокна -почти такие же, как и в водном растворе. Хинке (1961) установил, что коэффициент активности калия в аксоплазме такой же, как и в морской воде. Гаррис (1954) показал, что электрическая подвижность 42 К в мышечном волокне лягушки также оказалась близкой к подвижности в водном растворе. Наконец, на то, что калий в цитоплазме находится в свободном состоянии, указывает и высокое значение электропроводности аксоплазмы —0,5>0,8 электропроводности морской воды.
Избыток положительных зарядов ионов калия внутри клеток компенсируется в основном органическими анионами. К ним относятся анионы аспарагиновой, уксусной, пировиноградной и других органических кислот. Содержание неорганических анионов в клетках сравнительно небольшое.
Согласно теории Ходжкина, Хаксли, Катца, клеточ ная мембрана в состоянии покоя проницаема в основ-ном только для ионов калия. Ионы калия диффунди-руют по концентрационному градиенту через клеточную
мембрану в окружающую жидкость; анионы не могут
проникать через мембрану и остаються на ее внутренней
стороне. Так как ионы калия имеют положительный за-ряд. а анионы, остающиеся на внутренней поверхности мембраны, — отрицательный, то внешняя — поверхность мембраны при этом заряжается положительно, а внут-ренняя — отрицательно (рис. 29). Понятно, что диффу-зия продолжается только до того момента, пока не установится равновесие между силами возникающего электрического поля и силами диффузии.
Рис 29. Влияние диффузии ионов калия, натрия и хлора на мембранный потенциал клеток.
Если принять, что потенциал покоя определяется диффузией только ионов калия из цитоплазмы наружу, то его величина Е может быть найдена из уравнения Нернста:
(5)
где [К]i и [К]е—активность ионов калия внутри и снаружи клетки.
Разность потенциалов между внутренней и наружной поверхностями мембраны различных клеток, рассчитанная по уравнению Нернста, оказалась очень близкой к измеренной в опыте с помощью внутриклеточных микроэлектродов. Кроме того, калиевый механизм возникновения потенциала покоя убедительно подтверждают эксперименты с изменением концентрации калия в окружающей клетку среде. При изменении наружной концентрации калия в широких пределах наблюдалось закономерное изменение величины потенциала покоя в соответствии с зависимостью, выраженной уравнением (5). В частности, когда концентрацию калия в окружающей клетку жидкости делали равной концентрации в клетке, потенциал покоя становился равным нулю.
Вторым фактором пропорциональности в уравнении (5) служит абсолютная температура. Величина потенциала покоя по теории должна быть прямо пропорциональной абсолютной температуре. Еще в прошлом веке было показано, что локальное согревание участка нерва делает его электроположительным по отношению к другим участкам, что качественно подтверждает справедливость уравнения (5) в его применении к описанию потенциала покоя клеток. Точные измерения Линга и других авторов показали, что температурный коэффициент
Q10 потенциала покоя клеток равен примерно 1,1. Такой температурный коэффициент характерен для физических процессов (см. главу 4). Таким образом, температурные зависимости потенциала покоя подтвердили, что в основе его возникновения лежит физический процесс, в частности диффузия.
При более точном измерении потенциала покоя выяснилось, что во многих случаях его измеренное значение соответствует значению, теоретически вычисленному по уравнению (5); в других случаях между измеренной и вычисленной величинами имеются значительные отличия. Это объясняется тем, что на величину потенциала покоя оказывает влияние диффузия других ионов.
Мембрана в состоянии покоя проницаема не только
для ионного калия, но и в небольшой степени для ионов
натрия и хлора. Мембранный потенциал клеток представляет собой результирующую электродвижущих сил,
генерируемых всеми этими тремя каналами диффузии.
Проникновение натрия из окружающей жидкости внутрь
клетки по концентрационному градиенту приводит к не
которому уменьшению мембранного потенциала (см.
рис. 29). Диффузия через мембрану ионов хлора, содержание которых в межклеточной жидкости большинства тканей выше, чем в клетках, вызывает некоторое увеличение мембранного потенциала. Следовательно, для более точного вычисления потенциала покоя необходимо учитывать не только диффузию ионов калия, но и диффузию натрия и хлора. Уравнение (5) позволяет описывать мембранный потенциал только в первом приближении; для более точного определения потенциала при меняют обобщенное уравнение Гольдмана: *
(6)
где Рк, РNa, РCl — коэффициенты проницаемости мембраны для ионов калия, натрия и хлора; [K], [N a], [С l] — их активности внутри ( i ) и вне (е) клетки. Уравнение (6) позволяет определять мембранный потенциал не только в состоянии покоя, но и при возбуждении клетки. Для этого необходимо знание коэффициентов проницаемости для ионов. Если мембрана проницаема только для одного вида ионов, например для ионов калия, то РNa=РCl=0 и уравнение (6) переходит в уравнение (5). По данным Ходжкина и Катца (1949),
для аксона кальмара в состоянии покоя отношение коэффициентов проницаемости РK : PNa : РCl= 1 : 0,04 : 0,45.
Кроме простой диффузии ионов калия и натрия через мембрану, приводящей к определенным изменениям мембранной разности потенциалов, наблюдается обменная диффузия этих ионов. Поскольку при обменной диффузии потоки ионов через мембрану в прямом и обратном направлениях равны, электронейтральность растворов с обеих сторон мембраны сохраняется, т. е. наличие обменной диффузии ионов не влияет на мембранный потенциал.
Имеются данные, что пассивный перенос калия через мембрану сопряжен с пассивным переносом натрия по типу ионообменной диффузии. При этом калий цитоплазмы заменяется на натрий внешнего раствора при сохранении постоянства мембранного потенциала.
Все клетки возбудимых тканей при действии различных раздражителей достаточной силы способны переходить в состояние возбуждения. К возбудимым относятся нервная, мышечная и железистая ткани, хотя четкой границы между возбудимыми и другими тканями провести нельзя. Возбудимость — это способность клеток к быстрому ответу на раздражение, проявляющемуся через совокупность физических, физико-химических процессов и функциональных изменений. Обязательным признаком возбуждения является изменение электрического состояния клеточной мембраны. Опыт показывает, что возбужденный участок клетки становится электроотицательным по отношению к невозбужденному, что указывает на перераспределение ионов в возбужденном участке. При возбуждении оно имеет временный характер, и после окончания возбуждения вновь восстанавливается исходный потенциал покоя. Общее изменение разности потенциалов между клеткой и средой, происходящее при пороговом и сверхпороговом возбуждении клеток, называется потенциалом действия. Потенциалы
действия обеспечивают проведение возбуждения по нервны волокнам и инициируют процессы сокращения
мышечных и секреции железистых клеток. Ю. Бернштейн — автор мембранной теории — полагал, что при возбуждении мембрана становится хорошо
2 Медицинская биофизика 177
проницаемой для всех ионов. Ионные градиенты вследствие этого исчезают и разность потенциалов на мембране уменьшается до нуля. Таким образом, согласно теории Бернштейна, потенциал действия не может быть больше потенциала покоя. Если измерить разность по тенциалов между возбужденным и невозбужденными
участками, то возбужденный участок будет электроотрицательным по отношению к невозбужденному, что и подтверждалось в опытах с отведением потенциалов от поверхности клеток.
Однако, когда применили методику внутриклеточного отведения потенциалов, то обнаружили, что при возбуждении мембранный потенциал не просто падает до нуля; он продолжает изменяться дальшеи достигает значи-
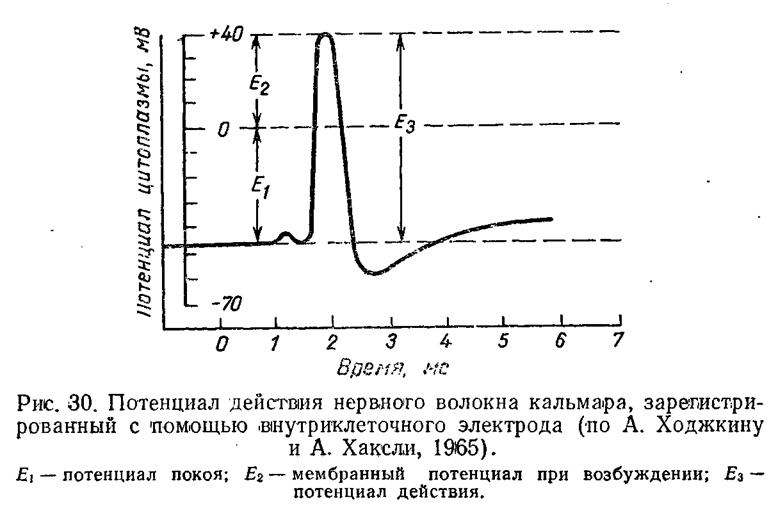
тельной величины. На рис. 30, где показано изменение мембранного потенциала при возбуждении, видно, что в состоянии покоя внутренняя сторона клеточной оболочки имеет отрицательный потенциал, примерно равный — 45 мВ, тогда как при возбуждении мембранный потенциал становится равным +40 мВ. Таким образом, полное значение потенциала действия составляет 85 мВ, что значительно превышает величину потенциала покоя. Современная теория возникновения потенциала действия базируется на данных, полученных методами внутриклеточного отведения потенциалов, фиксации на-
пряжения на мембране, радиоактивных изотопов, перфузии нервных волокон, электропроводности и др.
Еще в 1938 г. Коул и Кертис показали, что возбуждение связано с кратковременным увеличением электропроводности клеточной мембраны. Согласно их данным, сопротивление мембраны аксона кальмара изменяется от 1000 Ом/см 2 в состоянии покоя до 25 Ом/см 2 в момент возбуждения, а клетки водоросли Nitella от 100 000 до 500 Ом/см 2 . При этом сопротивление цитоплазмы клеток практически не изменялось. Уменьшение электрического сопротивления мембраны при возбуждении может быть объяснено только увеличением ее проницаемости для ионов, поскольку последние являются переносчиками электричества в тканях.
Дальнейшее развитие теории потенциала действия было связано с применением метода фиксации напряжения на мембране (метод Ходжкина, Хаксли, Катца). Сущность этого метода заключается в том, что мембранный потенциал на участке мембраны смещают до некоторой величины с помощью двух электродов, расположенных на ее противоположных сторонах, и удерживают на этом уровне с помощью электронной схемы с отрицательной обратной связью. Ток, протекающий через этот участок мембраны, служит мерой ее проницаемости для ионов при данном напряжении и измеряется отдельным усилителем. Метод фиксации напряжения позволил раздельно изучить изменение проницаемости мембраны для ионов натрия и калия при возбуждении.
Было показано, что возникновение потенциала действия связано с увеличением проницаемости мембраны для ионов натрия и последующим усилением диффузии этих ионов по концентрационному градиенту внутрь клетки, что приводит к изменению (уменьшению) мембранного потенциала. При этом обнаружилось, что если мембранный потенциал уменьшается до некоторой критической величины (на 10 — 30 мВ), то, независимо от того, чем вызвано это уменьшение — наложением внешнего электрического поля или же действием другого раздражители, между проницаемостью мембраны для натрия и уменьшением ее мембранного потенциала (деполяризацией) возникает регенеративная или положительная обратная связь. Уменьшение мембранного потенциала ниже критического уровня приводит к увеличению про-ницаемости мембраны для натрия, а увеличение про-
I
ницаемости сопровождается усилением диффузии натрия в цитоплазму, что вызывает еще более значительную деполяризацию мембраны (рис. 31). Благодаря наличию положительной обратной связи деполяризация мембраны при возбуждении происходит с ускорением и поток ионов натрия в клетку все время возрас тает. Интенсивность же потока ионов калия, направленного из клетки наружу, в первые моменты возбуждения остается прежней. Усиленный поток положительно заряженных ионов натрия (внутрь клетки вызывает вначале исчезновение избыточного отрицательного заряда на внутренней поверхности мембраны, а затем приводит к перезарядке мембраны. Поступление ионов натрия в клетку (Продолжается до тех пор, пока внутренняя поверхность мембраны не приобретет положительный заряд, достаточный для уравновешивания градиента концентрации натрия и (прекращения его дальнейшего перехода внутрь клетки. Описанные процессы изменения проницаемости мембраны для ионов характерны для первой фазы потенциала действия — фазы деполяризации. По данным Ходжкина, отношение коэффициентов проницаемости мембраны аксона кальмара в это время РK : РNa : РCl=1: 20 : 0,45. Если сравнить его с аналогичным соотношением в состоянии покоя РK : РNa : РCl=1 : 0,04 : 0,45, то видно, что для калия и хлора в первой фазе возбуждения проницаемость не изменилась, а для натрия она увеличилась в 500 раз.
где ЕM — мембранный потенциал при возбуждении.
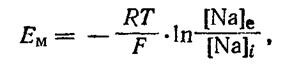
Общее изменение мембранного потенциала при возбуждении будет складываться из потенциала покоя и мембранного потенциала при возбуждении:
где Е — потенциал действия.
Благодаря этому амплитуда потенциала действия достигает 90 — 130 мВ (см. табл. 3) и, естественно, превышает величину потенциала покоя.
Натриевый механизм возникновения потенциала действия подтверждают опыты с изменением внешней и внутренней концентрации этих ионов. Было показано, что десятикратному изменению концентрации ионов натрия во внешней или внутренней среде клетки соответствует изменение потенциала действия на 58 мВ, что следует и из уравнения (8). При этом выяснилось, что изменяется именно та часть пика потенциала действия, которая превышала потенциал покоя, т.е. возникала за счет перезарядки мембраны при диффузии натрия в клетку. В этих опытах внутренняя концентрация ионов натрия изменялась при помощи микроинъекции солей натрия в клетки. При полном удалении ионов натрия из окружающей клетку жидкости потенциалы действия не возникали (если отсутствовали ионы лития и аммония — возможные заменители ионов натрия).
Таким образом, на основе обобщения большого экспериментального материала было установлено, что потенциалы действия возникают в результате избыточной по сравнению с покоем диффузии ионов натрия из окружающей жидкости внутрь клетки.
Период, в течение которого проницаемость мембраны для ионов натрия при возбуждении клетки возрастает, является небольшим (0,5 — 1 мс); вслед за этим наблюдается повышение проницаемости мембраны для ионов калия и, следовательно, усиление диффузии этих ионов из клетки наружу. Увеличение ионного потока калия, направленного из клетки наружу, приводит к уменьшению мембранного потенциала, что в свою очередь обусловливает уменьшение проницаемости мембраны для ионов натрия, которая, как указывалось, является функцией мембранного потенциала. Таким образом, второй этап возбуждения характеризуется тем, что поток ионов калия из клетки наружу возрастает, а встречный
181
поток ионов натрия уменьшается. Это продолжается до тех пор, пока не произойдет восстановления потенциала покоя — реполяризация мембраны. После этого проницаемость для ионов калия также падает до исходной величины. Наружная поверхность мембраны за счет вышедших в среду положительно заряженных ионов калия опять приобретает положительный потенциал по отношению к внутренней. Эта фаза, в течение которой мембранный потенциал возвращается до уровня потенциала покоя, называется фазой реполяризации. Она всегда продолжительнее фазы деполяризации и на кривой потенциала действия представлена в виде более пологой нисходящей ветви. Таким образом, реполяризация мембраны происходит не в результате обратного перемещения ионов натрия, а вследствие выхода из клетки эквивалентного количества ионов калия.
В некоторых случаях проницаемость мембраны для ионов натрия и калия после окончания возбуждения остается повышенной. Это приводит к тому, что на кривой потенциала действия регистрируются так называемые следовые потенциалы, характеризующиеся малой амплитудой и сравнительно большой длительностью. Если скорость падения (проницаемости мембраны для натрия в фазе реполяризации замедляется, то возникает отрицательный следовой потенциал. Положительный следовой потенциал выражается в гиперполяризации (увеличении потенциала покоя) мембраны и обусловлен тем, что проницаемость мембраны для калия в восстановительный период некоторое время остается повышенной.
Таким образом, формирование потенциала действия обусловлено двумя ионными потоками через мембрану: поток ионов натрия внутрь клетки приводит к перезарядке мембраны, а противоположно направленный поток ионов калия обусловливает восстановление исходного потенциала покоя. Потоки приблизительно равны по величине, но сдвинуты во времени. Благодаря этому сдвигу во времени и возможно появление потенциала действия. Если бы потоки натрия и калия через мембрану совпадали во времени, то они бы компенсировали друг друга и никакого изменения мембранного потенциала не могло бы происходить. На рис. 32 показаны кривые изменения потоков натрия и калия через мембрану во время развития потенциала действия аксона
кальмара, полученные по данным метода фиксации напряжения. Ионные потоки выражались в единицах электрической проводимости.
Непосредственное измерение ионных потоков калия и натрия при возбуждении было произведено с помощью радиоактивных 42 К и 24 Nа. Так, Кейнесом (1951) было показано, что в гигантском нервном волокне каракатицы за каждый импульс в клетку поступает 3,7 пикомоль (1 пикомоль = 10 -12 моль) натрия на 1 см 2 поверхности волокна. Примерно такое же количество ионов калия за один импульс выходит из клетки. По данным Флойда, суммарный перенос натрия в клетку и калия из клетки за один импульс в аксонах кальмаров составляет величины от 3 до 4,5 пикомоль/см 2 у разных видов.
Таким образом, при каждом акте возбуждения клетка приобретает определенное количество ионов натрия и теряет такое же количество ионов калия. А. Ходжкиным подсчитано, что концентрационные градиенты калия
и натрия гигантского аксона кальмара за один нервный импульс уменьшаются на одну миллионную долю от исходной величины. Благодаря такому экономному использованию энергии градиентов клетки способны генерировать сотни тысяч импульсов без подзарядки своих концентрационных батарей, что и обусловливает высокую работоспособность и неутомляемость нерва. Но в конечном итоге диффузия натрия и калия по градиентам должна бы приводить к выравниванию концентраций этих ионов между наружным раствором и цитоплазмой. В действительности этого не наблюдается. В периоды покоя концентрационные градиенты калия и натрия восстанавливаются в результате работы натрий-калиевого насоса, обеспечивающего перенос этих ионов против градиентов.
Благодаря регенеративным свойствам мембраны и тому, что величина потенциала действия определяется величиной ионных градиентов, при возбуждении клеток наблюдается ответ по типу «все или ничего». Если внешний стимул способен деполяризовать мембрану до критической величины, то возникает положительная обратная связь — «деполяризация — проницаемость для натрия» и в дальнейшем потенциал действия генерируется автоматически за счет энергии ионных градиентов. Если величина ионных градиентов с течением времени не изменяется, то и возникающие потенциалы действия будут иметь одинаковую амплитуду. При этом внешний стимул по отношению к энергии ионных градиентов играет лишь роль спускового механизма.
При действии подпороговых стимулов проницаемость мембраны для натрия возрастает незначительно и деполяризация не достигает критического значения. Деполяризация мембраны меньше критического уровня называется местным потенциалом. Местные потенциалы не способны распространяться на значительные расстояния, а затухают вблизи места своего возникновения. Эти потенциалы не подчиняются закону «все или ничего» — их амплитуда и длительность пропорциональны интенсивности и длительности раздражения. При повторном действии подпороговых стимулов местные потенциалы могут суммироваться, достигать критического значения и вызывать появление распространяющихся потенциалов действия. Таким образом, местные потенциалы могут предшествовать возникновению потенциалов действия.
Особенно отчетливо это наблюдается в клетках проводящей системы сердца, где медленная диастолическая деполяризация, развивающаяся спонтанно, вызывает появление потенциалов действия.
Следует отметить, что натрий-калиевый механизм генерирования потенциала действия является не единственным. В клетках водорослей Хара реверсия мембранного потенциала обусловлена диффузией в клетку ионов хлора. Обнаружены также клетки, у которых реверсия мембранного потенциала обусловлена диффузией ионов кальция. К таким, в частности, относятся волокна гладких мышц кишечника, матки, сосудов и других полых органов.
ПРОВЕДЕНИЕ ВОЗБУЖДЕНИЯ
Потенциал действия, возникнув в одном участке нервной клетки, быстро распространяется по всей ее поверхности. Распространение потенциала действия обусловлено возникновением так называемых локальных токов, циркулирующих между возбужденным и невозбужденным участками клетки. В состоянии покоя внешняя поверхность клеточной мембраны имеет положительный потенциал, а внутренняя — отрицательный. В момент возбуждения полярность мембраны изменяется на обратную: ее внешняя поверхность заряжена отрицательно по отношению к внутренней (рис. 33). В результате этого между возбужденным и невозбужденным участками мембраны (В и H на рис. 33) имеется разность потенциалов. Наличие разности потенциалов приводит к появлению между этими участками электрических токов, называемых локальными токами или токами действия. На поверхности клетки локальный ток течет от невозбужденного участка к возбужденному; внутри клетки он течет в обратном направлении. Локальный ток, как и любой электрический ток, оказывает раздражающее действие на соседние невозбужденные участки и вызывает увеличение проницаемости их мембран. Это приводит к снижению в них потенциала покоя. Когда деполяризация достигает критического значения, в этих участках возникают потенциалы действия, а в том участке, который ранее был возбужденным, в это время уже происходят восстановительные процессы реполяри-
185
зации. Вновь возбужденный участок в свою очередь становится электроотрицательным и возникающий локальный ток раздражает следующий за ним участок. Этот процесс многократно повторяется и обусловливает распространение импульсов возбуждения по всей длине клетки в обоих направлениях. В нервной системе прохождение импульсов только в определенном направлении обусловлено наличием синапсов, обладающих односторонней проводимостью.
Под влиянием локальных токов волна возбуждения распространяется вдоль волокна без затухания (бездекрементное проведение). Это обусловлено тем, что локальные токи только деполяризуют мембрану до критического уровня, а потенциалы действия в каждом участке мембраны поддерживаются независимыми ионными потоками, перпендикулярными к направлению распространения возбуждения.
Скорость уменьшения мембранного потенциала до критического уровня зависит от разности потенциалов между возбужденным и невозбужденным участками и от кабельных свойств волокна: электрической емкости и сопротивления мембраны, сопротивлений аксоплазмы и окружающей среды. Кабельные свойства волокна обеспечивают деполяризацию мембраны до критического уровня, а последующая диффузия натрия в клетку усиливает деполяризацию и обеспечивает незатухающее проведение импульса. Количественно процесс может быть представлен следующим образом. Скорость рас-
пространения потенциала действия определяется в основном тем временем, которое необходимо для критической деполяризации мембраны. Обозначим деполяризацию до критического уровня ΔFi. Тогда ΔFi, емкость С мембраны и заряд Δq, необходимый для деполяризации мембраны на ΔFi, будут связаны известным из физики соотношением:
(9)
Заряд мембраны и ее потенциал изменяется вследствие протекания локального тока I. Тогда время t , в течение которого заряд мембраны изменится на Δq, а потенциал на ΔFi, будет равно:
(10)
Из уравнений (9) и (10) получим:
(11)
Величина локального тока I по закону Ома определяется разностью потенциалов V между возбужденным и невозбужденным участками мембраны и сопротивлением R всех участков, по которым протекает локальный ток:
(12)
Сопротивление R суммируется из сопротивлений всех последовательных участков, по которым протекает локальный ток: мембраны, цитоплазмы, окружающей клетку жидкости. В основном оно определяется сопротивлением мембраны. Подставляя значение I в уравнение (11), получим:
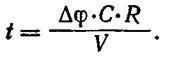
Учитывая, что ΔFi и V величины постоянные, можно написать:
(14)
где k — коэффициент пропорциональности.
187
Уравнение (14) показывает, что время деполяризации мембраны и, следовательно, время проведения возбуждения пропорциональны произведению R С, называемому постоянной времени мембраны. Тогда скорость проведения возбуждения будет обратно пропорциональна постоянной времени мембраны.
Согласно рассмотренной теории локальных токов, скорость проведения возбуждения должна иметь обратную зависимость от сопротивления внешней среды и цитоплазмы. Это положение получило экспериментальное подтверждение. Так, когда нервные волокна переносили из морской воды в масло, имеющее более высокое удельное сопротивление, то скорость проведения импульсов уменьшалась в 1,3 — 2 раза в зависимости от диаметра волокна. Напротив, при уменьшении сопротивления внешней среды путем помещения волокна на металлические полоски с закороченными концами скорость проведения импульса возрастала на 16%. Такой небольшой эффект обусловлен тем, что нервное волокно, имеющее цилиндрическую форму, контактирует с металлом на небольшом участке.
Скорость проведения импульса возрастает с увеличением диаметра волокна. Это объясняется тем, что с увеличением диаметра уменьшается сопротивление, приходящееся на единицу длины волокна.
В нервных волокнах характер распространения возбуждения зависит от наличия, или отсутствия в них миелиновых оболочек. В безмякотных волокнах возбуждение распространяется непрерывно вдоль всей мембраны. Все участки мембраны при этом в свое время становятся возбужденными. В мякотных нервных волокнах возбуждение распространяется несколько по иному. Мякотные нервные волокна имеют толстые миелиновые оболочки, которые через 1 — 3 мм прерываются с образованием так называемых перехватов Ранвье (см. рис. 33, II). В электрическом отношении миелин является изолятором; его удельное сопротивление в 10 млн. раз превышает удельное сопротивление раствора Рингера. В результате этого локальные токи через миелиновые оболочки протекать не могут; они циркулируют между перехватами Ранвье. При возбуждении одного перехвата Ранвье между ним и следующим перехватом возникают локальные токи и импульс как бы перескакивает на второй перехват, со второго — на третий и т.д.
Такой способ проведения нервного импульса называется сальтаторным. При блокировании одного перехвата Ранвье каким-либо анестезирующим веществом, например кокаином, импульс сразу передается на третий перехват. При блокировании сразу двух перехватов импульс дальше распространяться не может: сопротивление между первым и четвертым перехватами велико, и локальный ток между ними не достигает порогового значения.
В результате сальтаторного способа передачи скорость распространения нервного импульса в мякотных волокнах примерно в 10 раз выше, чем в безмякотных, при одинаковом диаметре волокон. Помимо этого, сальтатор-ный способ проведения возбуждения является более экономичным, поскольку в этом случае ионные потоки проходят не через всю поверхность клетки, как при непрерывном распространении, а только через поверхность в области перехватов Ранвье.
иффузионный потенциал. Уравнение Гендерсона.
Читайте также:
|











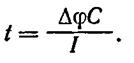

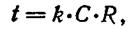
 (1)
(1)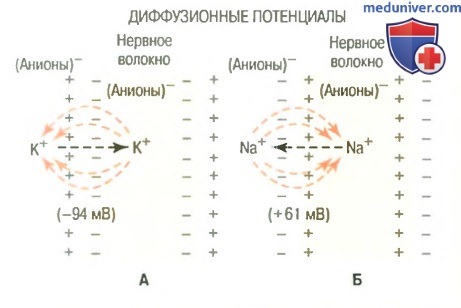 А. Установление диффузионного потенциала по обе стороны мембраны нервного волокна в связи с диффузией ионов калия изнутри клетки наружу через мембрану, избирательно проницаемую только для калия.
А. Установление диффузионного потенциала по обе стороны мембраны нервного волокна в связи с диффузией ионов калия изнутри клетки наружу через мембрану, избирательно проницаемую только для калия.