Урок химии в 8-м классе по теме «Химические уравнения»
Разделы: Химия
Цель: научить учащихся составлять химические уравнения. Научить их уравнивать с помощью коэффициентов на основе знания закона сохранения массы вещества М.В. Ломоносова.
Задачи:
- Образовательные:
- продолжить изучение физических и химических явлений с введением понятия «химическая реакция»,
- ввести понятие «химическое уравнение»;
- научить учащихся составлять химические уравнения, уравнивать уравнения с помощью коэффициентов.
- Развивающие:
- продолжить развивать творческий потенциал личности учащихся через создание ситуации проблемного обучения, наблюдения, проведения опытов химических реакций.
- Воспитательная:
- воспитать умение работать в команде, группе.
Оборудование: табличный материал, справочники, алгоритмы, набор заданий.
Д/О: «Горение бенгальских огней»:, спички, сухое горючее, железный лист/ ТБ при работе с огнём.
I. Организационный момент
Определение цели урока.
II. Повторение
1) На доске набор физических и химических явлений: испарение воды; фильтрование; ржавление; горение дров; скисание молока; таяние льда; извержение вулкана; растворение сахара в воде.
Задание:
Дать пояснение каждому явлению, назвать практическое применение данного явления в жизни человека.
На доске нарисована капля воды. Создать полную схему превращения воды из одного агрегатного состояния в другое. Как называется данное явление в природе и каково его значение в жизни нашей планеты и всего живого?
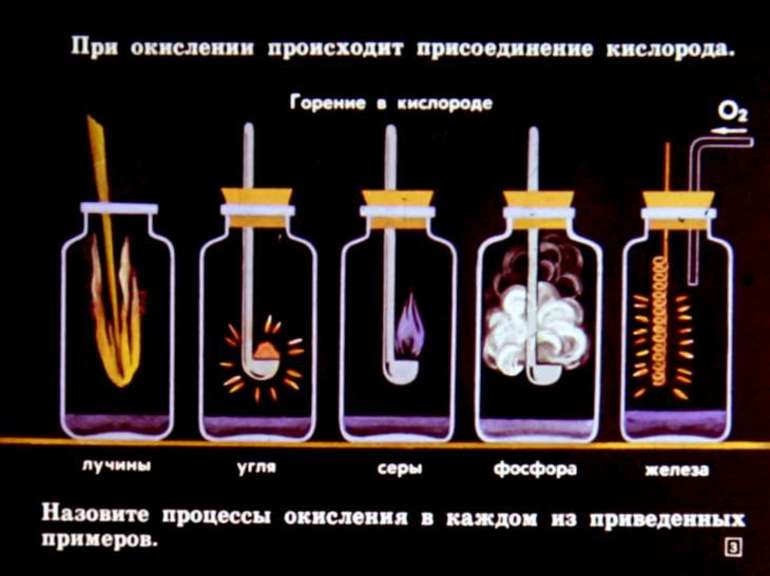
III. Д/О «Горение бенгальских огней»
1. Что происходит с магнием, который составляет основу бенгальского огня ?
2. Что явилось основной причиной такого явления?
3. К какому типу относится данная химическая реакция?
4. Попробуйте схематично изобразить химическую реакцию, которую вы наблюдали в этом опыте.
– Предлагаю попробовать составить схему данной реакции:
– Как мы узнали, что получилось другое вещество? (По признакам химической реакции: изменение окраски, появление запаха.)
– Какой газ находится в воздухе, который поддерживает горение? (Кислород – О)
IV. Новый материал
Химическую реакцию можно записывать с помощью химического уравнения.
Можно вспомнить понятия «уравнение», которое дается в математике. В чем суть самого уравнения? Что-то уравнивают, какие-то части.
Попробуем дать определение «химического уравнения», можно смотреть на схему и попытаться дать определение:
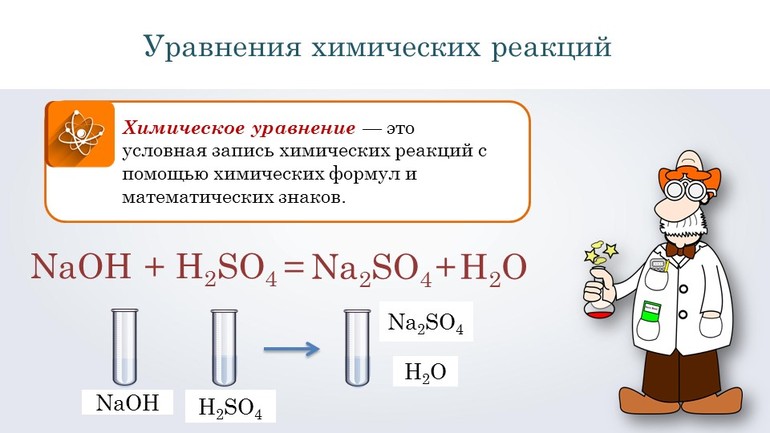
Химическое уравнение – это условная запись химической реакции с помощь химических знаков, формул и коэффициентов.
Химические уравнения записываются на основе Закона сохранения массы вещества, открытого М.В.Ломоносовым в 1756 году, который гласит (учебник стр. 96): «Масса веществ, вступивших в реакцию, равна массе веществ, получившихся в результате её».
– Надо научиться уравнивать химические уравнения с помощью коэффициентов.
– Для того чтобы хорошо научиться составлять химические уравнения, нам необходимо вспомнить:
– Что такое коэффициент?
– Что такое индекс?
Не забываем алгоритм «Составление химических формул».
Предлагаю пошаговый алгоритм составления химического уравнения:
V. Составления химического уравнения
1. Записываю в левой части уравнение вступающие в реакцию вещества: Al + O2
2. Ставлю знак «=» и записываю образующиеся вещества в правой части уравнения – продукты реакции: Al + O2 = Al2O3
3. Уравнивать начинаю с того химического элемента, которого больше или с кислорода, затем составляю конструкцию:
вступило кислорода «2», а получилось «3», их число не равно.
4. Ищу НОК (наименьшее общее кратное) двух цифр «2» и «3» – это «6»
5. Делю НОК «6» на число «2» и «3»и выставляю в качестве коэффициентов перед формулами.
6. Начинаю уравнивать следующие химические элементы – Al, рассуждаю так же. Вступило Al «1», а получилось «4», ищу НОК
Коэффициент «1» в уравнениях не пишется, но учитывается при составлении уравнения.
7. Читаю всю запись химического уравнения.
Такое долгое рассуждение позволяет быстро научиться уравнивать в химических уравнениях, учитывая, что правильное составление уравнений реакций для химии имеет большое значение: решение задач, написание химических реакций.
VI. Задание на закрепление
Фосфор + кислород = оксид фосфора (V)
Серная кислота + алюминий = сульфат алюминия + водород
Вода = водород + кислород
– Работает на доске один сильный ученик.
– Расставить коэффициенты в уравнениях химических реакций.
Химические уравнения отличаются по типам, но это мы рассмотрим на следующем уроке.
VII. Подведение итогов урока
Вывод. Выставление оценок.
VIII. Домашнее задание: § 27, упр. 2, с. 100.
Дополнительный материал: Р.т.с. 90-91, упражнение 2 – индивидуально.
Как решать химические уравнения — схемы и примеры решения для разных реакций
Основные термины и понятия
Составление уравнений химических реакций невозможно без знания определённых обозначений, показывающих, как проходит реакция. Объединение атомов, имеющих одинаковый ядерный заряд, называют химическим элементом. Ядро атома состоит из протонов и нейтронов. Первые совпадают с числом атомного номера элемента, а значение вторых может варьироваться. Простейшими веществами называют элементы, состоящие из однотипных атомов.
Любой химический элемент описывается с помощью символов, условно обозначающих структуру веществ. Формулы являются неотъемлемой частью языка науки. Именно на их основе составляют уравнения и схемы. По своей сути они отражают количественный и качественный состав элементов. Например, запись HNO3 сообщает, что в соединении содержится одна молекула азотной кислоты, а оно само состоит из водорода, азота и кислорода. При этом в состав одного моля азотной кислоты входит по одному атому водорода и азота и 3 кислорода.
Символика элементов, условное обозначение, представляет собой химический язык. В значке содержится информация о названии, массовом числе и порядковом номере. Международное обозначение принято, согласно периодической таблице Менделеева, разработанной в начале 1870 года.
Взаимодействующие между собой вещества называются реагентами, а образующиеся в процессе реакции — продуктами. Составление и решение химических уравнений фактически сводится к определению результатов реакций, поэтому просто знать формулы веществ мало, нужно ещё уметь подбирать коэффициенты. Располагаются они перед формулой и указывают на количество молекул или атомов, принимающих участие в процессе. С правой стороны от химического вещества ставится индекс, указывающий место элемента в системе.
Записывают уравнения в виде цепочки, в которой указываются все стадии превращения вещества начиная с левой части. Вначале пишут формулы элементов в исходном состоянии, а затем последовательно их преобразование.
Виды химических реакций
Химические явления характеризуются тем, что из двух и более элементов образуются новые вещества. Уравнения описывают эти процессы. Впервые с объяснениями протекания реакций знакомят в восьмом классе средней образовательной школы на уроках неорганической химии. Ученикам демонстрируют опыты, в которых явно наблюдаются различия в протекании реакций.
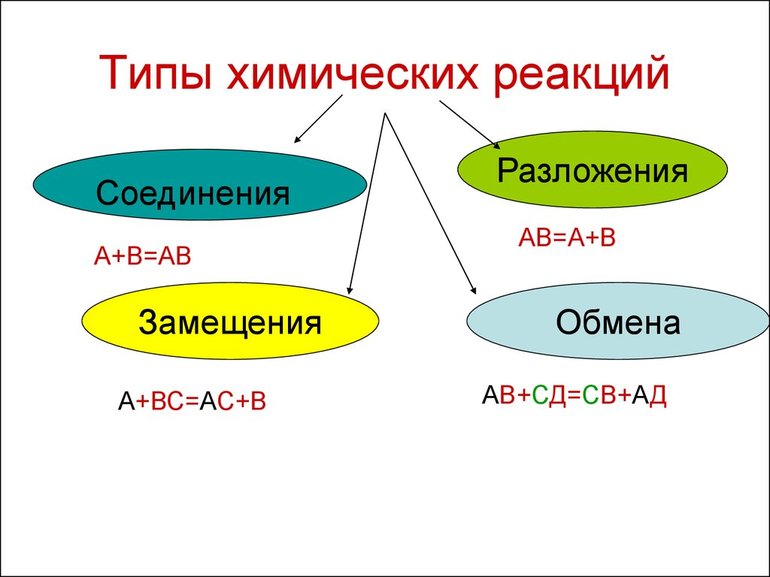
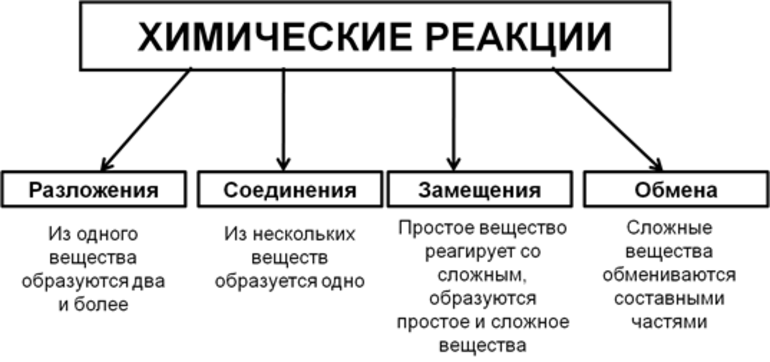
Всего существует 4 типа химического взаимодействия веществ:
- Соединение. В реакцию могут вступать 2 простых вещества: металл и неметалл или неметалл и неметалл. Например, алюминий с серой образуют сульфид алюминия. Кислород, взаимодействуя с водородом, превращается в воду. Объединятся могут 2 оксида с растворимым основанием, как оксид кальция с водой: CaO + H2O = Ca (OH)2 или основной оксид с кислотным: CaO + SO3 = CaSO4.
- Разложение. Это процесс обратный реакции соединения: было одно вещество, а стало несколько. Например, при пропускании электрического тока через воду получается водород и кислород, а при нагревании известняка 2 оксида: CaCO3 = CaO + CO2.
- Замещение. В реакцию вступают 2 элемента. Один из них простой, а второй сложный. В итоге образуются 2 новых соединения, при котором атом простого вещества заменяет сложный, как бы вытесняя его. Условие протекания процесса: простое вещество должно быть более активным, чем сложное. Например, Zn + 2HCl = ZnCl2 + H2. Величину активности можно узнать из таблицы ряда электрохимических напряжений.
- Обмен. В этом случае между собой реагируют 2 сложных элемента, обменивающиеся своими составными частями. Условием осуществления такого типа реакции является обязательное образование воды, газа или осадка. Например, CuO + 2HCl = CuCl2 + H2O. Чтобы узнать, смогут ли вещества прореагировать, используют таблицу растворимости.
Основными признаками химических реакций является изменение цвета, выделение газа или образование осадка. Различают их по числу веществ, вступивших в реакцию и образовавшихся продуктов. Правильное определение типа реакции особо важно при составлении химических уравнений, а также определения свойств и возможностей веществ.
Окислительно-восстановительный процесс
Составление большинства реакций сводится к подбору коэффициентов. Но при этом могут возникнуть трудности с установлением равновесия, согласно закону сохранения массы веществ. Чаще всего такая ситуация возникает при решении заданий, связанных с расстановкой количества атомов в уравнениях окислительно-восстановительных процессов.
Под ними принято понимать превращения, протекающие с изменением степени окисления элементов. При окислении происходит процесс передачи атомом электронов, сопровождающийся приобретением им положительного заряда или ионом, после чего он становится нейтральным. При этом также происходит процесс восстановления, связанный с присоединением элементарных частиц атомом.
Для составления уравнений необходимо определить восстановитель, окислитель и число участвующих в реакции электронов. Коэффициенты же подбирают с помощью метода электронно-ионного баланса (полуреакций). Его суть состоит в установлении равенства путём уравнивания количества электронов, отдаваемых одним элементом и принимаемым другим.
Классический алгоритм
В основе решения задач этим методом — закон сохранения массы. Согласно ему, совокупная масса элементов до реакции и после остаётся неизменной. Другими словами, происходит перегруппировка частиц. Если рассматривать решение химического уравнения поэтапно, оно будет состоять из трёх шагов:
- Написания формул элементов, вступающих в реакцию с левой стороны.
- Указания справа формулы образующихся веществ.
- Уравнивания числа атомов с добавлением коэффициентов.
Перед тем как переходить к сложным соединениям, лучше всего потренироваться на простых. Например, нужно составить уравнение, описывающее взаимодействие двух сложных веществ: гидроксида натрия и серной кислоты. При таком соединении образуется сульфат натрия и вода.
Согласно алгоритму, в левой части уравнения необходимо записать реагенты, а в правой продукты реакции: NaOH + H2SO 4 → Na 2SO4 + H2O. Теперь следует уравнять коэффициенты. Начинают с первого элемента. В примере это натрий. В правой части содержится 2 его атома, а в левой один, поэтому необходимо возле реагента поставить цифру 2. Затем нужно уровнять водород. В результате получится выражение: 2 NaOH + H2SO 4 → Na2 SO4 +2H2O.
Ещё одним наглядным примером является процесс реакции тринитротолуола с кислородом. При их взаимодействии образуется: C7H5N3O6 + O2 → CO2 + H2O + N2. Исходя из того, что слева находится нечётное число атомов H и N, а справа чётное, нужно их уравнять: 2C7H5N3O6 + O2 → CO2 + H2O + N2.
Теперь становится понятным, что 14 и 10 атомов углерода и водорода должны образовать 14 долей диоксида и 5 молекул воды. При этом 6 атомов азота превратятся в 3. Итоговое уравнение будет выглядеть как 2C7H5N3O6 + 10,5O2 → 14CO2 + 5H2O + 3N2.
Перед тем как начинать тренировку по составлению уравнений, следует научиться расставлять валентность. Это параметр, равный числу соединившихся атомов каждого элемента. Фактически это способность к соединению. Например, в формуле NH3 валентность атома азота равна 3, а водорода 1.
Решение методом полуреакций
Алгоритм для решения примеров химических уравнений проще рассмотреть на конкретном задании. Пускай необходимо описать процесс окисления пирита азотной кислоты с малой концентрацией: FeS2 + HNO3. Решать этот пример необходимо в следующей последовательности:
- Определить продукты реакции. Так как кислота является сильным окислителем, сера получит максимальную степень оксидации S6+, а железо Fe3+. HNO3 может восстановиться до одного из двух состояний NO2 или NO.
- Исходя из состава ионов и правила, что вещества, переходящие в газовую форму или плохо растворимые, записываются в молекулярном виде, верным будет записать: FeS2 — Fe3+ + 2SO2−4. Гидролизом можно пренебречь.
- В записи уравнивают кислород. Для этого в левую часть добавляют 8 молекул воды, а в правую 16 ионов водорода: FeS2 + 8H20 — Fe3+ + 2SO2−4 + 16H+. Так как заряда в левой части нет, а в правой он равный +15, то серное железо должно будет отдать 15 электронов. Значит, уравнение примет вид: FeS2 + 8H20 — 15e → Fe3+ + 2SO2−4 + 16H+.
- Теперь переходят к реакции восстановления нитрата иона: NO-3 →NO. Для её составления нужно отнять у оксида азота 2 атома кислорода. Делают это путём прибавления к левой части 4 ионов водорода, а правой — 2 молекул воды. В итоге получится: NO-3 + 4H+ → NO + 2H2O.
- Полученную формулу уравнивают добавлением к левой части 3 электронов: NO-3 + 4H+ 3e → NO + 2H2O.
- Объединяют найденные выражения и записывают результат: FeS2 + 8H20 + 5NO-3 + 20H+ → Fe3+ + 2SO2−4 + 16H+ + 5NO + 10H2O.
Уравнение можно сократить на 16H + и 8H2O. В итоге получится сокращённое выражение окислительно-восстановительной реакции: FeS2 + 5NO — 3 + 4 H + = Fe3 + + 2SO 2- 4 + 5NO + 2H2O.
Такой алгоритм считается классическим, но для упрощения понимания лучше использовать способ электронного баланса. Процесс восстановления переписывают как N5+ + 3e → N2+. Степень же окисления составить сложнее. Сере нужно приписать степень 2+ и учесть, что на 1 атом железа приходится 2 атома серы: FeS2 → Fe3++ 2S6+. Запись общего баланса будет выглядеть: FeS2 + 5N5+ = Fe3+ + 2S6+ + 5N2+.
Пять молекул потратятся на окисление серного железа, а ещё 3 на образование Fe (NO3)3. После уравнения двух сторон запись реакции примет вид, аналогичный полученному с использованием предыдущего метода.
Использование онлайн-расчёта
Простые уравнения решать самостоятельно довольно просто. Но состоящие из сложных веществ могут вызвать трудности даже у опытных химиков. Чтобы получить точную формулу и не подбирать вручную коэффициенты, можно воспользоваться онлайн-калькуляторами. При этом их использовать сможет даже пользователь, не особо разбирающийся в науке.
Чтобы расстановка коэффициентов в химических уравнениях онлайн происходила автоматически, нужно лишь подключение к интернету и исходные данные. Система самостоятельно вычислит продукты реакции и уравняет обе стороны формулы. Интересной особенностью таких сайтов является не только быстрый и правильный расчёт, но и описание правил с алгоритмами, по которому выполняются действия.
После загрузки калькулятора в веб-обозревателе единственное, что требуется от пользователя — правильно ввести реагенты в специальные формы латинскими буквами и нажать кнопку «Уравнять». Иногда возникает ситуация, когда запись сделана верно, но коэффициенты не расставляются. Это происходит, если суммы в уравнении могут быть подсчитаны разными способами. Характерно это для реакций окисления. В таком случае нужно заменить фрагменты молекул на любой произвольный символ. Таким способом можно не только рассчитать непонятное уравнение, но и выполнить проверку своих вычислений.
Уравнения химических реакций

Средняя оценка: 4.3
Всего получено оценок: 979.
Средняя оценка: 4.3
Всего получено оценок: 979.
Запись химического взаимодействия, отражающая количественную и качественную информацию о реакции, называют уравнением химических реакций. Записывается реакция химическими и математическими символами.
Основные правила
Химические реакции предполагают превращение одних веществ (реагентов) в другие (продукты реакции). Это происходит благодаря взаимодействию внешних электронных оболочек веществ. В результате из начальных соединений образуются новые.
Чтобы выразить ход химической реакции графически, используются определённые правила составления и написания химических уравнений.
В левой части пишутся изначальные вещества, которые взаимодействуют между собой, т.е. суммируются. При разложении одного вещества записывается его формула. В правой части записываются полученные в ходе химической реакции вещества. Примеры записанных уравнений с условными обозначениями:
- CuSO4 + 2NaOH → Cu(OH)2↓+ Na2SO4;
- CaCO3 = CaO + CO2↑;
- 2Na2O2 + 2CO2 → 2Na2CO3 + O2↑;
- CH3COONa + H2SO4(конц.) → CH3COOH + NaHSO4;
- 2NaOH + Si + H2O → Na2SiO3 + H2↑.
Коэффициенты перед химическими формулами показывают количество молекул вещества. Единица не ставится, но подразумевается. Например, уравнение Ba + 2H2O → Ba(OH)2 + H2 показывает, что из одной молекулы бария и двух молекул воды получается по одной молекуле гидроксида бария и водорода. Если пересчитать количество водорода, то и справа, и слева получится четыре атома.
Обозначения
Для составления уравнений химических реакций необходимо знать определённые обозначения, показывающие, как протекает реакция. В химических уравнениях используются следующие знаки:
- → – необратимая, прямая реакция (идёт в одну сторону);
- ⇄ или ↔ – реакция обратима (протекает в обе стороны);
- ↑ – выделяется газ;
- ↓ – выпадает осадок;
- hν – освещение;
- t° – температура (может указываться количество градусов);
- Q – тепло;
- Е(тв.) – твёрдое вещество;
- Е(газ) или Е(г) – газообразное вещество;
- Е(конц.) – концентрированное вещество;
- Е(водн.) – водный раствор вещества.
Вместо стрелки (→) может ставиться знак равенства (=), показывающий соблюдение закона сохранения вещества: и слева, и справа количество атомов веществ одинаково. При решении уравнений сначала ставится стрелка. После расчёта коэффициентов и уравнения правой и левой части под стрелкой подводят черту.
Условия реакции (температура, освещение) указываются сверху знака протекания реакции (→,⇄). Также сверху подписываются формулы катализаторов.
Какие бывают уравнения
Химические уравнения классифицируются по разным признакам. Основные способы классификации представлены в таблице.
Признак
Реакции
Описание
Пример
По изменению количества реагентов и конечных веществ
Из простого и сложного вещества образуются новые простые и сложные вещества
Несколько веществ образуют новое вещество
Из одного вещества образуется несколько веществ
Обмен составными частями (ионами)
По выделению тепла
По типу энергетического воздействия
Действие электрического тока
Действие высокой температуры
По агрегатному состоянию
Существует понятие химического равновесия, присущее только обратимым реакциям. Это состояние, при котором скорости прямой и обратной реакции, а также концентрации веществ равны. Такое состояние характеризуется константой химического равновесия.
При внешнем воздействии температуры, давления, света реакция может смещаться в сторону уменьшения или увеличения концентрации определённого вещества. Зависимость константы равновесия от температуры выражается с помощью уравнений изобары и изохоры. Уравнение изотермы отражает зависимость энергии и константы равновесия. Эти уравнения показывают направление протекания реакции.

Что мы узнали?
В уроке химии 8 класса была рассмотрена тема уравнений химических реакций. Составление и написание уравнений отражает ход химической реакции. Существуют определённые обозначения, показывающие состояние веществ и условия протекания реакции. Выделяют несколько видов химических реакций по разным признакам: по количеству вещества, агрегатному состоянию, поглощению энергии, энергетическому воздействию.
http://nauka.club/khimiya/khimicheskie-uravneniya.html
http://obrazovaka.ru/himiya/uravneniya-himicheskih-reakciy-8-klass.html