Уравнение изотермы полимолекулярной адсорбции теории бэт
Любые гетерогенные процессы, например, разложение или образование химического соединения, растворение твердых тел, газов или жидкостей, испарение, возгонка и т.п., а также многие другие процессы проходят в присутствии поверхностей раздела фаз (твердое тело — газ, твердое тело — жидкость, газ – жидкость). Состояние вещества у поверхности раздела соприкасающихся фаз отличается от его состояния внутри этих фаз вследствие различия молекулярных взаимодействий в разных фазах. Это различие вызывает особые поверхностные явления на границе раздела фаз.
Представим себе поверхность твердого тела на границе с газом. Внутри твердого тела частицы (атомы, ионы или молекулы), образующие его решетку, правильно чередуются в соответствии с кристаллической структурой, причем их взаимодействия уравновешены. Состояние же частицы, находящейся на поверхности, иное — взаимодействия таких частиц не уравновешены, и поэтому поверхность твердого тела притягивает молекулы вещества из соседней газовой фазы. В результате концентрация этого вещества на поверхности становится больше, чем в объеме газа, газ адсорбируется поверхностью твердого тела.
Таким образом, адсорбция представляет собой концентрирование вещества на поверхности раздела фаз. Вещество, на поверхности которого происходит адсорбция ‒ адсорбент , а поглощаемое из объемной фазы вещество — адсорбат .
Адсорбент поглощает из объемной фазы тем больше вещества, чем больше развита его поверхность. Поверхность, приходящаяся на 1 г адсорбента, называют удельной поверхностью. Величина удельной поверхности у различных адсорбентов может быть весьма различной. Непористые тела имеют удельную поверхность от нескольких м 2 /г до сотен м 2 /г. Большое увеличение поверхности связано обычно с наличием в твердом теле узких пор. Примерами таких высокодисперсных пористых тел с удельной поверхностью до нескольких тысяч м 2 /г являются активированный уголь и силикагель.
Количественно адсорбция может быть выражена с помощью нескольких величин:
- величиною а, представляющей собой количество адсорбата, находящегося в объеме адсорбционного слоя, отвечающего единице массы адсорбента (моль/г).
- величиною Г, представляющей собой избыток числа молей адсорбата в объеме поверхностного слоя площадью 1 см 2 по сравнению с числом его молей в том же объеме, если бы у межфазной границы не происходило изменение концентрации адсорбата (Г>0 — адсорбция, Г адсорбционного равновесия , аналогичное равновесию между испарением и конденсацией. Адсорбционное равновесие — это динимическое равновесие которое наступает тогда, когда скорость процесса адсорбции равна скорости обратного процесса десорбции. Понятно, что чем выше концентрация адсорбата, тем больше адсорбция. Также ясно, что чем выше температура, тем меньше физическая адсорбция. Для каждой температуры существует свое адсорбционное равновесие.
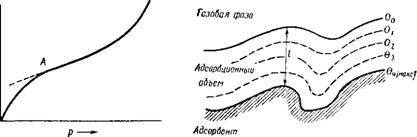
Адсорбцию принято характеризовать зависимостью количества адсорбированного вещества а от концентрации (или равновесного давления). Графики а=f(c) или а=f(р) при Т=const называют изотермами адсорбции . Вид обычной изотермы показан на рис.9.1.
Рисунок 9.1 ‒ Типичный вид изотермы адсорбции
Как можно видеть, изотерма имеет три характерных участка. Начальный круто поднимающийся вверх почти прямолинейный участок кривой показывает, что при малых концентрациях адсорбция пропорциональна концентрации. Это область, в которой выполняется закон Генри:[TEX]а=К\cdot<с>[/TEX], где К – константа Генри, не зависящая от концентрации с. В области I поверхность адсорбента в значительной степени свободна.
Почти горизонтальный участок III соответствует большим концентрациям и отвечает поверхности адсорбента, полностью насыщенной адсорбатом. В. этих условиях, если на поверхности может образоваться лишь мономолекулярный слой адсорбата, количество его практически перестает зависеть от концентрации. Средний участок II кривой соответствует промежуточным степеням заполнения поверхности.
Важной задачей теории адсорбции является вывод уравнения изотермы адсорбции. В настоящее время эта задача еще далека от разрешения. Для описания изотермы адсорбции предложен ряд эмпирических формул. Из них наиболее широко используется уравнение Фрейндлиха :
где X — количество адсорбированного вещества, моль; m — масса адсорбента; с — равновесная концентрация, b и 1/n – константы.
Константы b и 1/n уравнения Фрейндлиха легко найти графически по изотерме, построенной в логарифмических координатах:
Это уравнение прямой. Тангенс угла наклона этой прямой равен 1/n, а отрезок, отсекаемый прямой на оси ординат, равен lnb. Константа b обычно колеблется в широких пределах. Физический смысл ее становится ясным, если принять с=1, тогда b представляет собой величину адсорбции при равновесной концентрации адсорбата 1 моль/л. Показатель 1/n принимается постоянным, лежащим в пределах 0,2 -1,0 для адсорбции из газовой среды и 0,1 — 0,5 для адсорбции из растворов. Поэтому уравнение Фрейндлиха пригодно лишь для концентраций, меньших 0,5 моль/л.2.
Мономолекулярная адсорбция. Изотерма адсорбции Ленгмюра
Фундаментальным вкладом в учение об адсорбции явилась теория Ленгмюра . Эта теория позволяет учесть наиболее сильные отклонения от закона Генри, связанные с ограниченностью поверхности адсорбента. Это обстоятельство приводит к адсорбционному насыщению поверхности адсорбента по мере увеличения концентрации адсорбируемого вещества. Это положение является основным в теории Ленгмюра и уточняется следующими допущениями:
- адсорбция локализована на отдельных адсорбционных центрах, каждый из которых взаимодействует только с одной молекулой адсорбата. На поверхности адсорбента образуется поэтому мономолекулярный слой адсорбата;
- адсорбционные центры энергетически эквивалентны;
- адсорбированные молекулы не взаимодействуют друг с другом.
Для вывода изотермы адсорбции Ленгмюра учтем, что при установлении в системе адсорбционного равновесия скорость адсорбции ([TEX]V\downarrow [/TEX])должна равняться скорости десорбции( [TEX]V\uparrow [/TEX] ). Для того, чтобы молекула адсорбировалась, она должна удариться о поверхность и попасть на незанятое место. Учитывая, что число ударов пропорционально концентрации С, а вероятность попасть на незанятое место пропорционально их числу, имеем
где[TEX]\Theta[/TEX]- доля занятых мест,[TEX]k_1[/TEX]- константа скорости адсорбции. Скорость десорбции прямо пропорциональна числу адсорбированных молекул:
где[TEX]k_2[/TEX]- константа скорости десорбции.
где[TEX] K=k_1/k_2[/TEX]- константа адсорбционного равновесия.
Обозначим символом[TEX]a_\infty[/TEX]максимальную адсорбцию или емкость адсорбционного монослоя. Тогда
Это уравнение носит название изотермы адсорбции Ленгмюра. Для газов и паров концентрацию можно заменить пропорциональным ей значением давления и изотерма адсорбции примет вид
Константы адсорбционного равновесия К и[TEX]K_p[/TEX]характеризуют энергию взаимодействия адсорбата с адсорбентом. Чем сильнее это взаимодействие, тем больше значение константы адсорбционного равновесия.
Важны экстраполяционные следствия уравнения изотермы Ленгмюра. При[TEX]C\rightarrow<0>[/TEX]имеем[TEX]a=a_\infty<\cdot>K\cdot
Эти выражения соответствуют закону Генри: величина адсорбции линейно растет с увеличением концентрации. Таким образом уравнение Ленгмюра является более общим соотношением, включающим и уравнение Генри.
При больших концентрациях, когда[TEX] K_c\gg1[/TEX]
Эти соотношения отвечают насыщению, когда вся поверхность адсорбента покрывается мономолекулярным слоем адсорбата. Экспериментальные результаты по определению изотермы адсорбции обычно обрабатывают с помощью уравнения Ленгмюра, записанного в линейной форме:
Методика нахождения коэффициентов уравнения Ленгмюра показана на рис. 9.2.
Рисунок 9.2 ‒ К нахождению констант уравнения Ленгмюра
Полимолекулярная адсорбция. Уравнение БЭТ
Опыт показывает, что наряду с изотермами адсорбции, которые описываются уравнением Ленгмюра и о которых мы говорили, часто встречаются изотермы, не имеющие участка, параллельного оси давлений и отвечающего насыщению поверхности адсорбента молекулами адсорбата. Такая изотерма — показана на рис 9.3. Это связано с явлением, при котором на активных центрах поверхности адсорбента образуются несколько слоев молекул или ионов адсорбата — полимолекулярная адсорбция .
Наиболее удачная теория (из многочисленных), описывающая подобные процессы была создана в 1935-1940 гг. Брунауэром, Эмметом, Теллером применительно к адсорбции паров. Их теория получила название теории БЭТ. Ее основные положения:
- Адсорбционные слои полимолекулярны, причем их толщина на разных участках поверхности различна.
- Адсорбционные силы тождественны силам, вызывающим конденсацию.
Рисунок 9.3 ‒ Изотерма полимолекулярной адсорбции
Последнее положение может быть обосновано следующим образом: лишь первый слой молекул адсорбата находится в непосредственной близости к поверхности твердого тела. Второй, и особенно последующие слои, прилегают к молекулам, подобным им, и их образование напоминает обычную конденсацию пара на поверхности жидкости.
На основании этих представлений Брунауэр, Эммет и Теллер вывели следующее уравнение изотермы адсорбции паров:
где[TEX]K_П[/TEX]- константа равновесия полимолекулярной адсорбции, Р — давление пара, [TEX]P_s[/TEX] — давление насыщенного пара при данной температуре,[TEX]a_\infty[/TEX]- емкость монослоя.
При низких давлениях, когда[TEX]p/p_s\ll 1[/TEX], учитывая, что[TEX]K_p=K_П\cdot<1/p_s>[/TEX], получаем уравнение Ленгмюра:
Уравнение изотермы полимолекулярной адсорбции БЭТ легко привести к линейной форме:
По наклону этой прямой и отсекаемому ею отрезку на оси ординат можно найти значения констант[TEX]a_\infty[/TEX]и[TEX]K_П[/TEX].
Теория БЭТ, так же как и теория Ленгмюра, указывает путь для определения удельной поверхности адсорбента (любого твердого вещества). Для этого находят емкость монослоя [TEX]a_\infty[/TEX] для паров простых веществ ( [TEX]N_2[/TEX] , Ar, Kr) при низких температурах. Затем, зная площадь [TEX]S_0[/TEX] , занимаемую одной молекулой простого вещества, вычисляют удельную поверхность адсорбента:
где [TEX]N_a[/TEX] — число Авогадро. Это метод определения удельной поверхности по БЭТ.
Энергетические параметры адсорбции на однородной поверхности
Между энергией Гиббса, энтальпией и энтропией адсорбции существует известное соотношение:
Адсорбция — самопроизвольный процесс, а всякому самопроизвольному процессу при P,T=const отвечает условие [TEX]\Delta [TEX]\Delta
Если адсорбция подчиняется уравнениям Генри и Ленгмюра, т.е. константа равновесия адсорбции в этих уравнениях не зависят от степени заполнения поверхности, то стандартная энергия Гиббса адсорбции может быть рассчитана по уравнению, справедливому для химических реакций:
Энтальпию адсорбции определяют из экспериментальной зависимости константы равновесия адсорбции от температуры в соответствии с уравнением изобары Вант-Гоффа
Принимая во внимание слабую зависимость изменения энтальпии от температуры, находим
Тангенс угла наклона прямой lnK — 1/T равен -[TEX]\Delta
Энтропию адсорбции, подчиняющейся закону Генри или уравнению Ленгмюра, легко рассчитать, если известны [TEX]\Delta
Данные соотношения для расчета энергетических параметров адсорбции получены, исходя из предположения, что поверхность адсорбента однородна (эквипотенциальна) и на ней образуется мономолекулярный слой адсорбата.
Если адсорбция происходит на неоднородной поверхности, то наиболее реакционноспособные адсорбционные центры будут заняты уже при малых равновесных концентрациях. Таким образом, энергетические параметры адсорбции зависят от степени заполнения поверхности адсорбатом. Например, дифференциальная теплота адсорбции будет уменьшаться по мере заполнения поверхности.
Взаимодействие частиц в адсорбционном слое и классификация изотерм адсорбции
Одним из опорных пунктов теории Ленгмюра является константа отсутствия взаимодействия частиц адсорбата в адсорбционном слое, Однако ленгмюровская адсорбция является лишь частным случаем в многообразном мире адсорбционных процессов. На рис. 9.4 показаны различные формы изотерм адсорбции из разбавленных растворов.
Рисунок 9.4 ‒ Формы изотерм адсорбции
Исходя из формы начального участка были выделены четыре характерных класса изотерм (S, L, H, C). Деление изотерм на отдельные типы внутри каждого класса связано с последующим изменением их формы при наиболее высоких концентрациях. Класс L (класс Ленгмюра) является наиболее общим. Изотермы типа L2 достигают насыщения, дальнейшая адсорбция выше этого уровня дает изотерму типа L3. Если достигается второе плато, то имеем дело с изотермой L4. Для изотерм типа L5 характерно наличие максимума. Максимум отражает изменение состояния вещества в растворе — например, ассоциацию молекул при определенной концентрации. Сходный, хотя и не столь полный, набор типов изотерм получен и для других классов.
Начальный участок изотерм S — класса выгнут относительно оси концентраций, однако далее часто следует точка перегиба, что и придает изотерме характерную S -обратную форму.
Изотермы класса Н (высокое сродство – higf) наблюдается при чрезвычайно сильной адсорбции при очень низких концентрациях; они пересекаются с осью ординат. Изотермы класса С (constant) имеют начальный линейный участок, что указывает на постоянное распределение растворенного вещества между раствором и адсорбентом (постоянная скорость адсорбции).
Теоретический анализ различных типов изотерм адсорбции позволяет получить много полезной информации о механизме адсорбции. При этом следует принимать во внимание величину энергии активации процесса удаления молекул адсорбата с поверхности адсорбента. Если взаимодействие между адсорбированными молекулами пренебрежимо мало, энергия активации не зависит от степени заполнения поверхностиf a это приведет к изотерме типа L или Н.
Если сила взаимодействия между адсорбированными молекулами больше силы взаимодействия между растворенным веществом и адсорбентом, энергия активации возрастает и адсорбция описывается изотермой типа S. В этом случае молекулы растворенного вещества стремятся расположиться на поверхности в виде цепей.
Изотермы типа Н наблюдаются в тех случаях, когда имеет место хемосорбция.
Изотерма типа С характерна для адсорбции на микропористых адсорбентах и соответствует таким условиям, при которых число адсорбционных центров остается постоянным в широкой области концентраций. По мере заполнения одних центров появляются новые, и доступная для адсорбции поверхность увеличивается пропорционально количеству адсорбированного вещества.
Уравнение изотермы полимолекулярной адсорбции теории бэт
В большинстве случаев реальная поверхность твердого тела не вполне однородна энергетически; адсорбция, как правило, не является строго локализованной; адсорбированные молекулы практически всегда взаимодействуют между собой; наконец, стехиометрия может нарушаться, вследствие чего адсорбция не будет ограничена образованием одного слоя. Поэтому реальные изотермы адсорбции всегда отклоняются от изотермы Ленгмюра. Еще самим Ленгмюром было показано, что если адсорбционные центры считать энергетически неоднородными, то суммарная адсорбция на всех центрах будет выражена следующим уравнением:
где i — количество групп одинаковых центров.
Брунауэр, Эммет и Теллер отказались от второго допущения Ленгмюра, приводящего к мономолекулярной адсорбции. Для случая, когда температура адсорбтива ниже критической (то есть, это еще пар) они разработали теорию полимолекулярной адсорбции. После анализа многочисленных реальных изотерм адсорбции ими была предложена их классификация на основе выделения пяти основных типов изотерм.
Изотермы типа I отражают мономолекулярную адсорбцию. Изотермы типа II и III обычно связывают с образованием при адсорбции многих слоев, то есть, с полимолекулярной адсорбцией. Приче м, в случае II взаимодействие адсорбент — адсорбат сильнее взаимодействия адсорбат — адсорбат, а в случае III — наобор от. Изотермы типа IV и V отличаются тем, что для них характерна конечная адсорбция при приближении давления пара к давлению насыщения ps. Изотермы типа II и III характерны для адсорбции на не пористом адсорбенте, а типа IV и V — на пористом твердом теле. Все пять типов изотерм адсорбции описываются теорией полимолекулярной адсорбции “БЭТ”, названной так по начальным буквам фамилий ее авторов.
Теория БЭТ сохраняет ленгмюровские представления о динамическом характере адсорбции. Адсорбция считается полислойной. Молекулы первого слоя адсорбируются на поверхности адсорбента в результате межмолекулярного взаимодействия адсорбент — адсорбат. Каждая адсорбированная молекула первого адсорбционного слоя может, в свою очередь, являться центром адсорбции молекул второго слоя и т.д. Так формируются второй и последующие сорбционные слои. Теплота адсорбции в первом слое q1 определяется взаимодействием адсорбат — адсорбент, во всех последующих слоях — взаимодействием адсорбат — адсорбат. Поэтому теплота адсорбции во всех слоях, начиная со второго, равна теплоте конденсации λ. Второй и последующие адсорбционные слои могут начинать образовываться и при незавершенном первом слое, как это показано на рисунке:
Составив уравнение адсорбционного равновесия для каждого слоя и просуммировав их, авторы теории БЭТ получили уравнение для полислойной адсорбции:
В приведенном уравнении АМ — емкость монослоя, С — константа, равная е (q1− λ) / RT . При малых относительных давлениях, когда р как частный случай уравнения БЭТ. В случаях, когда q1 > λ , т.е. энергия взаимодействия адсорбент — адсорбат больше энергии взаимодействия адсорбат — адсорбат, изотерма адсорбции выпукла и относится к типу II или IV. Если же энергия взаимодействия адсорбат — адсорбат больше теплоты адсорбции ( λ > q1 ), то изотерма адсорбции вогнута и относится к типу III или V.
Уравнение изотермы адсорбции БЭТ широко используется для определения величины удельной поверхности адсорбентов. Изотерма адсорбции выражается прямой линией, отсекающей на оси ординат отрезок, равный 1 / АМ С , а тангенс угла ее наклона к оси абсцисс равен (С − 1) / АМ С.
Из этих значений можно найти величину АМ, а зная ее, рассчитать по уравнению удельную поверхность адсорбента. Стандартной методикой для определения удельной поверхности адсорбентов принято считать измерение изотермы адсорбции азота при 77 К. В этом случае wо = 0.162 нм 2 .
- Источник: Пальтиель Л.Р., Зенин Г.С., Волынец Н.Ф. КОЛЛОИДНАЯ ХИМИЯ: Учеб. пособие. – СПб: СЗТУ, 2004. – 68 с.
- Источник: Кукушкина И.И., Митрофанов А.Ю. Коллоидная химия, Кемерово:2009 — 185 с.
Лако-красочные материалы — производство
Технологии и оборудование для изготовления красок, ЛКМ
ТЕОРИЯ ПОЛИМОЛЕКУЛЯРНОИ АДСОРБЦИИ ПОЛЯНИ И ТЕОРИЯ БЭТ
Опыт показал, что наряду с изотермами адсорбции, вид которых показан на рис. IV, 1, довольно часто на практике встречаются изотермы, не имеющие второго участка, почти параллельного оси давлений и отвечающего насыщению поверхности адсорбента молекулами адсорбтива. Вид таких изотерм изображен на рис. IV, 5. Как можно видеть, в точке А изотерма Ленгмюра круто поднимается кверху. Очевидно, связывание адсорбтива адсорбентом не прекращается после образования мономолекулярного слоя, а продолжается дальше. Форму подобных изотерм нельзя объяснить
Рис. IV, 5. Вид изотермы, характерной для полимолекуляр- иой адсорбции.
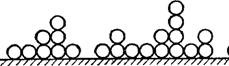
Рис. IV, 6. Схема адсорбционного объема по представлениям полимолекулярной теории адсорбции.
Как следствие капиллярной конденсации, так как такая изотерма наблюдается и у непористых адсорбентов, когда капиллярная конденсация невозможна.
Для объяснения этого явления Поляни в 1915 г. предложил теорию полимолекулярной адсорбции, называемую также потенциальной. Рассмотрим кратко исходные положения этой теории, особенно пригодной в случае адсорбции паров на твердом теле.
1. Адсорбция обусловливается чисто физическими силами.
2. На поверхности адсорбента нет активных центров, а адсорбционные силы действуют вблизи от поверхности адсорбента и образуют около этой поверхности со стороны газовой фазы непрерывное силовое поле.
3 Адсорбционные силы действуют на сравнительно большие расстояния, во всяком случае большие, чем размеры отдельных молекул адсорбтива, и поэтому можно говорить о существовании У поверхности адсорбента адсорбционного объема, который заполняется при адсорбции молекулами адсорбтива.
4. Действие адсорбционных сил по мере удаления от поверхности уменьшается и на некотором расстоянии практически стано — вится равным нулю.
5. Притяжение данной молекулы поверхностью адсорбента не зависит от наличия в адсорбционном пространстве других молекул, вследствие чего возможна полимолекулярная адсорбция.
6. Адсорбционные силы не зависят от температуры, и, следовательно, с изменением температуры адсорбционный объем не изменяется Это не противоречит тому, что с повышением температуры адсорбция уменьшается; в этом случае снижение адсорбции обусловливается не уменьшением адсорбционных сил, а увеличением в результате нагревания интенсивности теплового движения адсорбированных молекул, что приводит к увеличению десорбции.
Из рассмотрения положений теории полимолекулярной адсорбции можно видеть, что силовое поле, возникающее у поверхности адсорбента, во многом сходно с гравитационным полем (ненасыщаемость поля молекулами адсорбтива, находящимися непосредственно на поверхности адсорбента; независимость сил, действующих в поле, от температуры).
На рис. IV, 6 схематически показан разрез адсорбционного объема, отвечающий представлению теории полимолекулярной адсорбции. Как и во всяком силовом поле, в адсорбционном поле можно представить себе эквипотенциальные поверхности, т е. поверхности с одним и тем же адсорбционным потенциалом. На рисунке они обозначены пунктирными линиями. Под адсорбционным потенциалом 0 следует понимать работу, совершаемую против адсорбционных сил при перемещении 1 моля адсорбтива (пара) из данный точки поля в газовую фазу. Очевидно, максимальный адсорбционный потенциал должен существовать на границе адсорбент — адсорбционный объем. На границе адсорбционный объем — газовая фаза, т. е. там, где кончается действие адсорбционных сил, потенциал 0 должен быть равным нулю.
Изменение адсорбционного потенциала обычно выражаетсн в теории полимолекулярной адсорбции не как функция расстояния I от поверхности адсорбента, а как функция адсорбционного объема V. Это обусловлено тем, что функция 0 = /(V) экспериментально сравнительно легко определяется, в то время как нахождение функции 0 = F(L) вызывает подчас иеопреодолимые трудности В самом деле, адсорбционный объем легко иайти, если работа ведется, например, при достаточно низких температурах Тогда адсорбтив находится в Адсорбционном пространстве в виде жидкости. В этом случае заполненный жидкостью адсорбционный объем Уж, отвечающий 1 г адсорбента, выражается следующим уравнением
Уж = вКмол (IV, 14)
Где а — количество адсорбтива (в молях), адсорбированного I г адсорбента; Умол — мольный объем конденсата.
Толщину слоя жидкости в адсорбционном объеме можио было бы иайтя по уравнению-
Где 5 — поверхность адсорбента
К сожалению, из-за сложности определения истиииой поверхности адсорбента эту величину часто очень трудно определить, поэтому Поляни и предложил выражать 0 ие как функцию /, а как функцию пропорциональной величины V.
Изменение адсорбционного потенциала 0 с изменением адсорбционного объема V, как это представлял Поляни, показано на рис. IV, 7. Подобные кривые, не зависящие от температуры и характерные для каждого данного адсорбента, Поляни называет характеристическими кривыми.
Теория полимолекулярной адсорбции принимает, что для адсорбционного объема применимо уравнение состояния газа. Поэтому изотермы, характеризующие зависимость плотности адсорбтива р от адсорбционного объема V для разных температур, напоминают йзотермы р, V.
В определенных условиях, например при достаточно низкой температуре, адсорбционные силы на поверхности могут вызвать конденсацию пара в жидкость плотностью рж. При температурах значительно более низких, чем критическая, в результате конденсации весь адсорбционный объем будет заполнен жидкостью, так что Vm = УМакс — В этом. случае кривая р = f(V) на участке, 1 соответствующем адсорбционному © объему, идет почти параллельно оси абсцисс в связи с малой сжимаемостью жидкости. Далее на границе адсорбционный объем — газовая фаза кривая резко опускается вниз И плот — Рис. IV, 7. Типичный вид ха — ность адсорбтива достигает значения рактеристической кривой, плотности газовой фазы ро.
При температурах значительно более высоких, чем критическая, адсорбтив будет вести себя как идеальный газ и график зависимости Р ОТ 7 выразится Кривой, СХОДНОЙ с изотермой ДЛ5Ґ идеального газа PV = RT. В этом случае адсорбированный газ будет обладать максимальной плотностью у поверхности адсорбента, минимальной — в непосредственной близости от газовой фазы. Плотность адсорбтива в адсорбционном объеме здесь нигде не достигает плотности жидкости.
Наконец, когда температура близка к критической, зависимость р от V выразится, очевидно, кривой, близкой по своему виду К изотерме, описываемой уравнением Ван-дер-Ваальса. В этом случае часть адсорбированного вещества будет находиться в адсорбционном’объеме в жидком состоянии, а часть—в газообразном. Понятно, наиболее резко кривая снижается в участке, отвечающем переходу от жидкости к газу.
Исходя из приведенных выше представлений, Поляни указал путь для построения характеристической кривой. Потенциал 0і, отвечающий точке і, находящейся на поверхности раздела жидкость — га» в адсорбционном объеме, мож» но представить как работу сжатия 1 моля газа при температуре Т;
Где р, — давление насыщенного пара над поверхностью жидкости, р0 — давление газа в газовой фазе
Так как V = RT/P, значение 0І можно вычислить по уравнению:
Значение pt для большинства веществ известно; значение р0 определяется из опыта. Для нанесения соответствующей точки на диаграмму, выражающую зависимость адсорбционного потенциала от адсорбционного объема, неооходимо знать, какому значению V, соответствует найденное значение 0,. Для этого пользуются вышеприведенным уравнением (IV, 14).
Определив V, и 0, для ряда значений р0 при температуре значительно более низкой, чем критическая, когда адсорбтив находится в адсорбционном объеме в основном в виде жидкости, можно построить график 0 = F(V). Наличие в правой части уравнения (IV, 17) множителя Т не указывает на то, что зависимость 0, от Vг должна меняться с температурой; а лишь показывает, что при другой температуре, но при том же значении р0 адсорбционный потенциал, соответствующий границе жидкость — газ, будет иным
М М. Дубинин показал, что потенциальная теория адсорбции дает возможность вычислить изотермы адсорбции различных паров на одном и том же адсорбенте по характеристической кривой, полученной из изотерм адсорбции одного пара, так как соотношение адсорбционных потенциалов различных паров практически не зависит от адсорбционного объема. Из этого следует, что координаты точек характеристических кривых для разных адсорбтивов в случае одного и того же адсорбента при всех значениях адсорбционного объема находятся в постоянном отношении р, т. е. эти кривые являются афинными. Отношение р называется коэффициентом афинности характеристических кривых. Отсюда следует, что построив характеристическую кривую по экспериментальной изотерме адсорбции одного адсорбтива и зная соответствующий коэффициент афинности для какого-нибудь другого адсорбтива, можно найти изотерму адсорбции для этого второго адсорбтива.
Мы рассмотрели кратко две теории адсорбции — теорию мономолекулярной адсорбции Ленгмюра и теорию полимолекулярной адсорбции Поляни, на первый взгляд исключающие друг друга. Возникает вопрос, какая из этих теорий более правильна? На это следует ответить, что обе теории ограничены в применении. В зависимости от природы адсорбента и адсорбтива и в особенности от условий адсорбции в одних случаях приложима одна, а в других— другая теория адсорбции. Теория Поляни применима только к явлениям чисто физической адсорбции. Теория Ленгмюра охватывает с известными ограничениями явления как физической, так и химической адсорбции. Однако теория Ленгмюра не может быть применена для объяснения адсорбции на тонкопористых адсорбен* тах, имеющих сужающиеся поры. В местах сужения, вследствие аддитивности дисперсионных сил, адсорбционный потенциал более высок и в таких местах происходит более интенсивная адсорбция. Это особенно заметно при температурах ниже критической температуры адсорбтива, т. е. при адсорбции паров, которые в этом случае заполняют наиболее узкие места капилляров в виде жидкости. Применение уравнения Ленгмюра к адсорбции тонкопористыми адсорбентами, имеющими поры с сужениями, затруднительно. Конечно, формально, уравнением Ленгмюра можно описать
адсорбцию такими адсорбентами. Однако константа йМакС в этом случае теряет смысл емкости плотного монослоя, и использование Этой константы для определения удельной поверхности таких адсорбентов уже не дает правильных результатов.
Делались попытки обобщить представления Ленгмюра и Поляни и описать изотермы различной формы с помощью одного уравнения. В частности, такая обобщенная теория была развита Брунауэром, Эмметом и Теллером в 1935—1940 гг. применительно к адсорбции паров. Их теория получила название теории БЭТ по первым буквам имен авторов. Основные положения теории БЭТ следующие.
1. На поверхности адсорбента имеется определенное число равноценных в энергетическом отношении активных центров, способных удерживать молекулы адсорбтива.
Рис. IV, 8. Схема полимолекуляриой адсорбции, принятая по теории БЭТ.
2. Для упрощения взаимодействием соседних адсорбированных молекул в первом и последующих слоях пренебрегают.
Оба эти допущения соответствуют ленгмюровской адсорбции на однородной поверхности без взаимодействия адсорбированных молекул.
3. Каждая молекула первого слоя представляет собой возможный центр для адсорбции и образования второго адсорбционного слоя; каждая молекула второго слоя является возможным центром адсорбции в третьем и т. д.
4. Предполагается, что все молекулы во втором и более далеких слоях имеют такую же сумму статистических состояний, как в жидком состоянии (в общем отличающуюся от суммы состояний первого слоя).
Таким образом, адсорбированная фаза может быть представлена как совокупность адсорбционных комплексов — молекулярных цепочек, начинающихся молекулами первого слоя, непосредственно связанных с поверхностью адсорбента. При этом цепочки энергетически не взаимодействуют друг с другом. Схема строения адсорбционного слоя по теории БЭТ показана на рис. IV, 8.
Все эти предпосылки достаточно условны. В частности, согласно теории БЭТ принимается, что каждая молекула жидкости имеет только двух ближних соседей (т. е. сверху и снизу в цепочке), в то время как у молекулы реальной жидкости гораздо больше ближайших соседей. Тем не менее эта теория оказалась в некоторых отношениях весьма плодотворной.
Теория Поляни не позволяет вывести уравнения изотермы адсорбции. Теория БЭТ, как и теория Ленгмюра, дает аналитическое уравнение для изотермы, которая в этом случае имеет S-образную форму (см. рис. IV, 5). Не приводя достаточно сложного вывода уравнения изотермы адсорбции Брунауэра, Эммета и Теллера, остановимся лишь на некоторых положениях, лежащих в основе этого вывода, и приведем само уравнение изотермы.
Брунауэр, Эммет и Теллер при выводе уравнения рассматривают адсорбцию молекул пара как серию квазихимических реакций образования единичных и кратных адсорбционных комплексов:
Пар + свободная поверхность единичные комплексы пар + единичные комплексы двойные комплексы пар + двойные комплексы тройные комплексы и т. д.
При этом теплота адсорбции первого слоя молекул Qi, т. е. теплота образования единичных комплексов, гораздо больше, чем для всех последующих слоев. Теплоты адсорбции всех последующих слоев приблизительно одинаковы и равны теплоте объемной конденсации L.
Для константы равновесия полимолекулярной адсорбции С можно написать следующее уравнение:
C = g’exp(-Јi—-) (IV, 18)
На основе этих представлений Брунауэр, Эммет и Теллер вывели следующие уравнения изотермы адсорбции паров:
Где Ps — давление насыщенного пара при данной температуре, P/Ps — относительное давление пара, ос, аМакс, а, амако, р — имеют те же значения, что и в уравнении Ленгмюра
При значениях р, далеких от и С > 1, адсорбция приводит к образованию мономолекулярного слоя и уравнения (IV, 19) и (IV, 20) переходят в уравнения адсорбции Ленгмюра (IV, 10) и (IV, 11). По мере приближения р к Ps число свободных активных Центров сокращается и кратность комплексов растет. При р = р„ происходит объемная конденсация пара.
Уравнение изотермы полимолекулярной адсорбции БЭТ легко привести к линейной форме
По наклону этой линии и отсекаемому ею отрезку на оси ординат можно найти значения констант амакс и С.
Теория БЭТ, так же как и теория Ленгмюра, указывает путь для определения удельной поверхности адсорбента. Найдя амАкс для паров простых веществ (N2, Аг, Кг) при низких температурах и зная площадь So, занимаемую молекулой адсорбтива, легко вычислить удельную поверхность адсорбента syA:
Где NA — число Авогадро.
Легко решить и обратную задачу. Для этого определяют с помощью адсорбции при низких температурах стандартного пара поверхность s-уд данного адсорбента, после чего, найдя экспериментально изотерму адсорбции пара исследуемого адсорбтива и значение емкости монослоя амакс, вычисляют значение S0:
Опыты по определению удельной поверхности одного и того же адсорбента при адсорбции различных паров дали близкие результаты, в общем совпадающие с результатами определения удельной поверхности другими, не адсорбционными методами. Это подтверждает правильность толкования формы изотермы с помощью теории БЭТ. Несмотря на ряд недостатков, теория БЭТ является в настоящее время лучшей и наиболее полезной теорией физической адсорбции.
http://www.sites.google.com/site/kolloidnaahimia/adsorbcia-svistat-vseh-na-poverhnost/teoria-polimolekularnoj-adsorbcii-teoria-bet
http://kraska.biz/kurs-kolloidnoj-ximii/teoriya-polimolekulyarnoi-adsorbcii-polyani-i-teoriya-bet/