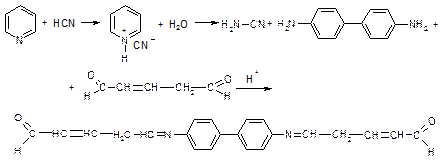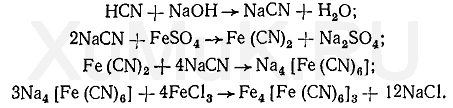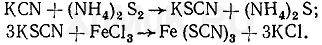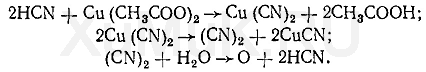Реакции обнаружении синильной кислоты
Первые порции дистиллята собирают в раствор щелочи для связывания летучей кислоты синильной и образования натрия цианида.
HCN + NaOH → NaCN + Н2О
1. Реакция с пиридинбензидиновым реактивом
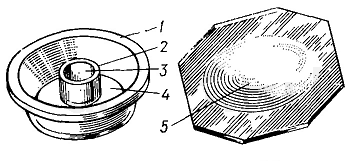
Рис.2. Прибор для микродиффузии: 1 – толстостенный сосуд; 2 – внутренний сосуд; 3 – внутренняя круглая камера; 4 – наружная камера; 5 — крышка
В наружную камеру (4) прибора для микродиффузии вносят 2-4 мл крови или мочи, 1 г гомогената ткани. Затем в ту же камеру вносят 3-4 капли 10% раствора кислоты серной. Во внутреннюю камеру (3) прибора вносят 3,3 мл 0,1 М раствора натра едкого. Прибор плотно закрывают крышкой (5) и оставляют на 3-4 ч при комнатной температуре. Затем из внутренней камеры прибора берут 1 мл жидкости, к которой прибавляют 1 мл 0,1 М раствора натра едкого, 2 мл 1 М раствора натрия фосфата двузамещенного и 1 мл 0,25% раствора хлорамина Т. Жидкость взбалтывают и через 2-3 мин прибавляют 3 мл реактива, содержащего кислоту барбитуровую и пиридина. Смесь перемешивают и оставляют на 10 мин. Появление красной окраски указывает на наличие цианидов в исследуемой жидкости.
2. Образование берлинской лазури
К 1 мл дистиллята прибавляют 1-4 капли разбавленного раствора железа сульфата (II) и такой же объем разбавленного раствора железа хлорида (III). Смесь хорошо перемешивают и нагревают на пламени газовой горелки почти до кипения, а затем охлаждают до комнатной температуры и прибавляют 10% раствор кислоты хлористоводородной до слабокислой реакции на лакмус. Появление синего осадка или синего окрашивания указывает на наличие кислоты синильной (цианидов) в дистилляте. При малых количествах кислоты синильной в растворах синяя окраска появляется только через 24-48 ч. При длительном отсутствии синего осадка к смеси прибавляют 5% раствор бария хлорида. При этом выпадает осадок бария сульфата и происходит соосаждение берлинской лазури.
Количественное определение: для количественного определения изолирование кислоты синильной проводят из отдельной навески биологического материала, как описано выше.
Объемный метод определения применяют при исследовании свежего биологического материала, а также для других объектов. Дистиллят собирают в
несколько приемников, содержащих определенное количество 0,1 М (0,01 М при малых количествах кислоты синильной) титрованного раствора серебра нитрата. Избыток серебра нитрата оттитровывают 0,1 М (или 0,01М) раствором аммония тиоцианата в присутствии индикатора железоаммонийные квасцы.
Весовой метод кислоты синильной применяют количественного определения в случае исследования несвежего биологического материала. Сероводород, образующийся в объекте исследования в результате процессов гниения, будет реагировать с серебра нитратом, образовывать серебра сульфид, искажая результаты. Дистиллят собирают в несколько приемников, содержащих определенное количество 0,2% раствора серебра нитрата. Дистиллят подкисляют кислотой азотной до кислой реакции среды. Выделившейся осадок серебра цианида с возможной примесью серебра сульфида отфильтровывают и прямо на фильтре обрабатывают 5-6 мл 25% раствора аммония гидроксида для растворения серебра цианида. Фильтрат подкисляют избыточным количеством 6 М раствора кислоты азотной, и выделившийся осадок серебра цианида вновь отфильтровывают, промывают водой очищенной и сушат вместе с фильтром. Фильтр затем сжигают и осадок прокаливают во взвешенном фарфоровом тигле до постоянного веса. Остаток металлического серебра взвешивают и пересчитывают на кислоту синильную.
Дата добавления: 2015-11-12 ; просмотров: 1702 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
§ 6. СИНИЛЬНАЯ КИСЛОТА
Синильная кислота (цианистоводородная кислота) — газ или бесцветная жидкость (г. кип. 25,6 °С, т. пл.— 13,3 °С, плотность 0,699), имеет запах горького миндаля, легко смешивается с водой и с рядом органических растворителей. При — 13,3 °С синильная кислота затвердевает, образуя волокнистую кристаллическую массу. Синильная кислота является слабой кислотой. Ее вытесняют из солей даже углекислота и слабые органические кислоты.
В свободном состоянии в природе синильная кислота не встречается. Она встречается в виде химических соединений, к числу которых относятся гликозиды (амигдалин, пруназин, дур-рин и др.). Амигдалин содержится в семенах горького миндаля, косточках персиков, абрикосов, слив, вишен, в листьях лавровишни и др. Этот гликозид под влиянием фермента эмульсина, а также под влиянием кислот разлагается на глюкозу, бензальдегид и синильную кислоту. Пруназин содержится в пенсильванской вишне, а дуррин — в просе. Синильная кислота может образовываться при горении целлулоида. Следы этой кислоты содержатся в табачном дыме.
Соли синильной кислоты (цианиды) легко гидролизуются d воде. При хранении водных растворов цианидов при доступе диоксида углерода они разлагаются:
KCN + H 2 O + СО 2 —> HCN + КНСО 3 KCN + 2H 2 O —> NH 3 + НСООК
В водных растворах разлагаются не только цианиды, но и сама синильная кислота:
Применение. Действие на организм. Синильная кислота и ее соли применяются для синтеза ряда органических соединений, при добыче золота, для дезинфекции и дезинсекции, для борьбы с вредителями растений и т. д. Из соединений синильной кислоты, применяемых в народном хозяйстве, большое значение имеют цианиды натрия и калия.
Синильная кислота и ее соли очень ядовиты. По токсичности синильная кислота превосходит многие известные яды. Поэтому с синильной кислотой и ее солями следует обращаться очень осторожно. Следует помнить, что от прибавления сильных кислот к цианидам сразу же выделяется синильная кислота, которая может быть причиной тяжелых, а иногда и смертельных отравлений. Отравления могут давать и различные соединения синильной кислоты (хлорциан, бромциан и др.). Отмечены случаи отравления людей семенами миндаля. По данным М. Д. Швайковой (1975), смерть у взрослых может наступить при поедании 40—60 штук, а у детей— 10—12 штук семян миндаля. При вдыхании больших концентраций синильной кислоты смерть может наступить мгновенно от остановки дыхания и сердца. Учитывая высокую токсичность синильной кислоты и ее солей, работать с ними в лаборатории можно только в вытяжном шкафу с хорошей вентиляцией.
Синильная кислота угнетает внутриклеточные железосодержащие дыхательные ферменты. При угнетении цитохромоксидазы синильной кислотой клетки организма не усваивают кислород, поступающий с кровью. В результате этого наступает клеточное кислородное голодание, несмотря на то, что кровь насыщенна кислородом. Цианиды также могут блокировать гемоглобин крови, нарушая его функции.
Синильная кислота может поступать в организм с вдыхаемым воздухом и частично через неповрежденную кожу, а цианиды — через пищевой канал.
Метаболизм. Метаболитом синильной кислоты является тиоцианат (роданид), который образуется в организме при конъюгации цианидов с серой под влиянием фермента роданазы.
Изолирование синильной кислоты и цианидов из биологического материала производят перегонкой с водяным паром. Для этой цели собирают 3—5 мл первого дистиллята в пробирку,
содержащую 2 мл 2 %-го раствора гидроксида натрия. Поскольку синильная кислота быстро разлагается в организме, исследование биологического материала на наличие этой кислоты и ее солей желательно проводить сразу же после вскрытия трупов.
При отравлении синильной кислотой и цианидами на химико-токсикологическое исследование берут желудок с содержимым, печень и почки. Ввиду быстрого разложения синильной кислоты и цианидов в тканях организма эти яды можно обнаружить в содержимом желудка и не обнаружить в паренхиматозных органах.
При заключении об отравлении синильной кислотой и цианидами (на основании результатов химико-токсикологического анализа биологического материала) следует учитывать то, что цианиды в небольших количествах (около 6 мкг %) могут быть в моче лиц, неподвергавшихся воздействию этих соединений. В моче курящих количество цианидов может быть почти в 3 раза больше, чем в крови некурящих. В крови цианиды могут образовываться и посмертно.
Для обнаружения синильной кислоты в дистиллятах применяют несколько реакций, из которых наиболее доказательной является реакция образования берлинской лазури. Другие описанные ниже реакции используют как вспомогательные, а также для обнаружения цианидов в порошках, жидкостях и в других объектах.
Реакции на синильную кислоту и ее соли выполняют под тягой.
Реакция образования берлинской лазури. От прибавления сульфата железа (II) к щелочному раствору цианидов, образуется цианид железа (II), который при взаимодействии с избытком цианидов, а затем с сульфатом или хлоридом железа (III) образует берлинскую лазурь:
При образовании берлинской лазури происходят и побочные реакции между солями железа и щелочью (образуются гидро-ксиды железа).
Для растворения гидроксидов железа и нейтрализации избытка щелочи прибавляют кислоту до кислой реакции. Большой избыток прибавленной кислоты может замедлить процесс образования берлинской лазури.
Выполнение реакции. К нескольким миллилитрам дистиллята, собранного в раствор щелочи, прибавляют 1—4 капли разбавленного раствора сульфата железа (II) и такой же объем разбавленного раствора хлорида железа (III). Смесь хорошо взбалтывают и нагревают на пламени газовой горелки почти до кипе-
ния, а затем охлаждают до комнатной температуры и прибавляют 10 %-й раствор соляной кислоты до слабокислой реакции на лакмус. Появление синего осадка или синей окраски указывает на наличие синильной кислоты (цианидов) в дистилляте.
Предел обнаружения: 20 мкг синильной кислоты в 1 мл раствора. Предельная концентрация 1 : 100000. При количествах синильной кислоты, превышающих 30 мкг в 1 мл, образуется синий осадок. При наличии 20—30 мкг синильной кислоты в 1 мл появляется зеленая или голубоватая окраска. При малых количествах синильной кислоты в растворах синяя окраска появляется только через 24—48 ч. При длительном отсутствии синего осадка или синей окраски к смеси прибавляют 5 %-ый раствор хлорида бария. При этом выпадает осадок сульфата бария и происходит соосаждение берлинской лазури.
Осадок берлинской лазури может быть представлен судебно-следственным органам как доказательство наличия синильной кислоты или цианидов в исследуемых объектах.
Реакция образования роданида железа. Эта реакция основана на том, что при нагревании цианидов с раствором полисульфида аммония образуется роданид, от прибавления к которому раствора хлорида железа (Ш) появляется кроваво-красная окраска:
Выполнение реакции. К 2—3 мл исследуемого раствора прибавляют 3—5 капель 10—20 %-го раствора полисульфида аммония и смесь упаривают на водяной бане до небольшого объема. К упаренной жидкости по каплям прибавляют 8 %-й раствор соляной кислоты до кислой реакции (по лакмусу), а затем прибавляют 1 каплю 10 %-го раствора хлорида железа (III). Появление кроваво-красной окраски указывает на наличие цианидов в растворе. При взбалтывании окрашенного раствора с диэтило-вым эфиром окраска переходит в эфирный слой.
Предел обнаружения: 10 мкг синильной кислоты в 1 мл.
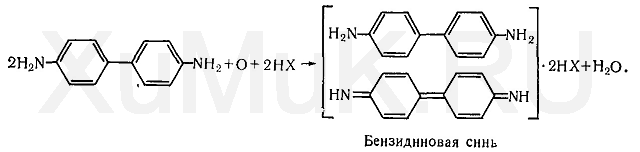
Реакция образования бензидиновой сини. Соли меди (II) с цианидами образуют дициан (CN) 2, при взаимодействии которого с водой выделяется кислород, окисляющий бензидин. Продуктом окисления бензидина является бензидиновая синь:
В колбу вносят 2—3 мл исследуемого раствора, к которому прибавляют 1 мл 10 %-го раствора винной кислоты. Колбу сразу же закрывают пробкой, к которой прикреплена влажная индикаторная бумага. Затем колбу нагревают несколько минут на водяной бане. При наличии синильной кислоты или ее солей в пробе бумага синеет.
Приготовление индикаторной бумаги (см. Приложение 1, реактив 6).
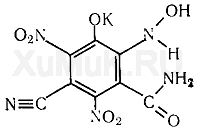
Реакция с пикриновой кислотой. От прибавления пикриновой кислоты и щелочи к цианидам образуется соль изопурпуровой кислоты, имеющая красную окраску:
Выполнение реакции. К 1 мл щелочного дистиллята прибавляют 1 мл 0,5 %-го раствора пикриновой кислоты и слегка нагревают на водяной бане. При наличии цианидов раствор приобретает красную окраску. Подобную окраску с пикриновой кислотой дают и некоторые другие вещества (альдегиды, ацетон, сульфиты и др.). Поэтому реакция с пикриновой кислотой на цианиды имеет значение только при отсутствии цианидов в дистилляте.
Уравнение качественных реакций на синильную кислоту
Определение синильной кислоты
Качественное определение. Проба с бензидиновой и пикратной бумажками. Исследуемый материал (содержимое желудка или кормовое вещество), предварительно хорошо растертый в ступке, в количестве 10—15 г помещают в коническую колбочку и слегка подкисляют 1%-ным раствором соляной кислоты. Колбочку плотно закрывают пробкой, к которой прикрепляют две индикаторные бумажки на синильную кислоту — бензидиновую и пикратную. Полоски бумажек прикрепляют так, чтобы они не касались испытуемого вещества. Колбочку помещают в термостат при температуре 30—35 °.С. При наличии синильной кислоты бензидиновая бумажка синеет, а пикратная приобретает красновато-оранжевую окраску. Если бумажки не изменяют своего цвета в течение 48 ч, можно считать, что синильной кислоты в исследуемом материале не содержится.
Проба с пикратной бумажкой может отчасти служить для грубого количественного определения синильной кислоты. В последнем случае она ставится несколько иным образом. Измельченный материал помещают в колбочку и, не подкисляя его, смачивают водой до консистенции полужидкой кашицы. Колбочку закрывают пробкой с прикрепленной к ней полоской пикратной бумажки и ставят в термостат при температуре 35—38 °С на 4 ч. Установлено, что слабо-розовая окраска пикратной бумажки соответствует примерно тысячным или еще меньшим долям процента синильной кислоты в исследуемом веществе; розовая до средней степени красной — сотым долям процента; интенсивно-красная до темно-красно-бурого цвета — десятым долям процента.
Приготовление бензидиновой бумажки: полоски фильтровальной бумаги пропитывают 3%-ным раствором ацетата меди и высушивают их; перед употреблением их смачивают 20%-ным раствором уксуснокислого бензидина .
Пикратная бумажка готовится таким образом: фильтровальную бумагу пропитывают 1%-ным раствором пикриновой кислоты, высушивают, затем смачивают 10%-ным раствором углекислого натрия; снова высушивают и нарезают узкими полосками. Бумажка имеет лимонно-желтую окраску.
Для грубого количественного определения синильной кислоты в исследуемом материале можно применить еще пробу с гваяковой бумажкой. Небольшое количество (10—15 г) исследуемого материала помещают в коническую колбочку, смачивают его дистиллированной водой и подкисляют 5—6 мл 5%-ного раствора виннокаменной кислоты. Колбу закрывают корковой пробкой с прикрепленной к ней полоской бумаги, пропитанной раствором гваяковой смолы. Такие бумажки готовят заранее, пропитывая их раствором следующего состава: 0,1 г гваяковой смолы растворяют в 50 мл 95-градусного этилового спирта, смешивают этот раствор с 15 мл водного раствора сернокислой меди (1 : 1000) и этим смешанным раствором пропитывают фильтровальную бумажку.
При наличии синильной кислоты во взятой навеске исследуемого материала в количестве 0,05 мг гваяковая бумажка тотчас же интенсивно посинеет, при содержании же синильной кислоты в количестве 0,001 мг посинение наступает через 1—2 мин. Если в течение некоторого времени бумажка не изменяет окраски, можно считать, что синильная кислота и ее соли в исследуемом корме отсутствуют.
Появление синего или сине-зеленого окрашивания может быть обусловлено наличием синильной кислоты, цианидами, окисляющими веществами и аммиаком. Поэтому настоящая реакция имеет безусловное значение только при отрицательном результате, который указывает на отсутствие синильной кислоты. В случае положительной качественной реакции при той или иной из вышеуказанных проб для уточнения вопроса о содержании синильной кислоты необходимо прибегнуть к дальнейшему исследованию корма более специфичными методами.
Реакция образования берлинской лазури
Перегонку следует вести медленно, регулируя ее нагреванием парообразователя. Сначала от одной пробы получают небольшое количество отгона, который подвергают испытанию на берлинскую лазурь. К дистилляту прибавляют раствор едкого натра до получения ясно выраженной щелочной реакции, затем по одной капле свежеприготовленных разбавленных растворов сернокислой закиси железа (FeS04) и хлорного железа (FeCl3), тщательно взбалтывают и подкисляют разбавленной соляной кислотой (1 : 3) до слабокислой реакции на лакмус. В зависимости от количества синильной кислоты появляется синий осадок или окрашивание — синее, сине-зеленое, зеленое. При очень малых количествах синильной кислоты осадок или окрашивание может появиться спустя 24—48 ч. Реакция эта специфична. Чувствительность реакций 1 : 5 000 000.
Для открытия очень малых количеств синильной кислоты в исследуемом веществе рекомендуется еще прибегнуть к постановке микро-реакции па синильную кислоту. Для воспроизведения таком реакции необходимо предметное стекло с лункой и подобранное к нему шлифованное покровное стекло. В углубление предметного стекла помещают каплю перегона, а на нижнюю поверхность покровного стекла — каплю 10%-ного раствора азотнокислого серебра, слегка подкрашенного метиленовым синим. При наличии в перегоне синильной кислоты капля жидкости на покровном стекле мутнеет от образопания и выпадения нерастворимого цианистого серебра. Под микроскопом можно увидеть мелкие кристаллики цианистого серебра в виде синих игл и палочек.
Проба с многосернистым аммонием [(NH4)2S2]. В фарфоровую чашечку помещают 5—10 мл полученного дистиллята, прибавляют несколько (5—7) капель 5%-ного раствора многосернистого аммония, 3—5 капель 10%-ного раствора едкого натра и осторожно выпаривают на водяной бане досуха. Полученный остаток после охлаждения подкисляют 10%-ным раствором азотной кислоты и затем добавляют 1 каплю 20%-ного раствора хлорида окисного железа (FeCl3). При наличии синильной кислоты раствор приобретает кроваво-красную окраску от образующегося роданида железа [Fe(CNS)3l.
Проба по Колыпгофу. В колбочку помещают около 10 мл исследуемого дистиллята, прибавляют 20 мг сульфата закиси железа и 10 капель раствора карбоната и гидрокарбоната натрия (8 г NaCOa-10Н3О и 8 г NaHCO-, па 100 мл дистиллированной воды), хорошо взбалтывают и оставляют в закрытом виде на полчаса, затем подкисляют серной кислотой. При наличии в дистилляте синильной кислоты (до 5 мг на 1 л) тотчас же после подкисления появляется синее окрашивание.
Количественное определение. Тонко размолотый материал (100 г) помещают в 2-литровую колбу, заливают 500 мл воды, подкисляют1 виннокаменной кислотой (50 мл 10%-ного водного раствора), размешивают и дают постоять сутки. На следующий день производят отгонку синильной кислоты. Для этого колбу закрывают пробкой с двумя пропущенными через нее изогнутыми трубками, причем одну трубку, доходящую почти до дна колбы, присоединяют к парообразователю, а другую, отводную, трубку — к холодильнику. Затем при одновременном нагревании колбы на кипящей водяной бане отгоняют синильную кислоту с водяным паром. Конец форштосса холодильника опускают в небольшое количество (15—20 мл) влитой в приемник воды с добавленными к ней 15 мл 0,5 и. раствора КОН. Перегонку следует вести медленно. Собирают 300—500 мл дистиллята, в которых дальше и определяют содержание синильной кислоты.
Аргентометрический метод (метод Либиха). Полученный дистиллят титруют 0,1 и. раствором азотнокислого серебра в присутствии нескольких капель йодистого калия (10%) до появления неисчезающей мути. При прибавлении по каплям раствора азотнокислого серебра к щелочному раствору HCN образуется на месте1 падения капель белый осадок цианистого серебра, тотчас исчезающий при взбалтывании жидкости, так как AgCN растворяется в избытке цианистого калия с образованием серебряносинеродистого калия: AgCN + KCN Ag (CN)aK.
Как только весь циан превращается в серебряносинеродистый калий, следующая за этим капля AgN03 дает неисчезающую муть: Ag(CN) 2K h AgN03 -> I\N03 + 2AgCN. Таким образом, одной молекуле AgN03 соответствуют две частицы CN.
Вычисление процента содержания HCN производится по формуле:
В случае, если исходная навеска исследуемого материала не равна 100 г, то полученное по формуле количество HCN нужно разделить на количество навески и умножить на 100.
Так как в исследуемых кормах HCN обычно присутствует в очень небольших количествах, титрование дистиллята лучше производить из микробюретки.
Меркурметрический метод. Этот метод по сравнению с арген-тометрическим считается более надежным, так как он позволяет более четко улавливать момент окончания титрования, вследствие чего более точно определяется содержание синильной кислоты в исследуемом материале. Этот метод основан на улавливании при перегонке синильной кислоты титрованным раствором азотнокислой ртути.
Навеску исследуемого материала грубо измельчают и помещают в плоскодонную колбу на 500 мл. В нее добавляют 3 мл серного эфира для улучшения в дальнейшем извлечения синильной кислоты, закрывают каучуковой пробкой и оставляют на 6 ч. Затем в колбу наливают 100 мл воды и оставляют в покое на 12—24 ч при температуре не выше 20 °С, взбалтывая в начале и перед отгонкой. За это время происходит гидролиз гликозидов в исследуемом материале.
Затем синильную кислоту отгоняют обычным путем (см. выше) с водяным паром, получаемым из парообразователя. Дистиллят, содержащий синильную кислоту, собирают в приемную колбу, в которую перед началом отгонки наливают 20 мл 0,01 н. раствора нитрата ртути (в зависимости от ожидаемого количества синильной кислоты количество раствора нитрата ртути должно быть увеличено или уменьшено) и 10 мл 8 н. раствора азотной кислоты (на каждые 100 мл отгона). Когда будет перегнано 150 мл жидкости, отгонку заканчивают, обмывают конец форштосса несколькими мл дистиллированной воды, охлаждают отгон (если это необходимо) и проводят титрование.
К отгону в приемнике прибавляют 2 мл индикатора (насыщенный раствор железо-аммиачных квасцов) и титруют непосредственно в нем 0,01 н. раствором роданистого аммония, помешивая до появления неисчезающего розового окрашивания. Перед титрованием устанавливают соотношение между используемым раствором роданида ртути и роданида аммония.
При расчете содержания синильной кислоты в исследуемом корме (материале) исходят из того, что 1 мл 0,01 н. раствора роданида ртути соответствует 0,00027 г (0,27 мг) синильной кислоты.
Содержание синильной кислоты (мг%) вычисляют по формуле:
Определение синильной кислоты в сорго. Очень простой способ определения синильной кислоты в сорго основан на существующей тесной зависимости между накоплением крахмала в стеблях растений и содержанием HCN в растениях. Растения, богатые синильной кислотой, обычно богаты и крахмалом в стеблях, в то время как нормально развивающиеся растения свободны от крахмала или содержат его очень мало.
Определение синильной кислоты в сорго производится следующим образом. Из разных мест поля берут по нескольку пробных растений, которые срезают у самого основания. После этого острым ножом или лучше бритвой из нижней части стебля вырезают тонкие поперечные срезы, которые обрабатывают раствором иода и просматривают под микроскопом, лупой или просто невооруженным глазом (на белом фоне). В случае присутствия большого количества крахмала в стеблях на срезах последних получается сплошное синее или черное окрашивание (при просматривании невооруженным глазом — просто темное). Такие растения обычно содержат не менее 0,1% HCN (на сухой вес) и являются опасными для скармливания животным. Если крахмальных зерен в стеблях мало, то синее или черное окрашивание появляется не сплошь на всем срезе, а лишь вокруг сосудисто-волокнистых пучков. В этом случае сорго содержит менее 0,1% HCN (на сухой вес) и неопасно для скармливания животным в утренние и вечерние часы. Если же срезы стеблей от иода совершенно не будут окрашиваться в синий цвет, то сорго не содержит HCN, и его можно скармливать скоту в любое время без всяких опасений.
http://xumuk.ru/toxicchem/43.html
http://zoovet.info/vet-knigi/111-kormlenie-zhivotnykh/kormovye-otravleniya/10798-opredelenie-sinilnoj-kisloty