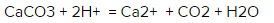Карбонат кальция: способы получения и химические свойства
Карбонат кальция CaCO3 — соль кальция и угольной кислоты. Белый, при прокаливании разлагается, плавится без разложения под избыточным давлением CO2. Практически не растворяется в воде.
Относительная молекулярная масса Mr = 100,09; относительная плотность для тв. и ж. состояния d= 2,93; tпл = 1242º C при избыточном давлении.
Способ получения
1. Карбонат кальция можно получить путем взаимодействия хлорида кальция и карбоната кальция , образуется карбонат кальция и хлорид натрия:
2. В результате взаимодействия при комнатной температуре оксида кальция и углекислого газа происходит образование карбоната кальция:
3. Гидроксид кальция вступает в взаимодействие с углекислым газом и образует карбонат кальция и воду:
Качественная реакция
Качественная реакция на карбонат кальция — взаимодействие его с раствором сильных кислот. В результате реакции происходит бурное выделение углекислого газа, образование которого можно проверить, если пропустить его через известковую воду, которая мутнеет из-за образования осадка:
1. При взаимодействии с хлороводородной кислотой, карбонат кальция образует хлорид кальция, углекислый газ и воду:
Химические свойства
1. Карбонат кальция разлагается при температуре выше 900 — 1200º С, с образованием оксида кальция и углекислого газа:
2. Карбонат кальция вступает в реакцию со многими сложными веществами :
2.1. Карбонат кальция реагирует с оксидами :
2.1.1. Карбонат лития вступает в взаимодействие с оксидом кремния при 800º С и образует на выходе силикат кальция и углекислый газ:
2.2. Карбонат кальция реагирует с кислотами :
2.2.1. При взаимодействии с разбавленной хлороводородной кислотой карбонат кальция образует хлорид кальция, углекислый газ и воду:
2.2.2. Карбонат кальция реагирует с разбавленной плавиковой кислотой . Взаимодействие карбоната кальция с плавиковой кислотой приводит к образованию фторида кальция, воды и углекислого газа:
2.2.3. Карбонат кальция взаимодействует с сероводородной кислотой при 900º С и образует сульфид кальция, воду и углекислый газ:
3. Карбонат кальция реагирует с простыми веществами:
3.1. Карбонат кальция при 800 — 850º С вступает в реакцию с углеродом (коксом) образуя оксид кальция и угарный газ:
CaCO3 + C = CaO + 2CO
При взаимодействии соляной кислоты (водного раствора хлороводорода) с карбонатом кальция образуется хлорид кальция, вода и углекислый газ : 2HCl + CaCO3 → CaCl2 + H2O + CO2 Вычисли, какая массa хлорид?
Химия | 5 — 9 классы
При взаимодействии соляной кислоты (водного раствора хлороводорода) с карбонатом кальция образуется хлорид кальция, вода и углекислый газ : 2HCl + CaCO3 → CaCl2 + H2O + CO2 Вычисли, какая массa хлорида кальция образуется при взаимодействии карбоната кальция с 2, 92 г хлороводорода.
2HCl + CaCO3 = CaCl2 + H2O + CO2
Считаем количество вещества хлороводорода
По уравнению реакции хлорида кальция образуется столько же
Считаем массу хлорида кальция
Укажите вещества, взаимодействию которых соответствует сокращенное ионное уравнение : Ca( + 2) + CO( — 2)³→CaCO³↓ 1) оксид кальция и карбонат натрия 2)карбонат магния и хлорид кальция 3) гидроксид кал?
Укажите вещества, взаимодействию которых соответствует сокращенное ионное уравнение : Ca( + 2) + CO( — 2)³→CaCO³↓ 1) оксид кальция и карбонат натрия 2)карбонат магния и хлорид кальция 3) гидроксид кальция и соляная кислота 4)хлорид кальция и карбонат калия.
Какой объём углекислого газа при н?
Какой объём углекислого газа при н.
У образуется при взаимодействии 200г карбоната кальция с соляной кислотой.
Определите массу хлорида кальция который образуется при взаимодействии 4 г кальция с соляной кислотой?
Определите массу хлорида кальция который образуется при взаимодействии 4 г кальция с соляной кислотой.
Вычислить объем углекислого газа который образуется при действии двухсотпятидесяти грамм раствора соляной кислоты на карбонат кальция?
Вычислить объем углекислого газа который образуется при действии двухсотпятидесяти грамм раствора соляной кислоты на карбонат кальция.
Определите массу хлорида кальция который образуется при взаимодействии 4 г кальция с соляной кислотой?
Определите массу хлорида кальция который образуется при взаимодействии 4 г кальция с соляной кислотой.
Сколько граммов хлорида кальция образуется при взаимодействии 200 граммов карбоната кальция с соляной кислотой?
Сколько граммов хлорида кальция образуется при взаимодействии 200 граммов карбоната кальция с соляной кислотой.
Вычислите массу CO2, который образуется при взаимодействии 25 г CaCO3 (карбонат кальция) с HCl (соляной кислотой)?
Вычислите массу CO2, который образуется при взаимодействии 25 г CaCO3 (карбонат кальция) с HCl (соляной кислотой).
При взаимодействии соляной кислоты (водного раствора хлороводорода) с карбонатом натрия образуется хлорид натрия, вода и углекислый газ 2HCl + Na2CO3 → 2NaCl + H2O + CO2 Вычисли, какое количество веще?
При взаимодействии соляной кислоты (водного раствора хлороводорода) с карбонатом натрия образуется хлорид натрия, вода и углекислый газ 2HCl + Na2CO3 → 2NaCl + H2O + CO2 Вычисли, какое количество вещества хлороводорода прореагировало с карбонатом натрия, если выделилось 2, 8 л (н.
У. ) углекислого газа.
Вычислите массу CO2, который образуется при взаимодействии 25 г CaCO3 (карбонат кальция) с HCl (соляной кислотой)?
Вычислите массу CO2, который образуется при взаимодействии 25 г CaCO3 (карбонат кальция) с HCl (соляной кислотой).
Вычисли объем углекислого газа (н?
Вычисли объем углекислого газа (н.
У. ) который образуется при взаимодействии соляной кислоты с 30г известняка, содержащего 85% карбоната кальция.
Вычисли, какая массa хлорида кальция образуется при взаимодействии карбоната кальция с 2, 92 г хлороводорода?
Вычисли, какая массa хлорида кальция образуется при взаимодействии карбоната кальция с 2, 92 г хлороводорода.
(Ответ впиши с точностью 2 знака после запятой).
На этой странице находится ответ на вопрос При взаимодействии соляной кислоты (водного раствора хлороводорода) с карбонатом кальция образуется хлорид кальция, вода и углекислый газ : 2HCl + CaCO3 → CaCl2 + H2O + CO2 Вычисли, какая массa хлорид?, из категории Химия, соответствующий программе для 5 — 9 классов. Чтобы посмотреть другие ответы воспользуйтесь «умным поиском»: с помощью ключевых слов подберите похожие вопросы и ответы в категории Химия. Ответ, полностью соответствующий критериям вашего поиска, можно найти с помощью простого интерфейса: нажмите кнопку вверху страницы и сформулируйте вопрос иначе. Обратите внимание на варианты ответов других пользователей, которые можно не только просмотреть, но и прокомментировать.
Правила работы со спиртовкой довольно просты : 1)не дуть на спиртовку и не направлять её в сторону людей 2)тушить спиртовку нужно закрыванием колпочка, а не дуновением на неё.
Алкани мають загальну формулу СnH2n + 2 атомна маса С = 12, а Н = 1 (дані з таблиці Мєндєлєєва) 12×n + 1 (2n + 2) = 58 12n + 2n + 2 = 58 14n = 56 n = 4 C4H10 12×4 + 10 = 48 + 10 = 58.
Объём водяного пара 6. 72 л. Решение на фото.
Безводный натрит алюминия имеет массу 213, следовательно 2, 13 г — это 2, 13 / 213 = 0, 1 моль 400 г этого раствора содержит 2, 13 г AI(NO3)3, следовательно концетрация (2, 13 / 400)х100 = 0, 53% Теперь нужно в таблицах найти плотность этого раствора..
С + О2 = СО2 Хг С — 4 моль газа 12 г — 1 моль Х = 48 г. С.
Извиняюсь, что так грязно.
Реакция не пойдет, т. К здесь два K. Может тут ошибка.
Каждую друг с другом сложи, но выбирай те реакции, которые будут с осадков. Ну, я так поняла.
Какое ионное уравнение реакции CaCO3 + 2HCl?
Каким будет ионное уравнение реакции CaCO3 + 2HCl = CaCl2 + CO2 + H20?
Объясните как составить ионное уравнение этой реакции?
Как составить ионное уравнение реакции CaCO3 (карбоната кальция) и 2HCl (хлорной кислоты)?
Тип реакции: кислотно-основный.
В результате реакции карбонат кальция и 2 молекул хлорной кислоты, HCl нейтрализуется с образованием слабой неустойчивой кислоты H2CO3, которая не может оставаться в таком виде, потому распадается на углекислый газ CO2 и воду H2O.
Чтобы составить ионную реакцию, нужно сделать следующее:
- Проанализировать компоненты молекулярной реакции.
- Разложить на ионы газы, жидкости и растворы, а твердые вещества не трогать.
- Убрать с обоих сторон одинаковые ионы, записать конечный вид ионной реакции CaCO3 и 2HCl.
Итак, вот молекулярное уравнение:
Теперь нужно разобрать каждую составляющую этого уравнения, чтобы составить правильное ионное уравнение:
- CaCO3 не растворяется (ведь это обычный мел);
- HCl — кислота, растворяющаяся в воде;
- CaCl2 — хлорид кальция, растворяющийся в воде.
- H20 — это вода, в ионной реакции она не участвует;
- CO2 — газ, в данной ионной реакции он не участвует.
Теперь можно разложить составляющие на ионы (раскладывается только 2HCL и CaCl2):
CaCO3 (твердый элемент) + 2Cl- + 2H+ = Ca2+ + 2Cl- + CO2 + H2O
Что мы имеем? В обеих частях уравнения есть ионы хлора, потому их можно сократить. И вот что мы получаем в итоге:
Если вы любознательны и хотите знать больше, читайте также вопросы:
http://himia.my-dict.ru/q/8608175_pri-vzaimodejstvii-solanoj-kisloty-vodnogo-rastvora/
http://vovet.ru/q/kakoe-ionnoe-uravnenie-reakczii-caco3-2hcl-dt2.html