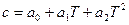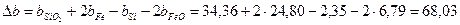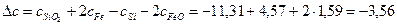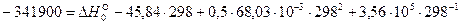От температуры. Закон Кирхгофа
Отношение бесконечно малого количества теплоты, сообщаемой телу, к тому изменению температуры, которое этим вызывается, называется истинной теплоемкостью:

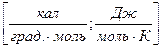
Для изохорных процессов
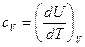
Для изобарных процессов
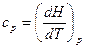
Эти равенства справедливы для любых веществ и для любого агрегатного состояния.
Для изохорного процесса тепловой эффект определяется величиной изменения внутренней энергии системы DU=U2-U1. Дифференцируя это равенство по температуре, получаем
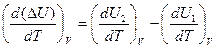
Так как 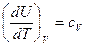
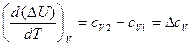
где сV1 и сV2 – изохорные теплоемкости системы в начальном и конечном состояниях, ΔсV – изменение изохорной теплоемкости при переходе из состояния 1 в состояние 2.
Аналогично для изобарного процесса:
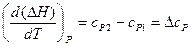
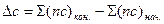
Уравнения (15) и (16) выражают закон Кирхгофа:
температурный коэффициент теплового процесса равен изменению теплоемкости системы, происходящему в результате процесса.
Тепловой эффект реакции при любой температуре и давлении, не сильно превышающем одну атмосферу, может быть рассчитан по уравнению Кирхгофа:
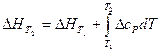
где ΔсР – разность между суммой изобарных теплоемкостей веществ, стоящих в правой части уравнения реакции, взятых с учетом стехиометрических коэффициентов, и такой же суммой теплоемкостей веществ, стоящих в левой части уравнения; 
Расчет может быть выполнен, если известны величина теплового эффекта реакции при какой-либо температуре Т1 (например, стандартной) и температурная зависимость теплоемкостей веществ, участвующих в реакции, в интервале Т1—Т2.
Таким образом, чем больше разность между теплоемкостями продуктов реакции и исходных веществ, тем сильнее зависимость теплового эффекта реакции от температуры.
Если теплоемкость с ростом температуры остается неизменной DсP=0 и 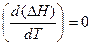
Зависимость теплоемкости от температуры обычно выражается эмпирическими приближенными уравнениями вида:
или 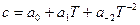
Если зависимость с(Т) известна в такой форме для всех веществ, участвующих в реакции, то по уравнению (17) определяют Δс=f(Т). Полученное выражение ( 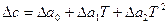
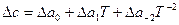
Пример. Составим уравнение температурной зависимости теплового эффекта реакции восстановления железа кремнием:
2FeO + Si = SiO2 + 2Fe.
Исходные данные для расчета приведены в таблице.
| Реагенты реакции |  , , 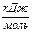 | 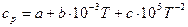 | ||
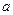 | 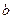 | 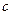 | ||
| FeO | 269,42 | 51,87 | 6,79 | -1,59 |
| Si | — | 24,13 | 2,35 | -4,57 |
| SiO2 | 880,74 | 47,01 | 34,36 | -11,31 |
| Fe | — | 17,51 | 24.80 | — |
Определим температурную зависимость приращения теплоемкости процесса по уравнению:
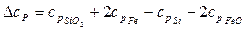
Можно вместо теплоемкостей веществ реакции подставить соответствующие выражения их температурной зависимости и привести выражение к стандартному виду или рассчитать коэффициенты уравнения и подставить их в уравнение
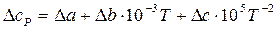
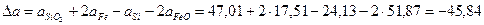
Получаем уравнение температурной зависимости приращения теплоемкости процесса:
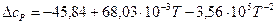
Подставив полученное выражение в уравнение Кирхгофа и проинтегрировав его в интервале температур от 0К до Т, получим уравнение зависимости теплового эффекта реакции от температуры:
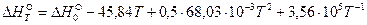
Для того чтобы найти тепловой эффект 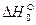
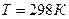
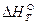
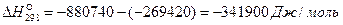
Выполнив вычисления, получаем 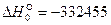
Уравнение температурной зависимости теплового эффекта реакции имеет вид: 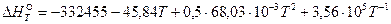
По данному уравнению можно рассчитать тепловые эффекты реакции для требуемых температур.
Тепловой эффект. Уравнение Кирхгофа
Тепловой эффект E процесса – это сумма количества теплоты, которую отдала система Q ‘ в этом процессе, и теплового эквивалента работы A
, элемент которой равняется:
= δ A — p d V ( 1 ) , где δ A считается элементарной полной работой системы, p d V – работой расширения.
Тогда получим, что:
Разрешается записать в виде E = — Q с Q , обозначающей количество теплоты, подведенное к системе. Согласно первому началу термодинамики:
E = — ∆ U — ∫ 1 2 p d V ( 3 ) , где ∆ U = U 2 — U 1 является изменением внутренней энергии системы, p – давлением, V – объемом.
Тепловой эффект применяется в термохимии. Тепловым эффектом химической реакции считается количество тепла, выделяемое в ходе данной реакции. При выделении теплоты реакция получила название экзотермической, при поглощении – эндотермической. Считается, что уравнение экзотермической реакции характеризуется E > 0 , а эндотермической –
Допустим, имеется химическая реакция, протекающая при V = c o n s t . Это говорит о тепловом эффекте реакции E V , который необходимо рассчитывать по формуле:
E V = U 1 — U 2 ( 4 ) .
Если прохождение этой реакции обусловлено наличием постоянного давления, то выражение ( 3 ) с использованием тепловой функции запишется:
H = U + p V ( 5 ) , E = H 1 — H 2 + ∫ 1 2 V d p ( 6 ) , то случай говорит о наличии теплового эффекта реакции с p = c o n s t :
E p = H 1 — H 2 ( 7 ) .
По уравнениям ( 4 ) , ( 5 ) видно прохождение теплового эффекта при изохорном и изобарном процессах в не зависимости от ее хода реакции (промежуточных стадий). Он определяется начальным и конечным состоянием системы. Данная формулировка получила название закона Гесса – первого закона термохимии. При твердых или жидких начальных и конечных продуктах реакции значения E p и E V практически аналогичны. Это происходит по причине неизменности системы. Реакции, имеющие газообразные составляющие, в виду существенной переменности объема тепловые эффекты E p и E V значительно отличаются, а тепловой эффект рассматривается при постоянном давлении. Наличие заданной температуры теплового эффекта E p почти не зависит от внешнего давления, которое является постоянным для данного процесса. Тепловой эффект, который определяется при t = 25 ° C и p = 760 м м р т . с т . называют стандартным.
Из закона Гесса вытекают следствия, упрощающие расчет химических реакций, в системах с p = c o n s t или V = c o n s t :
- Тепловой эффект реакции разложения химического соединения численно равен и противоположен по знаку тепловому эффекту реакции синтеза этого соединения из продуктов разложения.
- Разность тепловых эффектов двух реакций, приводящих из разных состояний к одинаковым конечным состояниям, равняется тепловому эффекту реакции перехода из одного начального состояния в другое.
- Разность тепловых эффектов двух реакций, приводящих из одного исходного состояния к разным конечным состояниям, равна тепловому эффекту реакции перехода из одного конечного состояния в другое.
Закон Гесса позволяет использовать термохимические уравнения в качестве алгебраических. Зависимость количества теплоты, которая выделяется в реакции E от теплового эффекта реакции E o , и количества вещества n b одного из участников реакции( вещества b в качестве исходного вещества или продукта реакции), выражается при помощи уравнения:
E = n b v b E 0 ( 8 ) , где v b — является количеством вещества b , задаваемое коэффициентом перед формулой вещества b в химическом уравнении.
Уравнение Кирхгофа
Большинство термохимических данных в справочниках приведено при температуре 298 К . Чтобы рассчитать тепловые эффекты, обладающие другими температурами, применяют уравнения Кирхгофа. Они записываются для изохорного E V и изобарного E p тепловых эффектов. Дифференциальная форма приобретает вид:
∂ E V ∂ T V = ∂ U 1 ∂ T V — ∂ U 2 ∂ T V = C V 1 — C V 2 = — ∆ C v ( 9 ) , ∂ E p ∂ T p = ∂ H 1 ∂ T p — ∂ H 2 ∂ T p = C p 1 — C p 2 = — ∆ C p ( 10 ) .
В ( 10 ) , ( 9 ) имеется C V , C p , являющиеся теплоемкостями веществ при соответствующих процессах.
Уравнение Кирхгофа для энтальпии изображается в интегральной форме вида:
H T 2 = H T 1 + ∫ T 1 T 2 ∆ C p T d T ( 11 ) , где ∆ C p = ∑ i v j C p B j — ∑ v i C p A i i считается разностью изобарных теплоемкостей продуктов реакции и исходных веществ. Зачастую выражение ( 11 ) применяют в химии.
Примеры задач на вычислыние теплового эффекта
Записать выражение для расчета изменения стандартной энтальпии реакции.
Для решения задания необходимо взять за основу закон Гесса.
Именно он способствует оперированию термохимическими уравнениями как алгебраическими. Получаем, что запись принимает вид:
∆ H = ∑ j v j H B j — ∑ i v i H A i ( 1 . 1 ) , с B j , являющейся продуктами реакции, A i – исходными веществами. В задании требуют записать формулу для расчета стандартной энтальпии. Отметим, что все энтальпии, записанные уравнениями ( 1 . 1 ) , выбираются при температуре T = 298 К . Реже это фиксируется в самой формуле.
Даны химические уравнения. Произвести вычисление теплового эффекта реакции E образования 1 моль F e 2 O 3 при стандартных условиях из F e и O 2 .
1 . 2 F e + O 2 = 2 F e O , H 298 К , 1 = — 529 , 6 к Д ж ; 2 . 4 F e O + O 2 = 2 F e 2 O 3 , H ( 298 К , 2 ) = — 585 , 2 к Д ж .
По условию видно, что следует рассчитать тепловой эффект образования 1 моль оксида железа F e 2 O 3 реакции вида:
3 . 2 F e + 1 , 5 O 2 = F e 2 O 3 ( 2 . 1 ) .
Из двух данных реакций, следует сформировать реакцию ( 2 . 1 ) . Далее нужно разделить коэффициенты в ( 2 ) на 2 и произвести сложение с ( 1 ) . Отсюда:
2 F e + O 2 + 2 F e O + 0 , 5 O 2 = 2 F e O + F e 2 O 3 ( 2 . 2 ) .
Проведем преобразование (сокращение):
2 F e + 1 , 5 O 2 = F e 2 O 3 .
Было получено уравнение ( 2 . 1 ) :
Выше перечисленная последовательность действий с уравнениями привела к необходимому ( 2 . 1 ) . При проведении аналогичной схемы действий с тепловыми эффектами, будет результат эффекта реакции ( 2 . 1 ) . Протекание всех процессов обусловлено стандартными условиями, то есть при T = 298 К . Следовательно формула примет вид:
E 3 = H ( 1 ) + 0 , 5 H ( 2 ) ( 2 . 3 ) , где находящиеся в скобках цифры обозначают номер химической реакции. Рассчитаем и получим:
E 3 = — 529 , 6 + 0 , 5 · — 585 , 2 = — 822 , 2 ( к Д ж ) .
Ответ: тепловой эффект реакции равняется — 822 , 2 к Д ж .
Тепловой эффект. Уравнение Кирхгофа
Вы будете перенаправлены на Автор24
Что такое тепловой эффект
Тепловым эффектом E процесса называют сумму количества теплоты, которое отдала система ($Q’$) в этом процессе и теплового эквивалента работы ($\tilde$), элемент которой равен:
\[\widetilde<\delta A>=\delta A-pdV\ \left(1\right),\]
где $\delta A$- элементарная полная работа системы, $pdV$ — работа расширения.
Можно записать, что $E=-Q$, где $Q$ — количество теплоты, подведенное к системе, тогда в соответствии с первым началом термодинамики, получим:
где $\triangle U=U_2-U_1$ — изменение внутренней энергии системы, $p$ — давление, $V$ — объем.
Понятие теплового эффекта часто применяется в термохимии. Тепловым эффектом химической реакции является количество тепла, которое выделяется в ходе этой реакции. Если тепло выделяется, то реакция называется экзотермической, если поглощается — эндотермической. Принято считать, что в экзотермической реакции $E>0$, в эндотермической — $E
Предположим, что химическая реакция протекает при $V=const$. В таком случае тепловой эффект реакции $E_V$ рассчитывается как:
В том случае, если реакция проходит при постоянном давлении, то выражение для теплового эффекта (3) удобнее записать, используя тепловую функцию (энтальпию — H):
В таком случае тепловой эффект реакции при $p=const$ равен:
Уравнения (4) и (5) показывают нам, что тепловой эффект реакции при изохорном и изобарном процессах не зависит от хода (промежуточных стадий) реакции, а определяется начальным и конечным состояниями системы. Это формулировка закона Гесса — первый закон термохимии. Если начальные и конечные продукты реакции — твердые или жидкие, то $E_p$ и $E_V$ почти не отличаются друг от друга. Это происходит из-за неизменности объема системы. В реакциях с газообразными составляющими в виду существенной переменности объема тепловые эффекты $E_p$ и $E_V$ существенно отличаются, чаще всего рассматривают тепловой эффект при постоянном давлении. При заданной температуре тепловой эффект реакции $E_p$ практически (а в идеальном газе совсем) не зависит от внешнего давления (которое поддерживают постоянным). Тепловой эффект определённый при t=250C и p=760 мм рт.ст. считается стандартным.
Из закона Гесса вытекают следствия, которые упрощают расчет химических реакций, в системе при $p=const$ или $V=const$:
- тепловой эффект реакции разложения химического соединения численно равен и противоположен по знаку тепловому эффекту реакции синтеза этого соединения из продуктов разложения;
- разность тепловых эффектов двух реакций, приводящих из разных состояний к одинаковым конечным состояниям, равна тепловому эффекту реакции перехода из одного начального состояния в другое;
- разность тепловых эффектов двух реакций, приводящих из одного исходного состояния к разным конечным состояниям, равна тепловому эффекту реакции перехода из одного конечного состояния в другое.
Закон Гесса позволяет оперировать термохимическими уравнениями, как алгебраическими. Зависимость количества теплоты, выделяющейся в реакции (E) от теплового эффекта реакции (Eo) и количества вещества (nb) одного из участников реакции (вещества b — исходного вещества или продукта реакции), выражается уравнением:
Здесь $\ <\nu >_b$— количество вещества b, задаваемое коэффициентом перед формулой вещества b в термохимическом уравнении.
Уравнение Кирхгофа
Большинство термохимических данных в справочниках приведено при температуре 298К. Для расчета тепловых эффектов при других температурах используют уравнения Кирхгофа. Уравнения Кирхгофа записываются для изохорного $(E_V)$ и изобарного $<(E>_p)$ тепловых эффектов. В дифференциальной форме они имеют вид:
В уравнениях (10) и (9) $C_V$, $C_p$- теплоемкости вещества при соответствующих процессах (изобарном и изохорном).
В интегральной форме уравнение Кирхгофа для энтальпии имеет вид:
где $\triangle C_p=\sum\limits_j<<\nu >_jC_p(B_j>)-\sum\limits_i<<\nu >_iC_p(A_i>)$ — разность изобарных теплоемкостей продуктов реакции и исходных веществ. Уравнением (11) в химии пользуются чаще всего.
Задание: Напишите выражение для расчета изменения стандартной энтальпии реакции.
Основой для решения поставленной задачи является закон Гесса.
Закон Гесса позволяет оперировать термохимическими уравнениями, как алгебраическими. Поэтому мы можем записать:
\[\triangle H=\sum\limits_j<<\nu >_j>H\left(B_j\right)-\sum\limits_i<<\nu >_i>H\left(A_i\right)\ \left(1.1\right),\]
где $B_j$ — продукты реакции, $A_i$- исходные вещества. Так как в задаче требуется записать формулу для расчета стандартной энтальпии. Необходимо отметить, что все энтальпии, которые записаны в уравнении (1.1), берутся при температуре T=298 K. Иногда это пишут непосредственно в формуле.
Задание: По приведенным ниже химическим уравнениям вычислите тепловой эффект реакции (E) образования 1 моль $
- $2Fe+O_2=2FeO,\ H\left(298K,\ 1\right)=-529,6\ кДж$
- $4FeO+O_2=2
_2O_3,\ H\left(298K,\ 2\right)=-585,2\ кДж$
Таким образом, необходимо рассчитать тепловой эффект образования 1 моль оксида железа ($
Получается, что из двух реакций, приведенных в условиях задачи, необходимо сформировать реакцию (2.1). Для этого разделим коэффициенты в реакции (2) на 2 и сложим с химическим уравнением (1), таким образом, получим:
Проведем сокращения, получим уравнение реакции:
Мы получили уравнение (2.1)
Так как приведенная выше последовательность манипуляций с химическими уравнениями 1 и 2 из условий задачи привела нас к требуемому уравнению (2.1), то проведя аналогичную схему действий с тепловыми эффектами, мы получим тепловой эффект реакции (2.1). Мы помним, что все процессы протекают в стандартных условиях, то есть при T=298K. Таким образом, получаем:
где цифры в скобках обозначают номер химической реакции. Проведем расчет:
\[E\left(3\right)=-529,6+0,5\cdot \left(-585,2\right)=-822,2\ \left(кДж\right).\]
Ответ: Тепловой эффект реакции -822, 2 кДж.
Получи деньги за свои студенческие работы
Курсовые, рефераты или другие работы
Автор этой статьи Дата последнего обновления статьи: 26 11 2021
http://zaochnik.com/spravochnik/fizika/termodinamika/teplovoj-effekt/
http://spravochnick.ru/fizika/termodinamika/teplovoy_effekt_uravnenie_kirhgofa/