Практикум по коллоидной химии (стр. 7 )
 | Из за большого объема этот материал размещен на нескольких страницах: 1 2 3 4 5 6 7 8 9 |
Изучив данную тему и выполнив относящиеся к ней лабораторные работы, студент должен знать:
— способы получения, классификацию, строение макромолекул ВМВ;
— физические состояния аморфных ВМВ и особенности поведения и эксплуатации их в каждом состоянии;
— поведение твердых ВМВ при контакте с растворителями (набухание, степень набухания, контракция, давление набухания);
— свойства растворов ВМВ;
— особенности вязкого течения растворов ВМВ;
— механизм установления мембранного равновесия;
— причины и механизм застудневания и коацервации растворов ВМВ;
— свойства студней и гелей.
Студент должен уметь:
— определять степень набухания полимерных образцов (в том числе растительного сырья);
— выяснять влияние различных факторов на процессы набухания и застудневания;
— рассчитывать среднюю молярную массу ВМВ по осмометрическим и вискозиметрическим данным;
— определять изоэлектрическую точку белков вискозиметрическим методом.
Студент должен получить или закрепить навыки:
— работы с вискозиметром Оствальда;
— работы с прибором для определения степени набухания;
— пользования мерной посудой и другим лабораторным оборудованием;
— расчётов по различным уравнениям;
— построения графиков и интерпретации экспериментальных и расчетных данных.
Высокомолекулярные вещества (ВМВ) характеризуются большой молекулярной массой от нескольких тысяч до многих миллионов.
Они способны к набуханию. Их растворы обладают повышенной вязкостью, способны к застудневанию, высаливанию, синерезису.
Увеличение объема ВМВ в результате поглощения низкомолекулярной жидкости называется набуханием.
Количественной характеристикой набухания служит степень набухания (α).
Степень набухания можно определить по приращению объема или массы вещества.
Различают ограниченное набухание, которое характеризуется переходом ВМВ в студень. При неограниченном набухании ВМВ переходит в раствор.
Процесс набухания сопровождается контракцией – уменьшением общего объема системы.
Это связано с ориентацией и уплотнением молекул растворителя в гидратной оболочке.
На набухание влияют анионы

Переход раствора ВМВ в студень (эластичную систему, обладающую рядом свойств твердого тела) называется застудневанием. При этом раствор ВМВ теряет свою текучесть.
К факторам, влияющим на застудневание можно отнести изменение температуры, концентрации раствора, pH среды, добавление электролита, форма молекул ВМВ, время застудневания.
Низкомолекулярные электролиты влияют на застудневание растворов белков противоположно влиянию на набухание. Ионы, увеличивающие набухание замедляют застудневание и наоборот.
При стоянии свежеприготовленные студни ВМВ часто претерпевают синерезис – уменьшение объема путем самопроизвольного выпресовывания среды из эластичного студня.
Вязкость – это свойство текучих тел оказывать сопротивление перемещению одной их части относительно другой.
Растворы ВМВ не подчиняются законам Ньютона, Пуазейля, Эйнштейна, которым подчиняются растворы низкомолекулярных веществ. Отличие объясняется наличием вытянутых и гибких макромолекул, наличием ассоциатов. Измеряя вязкость растворов ВМВ можно вычислить приведенную вязкость (ηуд./с), найти характеристическую вязкость [η] – значение приведенной вязкости в бесконечно разбавленных растворах.
Зависимость [η] от молекулярной массы описывается уравнением Марка-Куна-Хаувинка.
[η]=КМα, где К и α – константы.
α – выражает степень свертывания молекул и гибкость цепи.
Молекулы некоторых ВМВ содержат ионогенные группы и в растворах способны распадаться на ионы. Такие ВМВ называются полиэлектролитами.
Полиэлектролиты, содержащие одновременно как кислотные так и основные группы, называются полиамфолитами. К ним относятся белки, содержащие группы –COOH и –NH2 или в ионизированной форме –COO– им NH3+. Схематически белковую молекулу можно изобразить так:

В нейтральной среде заряд белковой молекулы определяется состоянием групп –COOH и –NH2 и степенью их диссоциации.
В кислой среде молекула белка приобретает положительный заряд:
NH2 – R – COOH + H+ àNH3+ — R – COOH (при электрофорезе перемещается к катоду)
В щелочной среде – отрицательный заряд:
NH2 – R – COOH + OH — àNH2 — R – COO-+Н2О (при электрофорезе перемещается к аноду).
В водном растворе при определенной концентрации водородных ионов молекула белка может находиться в изоэлектрическом состоянии, когда число ионизированных групп основных равно числу ионизированных групп кислотных. Значение pH, при котором белок находится в изоэлектрическом состоянии и заряд молекулы белка равен нулю, называется изоэлектрической точкой (ИЭТ).
Существует ряд методов определения изоэлектрической точки:
1. по электрофоретической подвижности;
2. по скорости желатинирования;
3. по величине степени набухания;
4. по минимуму вязкости;
5. по степени коагуляции белков («схема Кройта»).
ВОПРОСЫ ТЕОРЕТИЧЕСКОГО МИНИМУМА ДЛЯ САМОПОДГОТОВКИ
1. Высокомолекулярные вещества (ВМВ). Методы получения, классификация. Использование ВМВ в фармации. Конформация макромолекул. Структура ВМВ (линейная, разветвлённая, пространственная).
2. Физические состояния ВМВ (стеклообразное, высокоэластичное, вязко-текучее). Температуры перехода между ними. Сходство растворов ВМВ с золями и истинными растворами низкомолекулярных веществ и отличие от них.
3. Набухание ВМВ и его значение в фармации и медицине. Термодинамика набухания и растворения ВМВ. Лиотропные ряды набухания. Давление набухания. Уравнение Позняка.
4. Вязкость растворов ВМВ. Виды вязкости (динамическая, относительная, кинематическая). Уравнения Ньютона, Пуазейля, Стокса. Вискозиметрия. Вискозиметры.
5. Удельная, приведенная и характеристическая вязкость растворов ВМВ. Уравнения Штаудингера и Марка — Хаувинка — Куна. Вискозиметрическое определение молярной массы ВМВ.
6. Полиэлектролиты. Полиамфолиты. Изоэлектрическая точка полиамфолитов и белков. Методы её определения.
7. Выделение ВМВ из растворов. Высаливание. Коацервация. Выделение под действием органических растворителей.
8. Застудневание растворов ВМВ и факторы, влияющие на него. Тиксотропия. Лиотропный ряд застудневания.
РЕШЕНИЕ ТИПОВЫХ ЗАДАЧ
Задача 1. Рассчитать относительную, удельную и приведенную вязкость 1,5%-ного раствора поливинилового спирта, если время истечения его, измеренное с помощью вискозиметра Оствальда, равно 80 с, а время истечения такого же объёма воды – 60 с.
РЕШЕНИЕ. Принимая плотность данного раствора из-за его малой концентрации приблизительно равной плотности воды, рассчитаем относительную вязкость по соотношению:
Приведенная вязкость представляет собой отношение удельной вязкости раствора к массовой концентрации полимера С:
Выражая массовую концентрацию поливинилового спирта в кг/м3 (С = 15 кг/м3), получим:
Задача 2. Рассчитать диаметр капилляра d, если по отрезку его длиной 5 см под давлением 19800 Па 15 мл дистиллированной воды протекают за 4 минуты 40 секунд. Динамическая вязкость воды 0,001 Па×с при Т = 25оС.
РЕШЕНИЕ. Воспользуемся уравнением Пуазейля:
где Q – объёмная скорость течения жидкости, равная отношению объёма жидкости V ко времени течения его по капилляру длиной 
Преобразуем уравнение для нахождения радиуса капилляра и решим его, подставляя данные в системе СИ:
Задача 3. Рассчитать среднюю молярную массу М полистирола по величине характеристической вязкости его толуольного раствора: [
РЕШЕНИЕ. Из уравнения [ 
Это уравнение удобнее решать с помощью логарифмирования:
ИЗУЧЕНИЕ КИНЕТИКИ НАБУХАНИЯ РАСТИТЕЛЬНОГО СЫРЬЯ
Цель работы: Построение изотермы набухания образцов растительного сырья; расчёт степени набухания.
Целевые задачи: Выяснение связи набухания с ориентацией растительных волокон; овладение методикой работы с прибором для изучения кинетики набухания.
УСТРОЙСТВО ПРИБОРА ДЛЯ ИЗУЧЕНИЯ КИНЕТИКИ НАБУХАНИЯ И МЕТОДИКА ИЗМЕРЕНИЙ
Прибор (рис. 4.1) состоит из цилиндрической измерительной ячейки 1 с перфорированными дном и крышкой и микрометра 3. В ячейке свободно перемещается поршень 2. Шток поршня упирается в шток микрометра. Исследуемый образец 4 помещается между поршнем и дном измерительной ячейки, которая устанавливается в штативе 5. К штативу прикреплен также и микрометр. После того, как прибор будет собран, измерительная ячейка с исследуемым образцом помещается в сосуд 6 с водой (или с другим растворителем). Пластина 8 штатива удерживает прибор в вертикальном положении на необходимой глубине. Перед погружением прибора с исследуемым образцом в растворитель необходимо поворотом рифленого кольца, окружающего микрометр по периметру, подвести ноль шкалы к стрелке. В момент погружения прибора в растворитель начинается отсчёт времени.
Измерения заключаются в отсчёте через определенные промежутки времени делений, на которые смещается стрелка, передвигаемая набухающим образцом. Отсчёт ведётся по чёрной шкале, градуированной на расширение. Цена деления соответствует 0,01 мм. Маленький циферблат микрометра служит для подсчёта числа полных оборотов стрелки.
ОСНАЩЕНИЕ РАБОЧЕГО МЕСТА
Приборы для изучения кинетики набухания Штангенциркуль
Образцы растительного сырья Секундомер
Обрезки фильтровальной бумаги Дистиллированная
1. Проверить оснащение рабочего места.
2. Получить у преподавателя 2 образца растительного сырья.
3. Измерить штангенциркулем длину, ширину и высоту обоих образцов и занести результаты измерений в таблицу 1.
Лекция №15.
План лекции:
Строение макромолекул
Основным признаком соединений является их высокая молекулярная масса, а, следовательно, и их большой размер молекул.
Свойства таких соединений зависят не только от химического состава, но также от размеров и формы больших молекул, называемых обычно макромолекулами.
Три основных типа молекул ВМС : линейная, плоская (двухмерная) и пространственная (трехмерная).
Свойства линейных макромолекул
К этому типу относится подавляющее большинство природных и искусственно получаемых ВМС. Такая форма отвечает наименьшей потенциальной энергии молекул.
Часто цепи дают ответвления и тогда они называются разветвленными цепями (б). В этом случае макромолекулу геометрически можно отнести к типу двухмерных молекул.
В более редких случаях однородные линейные макромолекулы под влиянием изменения внешних условий (например, температуры и давления) или добавок посторонних веществ могут вступать друг с другом в химическую (валентную) связь, устанавливающуюся в отдельных участках цепи на ее длине в виде “мостов” или “перемычек” (в). Такие молекулы получили название “сшитых” молекул (“сшитых” структур). Так как такое “сшивание” происходит в пространстве, то макромолекулы становятся трехмерными образованиями и превращаются в жесткие системы с характерными для них свойствами (нерастворимостью, отсутствием плавкости, эластичности, пластичности и пр.) Типичными ВМС с трехмерными молекулами являются фенолформальдегидные смолы.
Длина цепочного типа макромолекул при наличии в них десятков тысяч атомов может достигать нескольких тысяч ангстрем.
От формы и строения макромолекул зависят и другие свойства ВМС — осмотическое давление, способность к набуханию, вязкость.
Все молекулярные вещества, вследствие их большого молекулярного веса, нелетучи и не способны перегоняться.
Влияние температуры на структуру ВМС
Межмолекулярные силы, действующие между отдельными атомами и их группами, препятствуют изменению формы макромолекул. Чтобы изменить форму макромолекул, надо преодолеть действие межмолекулярных сил, что сопряжено с затратой определенного количества энергии. С повышением температуры растет энергия макромолекул, причем энергия теплового движения может оказаться больше энергии взаимодействия молекул друг с другом, в результате чего вероятность изменения конфигурации и взаимного расположения молекул увеличивается. Наоборот, при охлаждении полимера перегруппировка макромолекул практически прекращается: в результате, полимер остается по своей неупорядоченной структуре в аморфно- жидком состоянии и при температурах значительно ниже температуры кристаллизации. Таким образом, даже при сильном охлаждении высокополимеры не переходят в упорядоченное (кристаллическое) состояние. В этом ВМС сходны со стеклами и такое состояние высокополимера называется стеклообразным. Процесс застекловывания идет часто в довольно значительном температурном интервале. Та температурная область, в которой происходит такой переход, называется температурой перехода, в частности для явления застекловывания она называется температурой застекловывания.
Выше температуры застекловывания полимер начинает переходить из стеклообразного состояния в высокоэластичное и сохраняет его при дальнейшем нагревании до некоторой температуры, называемой температурой текучести. Выше этой температуры у полимера появляется необратимое и самопроизвольное перемещение макромолекул относительно друг друга (текучесть).
Способность к течению высокомолекулярных веществ при повышении температуры используется в технике для смешения каучуков и пластиков с инградиентами и для формирования изделий из пластмасс прессованием.
Не все аморфные ВМС могут находиться во всех трех указанных состояниях.
Общая характеристика растворов высокомолекулярных соединений
Растворы ВМС термодинамически устойчивы и при соответствующих предосторожностях могут существовать сколько угодно долго. При растворении ВМС всегда образуется гомогенная система, причем, растворение сопровождается уменьшением термодинамического потенциала. Коллоидные растворы, наоборот термодинамически неустойчивы и способны стареть.
Растворение ВМС не требует присутствия в системе стабилизатора. Наконец, растворы ВМС находятся в термодинамическом равновесии и являются обратимыми системами. К таким системам применимо правило фаз Гиббса (в отличие от коллоидных систем).
Следует также учитывать, что равновесное состояние в растворах высокомолекулярных веществ устанавливается медленно.
Для растворов ВМС характерны три группы свойств. Первые две присущи истинным и коллоидным растворам, а третья группа характерна только для растворов ВМС: набухание и студнеобразование.
Характеристика первой и второй группы свойств
Растворам ВМС присуще осмотическое давление, которое вычисляется по формуле:
p = (с/М) R Т + b с 2 (15.1)
с, М — концентрация и молекулярная масса ВМС, b — второй вириальный коэффициент (отражает флуктуацию конформационных линейных структур макромолекул)
Разделим левую и правую части уравнения на концентрацию:
p /с = R Т/М + b с (15.2)
Величина p /с — приведенное осмотическое давление. Для идеальных растворов и большинства коллоидных растворов величина приведенного осмотического давления постоянна и не зависит от концентрации. Для растворов ВМС эта величина зависит от концентрации ВМС (что и отражено в уравнении 15.2).
В координатах “ p /с — с” уравнение 15.2 является уравнением прямой, тангенс угла наклона которой равен коэффициенту b , а отрезок, отсекаемый этой прямой на оси ординат соответствует величине R Т/М.
Таким образом, по значению осмотического давления можно определить молекулярную массу макромолекулы растворенного ВМС.
Вязкость растворов ВМС зависит от концентрации вещества в растворе. В отличие от других растворов незначительная концентрация ВМС порой приводит к значительному увеличению вязкости раствора.
Вязкость растворов ВМС зависит от условий определения, в частности, от давления. Это объясняется тем, что одни и те же макромолекулы могут находиться в различных конформационных состояниях: от линейных до глобул, поэтому вязкость растворов ВМС может быть неодинакова в различных направлениях. Вязкость макромолекул с выпрямленными хаотично расположенными звеньями выше, чем вязкость макромолекул, которые имеют форму клубка.
Если вязкий полимер или его раствор продавить через капилляр, то молекулы будет выпрямляться и располагаться ориентированно, а вязкость будет снижаться.
Вязкость растворов ВМС зависит также от свойств и температуры растворителя.
Для растворов ВМС различают относительную, удельную, приведенную и характеристическую вязкости.
Относительная вязкость — отношение вязкости раствора h р к вязкости растворителя h 0 :
t р время истечения раствора ВМС, t 0 — время истечения растворителя(эти величины определяются с помощью вискозиметра).
Удельная вязкость — показывает, насколько увеличилась вязкость раствора ВМС по сравнению с вязкостью растворителя:
Приведенная вязкость — отношение удельной вязкости к концентрации:
Обычно приведенная вязкость линейно зависит от концентрации (рис.15.2).При экстраполяции прямой до пересечения с осью ординат получают величину / h /, которую называют характеристической вязкостью:
/ h / = l i m h уд /с (15.6)
SHAPE \* MERGEFORMAT
Рис.15.2.Изменение приведенной вязкости в зависимости от концентрации ВМС.
Характеристическую вязкость определяют на основании вискозиметрических измерений, используя значение относительной, удельной и приведенной вязкостей.
Характеристическая вязкость для данной пары веществ является величиной условной, но постоянной, она не зависит от концентрации растворителя и состояния макромолекул, кроме того, она связана с молекулярной массой макромолекул.
/ h / = k М а , l g / h / = l g k + а l g М (15.7)
М — средняя молекулярная масса ВМС, а, k — коэффициенты.
Уравнение 15.7 — уравнение Марка-Куна-Хаувинка.
Для растворов полимеров с короткими и жесткими цепями а = 1 и уравнение 15.7 упрощается:
/ h / = k М, l g / h / = l g k + l g М (15.8)
Коэффициент a зависит от формы молекул. Значение коэффициентов определяют экспериментально, это позволяет по значению характеристической вязкости рассчитать молекулярную массу макромолекул. Зная массу, можно определить средний размер r макромолекул:
Уравнение марка куна для вязкости
1.3.1. Гидродинамические методы
В соответствии с законом Ньютона сила, необходимая для сдвига двух соседних гипотетических слоев жидкости, отнесенная к единице площади их соприкосновения (так называемое напряжение сдвига τ), пропорциональна скорости сдвига (или градиенту скорости сдвига 
Коэффициент пропорциональности η в этом уравнении называется коэффициентом вязкости (или вязкостью). Жидкости, вязкости которых в изотермических условиях остаются постоянными при любых значениях τ и 
Перечень используемых в лабораторно-технологической практике вискозиметрических терминов приведен в табл. 1.1.
Значения [η] оцениваются экстраполяцией значений приведенной или приведенной логарифмической вязкости к «нулевой» концентрации полимера (рис. 1.8), т.е.
Таблица 1.1. Вискозиметрические характеристики
Величину M v высокомолекулярных соединений определяют обычно по вязкости разбавленных растворов, концентрация которых не превышает 1/[η]. Эту величину называют средневязкостной молекулярной массой.
Для измерения вязкости разбавленных растворов применяют капиллярные вискозиметры. Схема одного из них приведена на рис. 1.9. Исследуемую жидкость заливают в вискозиметр и тщательно термостатируют. Закрыв патрубок 3, раствор из баллона 4 переводят в баллон 1. Для обеспечения постоянства перепада давления в вискозиметре создают «висящий» слой, для чего открывают патрубок 3. Контролируют время истечения жидкости через калиброванный капилляр между метками измерительного баллона 1.
В соответствии с законом Гагена — Пуазейля
где r — радиус капилляра; l — длина капилляра; ΔР — давление, действующее на жидкость; Q — объем жидкости, вытекающей за время t.
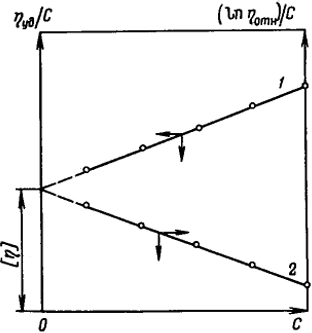
Рис. 1.8. Зависимость приведенной (1) и приведенной логарифмической (2) вязкости от концентрации полимера
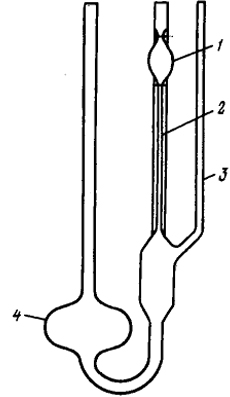
Рис. 1.9. Схема вискозиметра с «висящим» уровнем:
1 — измерительный баллон; 2 — калиброванный капилляр; 3 — патрубок; 4 — приемный баллон
Очевидно, что ΔР = Δhр, где Δh — высота столба жидкости, а ρ — плотность жидкости. Следовательно,
где К‘ = πr 4 Δh/(8 Ql) [K‘ — величина, постоянная для данного вискозиметра].
Так как плотность разбавленного раствора ρ и плотность растворителя ρ0 практически одинаковы, то η = K‘t. Тогда ηотн = t/t0, где t и t0 — время истечения раствора и растворителя.
Вискозиметрическим методом обычно определяется средневязкостная молекулярная масса M v.
Значение [η] связано с величиной молекулярной массы следующей зависимостью (уравнение Марка-Хаувинка-Флори):
где Kη и α — константы, определяемые экспериментально для данной системы полимер-растворитель при выбранной температуре.
Значение α зависит от конформации макромолекул, термодинамического качества растворителя и температуры (см. гл. 2). Оно может изменяться от 0,5 для статистического молекулярного клубка в θ-растворителе до 2,0 для абсолютно жесткой молекулы. Величина Кη имеет размерность дл/г, изменяется обычно в пределах от 10 -2 до 10 -5 и зависит от выбора системы полимер — растворитель, полидисперсности, разветвленности, тактичности полимера, температуры и других факторов. В этом отношении выбор значений Kη и α для вычисления M v условен.
Значения Кη и α для ряда волокнообразующих полимеров приведены в Приложении 6.
Для получения сопоставимых результатов по M v целесообразно для каждого полимера использовать регламентированные условия определения [η] (температура, растворитель) и постоянные значения Кη и α.
Вопрос. Для сополимеров переменного состава, характеризующихся случайным статистическим распределением звеньев вдоль цепи, а также химической неоднородностью фракций (карбоцепные сополимеры, не полностью замещенные эфиры целлюлозы), определение Кη и α не имеет смысла. Объясните причину этого утверждения.
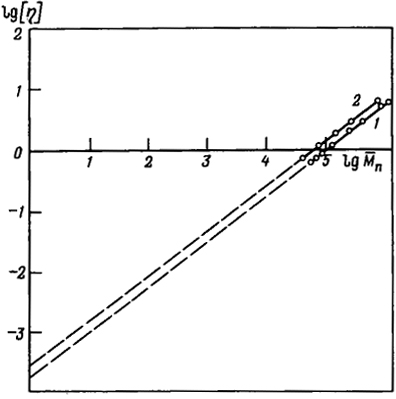
Рис. 1.10. Зависимость lg[η] = f(lg Mn) для полиакрилонитрила в диметилформамиде при 25°С:
1 — фракционированный; 2 — нефракционированный полимер
Ответ. Статистические сополимеры не являются соединениями постоянного химического строения и состава. Поэтому при определении значения M v можно подобрать значения Kη и α лишь для данного препарата в данном растворителе. Другой образец этого сополимера, отличающийся хотя бы особенностями чередования звеньев полимерной цепи, а тем более химическим строением их, характеризуется иными гидродинамическими показателями, другими значениями Кη и α при изотермических условиях.
Вместе с тем при одинаковом составе сополимеров, синтезированных в идентичных условиях, возможна оценка молекулярных масс вискозиметрическим способом на основании значений Kη и α, определенных независимым способом. Например, для волокнообразующего сополимера акрилонитрила (40%), винилхлорида (58%) и n-стиролсульфокислоты (2%) Kη = 1,21·10 и α = 0,82 в ацетоне при 25°С.
Задача. Для вычисления значений Kη и α для полиакрилонитрила, синтезированного полимеризацией в присутствии персульфата калия, полимер был подвергнут фракционированию. Получено 8 фракций, различающихся по величине [η]. Осмометрическим методом при 25°С в диметилформамидных растворах были определены значения М для каждой фракции. В тех же условиях были определены [η] и М n пяти образцов нефракционированного, полиакрилонитрила. Результаты измерений приведены на рис. 1.10. Определить значения Кη и α.
Решение. Логарифмируя уравнение (1.32), получаем
Очевидно, что тангенс угла наклона прямой к оси абсцисс равен α. В данном случае он одинаков для прямых 1 и 2 (рис. 1.10) и составляет
Значения Кη определяют, экстраполируя прямые 1 и 2 до пересечения с осью ординат (lg M v = 0). Для нефракционированного полиакрилонитрила Kη = 2,37·10 -4 , для фракционированного Кη = 17,5·10 -4 .
Задача. Для установления значений Кη и α для растворов поливинилацетата в ацетоне были выделены узкие фракции, определены их молекулярные массы М п (осмометрически) и характеристические вязкости [η]. Оказалось, что для фракции с М п = 22500 [η] = 0,194, а для фракции с М n = 40000 [η] = 0,289. Вычислить значения Kη и α.
Решение. Составляем систему уравнений:
Решая эту систему уравнений, находим Кη и α:
0,289/0,194 = (40000/22500) α ; α = 0,686;
В некоторых случаях значение [η] может быть оценено по результатам определения Луд при одной концентрации. Этот способ является применимым и достаточно точным только для тех систем полимер — растворитель, для которых график ηуд/С от С — прямая, а угол ее наклона — постоянный. Этот способ оценки [η] может быть использован для определения молекулярных характеристик волокнообразующих полимеров, синтезированных в одинаковых условиях. Для таких расчетов используют формулу Соломона-Сьюта:
Задача. Рассчитать средневязкостную молекулярную массу и степень полимеризации полиэтилентерефталата, если относительная вязкость ηотн полимера в о-хлорфеноле при концентрации 0,50 г/100 см 3 равна 1,340.
Решение. В соответствии с формулой (1.33) имеем
[η] = 2(0,34 — ln1,34) 0,5 0,5 -1 = 0,87.
Элементарное звено полиэтилентерефталата
имеет молекулярную массу M0 = 192. Для о-хлорфенола, являющегося растворителем этого полимера, при 25°С значения Кη = 6,56·10 -4 , α = 0,73.
Молекулярная масса, определяемая вискозиметрическим способом и называемая средневязкостной молекулярной массой M v, существенно зависит от наличия в полимере высокомолекулярных фракций:
Средневязкостная молекулярная масса эквивалентна истинной молекулярной массе гипотетической однородной фракции с тем же значением [η], что и у данного полимера.
Для относительно гибких макромолекул, когда 0,5 ≤ α ≤ 1, М п ≤ M v ≤ M w. Для жестких молекул, когда α > 1, M v > М w. Отличия в значениях M v и M w иногда достигают 40%.
Задача. Рассчитать средневязкостную молекулярную массу М v и степень полимеризации Р поливинилового спирта (раствор в воде при 25°С), если известны значения приведенных логарифмических вязкостей растворов:
| С, г/100 см 3 | 0,1 | 0,2 | 0,3 | 0,4 |
| ln ηотн/С | 2,1 | 1,6 | 1,0 | 0,2 |
Решение. Графическая зависимость ln ηотн/С — С для водных растворов поливинилового спирта дает [η] = 2,8. Аналитическое решение этой зависимости позволяет получить уравнение прямой линии: ln ηотн/С = 2,8 — 6,3С (при этом σ 2 = 5,75·10 -3 ). При С → 0 ln ηотн/С = [η] = 2,8. Согласно уравнению (1.32) в соответствии с Приложением 6 имеем
Kη = 5,95·10 -4 ; α = 0,63; М
| α |
| v |
= [η]/Кη;
M
| 0,63 |
| v |
= 2,8/(5,95·10 -4 ); M v = 6,7·10 5 ; М0 = 44; P n = 15350.
Вискозиметрическое определение средней молекулярной массы M v является наиболее удобным способом оценки этой важнейшей характеристики волокнообразующих полимеров и поэтому применяется как в лабораторных исследованиях, так и при оценке характеристик качества полимерного сырья. Значения Kη и α в уравнении Марка-Хаувинка-Флори (1.32) для ряда волокнообразующих полимеров приведены в Приложении 6.
http://www.trotted.narod.ru/collchem/lec-15.htm
http://bibl.tikva.ru/base/B1223/B1223Part12-32.php






















