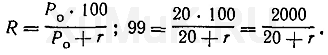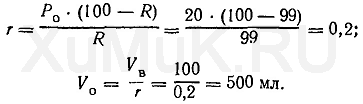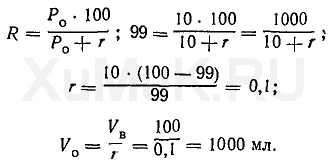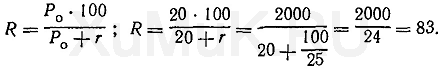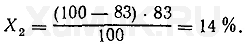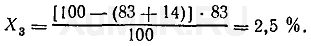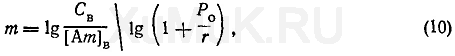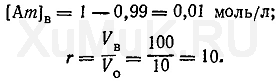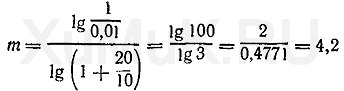Лекция 16 «Экстракция»
16.1. ЭКСТРАКЦИЯ В СИСТЕМЕ ЖИДКОСТЬ — ЖИДКОСТЬ
16.1.1. ОБЩИЕ СВЕДЕНИЯ
Экстракцией в системе жидкость — жидкость называют процесс извлечения растворенного вещества или веществ из жидкости с помощью специальной другой жидкости, не растворяющейся или почти не растворяющейся в первой, но растворяющей экстрагируемые компоненты.
Принципиальная схема экстракции приведена на рис. 16.1.1.
Рис. 16.1.1. Принципиальная схема экстракции
В экстрактор загружаются исходный раствор F, содержащий распределяемое (экстрагируемое) вещество или вещества М, и растворитель L. Жидкость, используемая для извлечения компонентов, называется экстрагентом (Е). Массообмен между фазами протекает при их непосредственном контакте. Полученная в результате экстракции жидкая смесь поступает в разделитель, где разделяется на экстракт (Э) — раствор экстрагированных веществ в экстрагенте и рафинат (R) — остаточный раствор, из которого экстрагированы извлекаемые компоненты. Разделение смеси на экстракт и рафинат происходит в результате отстаивания или сепарирования.
Процесс экстракции проводится в аппаратах различной конструкции — экстракторах.
Экстракцию широко используют для извлечения ценных продуктов из разбавленных растворов, а также для получения концентрированных растворов.
Основное преимущество экстракции — низкая рабочая температура процесса, что позволяет разделять жидкие смеси термолабильных веществ, например антибиотиков, разлагающихся при повышенных температурах.
Во многих случаях экстракцию применяют в сочетании с ректификацией. Поскольку расход теплоты на ректификацию уменьшается с увеличением концентрации исходного раствора, предварительное концентрирование раствора экстракцией позволяет сократить расход теплоты на разделение исходной смеси.
16.1.2. РАВНОВЕСИЕ В СИСТЕМЕ ЖИДКОСТЬ—ЖИДКОСТЬ
Переход распределяемого вещества из одной жидкой фазы (исходного раствора) в другую (экстрагент) происходит до установления равновесия, т. е. до выравнивания химических потенциалов в фазах. В процессе участвуют три компонента (К=3) и две фазы (Ф=2). Согласно правилу фаз вариантность системы F=3. Однако температура и давление при проведении процесса экстракции, как правило, поддерживаются постоянными. Тогда вариантность экстракционной системы будет равняться единице.
Следовательно, данной концентрации распределяемого вещества в одной фазе в состоянии равновесия соответствует определенная концентрация в другой.
Равновесие в процессах экстракции характеризует коэффициент распределения φ, который равен отношению равновесных концентраций экстрагируемого вещества в обеих жидких фазах — в экстракте и рафинате.
В простейших системах достаточно разбавленных растворов, подчиняющихся закону Бертло — Нернста, при постоянной температуре коэффициент распределения не зависит от концентрации распределяемого вещества и φ=ур/х, где ур, х — равновесные концентрации распределяемого вещества в экстракте и рафинате. В этом случае линия равновесия — прямая:

Уравнению отвечают начальные участки изотерм экстракции. При наличии диссоциации и ассоциации молекул растворённого вещества и его химического взаимодействия с экстрактом коэффициент распределения изменяется с концентрацией и изотермы экстракции отклоняются от прямой. В области высоких концентраций такие отклонения вызваны изменением коэффициентов активности в фазах.
Коэффициент распределения, как правило, в промышленных системах определяется экспериментальным путём.
Если считать обе жидкие фазы нерастворимыми друг в друге, то каждая из фаз будет представлять собой двухкомпонентный раствор. В этом случае процесс экстракции по аналогии с другими массообменными процессами может быть изображён в координатах y—x.
При частичной взаимной растворимости жидких фаз каждая из них при экстракции будет представлять собой трёхкомпонентный раствор. Составы трёхкомпонентных смесей представляют в треугольной системе координат (Рис. 16.1.2).
Рис. 16.1.2. Треугольная диаграмма
В вершинах равностороннего треугольника L, M, E отложены составы частых (100% — ных) компонентов: растворитель исходного раствора L, экстрагент E и распределяемое вещество M. Каждая точка на сторонах LM, ME, и EL соответствует составу двухкомпонентных растворов.
Площадь, заключённая внутри треугольника, соответствует составам трёхкомпонентных растворов (тройным смесям). Для определения содержания каждого компонента в растворе на сторонах диаграммы нанесены шкалы отсчёта. Длина каждой стороны принята за 100% (массовых, объёмных или мольных).
Состав раствора или смеси определяется длиной отрезков, проведенных параллельно каждой стороне треугольника до пересечения с двумя другими.
Например, точка N характеризует тройную смесь, состоящую из 30% растворителя L, 41% экстрагента Е и 30% распределяемого вещества М.
На треугольной диаграмме изображаются процессы изменения состава трехкомпонентных смесей. При прибавлении к раствору, характеризуемому точкой N (рис. 16.1.3, а), распределяемого вещества М содержание компонентов Е и L не изменяется, а точки, определяющие составы полученных растворов, будут находиться на прямой NM, приближаясь к вершине треугольника М, в зависимости от количества прибавленного компонента М.
При извлечении распределяемого вещества М из смеси N и точки, соответствующие получаемым составам, будут лежать на прямой РМ, и чем более будет разбавлен раствор, тем ближе к стороне треугольника LE.
Рис. 16.1.3. Изменение состава трёхкомпонентных смесей на треугольной диаграмме:
а — концентрирование и разбавление смеси; б — смешивание двух трёхкомпонентных смесей
Разбавление смеси состава N экстрагентом Е характеризует линия NE.
С помощью треугольной диаграммы по известному количеству и составу исходной смеси (точка N) и составам, получаемым при ее разделении на экстракт (точка Э) и рафинат (точка R), можно определить количество этих фаз (рис. 16.1.3, б) по уравнению материального баланса
где: R, Э, N — масса соответственно рафината, экстракта, исходной смеси, кг.
По правилам рычага имеем

Изобразим линию равновесия в треугольной диаграмме. Примем условие, согласно которому распределяемое вещество М неограниченно растворяется в обеих жидких фазах L и Е, а сами растворители имеют ограниченную растворимость друг в друге (рис. 16.1.4).
Рис. 16.1.4. Линия равновесия в треугольной диаграмме
Составы однородных двухкомпонентных растворов М и L и М и Е характеризуются точками на сторонах диаграммы LM и ЕМ. Растворители L и Е образуют однородные растворы только на небольших участках LR и ЭЕ. Смесь растворителей на участке RЭ расслаивается на два однородных двухкомпонентных насыщенных раствора R (насыщенный раствор Е в L) и Э (насыщенный раствор L в Е). Причем количество насыщенных растворов в каждом из двух слоев определяется положением точки N и находится по правилу рычага [(см. уравнение (16.1.2)].
При добавлении вещества М в смесь состава N образуется тройная смесь состава, характеризуемого точкой N1 лежащей на прямой NM. Смесь состава 

Бинодальная кривая на треугольной диаграмме разграничивает области, соответствующие двухфазным смесям (под бинодальной кривой) и однофазным растворам (вне бинодальной кривой).
Приведенная на рис. 16.1.4 диаграмма равновесия составлена для постоянной температуры и называется изотермой.
На практике приходится иметь дело с компонентами, обладающими частичной растворимостью в определенных интервалах концентраций. Соответственно поведению компонентов треугольные диаграммы бывают с двумя и тремя зонами ограниченной растворимости.
На равновесие системы влияет также температура. Взаимная растворимость компонентов, как правило, с повышением температуры увеличивается, следовательно, область существования гетерогенных систем уменьшается. С увеличением температуры бинодальная кривая на рис. 16.1.4 будет приближаться к оси LE, при этом площадь под линией RKЭ будет уменьшаться.
16.1.3. МАССОПЕРЕДАЧА ПРИ ЭКСТРАКЦИИ
Кинетические закономерности процесса экстракции определяются основными законами массопередачи.
Для увеличения площади поверхности фазового контакта одну из фаз диспергируют в виде капель в другой сплошной фазе. Площадь поверхности фазового контакта определяется задержкой дисперсной фазы в экстракторе и средним поверхностно-объемным диаметром капель. Распределяемое вещество диффундирует из сплошной фазы к поверхности капель, а затем внутрь капли либо, наоборот, из капли через поверхность раздела фаз в сплошную фазу.
Массопередача внутри капель осуществляется молекулярной и конвективной диффузией. Конвекция внутри капель возникает за счет циркуляции жидкости. Форма и размер капель в процессе экстракции многократно меняются за счет диспергирования и коалесценции. При этом происходит обновление поверхности межфазного контакта.
Для описания массопередачи в процессах экстракции пользуются вторым законом Фика.
В общем случае, когда диффузионным сопротивлением в сплошной и дисперсной фазах пренебречь нельзя, коэффициент массопередачи определяется выражениями



где: 

В случае, если диффузионное сопротивление сосредоточено в сплошной фазе, из уравнений (16.1.3) и (16.1.4) получим 
В случае, если основное диффузионное сопротивление сосредоточено в дисперсной фазе, т. е. внутри капель, 

Коэффициенты массоотдачи в фазах рассчитывают по критериальным уравнениям, которые получают на основании экспериментальных данных. Критериальные уравнения приводятся ниже при описании конструкций экстракторов.
Среднюю движущую силу рассчитывают с учетом фактора масштабного перехода с введением в расчетные уравнения его значения.
16.1.4. СХЕМЫ И РАСЧЕТ ПРОЦЕССОВ ЭКСТРАКЦИИ
В промышленности используют периодическую или непрерывную экстракцию по следующим схемам: одноступенчатой, многоступенчатой противоточной и многоступенчатой с перекрестным током экстрагента.
Одноступенчатая экстракция применяется в тех случаях, когда высок коэффициент разделения. Она может осуществляться периодическим и непрерывным способами по схеме, приведенной на рис. 16.1.5,а. В аппарат — смеситель загружают исходный раствор F в количестве L кг растворителя концентрацией Хн и экстрагент Е, которые перемешиваются мешалкой, а затем разделяются на два слоя: экстракт Э и рафинат R.
Рис. 16.1.5. Схема одноступенчатой экстракции: (а) и изображение процесса в координатах у—х (б) и на треугольной диаграмме(в)
Для разделения эмульсии используются отстойники, для трудноразделимых эмульсий — сепараторы.
Материальный баланс по распределяемому веществу

Полагая, что у=φx и модуль экстракции m=E/L, получим концентрации рафината


При этом степень извлечения

где: ε – экстракционный фактор;
Рассмотрим процесс одноступенчатой экстракции на треугольной и прямоугольной диаграммах (рис. 16.1.5, б, в). При перемешивании исходного раствора с экстрагентом образуется тройная смесь, состав которой характеризует точка N, расположенная на линии смешения FE. После расслаивания этой смеси образуются экстракт и рафинат, составы которых определяются точками R и Э, лежащими на хорде равновесия, проходящей через точку N. Модуль экстрагента определяется по правилу рычага: E/F=FN/(EN)
Количество рафината R=

Состав рафината определяет точка RK, а экстракта — точка Эк на стороне треугольника LM.
Экстремальные значения модулей экстрагента определяют точки N1 и N2 на бинодальной кривой: и .
При взаимной нерастворимости исходного раствора и экстрагента на диаграмме у—х процесс экстракции изображается прямой линией АВ, для построения которой из точки хн проводят линию под углом 
Модуль экстрагента для получения рафината с заданной концентрацией хк
Чем больше модуль экстрагента, тем меньше тангенс угла наклона и концентрации экстрагируемого компонента в рафинате и экстракте: 

настои. Дайте общую краткую характеристику массообменных процессов и перечислите их
| Название | Дайте общую краткую характеристику массообменных процессов и перечислите их |
| Анкор | настои.docx |
| Дата | 16.01.2018 |
| Размер | 15.39 Mb. |
| Формат файла |  |
| Имя файла | настои.docx |
| Тип | Документы #14262 |
| страница | 3 из 5 |
| Подборка по базе: Практическое задание 1, Модуль 1. Введение в общую психологию. Ф, Практическое задание 1, Модуль 1. Введение в общую психологию.do, ПР 1, м.1. Введение в общую психологию.docx, Леонова А.В. Практическое задание 1, Модуль 1. Введение в общую , Практическое задание 1, Модуль 1. Введение в общую психологию.rt, Задание 1 физическая культура. Дайте определение следующим понят, Основы общей психологии Введение в общую психологию.docx, Основы общей психологии Введение в общую психологию.docx, Основы общей психологии Введение в общую психологию.docx, Основы общей психологии Введение в общую психологию.docx Стадии экстрагирования. Материальный баланс процесса экстракции. Процесс экстрагирования состоит из трех стадий:
3. Удаление и регенерация растворителя из каждой образовавшейся фазы. Оно может в зависимости от свойств веществ осуществляется дистилляцией, ректификацией, сушкой, сублимацией и т.д. Экстрагирование может осуществляться периодическим или непрерывным способами при противоточном или перекрестном движении фаз в аппаратах различных конструкций. Анализ процессов экстрагирования осуществляется с использованием треугольных диаграмм, т.к. всегда приходится иметь дело как минимум с тремя компонентами. Если принимать, что один из компонентов является полностью нерастворимым в другом, то такие процессы могут быть изображены в обычных прямоугольных координатах. При этом по оси X откладывают значение концентрации распределяемого между фазами вещества в одной фазе (начальной или исходном растворе и полученном рафинате), а по оси Y в другой фазе (исходном растворителе и полученном экстракте). Если участвующие в процессе экстракции фазы практически нерастворимы, то материальный баланс процесса описывается общим уравнением. При однократном взаимодействии фаз (периодическая экстракция) материальный баланс процесса по потокам принимает вид уравнения: где F, S-количества исходного paствоpa и экстрагента соответственно, кг. Е и R — количества полученного экстракта и paфинатa соответственно, кг. Уравнение материального баланса может быть использовано и для непрерывного процесса при условии, что все входящие в него величины выражаются в единицах расхода, например в кг/с. Для рассматриваемого случая уравнение рабочей линии процесса экстракции описывается общим для массообменных процессов уравнением. Поэтому для анализа и расчета процесса экстракции в условиях взаимной нерастворимости фаз можно использовать известный метод графического построения равновесной и рабочей линии на фазовой диаграмме у — х, с помощью которого определяют движущую силу процесса и высоту экстрактора (например, через ЧТТ или ЧЕП). Однако чаще участвующие в жидкостной экстракции фазы обладают частичной взаимной растворимостью. Поэтому количества потоков по высоте экстрактора будут изменяться, и на диаграмме у — х рабочая линия будет криволинейной. Поскольку в этом случае система является как минимум трехкомпонентной, то для анализа таких систем целесообразно воспользоваться треугольной диаграммой для построения не только равновесных, но и рабочих концентрационных зависимостей.
заполните таблицу:Экстракторы и .Основные способы экстрагирования
Процесс экстрагирования из твердого тела очень сложен, и, прежде всего потому, что он существенным образом зависит от структуры каркаса обрабатываемого материала, который к тому же может сильно изменяться в самом процессе избирательного многокомпонентного растворения. К тому же, исходным сырьем для процесса экстрагирования из твердого тела чаще всего являются продукты естественного происхождения, свойства которых не только плохо изучены, потому что чрезвычайно сложны, но и могут непредсказуемым образом меняться даже внутри одной партии сырья. В отличие от сравнительно хорошо изученного случая экстракции в системе жидкость-жидкость, математическое описание процесса экстрагирования из твердого тела в промышленных экстракционных установках еще не получено. Сегодня очень многие биологически активные вещества получают из природного сырья растительного или животного происхождения. Каждый третий лекарственный препарат, из имеющихся, в арсенале современной медицины — продукт растительного происхождения. Следует также отметить, что в терапии отдельных заболеваний препараты из растений занимают доминирующее положение. Так, на долю препаратов растительного происхождения приходится 80% маточных, 77% сердечных, 72—74% отхаркивающих, противоглистных, желудочных средств. Экстрагированием в системе твердое тело-жидкость получают многие биологически активные вещества животного происхождения: ферменты (трипсин, химотрипсин, дезоксирибонуклеаза, рибонуклеаза, гепарин), гормоны (тироксин, эстрогены, АКТГ, тиреоидин, кортин), витаминные препараты (камполон, антианемин, Битами Эй др.).
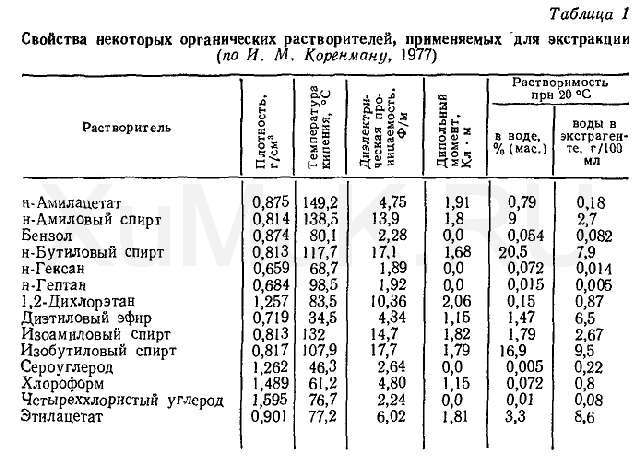
Под экстракцией, или экстрагированием, обычно понимают процесс жидкостной экстракции, заключающийся в извлечении вещества, растворенного в одном растворителе, с помощью другого растворителя, не смешивающегося с первым. В качестве двух таких жидких сред используются водный металлосодержащий раствор химических реагентов и органическая жидкость. Основными достоинствами процесса экстракции, по сравнению другими процессами разделения жидких смесей, являются: низкая рабочая температура (процесс, как правило, проводится при комнатной температуре); большая скорость массообмена между двумя контактирующими фазами (вследствие очень значительной площади их контакта при эмульгировании органической фазы в водном растворе); высокая селективность экстрагентов, позволяющая разделить родственные, трудноразделимые элементы; легкость разделения двух фаз (несмешивающиеся жидкости с разной плотностью); возможность регенерации затрачиваемых реагентов; возможность полной механизации и автоматизации процесса. Принята следующая терминология экстракции. Участвующие в процессе два растворителя (водный и органический) в исходном состоянии называются «исходный раствор» и «экстрагент». В момент контактирования (при экстракции) они называются «водной» и «органической» фазами, а после экстракции (отстаивания и разделения) — «рафинатом» и «экстрактом». Процесс экстракции состоит из следующих стадий: подготовка исходного раствора и экстрагента; контактирование этих растворов с эмульгированием органической и водной фаз; отстаивание и расслаивание этих фаз (хорошо наблюдаемое визуально); разделение рафината и экстракта. В простейшем случае экстракции (вода — растворитель — распределяющееся вещество) причиной изменения структуры водной фазы служат удаление из нее частиц экстрагируемого компонента и встраивание их в структуру органической фазы. Фактически жидкая двухфазная система, как и отдельно взятый раствор, представляет собой саморегулирующуюся систему. Преобразование структур в ней происходит не только путем перераспределения между фазами существующих частиц, но и путем возникновения новых частиц. Благодаря структурно-энергетическому различию водной и органической фаз при экстракции запускается процесс выравнивания значений свободной энергии этих фаз. Выравнивание идет в ходе преобразования структур — процесса, в котором принимают участие частицы экстрагируемого вещества. Органическая и водная фазы потребляют их в разных количествах, определяя тем самым константу распределения для одной формы вещества или коэффициент распределения для всех форм извлекающегося вещества. Следовательно, коэффициент распределения, строго говоря, не может быть постоянной величиной.
В качестве экстрагентов применяются органические соединения. Идеальный экстрагент должен отличаться следующими свойствами: быть достаточно селективным (то есть избирательно извлекать из водных растворов, содержащих сумму металлов, только интересующие нас компоненты); обладать высокой экстракционной способностью (поглощать в единице своего объема значительное количество экстрагируемого компонента); обеспечивать достаточно легко осуществимую регенерацию экстрагента с извлечением металла из органической фазы; быть безопасным при работе (не токсичным, не летучим, не воспламеняться); сохранять устойчивость во время хранения или при контакте с кислотами и щелочами; быть достаточно дешевым. Найти такой идеальный экстрагент почти невозможно, поэтому обычно принимается компромиссное решение. С учетом того, что в механизме экстракционного разделения важную роль играет массоперенос, одним из главных физических свойств органической фазы является вязкость. Знание характеристик вязкости, энергии межфазной границы, плотности сред крайне необходимо для суждения о кинетике процесса экстракции не только в смысле массопереноса, но и с точки зрения диспергирования фаз и скорости отстаивания приведенных в равновесие жидких фаз. Кроме того, для хорошего расслаивания фаз после экстракции надо иметь достаточную разность в плотностях этих фаз, то есть экстрагент должен быть значительно легче водного раствора. Поэтому на практике экстрагент редко используют в чистом виде; его обычно разбавляют дешевым органическим растворителем, чтобы снизить вязкость и плотность. Этот вспомогательный растворитель, как правило, является инертным и не участвует в процессе экстракции. В такой системе из двух органических растворителей органическое соединение, участвующее в химических реакциях экстракции, называется экстракционным реагентом, а растворитель экстракционного реагента называется разбавителем. Весь же органический раствор — это экстрагент. Следует заметить, что разбавитель применяется не только для снижения вязкости и плотности органической фазы, но и для растворения образующихся продуктов при экстракционной реакции. Наиболее широко применяются следующие типы органических растворителей: углеводороды и их галоидопроизводные; Главной характеристикой любого экстракционного процесса, является коэффициент распределения (D). Коэффициент распределения определяется отношением концентрации экстрагирующегося вещества в органической фазе к концентрации вещества в водной фазе после того, как наступило равновесие, т.е.
Для того чтобы понять, какая часть вещества перешла в органическую фазу, следует пользоваться другой характеристикой — коэффициентом извлечения (α), который является той долей вещества, что перешла в органическую фазу. Существует связь между коэффициентом распределения и коэффициентом извлечения:
где Vводн — объем водной фазы; Vорг — объем органической фазы. Из формулы видно, что чем больше объем органической фазы, тем больше коэффициент извлечения, т.е. тем больше вещества переходит в органическую фазу. Коэффициент извлечения является важным аналитическим параметром, так как всегда важно знать при разработке аналитической методики полноту извлечения определяемого вещества. § 1. МЕТОД ЭКСТРАКЦИИВ современном химико-токсикологическом анализе метод экстракции широко используется для изолирования токсических веществ из объектов биологического происхождения, для очистки вытяжек из биологического материала от примесей, для выделения токсических веществ из предварительно очищенных вытяжек. Этот метод применяется для обнаружения токсических веществ при помощи некоторых качественных реакций, для количественного определения этих веществ экстракционно-фото-метрическими методами, для концентрирования исследуемых веществ, находящихся в сильно разбавленных растворах, и для ряда других целей. Экстракция — процесс извлечения растворителями соответствующих веществ из различных объектов. Объекты, из которых извлекают соответствующие соединения, могут быть твердыми веществами и жидкостями. Поэтому процессы извлечения подразделяют на экстракцию в системе твердое тело — жидкость и на экстракцию в системе жидкость — жидкость (жидкостную экстракцию). Для экстракции веществ в системе твердое тело — жидкость в качестве экстрагентов применяют органические растворители. Извлечение соответствующих веществ из твердых тел водой называется выщелачиванием. В химико-токсикологическом анализе метод экстракции в системе твердое тело — жидкость и метод выщелачивания применяются для изолирования исследуемых веществ (целевых компонентов) из органов трупов, растений, почвы и других объектов. Процесс экстракции (выщелачивания) целевых компонентов из биологического материала является многостадийным. Основными стадиями этого процесса являются: проникновение экстра-гента в клетки и ткани трупного материала и в другие объекты, в которых находится исследуемое вещество, растворение целевого компонента в экстрагенте или взаимодействие целевого компонента с экстрагентом в клетках и тканях биологического материала, перенос растворенного целевого компонента через оболочки клеток в межклеточное пространство и смешивание извлеченных из клеток веществ с основной массой экстрагента. Степень изолирования исследуемых веществ из биологического материала зависит от растворимости извлекаемых веществ в экстрагенте, структуры (пористости) биологического материала, проникающей способности экстрагентов в клетки и ткани биологического материала, степени его измельчения, интенсивности перемешивания смеси измельченного биологического материала и экстрагента, кратности настаивания биологического материала с экстрагеитом, температуры, рН среды и ряда других факторов. Влияние отдельных перечисленных выше факторов на изолирование токсических веществ из биологического материала приводится ниже (см. гл. V, § 2—4). Жидкостная экстракция — процесс распределения растворенного вещества между двумя несмешивающимися жидкими фазами, одной из которых в большинстве случаев является вода, а второй — несмешивающийся с водой органический растворитель. Извлечение вещества из фазы органического растворителя в водную фазу называется реэкстρакцией. Некоторыми преимуществами метода экстракции объясняется широкое применение его не только в токсикологической химии, но и в химической технологии, фармации, биохимии и т. д. При использовании методов экстракции отсутствует химическое превращение разделяемых веществ и не образуются побочные продукты. Вещества, выделенные с помощью метода экстракции, как правило, не содержат примесей, связанных с процессами адсорбции и окклюзии. Этот метод оправдывает себя при разделении термолабильных веществ. Использование метода экстракции для концентрирования позволяет переводить вещества из сильно разбавленных растворов в небольшой объем органического растворителя. Переход экстрагируемого вещества из одного растворителя в другой происходит в результате разности концентраций и неодинаковой растворимости этого вещества в обоих растворителях. Этот процесс происходит до тех пор, пока не наступит равновесие концентраций извлекаемого вещества в одном и другом растворителях. Исследования показали, что экстрагируемость химических соединений зависит от растворимости их в воде и в несмешивающихся с водой органических растворителях, применяемых для экстракции. Подтверждением этого является то, что коэффициент распределения некоторых веществ приблизительно равен отношению их растворимостей в органическом растворителе и в воде. Органические растворители, которые применяются для экстракции органических соединений, оказались непригодными для экстракции большого числа неорганических соединений. Поэтому сделаны попытки найти подходящие экстрагенты для извлечения неорганических соединений из водных растворов. Проведенные исследования показали, что для экстракции неорганических соединений в качестве экстрагентов с успехом могут быть использованы некоторые карбоновые и сульфоновые кислоты, отдельные фосфорорганические соединения, высокомолекулярные амины, соли четвертичных аммониевых оснований и др. Эти вещества при экстракции взаимодействуют с неорганическими соединениями и их ионами. Кроме перечисленных соединений в качестве экстрагентов для ионов металлов предложены так называемые хелатирующие агенты (вещества, растворы которых с ионами металлов образуют хелаты). К числу хелатирующих агентов относятся; купферон, 8-оксихинолин, дитизон, дитиокар-баматы и др. В связи с применением перечисленных выше веществ для экстракции неорганических соединений и их ионов изменилось представление об экстрагентах. В настоящее время под экстрагентом понимают органический растворитель (содержащий или не содержащий другие компоненты), который извлекает вещество из водной фазы. Составная часть экстрагента, химически взаимодействующая с извлекаемым веществом, называется реа гентом. В зависимости от состава и свойств экстрагентов экстракционные системы подразделяются на две группы. К первой группе относятся экстракционные системы с так называемым «физическим» распределением компонентов. В этих системах отсутствует химическое взаимодействие между экстрагентом (органическим растворителем) и экстрагируемыми веществами. Различная растворимость некоторых веществ, а следовательно, и неодинаковая экстрагируемость их объясняются физическими свойствами этих веществ и экстрагеитов (дипольный момент, диэлектрическая проницаемость и др.). Свойства некоторых органических растворителей, применяемых в качестве экстрагентов, приведены в табл. 1. Ко второй группе относятся экстракционные системы, в которых экстракция осуществляется за счет химического взаимодействия извлекаемых веществ с экстрагентами. Эффективность разделения веществ в таких системах зависит от прочности образующихся соединений или комплексов. Эти экстракционные системы используются для извлечения неорганических веществ. Экстракция с помощью экстрагентов, взаимодействующих с экстрагируемыми веществами, является более сложным процессом, чем экстракция, основанная на физическом распределении. При использовании экстрагентов, взаимодействующих с экстрагируемыми веществами, процессы экстракции могут осложняться побочными реакциями. В ряде случаев одновременно может происходить экстракция нескольких различных соединений. Основные количественные характеристики процессов экстракции Несмотря на то что экстракция как метод разделения длительное время применяется в аналитической химии и химической технологии, теоретические основы этого метода долгое время оставались неизученными. В частности, долгое время оставались неизученными основные количественные характеристики экстракционных процессов, что было определенным препятствием для широкого внедрения экстракции в практику. Для расчета количества вещества, которое экстрагируется органическими растворителями, необходимо знать константу и коэффициент распределения, степень экстракции и т. д. М. Бертло и Ю. Юнгфлейш были первыми исследователями, которые в 1872 г. на основании экспериментальных данных показали, что отношение равновесных концентраций вещества, распределяющегося между двумя жидкими фазами, является постоянным. Это отношение термодинамическим путем было выведено В. Нернстом, который в 1891 г. сформулировал закон распределения. Согласно закону распределения, вещество, растворенное в двух несмешивающихся или ограниченно смешивающихся жидкостях, распределяется между ними в постоянном отношении. Это отношение для идеальных систем зависит только от температуры, природы вещества и не зависит от концентрации. Из этого закона следует, что при одновременном растворении нескольких веществ каждое из них распределяется между обеими жидкими фазами таким образом, как будто в системе нет никаких других веществ, подлежащих распределению. Закон распределения справедлив лишь в том случае, если распределяемое вещество в обеих фазах находится в одной и той же форме. Константа распределения вещества. Постоянная величина, выражающая отношение концентраций распределяемого вещества, находящегося в обеих фазах (после наступления равновесия) в одной и той же форме, называется константой распределения: где Р о — константа распределения: [А] о —концентрация вещества в фазе органического растворителя, моль/л; [А] В — концентрация вещества в водной фазе, моль/л. Величина константы распределения зависит от природы распределяемого вещества, состава и свойств применяемого экстрагента, температуры, при которой производится экстракция. Эта константа не зависит от равновесных концентраций экстрагируемого вещества и объемов водной и неводной фаз. Числовое значение константы распределения можно вычислить и по другой формуле (9), исходя из величины степени экстракции соответствующего вещества и объемов жидких фаз. Коэффициент распределения. При расчетах константы распределения вещества по формуле (1) необходимо быть уверенным в том, что распределяемое вещество в обеих фазах находится в одинаковой форме (в одинаковом молекулярном состоянии). Однако во многих экстракционных системах не соблюдается указанное выше условие. В одной из жидких фаз могут происходить диссоциация, ассоциация, сольватация, гидролиз распределяемого вещества, образование комплексов и т. д. Для расчетов экстракционных равновесий в таких системах не принимают во внимание форму существования вещества в каждой фазе, а учитывают только отношение суммарных (аналитических) концентраций распределяемого вещества в обеих фазах. На основании определения суммарных концентраций можно рассчитать не константу, а коэффициент распределения данною вещества в применяемой системе растворителей (вода — органический растворитель). Коэффициент распределения — это отношение суммарной аналитической концентрации вещества в фазе органического растворителя к суммарной аналитической концентрации этого вещества в водной фазе (без учета того, в какой форме находится вещество в каждой фазе): где D — коэффициент распределения; С о — суммарная аналитическая концентрация вещества в фазе органического растворителя, моль/л; С В — суммарная аналитическая концентрация вещества в водной фазе, моль/л. Степень экстракции. Степень экстракции (процент экстракции) — это отношение количества экстрагированного вещества к общему (начальному) количеству этого вещества в водном растворе: где R — степень экстракции вещества, %; А — количество вещества, которое экстрагировалось органическим растворителем; N — общее (начальное) количество вещества в водном растворе. Количество вещества А, которое экстрагируется органическим растворителем, можно определить экспериментальным путем, применив соответствующий метод количественного определения. Зная начальное количество вещества и количество этого вещества, перешедшего в органический растворитель, рассчитывают степень экстракции. Степень экстракции вещества можно определить не только экспериментальным путем, но и путем соответствующих расчетов, зная константу или коэффициент распределения вещества, а также отношение объемов водной фазы и фазы органического растворителя. Степень экстракции с указанными величинами связана следующим соотношением: где R —степень экстракции; Р о — константа распределения; V B — объем водной фазы, мл; V o — объем фазы органического растворителя, мл. В формуле (4) отношение объема водной фазы к объему фазы органического растворителя заменяют величиной г: Объем органического растворителя, необходимого для экстракции, рассчитывают по формуле После соответствующего преобразования формулы (4) степень экстракции рассчитывают по уравнению Из формулы (7) можно рассчитать величину r: Если известна степень экстракции R и отношение объемов фаз r , то константу распределения Р 0 можно рассчитать при помощи следующего уравнения: На основании числовых значений константы распределения и степени экстракции можно рассчитать ряд других количественных характеристик процессов экстракции. Ниже мы приведем несколько примеров расчетов ряда количественных характеристик экстракционных процессов неэлектролитов, к числу которых относятся многие органические соединения, имеющие значение в фармации и токсикологии. Расчет объема органического растворителя, необходимого для однократной экстракции. Примеры этих расчетов приведены ниже. Пример 1. Вычислить объем органического растворителя, который необходимо взять для однократной экстракции 99 % вещества из 100 мл раствора, если константа распределения Р 0 этого вещества между органическим растворителем и водной фазой равна 20. Для решения этой задачи пользуются формулой (7): Значение r рассчитывают по формуле (8), а значение V o — по формуле (6): Таким образом, для однократной экстракции 99 % вещества (Р о =20) из 100 мл водного раствора требуется 500 мл органического растворителя. Пример 2. Какой объем органического растворителя необходимо взять для однократной экстракции 99 % вещества из 100 мл водного раствора, если Ρ = 10? Эту задачу решают аналогично предыдущей: Расчеты показывают, что для однократной экстракции 99 % вещества (Р о = 10) из 100 мл водного раствора требуется 1000 мл органического растворителя. На основании произведенных выше расчетов (см. примеры 1 и 2) можно сделать такие выводы: чем больше константа распределения Р о вещества, тем меньший объем органического растворителя требуется для однократной экстракции его из водных растворов; степень экстракции R вещества тем больше, чем меньше величина r, т. е. чем больший объем органического растворителя применяется для однократной экстракции. Расчет объема органического растворителя для многократной экстракции. Из приведенных выше расчетов (см. примеры 1 и 2) следует, что для однократной экстракции вещества из водных растворов необходимо брать органические растворители, объемы которых значительно больше объемов водных растворов. Учитывая это, для извлечения веществ из водных растворов производят многократную экстракцию их малыми объемами органических растворителей вместо однократной экстракции большим объемом того же растворителя. Преимущество многократной экстракции веществ малыми объемами растворителей перед однократной экстракцией большими объемами этих растворителей показано на приведенных ниже примерах. Пример 3. Какой общий объем органического растворителя необходимо использовать для многократной экстракции, чтобы из 100 мл водного раствора извлечь 99 % вещества, если Р о = 20, а на каждую экстракцию берут по 25 мл органического растворителя? Для решения этой задачи пользуются формулой (7). Вначале определяют степень экстракции вещества, %: Расчеты показывают, что степень экстракции вещества при указанных выше условиях составляет 83 %. Следовательно, и при каждой последующей экстракции тоже будет экстрагироваться 83 % от оставшегося в водном растворе вещества. При второй экстракции из водного раствора будет извлекаться Χ 2 вещества: При третьей экстракции из водного раствора будет извлекаться Х 3 вещества: Эти расчеты показывают, что при трех последовательных экстракциях из водного раствора извлекается около 99,5 % вещества и при этом расходуется только 75 мл органического растворителя, в то время как для однократной экстракции 99 % того же вещества (см. пример 1) необходимо затратить 500 мл органического растворителя. Приведенные выше расчеты показывают, что для извлечения вещества из водных растворов необходимо производить многократную экстракцию небольшими объемами органических растворителей вместо однократной экстракции большим объемом этих растворителей. Количество экстракций, необходимых для извлечения заданного количества вещества из раствора. Для расчета полноты экстракции вещества определяют, сколько раз необходимо экстрагировать его из водного раствора, чтобы добиться извлечения заданного количества этого вещества. С этой целью пользуются следующей формулой: где т — количество экстракций, необходимых для извлечения заданного количества вещества; С В — начальная концентрация вещества в водном растворе, моль/л; [Ат] В — концентрация оставшегося в водной фазе вещества после т экстракций, моль/л. Пример 4. Рассчитать число экстракций, необходимых для извлечения 99 % вещества органическим растворителем (порциями по 10 мл) из 100 мл 1 Μ водного раствора, если Р о =20. Для решения этой задачи вначале необходимо определить [Am] в и r: Подставим значения соответствующих величин в формулу (10). Приведенный пример показывает зависимость числа экстракций от объемов органического растворителя и водной фазы, степени экстракции и константы распределения вещества. Механизм процесса экстракции. Согласно теории растворов, растворение вещества в воде или в органических растворителях сопровождается образованием малопрочных соединений молекул этого вещества с молекулами растворителя. Если растворителем является вода, то в растворе образуются гидраты, а если растворителем является органический растворитель, то в растворах образуются сольваты молекул растворенного вещества. Гидраты и сольваты молекул являются малопрочными. При взбалтывании водного раствора вещества с органическим растворителем, который не смешивается с водой, гидратная оболочка молекул растворенного вещества разрушается. Молекулы воды в гидратной оболочке замещаются молекулами органического растворителя, в результате чего образуются сольваты молекул растворенного вещества, которые легко переходят в органический растворитель. Хорошо экстрагируются молекулы тех веществ, сольваты которых в фазе органического растворителя являются более прочными, чем гидраты этих молекул в воде. Более сложными являются процессы экстракции электролитов, которые в водных растворах частично или полностью распадаются на ионы. Ионы, несущие определенный заряд, хорошо гидратируются диполями воды. Связь ионов с диполями воды относительно прочная. Поэтому ионы, имеющие прочные гидрат-ные оболочки, остаются в водной фазе и не экстрагируются органическими растворителями. Ими могут экстрагироваться только недиссоциированные молекулы соответствующего вещества. Это необходимо учитывать при экстракции органических веществ, являющихся слабыми электролитами. Степень экстракции этих веществ зависит от рН среды. С изменением рН раствора изменяется степень диссоциации молекул, а следовательно, изменяется и относительное количество недиссоциированных молекул вещества. С увеличением количества недиссоциированных молекул увеличивается степень экстракции слабых электролитов и наоборот. Экстракция органических кислот. Недиссоциированные молекулы органических кислот в водных растворах являются электронейтральными и слабо гидратируются молекулами воды. При контакте водных растворов с органическими растворителями электронейтральные молекулы кислоты легко сольватируются, и поэтому переходят в слой органического растворителя. Ионы, образующиеся в водных растворах при диссоциации слабых кислот, имеют соответствующие заряды, и поэтому легко гидратируются диполями воды. Связь молекул воды с ионами кислоты относительно прочная. Поэтому такие ионы слабо сольватируются молекулами органических растворителей и не экстрагируются органическими растворителями из водных растворов. Изменение концентрации водородных ионов в водной фазе приводит к относительному увеличению или уменьшению количества недиссоциированных молекул, а следовательно, и к изменению экстрагируемости кислоты. С повышением рН (т. е. с уменьшением концентрации водородных ионов в водном растворе) увеличивается диссоциация кислоты в растворе, что приводит к уменьшению ее недиссоциированных молекул. В результате этого понижается экстрагируе-мость слабой кислоты органическими растворителями из таких растворов. При повышении концентрации водородных ионов (т. е. с понижением рН) в водном растворе увеличивается число молекул недиссоциированной кислоты, а следовательно, возрастает ее экстрагируемость органическими растворителями. При значительном повышении концентрации водородных ионов в водном растворе слабую кислоту практически полностью можно перевести в недиссоциированное состояние и этим повысить ее экстрагируемость. Экстракция оснований. Многие органические основания, к числу которых относятся алкалоиды и их многочисленные синтетические аналоги, являются фармацевтическими препаратами. Эти основания в нейтральной среде находятся в недиссоциированном состоянии. При действии кислот на органические основания образуются их соли, которые в водных растворах диссоциируют на ионы. Недиссоциированные молекулы органических оснований слабо гидратируются молекулами воды, но хорошо сольватируются молекулами органических растворителей. Поэтому недиссоциированные молекулы органических оснований хорошо экстрагируются из водных растворов органическими растворителями. Ионы, образующиеся при диссоциации солей органических оснований, хорошо гидратируются молекулами воды и слабо сольватируются молекулами органических растворителей. Поэтому соли органических оснований (за небольшим исключением) не экстрагируются органическими растворителями. Органические основания являются слабыми электролитами. Степень диссоциации их зависит от рН среды. От прибавления кислот к органическим основаниям они переходят в соли. При этом увеличивается количество ионов и уменьшается количество недиссоциированных молекул, а следовательно, уменьшается степень экстракции этих веществ органическими растворителями. От прибавления щелочей к солям органических оснований уменьшается количество ионов и увеличивается количество недиссоциированных молекул этих оснований. В результате этого в щелочной среде увеличивается степень экстракции органических оснований. Экстракция амфотерных соединений. К числу амфотерных соединений, имеющих токсикологическое значение, относятся вещества, в молекулах которых содержится аминный азот и фенольные группы (морфин, сальсолин и др.), а также соединения, содержащие аминный азот и карбоксильную группу (аминокислоты и др.). Эти соединения в зависимости от рН среды диссоциируют как основания (в кислой среде) и как кислоты (в щелочной среде). Экстракция амфотерных соединений зависит от рН среды, так как при изменении рН изменяется количество ионов и недиссоциированных молекул амфотерных соединений. Амфотерные соединения, находящиеся в молекулярном состоянии, экстрагируются органическими растворителями. Ионы амфотерных соединений хорошо гидратируются молекулами воды и почти не экстрагируются органическими растворителями. Наибольшие количества амфотерных соединений экстрагируются при рН, соответствующем изоэлектрической точке этих веществ. Это объясняется тем, что в изоэлектрической точке молекулы амфотерных соединений не имеют электрического заряда. Влияние различных факторов на экстракцию На экстракцию веществ органическими растворителями оказывают влияние различные факторы (природа экстрагируемого вещества, природа экстрагента, температура, рН среды, присутствие электролитов в водных растворах, скорость взбалтывания и др.). Влияние температуры на экстракцию. Изменение температуры влияет на константу распределения экстрагируемого вещества. Это объясняется тем, что при изменении температуры изменяется растворимость экстрагируемых веществ в каждой фазе, а также изменяется взаимная растворимость органической и водной фаз. Причем с изменением температуры растворимость вещества в каждой фазе изменяется неодинаково. Это является одной из причин изменения константы распределения вещества при изменении температуры. При изменении температуры может изменяться диссоциация и ассоциация вещества в соответствующей фазе. Поэтому при изменении температуры изменяется гидратация (сольватация) и экстрагируемость химических соединений. Влияние рН среды на экстракцию. Экстрагируемость органических веществ зависит от ряда факторов, в том числе и от рН среды. Количество экстрагированного вещества зависит от диссоциации его в водной фазе. Это связано с тем, что недиссоциированные молекулы вещества и его ионы неодинаково экстрагируются органическими растворителями из водных растворов. При экстракции недиссоциированные молекулы переходят в органическую фазу, а ионы, которые хорошо гидратированы молекулами воды, остаются в водной фазе. Поэтому сильные электролиты, хорошо диссоциирующие в воде на ионы, не экстрагируются органическими растворителями. Влияние электролитов на экстракцию. Прибавление хорошо растворимых солей к водному раствору другого вещества может понижать или повышать его растворимость в воде. Понижение растворимости веществ в водных растворах под влиянием электролитов называется высаливанием, а повышение растворимости — всаливанием. Высаливание является фактором, понижающим растворимость веществ в воде и повышающим их экстрагируемость органическими растворителями из водных растворов. Высаливающее действие электролитов зависит от природы и свойств высаливаемого вещества, от природы и свойств высаливателя, концентрации и радиуса ионов высаливателя и т. д. Ионы высаливателя с малым радиусом имеют большую плотность заряда, чем ионы с большим радиусом. Поэтому ионы с малым радиусом гидратируются лучше, чем ионы с большим радиусом. В связи с этим высаливающее действие ионов с малым радиусом большее, чем высаливающее действие крупных ионов. Однако это правило имеет и ряд исключений. Установлено, что высаливающим действием обладают и некоторые хорошо растворимые в воде неэлектролиты. Так, например, этиловый спирт хорошо высаливает уксусную кислоту из ее водных растворов при экстракции этой кислоты этилацетатом и т. д. Вещества, проявляющие свойства всаливателей, применяются для повышения растворимости слаборастворимых веществ в воде. Известно несколько теорий, объясняющих процесс всаливания. Согласно одной из них, всаливание объясняется химическим взаимодействием всаливателей и всаливающихся веществ в экстракционных системах. В результате этого могут образовываться соединения или комплексы, хорошо растворимые в воде, которые не экстрагируются органическими растворителями. Требования, предъявляемые к органическим растворителям для экстракции. К органическим растворителям, применяемым для экстракции, предъявляется ряд требований. 1. Органический растворитель должен хорошо извлекать исследуемое вещество из водной фазы. 2. Желательно, чтобы применяемый растворитель был избирательным или селективным. Он должен извлекать из растворов только одно вещество или группу родственных соединений. 3. Растворитель должен иметь незначительную растворимость в воде, а вода не должна заметно растворяться в этом растворителе. При использовании для экстракции органических растворителей, растворяющихся в воде или растворяющих воду, конечные объемы фаз после взбалтывания не будут равны начальным объемам этих фаз. Это может быть источником ошибок при расчетах константы и коэффициента распределения, а также при вычислении степени экстракции. Чтобы исключить возможные ошибки при расчетах, органический растворитель насыщают водой, а воду — органическим растворителем. Только после этого производят экстракцию. 4. Органический растворитель по возможности не должен быть низкокипящим. Температура кипения растворителя должна быть выше 50 °С. Низкокипящие органические растворители даже при комнатной температуре быстро улетучиваются. Поэтому при экстракции их объемы уменьшаются, а концентрация экстрагированных веществ в этих растворителях увеличивается. Это может быть одним из источников ошибок при расчетах константы или коэффициента распределения экстрагируемого вещества. Однако низкая температура кипения органических растворителей является положительным фактором с точки зрения регенерации их после экстракции. 5. Плотность органических растворителей по возможности должна отличаться от плотности воды и водных растворов. При большой разности плотностей указанных жидкостей разделение фаз происходит быстро. 6. Растворители не должны быть огнеопасными или ядовитыми. Есть и некоторые другие требования, предъявляемые к растворителям. источники: http://topuch.ru/dajte-obshuyu-kratkuyu-harakteristiku-massoobmennih-processov/index3.html http://xumuk.ru/toxicchem/34.html |