Материальный и тепловой балансы химического процесса (стр. 1 )
 | Из за большого объема этот материал размещен на нескольких страницах: 1 2 3 |
МАТЕРИАЛЬНЫЙ И ТЕПЛОВОЙ БАЛАНСЫ ХИМИЧЕСКОГО ПРОЦЕССА
Материальный и тепловой балансы химического процесса: составляются на основе законов сохранения массы и энергии.
Уравнения материального и теплового балансов служат основой расчета реакционного объема аппарата (при заданной степени превращения) или степени превращения в реакторе (при заданных условиях). При расчете чаще всего пользуются выражением общего баланса, составленного по одному из исходных веществ, участвующих в химическом процессе. Вид уравнения зависит от типа реактора, в котором протекает процесс химического превращения веществ. Материальный баланс представляет собой основу для вывода зависимости связи между степенью превращения, скоростью и временем химического процесса, которая является необходимым элементом его расчета и носит название характеристического уравнения реактора. Если химическое превращение вещества протекает в неизотермических условиях, тепловой баланс процесса следует рассматривать совместно с его материальным балансом.
1. Общий материальный баланс реакционной системы равен сумме материальных балансов по каждому из реагирующих веществ:
где М — общее количество реакционной смеси, кмоль; t — время реакции, с;. D Мобщ — изменение общего количества реакционной смеси, кмоль×с-1.
2. Общее уравнение материального баланса для i-ro вещества, участвующего в реакции:
где Mi — количество i-го вещества в системе, кмоль; DMi — изменение количества i-го вещества, кмоль×с-1; ri —скорость химической реакции, выраженная по i-му веществу, кмоль×м-3×с-1; V — реакционный объем, м3.
3. Уравнения материального баланса для различных типов. химических реакторов.
Периодически действующий реактор идеального смешения:
где Ci — концентрация i-го вещества в системе, кмоль×м-3.
Непрерывнодействующий реактор идеального смешения:

где 

Каскад n непрерывнодействующих реакторов идеального смешения:

.где ,- концентрация i-ro вещества в системе на выходе из п-го реактора, кмоль×м-3; rin —скорость реакции по i-му веществу в n-м реакторе, кмоль×м-3×с-1
Непрерывнодействующий реактор идеального вытеснения:
где S — площадь поперечного сечения потока реагирующей системы, м2; L — длина реактора, м.
Полунепрерывнодействующий реактор идеального смешения:
По i-му веществу для этого реактора имеем:
где 


4. Общий вид уравнения теплового баланса:
где U — внутренняя энергия реакционной системы, кДж-кмоль»1; / — энтальпия системы, кДж×кмоль-1; . — коэффициент теплопередачи, Вт(м2×К)-1; F — площадь поверхности теплопередачи, м2; Тр — температура реакции, К или °С; Тх—температура теплоносителя (хладоагента), К или °С; р — давление в системе, Па.
5. Уравнения теплового баланса для различных типов химических реакторов.
Периодически действующий реактор идеального смешения при V = const:
где сu — удельная теплоемкость смеси реагирующих веществ при постоянном объеме, кДж(кмоль×К)-1; DHr — тепловой эффект реакции, кДж×кмоль-1.
Непрерывнодействующий реактор идеального смешения с внешним теплообменом:

где u0 — объемная скорость подачи реагирующих веществ, м3×с-1; Со — начальная концентрация реагирующих веществ, кмоль×м-3; х — степень превращения; То—начальная температура реакционной смеси, К или °С; Т1 — конечная температура реакционной смеси, К или °С; ср — удельная теплоемкость смеси реагирующих веществ при постоянном давлении, кДж(кг×К)-1
Непрерывнодействующий реактор идеального вытеснения с внешним теплообменом при постоянных температуре и составе по поперечному сечению потока:
где S — площадь поперечного сечения, м2; Rr — гидравлический радиус, м..
Непрерывнодействующий реактор идеального смешения, работающий в автотермическом режиме:
Адиабатический yепрерывнодействующий реактор идеального вытеснения с теплообменом между реагентом и продуктами реакции (система теплообменник — реактор):
где 
u0rcp(T0—
где 

Непрерывнодействующий реактор идеального вытеснения с внутренним теплообменом между исходными веществами и реакционной смесью (при подогреве исходных веществ):
где Ti— температура реакционной смеси во внутреннем подогревателе, К или °С.
Пример 2-1. В реакторе идеального смешения происходят следующие реакции:
где D — целевой продукт реакции; СRа = CSo = СТo = CDo = 0 — начальные концентрации промежуточных и конечных продуктов.
Начальная концентрация исходного вещества СА = 1 кмоль × м-3; текущие концентрации веществ (в кмоль × м-3); СА = 0,44; Св=1,06; СR = 0,05; CS = 0,33; СT = 0,14. Скорость подачи исходных веществ u0 = 5 × 10-3 м3 × с-1.
Определить производительность реактора GB по веществу В:
Решение. Составляем материальный баланс для реактора смешения. На основании стехиометрических соотношений реакций (а) и (г); (а) и (б); (а), (б), (в) и (г); (г) запишем:
CBo-CB = (3/2)CT + 2C’R+ C’S + CD, (3)
Комбинируя уравнения (1), (2), (4) и (5), а также (2) — (5), получаем:
CAo-CA = CR + CS + CD, (6)
CBo-CB=(3/2)CT + 2CR + 3CS-2CD. (7)
Из уравнения (6) определяем концентрацию продукта D:
CD = 1 — (0,44 + 0,05 + 0,33) = 0,18 кмоль × м-3.
Тогда производительность по продукту D будет равна:
Из уравнения (7) определяем концентрацию исходного вещества В
СВо= (3/2) 0,14 + 2 × 0,05 — 2 × 0,18+ 1,06 = 2 кмоль × м-3,
а затем производительность по веществу В:
Пример 2-2. В реакторе идеального смешения, работающем в адиабатических условиях, происходят реакции:
2R®S, (в)
где R — продукт реакции.
Начальные концентрации исходных веществ и продуктов (в кмоль × м-3): САо = 0,1; СВо=0,3; CRo = CDa = СРо =CSo = 0. Текущие концентрации взаимодействующих веществ (в кмоль х м-3): СА = 0,016; СР = 0,028; CS = 0,012; CD = 0,034.
Тепловой эффект реакции —DНr= 1,5 × 108 Дж (кмоль × В) -1. Плотность смеси r = 860 кг× м-3, теплоемкость смеси ср = = 2,85 × 103 Дж(кг×К)-1, скорость подачи u0 = 2,6×10-2×м3 ×с-1.
Определить производительность реактора по продукту R и температуру на выходе реактора, если начальная температура 12 °С (285 К).
Решение. Составляем уравнения материального и теплового баланса. Из стехиометрических соотношений уравнений реакции (а), (б) и (в) следует:
Тогда из уравнений (1) и (3) получим:
= 0,026 кмоль • м -3.
Из уравнений (2) и (3) находим:
СB = СВо — (СAо — СA) — 2СР = 0,30 — (0,1 —0,016) —2 • 0,028 =
= 0,160 кмоль • м -3.
Таким образом, производительность реактора по продукту R:
GR = CRu0 = 0,026 • 2,6 •10 -2 = 6,76•10 -4 кмоль • с -1.
где QP = (—DНr) (CBo —CB) u0 — тепловой поток, который выделяется в результате реакций; QH = cppu0 DT— тепловой поток, который затрачивается на нагревание реакционной смеси при адиабатических условиях работы реактора идеального смешения.
Из уравнения (4) после преобразования получаем:
Следовательно, температура на выходе из реактора равна 285 + 8,6 = 393,6 К или 20,6 °С.
Пример 2-3. В реакторе идеального вытеснения, работающем т адиабатических условиях, происходит жидкофазная реакция первого порядка
Константа скорости реакции kA (в с -1):
Начальные концентрации веществ (в кмоль×м-3): СAо=4,5; СB = 0. Тепловой эффект реакции—DHr=2×107 Дж(кмоль×А)-1, теплоемкость реакционной смеси ср:=2,2×103 Дж(кг×К)-1, плотность реакционной смеси r = 850 кг×м-3, температура исходной смеси Т0 = 300 К, скорость подачи uо= 10-3 м3 × с-1, объем реактора V = 5 м3.
Определить производительность реактора по продукту В и температуру смеси на выходе.
Решение. Тепловой баланс:
где QP = (—DHr) (СAо—CA) uо — тепловой поток, который выделяется в результате реакции; QH = срruо (Tк — Т0) — тепловой поток, который затрачивается на нагревание исходных веществ и продуктов реакции; Тк — температура реакционной смеси на выходе из реактора; Т0 — температура исходной смеси, подаваемой в реактор.
Характеристическое уравнение для необратимой реакции первого порядка, протекающей в реакторе идеального вытеснения:

Так как процесс протекает при адиабатических условиях, константа скорости реакции будет изменяться по ходу реакции. Используем метод конечных разностей:

где ki = 1013ехр(—1,2-104 Ti-1).
Для определения концентрации вещества А на выходе из реактора проводим последовательные приближения по Ti при шаге DT = 2 К. Тогда из уравнения материального баланса
определяем для каждого значения Тi соответствующее значение 


Тогда производительность реактора по продукту В:
= 1/2 (4,500 — 0,386) •= 2,06 •кмоль • с.
Пример 2-4. Установка состоит из следующих последовательно соединенных реакторов: идеального смешения (V1 = 2 м3), идеального вытеснения (V2 = 2 м3) и идеального смешения (V3 = 3 м3). Начальная концентрация вещества САo = = 1 кмоль • м -3, скорость подачи uо = 5×10-2 м3×с-1, скорость реакции (-rA) =5,1 • 10-3CA0,28. В начальный момент времени продукт в системе отсутствует. Плотность реакционной смеси не меняется.
Определить концентрацию исходного вещества после каждого реактора и рассчитать графически производительность установки по продукту, если известно, что 1 моль исходного вещества дает 2 моль продукта.
Решение. Составляем материальный баланс по веществу А для 1-го реактора смешения:
Для нахождения времени пребывания в реакторе идеального вытеснения интегрируем кинетическое уравнение:

Составляем материальный баланс по веществу А для 2-го реактора смешения:

Материальный и тепловой балансы реакторов
Читайте также:
|










 (58)
(58) – массовый расход
– массовый расход (59)
(59) – масса вещества А, вступившего в реакционном объеме в химическую реакцию в единицу времени;
– масса вещества А, вступившего в реакционном объеме в химическую реакцию в единицу времени; 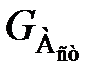 – сток вещества А – масса вещества А, выходящего из реакционного объема в единицу времени;
– сток вещества А – масса вещества А, выходящего из реакционного объема в единицу времени;  – накопление вещества А – масса вещества А, остающегося в реакционном объеме в неизменном виде в единицу времени.
– накопление вещества А – масса вещества А, остающегося в реакционном объеме в неизменном виде в единицу времени.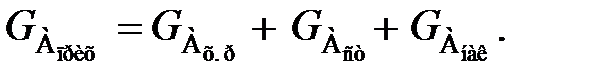 (60)
(60) и выходящего из него
и выходящего из него  – это масса вещества А, переносимого конвективным потоком
– это масса вещества А, переносимого конвективным потоком 
 (61)
(61) (62)
(62) (63)
(63) в уравнении баланса (62).
в уравнении баланса (62). (суммарный перенос вещества называют конвективным массообменном, или конвективной диффузией).
(суммарный перенос вещества называют конвективным массообменном, или конвективной диффузией).
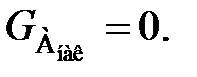



 (71)
(71) . (72)
. (72) . (73)
. (73) (74)
(74) (75)
(75) (1)
(1)
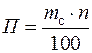
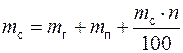 (2)
(2) (3)
(3)

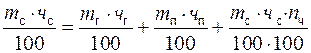
 (4)
(4)
 (5)
(5) (6)
(6) (7)
(7) (8)
(8)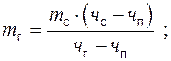 (9)
(9) (10)
(10) (11)
(11)

 чг На внутренних сторонах треугольника
чг На внутренних сторонах треугольника чс – чп располагают величину разности между массовыми долями составных частей молока (расположенными в вершинах треугольника), полученную вычитанием из большей величины меньшей.
чс – чп располагают величину разности между массовыми долями составных частей молока (расположенными в вершинах треугольника), полученную вычитанием из большей величины меньшей.