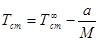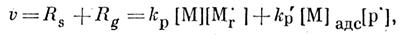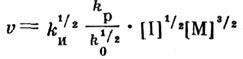Полимеризация акрилонитрила
На способность акрилонитрила к полимеризации впервые обратил внимание ван-дер-Бург. Позднее это свойство было изучено рядом авторов.
Абсолютно чистый акрилонитрил является устойчивым соединением. Он не изменяется даже при длительном нагревании до температуры 150—160° и не окисляется кислородом воздуха. С этим свойством связано то обстоятельство, что присутствие воздуха продлевает индукционный период полимеризации, инициированной перекисью. Не совсем чистый мономер полимеризуется уже в процессе хранения, а еще быстрее при нагревании. Быстрая полимеризация происходит либо под влиянием ультрафиолетового света, особенно в присутствии α-диоксосоединений, например диацетила, либо под влиянием соединений, которые разлагаются на радикалы по неполярному механизму. Из таких соединений в качестве инициаторов полимеризации были использованы полиалкилированные дифенилэтаны, неорганические и органические перекиси, N-нитрозоацетанилид и его производные, азоизобутиронитрил, фтороборат п-бромбензолдиазония и диазоаминобензол. Лучше всего изучена полимеризация, вызываемая перекисью дибензоила. Если эту реакцию проводят без разбавителя, то ее скорость зависит главным образом от количества катализатора и от температуры. С ростом температуры скорость полимеризации возрастает. При концентрации перекиси дибензоила 1% и температуре 30° полимеризация почти не протекает; при температуре 100° реакция заканчивается за 20 мин. Индукционный период весьма мал, однако интенсивность полимеризации резко падает по мере расхода инициатора. При полимеризации больших количеств остается до 40% непрореагировавшего мономера. При концентрации свыше 1% перекись дибензоила вызывает необычайно бурную полимеризацию, часто оканчивающуюся взрывом. В процессе полимеризации, инициированной перекисью дибензоила, всегда выделяется цианистый водород, образующийся, очевидно, в результате побочной реакции:
Если полимеризацию проводят в растворе, то индукционный период удлиняется и процесс протекает более гладко. Менее активными инициаторами являются перекись тетралина и диазоаминобензол. При использовании последнего скорость полимеризации гораздо меньше, но проходит она также более гладко, поскольку концентрация радикалов, образующихся неполярным разложением, хотя и ниже, но она поддерживается на постоянном уровне.
Механизм полимеризации акрилонитрила и строение полимера недостаточно ясны, хотя полиакрилонитрилу обычно и приписывают структуру:
Это следует из того, что при окислении полиакрилонитрила в полиакриловую кислоту путем нагревания с концентрированной щелочью количество выделяющегося аммиака, как правило, бывает меньше расчетного (94—95% от теоретического); по-видимому, какое-то количество нитрильных групп принимает участие в образовании линейной макромолекулы полимера.
Полимеризацию можно вызвать не только свободными радикалами, но также и основаниями, а лучше всего металлорганическими соединениями, например реактивами Гриньяра. Такая анионоидная полимеризация акрилонитрила ведет к образованию полимера с количественным выходом даже при температуре –10°. В противоположность этому акрилонитрил нельзя полимеризовать, действуя металлическим натрием даже при температуре 90°.
В результате полимеризации акрилонитрила, проводимой как в мономере, так и в обычных органических растворителях, всегда получают нерастворимый полимер независимо от условий. Полиакрилонитрил образует вязкие растворы только при растворении в диметилформамиде, тетраметилдиамиде щавелевой кислоты, 1,2-дицианэтане, диметилцианамиде и в растворах некоторых солей, особенно бромистого лития, роданистого натрия или хлористого цинка. Эти растворы применяют при производстве синтетического волокна, получившего название «орлон». Полиакрилонитрил представляет собой бесцветную или слегка желтоватую аморфную массу, легко растирающуюся в порошок. Средняя степень полимеризации составляет минимум 270, молекулярный вес обычных полимеров колеблется в широком интервале от 15 000 до 250 000. Полимер не термопластичен, при температуре 300—350° он частично превращается, не деполимеризуясь, с образованием летучих точно не идентифицированных основных соединений. При щелочном и кислом гидролизе полимер превращается в полиакриловую кислоту. По описанным свойствам полиакрилонитрил диаметрально противоположен полиметакрилонитрилу (см. ниже).
На практике полимеризацию проводят в растворе или, чаще всего, в водной эмульсии в присутствии эмульгаторов. Точно таким же образом получают смешанные полимеры акрилонитрила с мономерами, например со стиролом и его замещенными, с хлористым винилом, с винилацетатом, с эфирами акриловой кислоты и главным образом с бутадиеном. Акрилонитрил придает смешанным полимерам высокую стойкость по отношению к органическим жидкостям, особенно к бензину, маслам и др. Вследствие этого сополимеры акрилонитрила имеют большее значение, нежели сам полиакрилонитрил. Из них наиболее известным и самым распространенным является смешанный полимер акрилонитрила с бутадиеном под названием «пербунан» или «буна-Н». Сополимер с хлористым винилом известен под названием «винилон».
Реферат: Технология производства полиакрилонитрила
| Название: Технология производства полиакрилонитрила Раздел: Рефераты по химии Тип: реферат Добавлен 13:36:12 02 марта 2011 Похожие работы Просмотров: 5529 Комментариев: 20 Оценило: 3 человек Средний балл: 5 Оценка: неизвестно Скачать | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Свойство | Значение |
| Плотность, г/см 3 | 1,14–1,15 |
Показатель преломления, n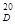 | 1,49–1,52 |
| Температура размягчения (с одновременной деструкцией), °С | 220–230 |
| Удельная теплоемкость, кДж/(кг*К) [кал/(г*°С)] | 1,51 |
| Прочность при растяжении (для волокна), Мн/м 2 (кгс/мм 2 ) | 600 (60) |
| Относительное удлинение, % | 10–35 |
| Влагопоглощение отпрессованного образца, % | 1–2 |
| Дипольный момент, к*м (D) | 1,13–10 -4 |
| Диэлектрическая проницаемость при | |
| 50 гц | 6,5 |
| 1 Мгц | 4,2 |
| Удельное объемное электрическое сопротивление, Том*м (Ом*см) | 1 (10 14 ) |
| Тангенс угла диэлектрических потерь при | |
| 50 гц | 0,11 |
| 1Мгц | 0,03 |
Для полиакрилонитрила характерны две температуры стеклования. Первая из них лежит в области от 86 до 96,5 °C. Зависимость ее от молекулярной массы хорошо описывается уравнением Флори:
где а=(2,8±0,1)*10 5 ; Т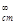
Полиакрилонитрил при нагревании в атмосфере азота не претерпевает никаких изменений до 200°С, но при более высокой температуре происходит его размягчение и появление газообразных продуктов, главным образом аммиака NH3 , и водорода Н2 . При 270°С наблюдается также выделение цианистого водорода HCN. Из жидких продуктов распада полимера можно выделить вещества, содержащие группы – NH2 и – С = N. Также присутствуют винилацетонитрил и вещества, являющиеся димерами, тримерами и тетрамерами акрилонитрила. Полимер окрашивается и становится нерастворимым.
Энергия активации термической деструкции 130 кДж/молъ (31 ккал / молъ).
При нагревании растворов полиакрилонитрила в диметилформамиде в токе воздуха, кислорода или в инертной атмосфере в течение 30–40 часовполиакрилонитрил также окрашивается в желтый и далее в темно-коричневый цвет; образующиеся при этом сопряженные системы растворимы в диметилформамиде [6, С. 44].
При температурах выше 700°С полиакрилонитрил подвергается химическому превращению в полимер циклической структуры, содержащий сопряженные двойные связи. В зависимости от условий пиролиза (вакуум или воздух, водород, азот и аммиак под давлением) образуются продукты с различными свойствами. В ряде случаев может быть получен продукт графитовой структуры, обладающий свойствами полупроводников (удельная электропроводность 10 -10 – 10 -13 Мом/см).
При длительной термической обработке полиакрилонитрильного волокна или ткани в азоте и на воздухе получен термостойкий материал, выдерживающий кратковременное воздействие пламени горелки и сохраняющий достаточную прочность.
Акрилонитрил в присутствии инициаторов легко вступает в редакцию полимеризации, сопровождающуюся выделением 73,3 кДж/моль тепла.
В качестве инициаторов применяют пероксиды, азо- и диазосоединения, а также элементоорганические соединения [1, С. 132].
Кислород ингибирует полимеризацию акрилонитрила, поэтому процесс проводят в среде азота. Скорость реакции значительно возрастает в присутствии следов ионов меди или железа.
При полимеризации акрилонитрила используют также окислительно-восстановительные системы. Чаще всего применяют персульфат аммония с тиосульфатом или гидросульфитом натрия, что позволяет проводить реакцию при более низких температурах и получать полимер с более высокой молекулярной массой.
В промышленности полиакрилонитрил получают радикальной полимеризацией акрилонитрила в гетерогенных или гомогенных условиях. Производство полиакрилонитрила может быть осуществлено как периодическим, так и непрерывным методами.
Непрерывный технологический процесс получения полиакрилонитрила состоит из стадий приготовления растворов, полимеризации акрилонитрила, демономеризации дисперсии и конденсации акрилонитрила, фильтрации, промывки и сушки полимера.
полиакрилонитрил химический карбоцепный
Таблица 2 Нормы загрузки компонентов
| Аппарат 4 | |
| Персульфат калия, кг | 3,0 |
| Вода обессоленная, м 3 | 0,44 |
| Аппарат 5 | |
| Метагидросульфит натрия, кг | 0,1 |
| Вода обессоленная, м 3 | 0,050 |
| Аппарат 6 | |
| НАК, м 3 /ч | 0,0224 |
| Раствор персульфата калия, м 3 /ч | 0,073 |
| Раствор метагидросульфита натрия, м 3 /ч | 0,0246 |
Полимеризация проводиться при различных температурах: зона 1 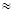
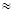
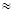
Полимеризацию акрилонитрила проводят в реакторе непрерывного действия в водной среде в присутствии окислительно-восстановительной инициирующей системы из персульфата калия и метагидросульфита натрия. Степень превращения мономера в полимер равна 80–85%.
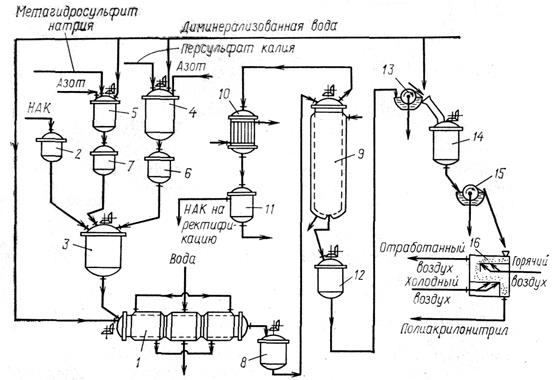
Рисунок 1 Схема процесса производства полиакрилонитрила: 1 – полимеризатор; 2, 6, 7 – напорные емкости; 3 – смеситель; 4, 5 – аппараты для растворения инициатора; 8 – промежуточная емкость; 9 – колонна демономеризации – 10 – холодильник кожух отрубный; 11 – отстойник; 12 – сборник дисперсии полимера; 13, 15 – барабанные фильтры; 14 – репульпатор; 16 – сушилка с кипящим слоем
НАК подается из напорной емкости 2 в смесительный аппарат 3. Водные растворы персульфата калия и метагидросульфита натрия готовят в аппаратах для растворения 4, 5, из которых они самотеком поступают в емкости 6, 7, а затем дозируются в аппарат 3.
Полученная дисперсия поступает в промежуточную емкость 8, а затем в колонну 9 для отделения непрореагировавшего акрилонитрила (демономеризации) путем отгонки. Демономеризация проводится при 50–60 °С и остаточном давлении 6,6–20,0 кПа.
Пары акрилонитрила и воды конденсируются в холодильнике 10. Конденсат поступает в отстойник 11, в котором он разделяется на два слоя: верхний слой – акрилонитрил, нижний слой – 7%-ный раствор акрилонитрила в воде.
Дисперсия полимера, из которой выделен акрилонитрил, из аппарата 9 поступает в сборник 12, откуда периодически насосом подается на вакуум-барабанный фильтр 13 для отделения полимера от маточного раствора. Полимер с барабана срезается ножом и попадает на транспортный желоб. Сюда же одновременно подается вода для смывания полимера в репульпатор 14. В аппарате 14 полимер отмывается от остатков мономера и инициатора. Из репульпатора пульпа подается на вакуум-барабанный фильтр 15. После фильтрации полимер с влажностью 80% сушат в сушилке с кипящим слоем 16 до содержания влаги 0,7–1,5% [1, С. 134].
Гетерофазная полимеризация акрилонитрила характеризуется самоускорением (примерно до степени превращения 20% при 60°С), которое обусловлено захватом макрорадикалов, выпадающим в осадок полимером. Эффективные скорости роста захваченных макрорадикалов зависят от температуры и степени экранирования активного центра свернутыми цепями, препятствующими диффузии акрилонитрила и других реагентов в твердую фазу.
Особенность гетерофазной полимеризации – увеличение молекулярной массы полиакрилонитрила с возрастанием степени превращения. Этот факт обусловлен захватом твердой фазой макрорадикалов, которые при температуре ниже 60°С не гибнут. Гетерофазная полимеризация акрилонитрила чувствительна к перемешиванию, центрифугированию, так как в этих условиях возрастает числе столкновений глобул и, следовательно, скорость обрыва цепи. Кислород в небольшом количестве способствует увеличению скорости полимеризации вследствие дополнительного образования перекисей и гидроперекисей акрилонитрила, служащих инициаторами. В присутствии большого количества кислорода процесс ингибируется и в пределе может прерваться. Поэтому полимеризацию с перемешиванием проводят в атмосфере инертного газа при охлаждении реактора в изотермических условиях.
Скорость гетерофазной полимеризации акрилонитрила vопределяется суммой скоростей Rs (в водном растворе акрилонитрила) и Rg (на глобулах полиакрилонитрила):
где kр и k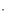
Добавки Cu2 O, Ni2 O, MgO, A12 O3 , SiO2 к жидкому акрилонитрилу при -78°C или к твердому акрилонитрилу при -196°С сенсибилизируют полимеризацию и повышают скорость процесса. Акрилонитрил быстро полимеризуется в твердой фазе (степень превращения
100%) в присутствии сильно измельченного катализатора (метод молекулярных пучков); процесс особенно интенсивен при -160°С и -130°С (точки фазовых переходов); при этом может иметь место взрывная полимеризация [6, С. 47].
Процесс полимеризации акрилонитрила непрерывным методом осуществляется в реакторе с мешалкой, в который непрерывно вводят акрилонитрил, водные растворы персульфата аммония, восстановителя-активатора, например бисульфита или тиосульфата натрия, и из которого непрерывно выводят суспензию полимера.
Радиационная полимеризация акрилонитрила под действием 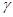
В жидкой фазе акрилонитрила полимеризуется с самоускорением из-за радиолиза образующегося поли акрилонитрила и, следовательно, повышенного выхода радикалов. Скорость (и) такогопроцесса (в массе) при обрыве цепи рекомбинацией определяется выражением:
где к – константа скорости роста; I– мощность дозы (17,2–430 мка/кг, или 4–100 р/мин). Энергии активации в интервале температур от -83 (т. пл.) до -116°С (твердая фаза), от -83 до 0 С С (жидкая фаза) и от 20 до 50 °С равны соответственно 0; 12,6 и 62,8 кДж/моль (0; 3 и 15 ккал / моль). При воздействии 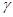
Производство полиакрилонитрила может осуществляться в водных растворах минеральных солей – гомогенная полимеризация.
Гомогенную полимеризацию акрилонитрила можно проводить в водных растворах солей NaCNS, Ca (CNS)2 , ZnCl2 +CaCl2 или MgCl2 , Mg(ClО4 )2 .Гомогенная полимеризация акрилонитрила в органических растворителях (диметилформамид, диметилацетамид) в присутствии динитрила азодиизомасляной кислоты возможна лишь при высоких концентрациях мономера в растворе до 25% [5, С. 46].
Скорость гомогенной полимеризации акрилонитрила определяется выражением:
где kи , kp , k0 – константы скорости соответственно инициирования, роста и обрыва; [I] – концентрация инициатора (или мощность дозы радиации); [М] -, концентрация мономера.
Процесс проводят непрерывным способом в аппарате, снабженном мешалкой, системой обогрева и охлаждения, при 79–80,5 °С и атмосферном давлении. В реактор, содержащий 50,5%-ный водный раствор роданида натрия, вводят смесь 92% акрилонитрила, 6% метилакрилата, 1% итаконовой кислоты, 0,1% инициатора – динитрила азобисизомасляной кислоты и другие добавки, способствующие регулированию роста цепи. Реакционная смесь непрерывно подается в аппарат снизу, а раствор полимера отводится сверху. Продолжительность полимеризации 1–1,5 ч. Конверсия мономера составляет около 78% [1, С. 135].
При получении полиакрилонитрила в среде органического растворителя (лаковый метод) полимеризации протекает в условиях, при которых мономер и образующийся полимер находятся в растворе. В качестве растворителей применяют диметилформамид (в большинстве случаев), диметилацетамид, 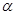
Технологический режим и аппаратурное оформление процесса мало отличаются от таковых при полимеризации акрилонитрила в водном растворе солей.
Полиакрилонитрил получается в виде лака, который используют в качестве прядильного раствора для получения волокна. При необходимости из полиакрилонитрила можно выделить твердый порошкообразный полимер.
Полимеризация акрилонитрила в массе, или в блоке, имеет ограниченное применение в промышленности и используется главным образом для получения сополимеров акрилонитрила с другими мономерами. В результате блочной полимеризации полиакрилонитрил получается в виде твердого порошка [1, С. 135].
Наиболее широко полиакрилонитрил применяется для изготовления волокна различного назначения. Для этой цели готовятся растворы полиакрилонитрила. Формование волокон осуществляется по мокрому или сухому способу.
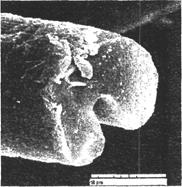
Рисунок 2. Электронно-микроскопическое изображение бобовидного среза углеродного волокна, полученного из ПАН волокна
При мокром способе прядения пригодны 15–20% растворы полимера в диметилформамиде. При 20°С они обладают высокой вязкостью, поэтому подача их в фильеры производится под давлением. Из фильер прядильный раствор поступает в ванны, в которых осаждающий раствор вместе с вспомогательными добавками нагревается до 60–90°С. В качестве осадителей используется вода с добавкой диметилформамида, смесь гексантриола с диметилформамидом (75:25) и др. Сформированная нить вытягивается в 8–12 раз при 100–130°С, затем проходит отжимные валы, горячие прядильные диски и подвергается термофиксации.
При сухом способе формования волокна раствор полиакрилонитрила продавливается через фильеры в шахту навстречу току горячего воздуха. После выхода из прядильной шахты волокно содержит 12–40% диметилформамида; его физико-механические свойства невысоки. Для улучшения свойств волокно подвергают вытяжке, но предварительно отмывают избыток растворителя горячей водой (90–100°С).
Полиакрилонитрильное волокно по своим свойствам напоминает шерсть и может быть окрашено различными красителями. Если ему сообщить основные свойства, то окрашиваемость улучшается. Для этого изготовляют сополимеры акрилонитрила, содержащие небольшие количества винилпиридина, N-бензилакриламида и других азотсодержащих непредельных соединений. Обработка их аммиаком или аминами (лучше всего гексаметилендиамином) дает возможность получить материалы с небольшим содержанием основных групп. Полиакрилонитрильное волокно обладает следующими свойствами [3, С. 356]:
Таблица 3. Свойства полиакрилонитрильного волокна
| Свойство | Величина |
| Плотность, г/см 3 | 1,17 |
| Предел прочности при растяжении, г/денъе | 3–4 |
| Относительное удлинение, % | 8–35 |
| Относительная прочность во влажном состоянии, % | 90–98 |
| Гигроскопичность (при 20 °С и 60% относительной влажности), % | 1,0 |
| Водопоглощение, % | 1–2 |
| Температура плавления, °С | 250 |
| Устойчивость: | |
| -к кислотам | Очень хорошая |
| -щелочам | Умеренная |
| -органическим растворителям | Очень хорошая |
Специальные ПАН волокна, которые обычно используются для производства углеродного волокна, имеют круглую форму поперечного среза, диаметр до 15 мкм, площадь поперечного сечения до 180 мкм 2 и низкую линейную плотность – до 0,17 текс. Коммерческое текстильное ПАН волокно имело бобовидную форму поперечного сечения, площадь сечения 530 мкм 2 , линейную плотность 0,56 текс, прочность при растяжении 226 МПа и относительное удлинение при разрыве 43,9% [4, С. 33].
Полиакрилонитрильное волокно используется для изготовления изделий широкого потребления, технических тканей (фильтры, войлок, специальные сукна), брезентов, транспортных лент, рыболовных сетей в качестве наполнителя слоистых пластиков.
Полиакрилонитрил представляет собой линейный карбоцепной полимер содержащий сильно полярную группу – СN, что в большей мере определяет его свойства. Этот полимер очень капризен в выборе растворителя, что необходимо учитывать как при его синтезе, так и при переработке.
Полиакрилонитрил – хорошее сырье для получения термоустойчивых материалов, воздействие повышенных температур позволяет модифицировать его свойства. Он хорошо сополимеризуется с большим числом мономеров, а полученные сополимеры являются востребованными промышленными продуктами (лаки, клеи, АБС пластик)
Волокна, получаемые из полиакрилонитрила, обладают широким спектром свойств. В частности, на основе полиакрилонитрила производят термостойкие углеродные волокна.
С момента открытия полиакрилонитрила прошло больше ста лет, но он продолжает оставаться востребованным и занимает не последнее место среди промышленных полимеров. Проводятся исследования по созданию все новых и новых материалов на его основе.
1. Коршак В.В. Технология пластических масс/ В.В. Коршак; под ред. В.В. Коршака. – 3-е изд., перераб. и доп. – М.: Химия, 1985. -560 с.
2. Лебедев, Н.Н. Химия и технология основного органического и нефтехимического синтеза/ Н.Н. Лебедев. – 3-е изд., перераб. – М.: Химия, 1975. -736 с.
3. Николаев А.Ф. Синтетические полимеры и пластические массы на их основе/А.Ф. Николаев. – 2-е изд., доп.-Л.: Химия, 1966. -768 с.
4. Процесс изготовления углеродных волокон на основе коммерческих полиакрилонитрильных волокон мокрого формования/ R. EslamiFarsani и [др.] // Химические волокна. – 2006. – №5. – С. 30–33.
5. Семчиков Ю.Д. Высокомолекулярные соединения: учебник для вузов/ Ю.Д. Семчиков. – М.: Академия, 2003. – 368 с.
6. Энциклопедия полимеров: энциклопедия. В 3 т. Т. 1. А-К. – М.: Советская энциклопедия, 1972. -1224 с.
Статья по теме: Полимеризация акрилонитрила
Предметная область: полимеры, синтетические волокна, каучук, резина
Полимеризация акрилонитрила проводится в реакторе 1 (рис. 18.2) непрерывного действия в водной среде в присутствии окислительно-восстановительной инициирующей системы из персульфата калия и метабисульфита натрия.[6, С.399]
Полимеризация акрилонитрила протекает под воздействием а,а- азобис(а,у-диметилвалеронитрила) [46], тетраметилентиу-рамсульфида, бензтиазолилдисульфида и других сульфидов [47]. Полимеризация акрилонитрила происходит в случае добавления его полимеров, полученных при фотополимеризации [48], а также деструктированных механически [49]. Акрилонитрил полимери-зуется под действием ультразвука [50]; имеется еще целый ряд веществ, которые также инициируют полимеризацию акрилонитрила [51—57].[13, С.439]
Полимеризация акрилонитрила замедляется в присутствии воды, уксусной кислоты, ацетальдегида, нитрила янтарной кислоты [58], 1,3-бутадиенацетилена, октатриен-1,3,7-ина-5-винил-ацетилена [59], моноалкильных эфиров гидрохинона [60] и полностью ингибируется /пранс-дибензоил этиленом [61]. При про-[13, С.439]
Полимеризация акрилонитрила на одном тетраэтил свинце шла гладко, хотя высокие степени превращения при этом не достигались. Ультрафиолетовое облучение повышало степень превращения, но уменьшало молекулярный вес образовывавшихся полимеров. Было найдено, что облучение необходимо для осуществления полимеризации акрилонитрила с помощью тетраэтил свинца при комнатной температуре. Ультрафиолетовый свет был также необходим для полимеризации в присутствии тетраэтилсвинца при комнатной температуре винилацетата, винилхлорида и метилметакрилата.[14, С.287]
Полимеризация акрилонитрила с катализатором TiCl4—A1 (иго-С4Н9)3 (1 : 1) при 20° осуществлена за счет уменьшения сорбции мономера на катализаторе путем введения конкурирующей добавки (ацетонитрила).[14, С.527]
Рис. 5. Полимеризация акрилонитрила в блоке в присутствии перекиси бензоила: А — 70°, 0,1% перекиси бензоила; Б—100°, 0,1%перекиси бензоила; В—100°, 0,25% перекиси бензоила.[4, С.26]
В присутствии третичного фосфина полимеризация акрилонитрила протекает с заметной скоростью при —70°, при 20° реакция сопровождается взрывом. Образующийся полимер содержит фосфор. В присутствии воды молекулярный вес пслимера уменьшается.[2, С.333]
Акрилонитрил не иолимеризуется под влиянием света и кислорода воздуха (в последнем случае даже при нагревании до 100°). Полимеризация акрилонитрила легко инициируется пере-[2, С.331]
Полимеризацию акрилонитрила можно проводить в растворе (например, в толуоле), а также водно-эмульсионным способом. Водно-эмульсионная полимеризация акрилонитрила является наиболее распространенным промышленным методом получения поли-акрилонитрила. В качестве инициатора процесса применяют ире-[2, С.332]
Катализаторы катиопиой полимеризации не вызывают образования полиакрнлонитрила. Это объясняется тем, что СМ-группа акрилонитрила, притягивая электроны it-связи, смещает электронную плотность к атому углерода, при котором находится замещающая группа. Полимеризация акрилонитрила происходит в присутствии катализаторов анионной полимеризации, например оснований. Такими катализаторами могут служить натрий в жидком аммиаке* или третичный фосфин**. В первом случае инициирование процесса можно представить в виде следующего уравнения:[2, С.333]
Опыт 3-08. Полимеризация акрилонитрила в растворе, инициированная персульфатом аммония. 124[5, С.6]
http://www.bestreferat.ru/referat-205313.html
http://polymer-tech.ru/ref/polimerizaci9_akrilonitrila.html



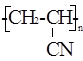
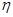 ], определяемой в диметилформамиде (С=2–20 г./л) при 20°С, выражается уравнением [
], определяемой в диметилформамиде (С=2–20 г./л) при 20°С, выражается уравнением [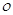 =2,5–3,2, а длина сегмента Куна 3,17 нм [5, С. 150].
=2,5–3,2, а длина сегмента Куна 3,17 нм [5, С. 150].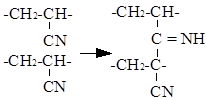
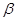 -диметиламинопропионитрила или
-диметиламинопропионитрила или 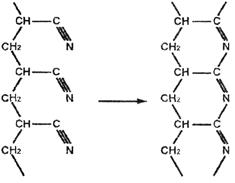
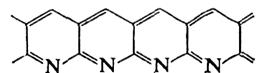
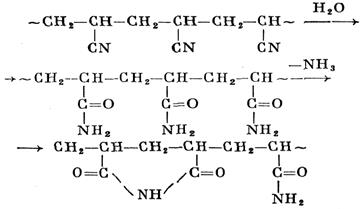
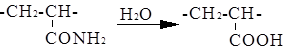
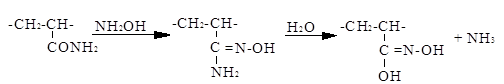
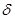 =30,8*10 -3 (Дж/м 3 ) 0,5 , а воды
=30,8*10 -3 (Дж/м 3 ) 0,5 , а воды 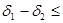 4 (Дж/м 3 ) 0,5 , т.е.
4 (Дж/м 3 ) 0,5 , т.е. 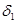 должен быть почти равен
должен быть почти равен 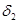 , что для воды и полиакрилонитрила не наблюдается [4, C. 99].
, что для воды и полиакрилонитрила не наблюдается [4, C. 99].