При гидрировании ацетилена избытком водорода образуется?
Химия | 10 — 11 классы
При гидрировании ацетилена избытком водорода образуется?
На первой стадии гидрирования образуется этилен.
на второй стадии — этан.
После гидрирования 107, 52 дм3 ацетилена смесь содержала 4, 48дм3 этана, 14, 56 дм3 водорода и этилен?
После гидрирования 107, 52 дм3 ацетилена смесь содержала 4, 48дм3 этана, 14, 56 дм3 водорода и этилен.
Какой объем этилена образовался и какой объем водорода был взят для гидрирования?
Помогите очень срочно нужно.
Какой обьём водорода понадобиться для гидрирования одного литра этилена?
Какой обьём водорода понадобиться для гидрирования одного литра этилена?
Какой объём водорода потребуется для полного гидрирования 11, 2л бутадиена?
Какой объём водорода потребуется для полного гидрирования 11, 2л бутадиена?
Какой объем водорода (н?
Какой объем водорода (н.
У) необходим для гидрирования 55.
Какой объём водорода необходим для полного гидрирования 5г дивинила?
Какой объём водорода необходим для полного гидрирования 5г дивинила.
Химические свойства алкенов 1)горение 2)присоединения водорода гидрирование?
Химические свойства алкенов 1)горение 2)присоединения водорода гидрирование.
Напишите, пожалуйста, на тетрадном листе :1?
Напишите, пожалуйста, на тетрадном листе :
если сможете, объясните как делать.
Найти объем водорода, необходимый для гидрирования 330 г этаналя?
Найти объем водорода, необходимый для гидрирования 330 г этаналя.
Как с помощью водорода получить ацетилен?
Как с помощью водорода получить ацетилен?
СРОЧНО?
Определите объем ацетилена (н.
У. ), образующегося при действии избытка воды на 8 кг технического карбида кальция, содержащего 10 % примесей.
Найдите молекулярную формулу углеводорода, состоящего из 85, 7% углерода, 14, 3 % водорода.
Относительная плотность вещества по водороду составляет 28.
Определите класс соединений и его название.
На странице вопроса При гидрировании ацетилена избытком водорода образуется? из категории Химия вы найдете ответ для уровня учащихся 10 — 11 классов. Если полученный ответ не устраивает и нужно расшить круг поиска, используйте удобную поисковую систему сайта. Можно также ознакомиться с похожими вопросами и ответами других пользователей в этой же категории или создать новый вопрос. Возможно, вам будет полезной информация, оставленная пользователями в комментариях, где можно обсудить тему с помощью обратной связи.
Na2Cr2O7 + 3Na2S + 7H2SO4 = 3S + Cr2(SO4)3 + 4Na2SO4 + 7H2O 2Cr( + 6) + 6e — — — > 2Cr( + 3) I 1 восстановление окислитель S( — 2) — 2e — — — — — — — > S(0) I 3 окисление восстановитель.
То1)Дано : Решение : m(Li2O) = 55г. 4Li + O2 = 2Li2O __________ М(Li) = 7г / моль m(Li) = ? N(Li) = 4 моль m = M * n m(Li) = 7г / моль * 4моль = 28г Ответ : m(Li) = 28г 2) 1)4Li + O2 = 2Li2O 2)Li2O + 2HBr = 2LiBr + H2O 3)LiBr + KOH = LiOH + KBr 4)L..
Чисто протонов это порядковый номер элемент. По таблице Менделеева вещество с порядковым номером 31 это галлий Ga.
А)20% б)12% в)33, 3% г)20% д)5, 2% е)30% ж)4, 2%.
Уравнение реакции ацетилена с избытком водорода
FOR-DLE.ru — Всё для твоего DLE 😉
Привет, я Стас ! Я занимаюсь так называемой «вёрсткой» шаблонов под DataLife Engine.
На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх.
Раньше я занимался простой вёрсткой одностраничных, новостных и т.п. шаблонов на HTML, Bootstrap. Однажды увидев сайты на DLE решил склеить пару шаблонов и выложить их в интернет. В итоге эта парочка шаблонов набрала неплохую популярность и хорошие отзывы, и я решил создать отдельный проект.
Кроме шаблонов я так же буду выкладывать полезную информацию для DataLife Engin и «статейки» для веб мастеров. Так же данный проект будет очень полезен для новичков и для тех, кто хочет правильно содержать свой сайт на DataLife Engine. Надеюсь моя работа вам понравится и вы поддержите этот проект. Как легко и удобно следить за обновлениями на сайте?
Достаточно просто зарегистрироваться на сайте, и уведомления о каждой новой публикации будут приходить на вашу электронную почту!
Задание 1
Напишите структурные формулы всех алкинов, содержащих четыре атома углерода, и назовите их.
| СH≡С―СH2―СH3 бутин-1 | СH3 ―C ≡С―СH3 бутин-2 |
Возможна ли для них цис-транс-изомерия? Возможна для бутина-2
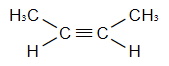 цис-бутин-2 | 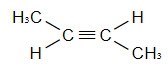 транс-бутин-2 |
Задание 2
Напишите формулу ацетиленового углеводорода, который содержит в 1,5 раза больше атомов водорода, чем углерода.
Общая формула ацетиленового углеводорода имеет вид CnH2n−2.
По условию задачи формула содержит в 1,5 раза больше атомов водорода, чем углерода, поэтому имеем уравнение:
(2n-2)/n=1,5
2n-2=1,5n
2n-1,5n=2
0,5 • n=2
n=2:0,5
n=4, следовательно, формула имеет вид C4H6
Ответ: C4H6
Задание 3
Приведите уравнения двух химических реакций получения ацетилена. Укажите условия их протекания.
CaC2 + 2H2O ⟶ Ca(OH)2 + C2H2↑
2CH4 1500°C ⟶ C2H2 + 3H2
Задание 4
Объясните, почему при равных объёмах этилена и ацетилена последний может присоединить в два раза больше водорода. Реакции присоединения происходят по месту кратности связи, поэтому к молекуле ацетилена присоединяются две молекулы водорода, а к молекуле этилена ― одна такая молекула.
Задание 5
Напишите в общем виде уравнения реакций присоединения к ацетиленовым углеводородам избытка:
а) водорода;
CnH2n-2 + 2H2 ⟶ CnH2n+2
б) брома.
CnH2n-2 + 2Br2 ⟶ CnH2n-2Br4
Задание 7
Напишите уравнение реакции ацетилена с хлороводородом, взятыми в соотношении 1:1.
CH≡CH + HCl ⟶ CH2=CHCl
Задание 8
Если бы ацетилен вступал в реакцию полимеризации подобно этилену, какова была бы формула образующегося полимера? ( ― CH=CH ― ) n
Задание 9
Сколько граммов карбида кальция необходимо для получения 4,48 л ацетилена (н.у.)?
Дано: V(C2H2)=4,48 л
Найти: m( CaC2 )-?
Решение
1-й способ
n( C2H2 )= V( C2H2 )/Vm=4,48 моль : 22,4 л/моль=0,2 моль
Составляем уравнение реакции: CaC2 + 2H2O ⟶ Ca(OH)2 + C2H2↑
По уравнению реакции n(CaC2)/1=n(C2H2)/1, поэтому
n( CaC2 )=n( C2H2 )=0,2 моль
Mr(CaC2)=Ar(Ca)+2•Ar(C)=40+2 •12=64 , поэтому M( CaC2 )=64 г/моль
m( CaC2 )=n( CaC2 ) • M( CaC2 )=0,2 моль • 64 г/моль=12,8 г
2-й способ
1. Составим химическое уравнение:
х г 4,48 л
CaC2 + 2H2O ⟶ Ca(OH)2 + C2H2↑
64 г 22,4 л
Над формулами соединений CaC2 и C2H2 записываем неизвестную массу карбида кальция (х г) и приведенный в условии задачи объём ацетилена (4,48 л), а под формулами соединений ― массу и объём соответствующего количества вещества согласно коэффициентам в химическом уравнении. При н.у. 1 моль газа занимает объем 22,4 л.
Mr(CaC2)=Ar(Ca)+2•Ar(C)=40+2 •12=64 , поэтому M( CaC2 )=64 г/моль. Масса 1 моль=64 г.
2. Массу карбида кальция рассчитываем с помощью пропорции:
х г / 64 г = 4,48 л / 22,4 л, отсюда
х=m( CaC2 )=64 г • 4,48 л : 22,4 л=12,8 г
Ответ: m( CaC2 )=12 ,8 г
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. источники: http://gdz.cool/h10_edl_2019/1130-h10_e_2019__7__.html http://acetyl.ru/o/a21d2d.php |







