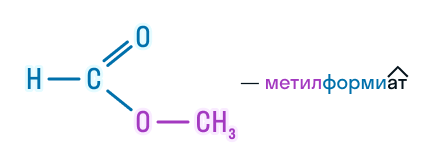Напишите пожалуйста уравнение реакции этерификации муравьиной кислоты с этанолом?
Химия | 10 — 11 классы
Напишите пожалуйста уравнение реакции этерификации муравьиной кислоты с этанолом.
HCOOH + C2H5OH = HCOOC2H5 + H2O.
Ребят?
Напишите схему реакции между : 1)пропановой кислотой и этанолом 2)бутанолом — 1 и муравьиной кислотой 3) этановой кислотой и метанолом.
Напишите уравнения реакций : Этанола с пропиновой кислотой?
Напишите уравнения реакций : Этанола с пропиновой кислотой.
Напишите уравнения реакции получения (этерификация) : — Этилового эфира масляной кислоты?
Напишите уравнения реакции получения (этерификация) : — Этилового эфира масляной кислоты.
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения : 1)Этиловый эфир муравьиной кислоты в этанол 2)Этанол в хлорэтан 3)Хлорэтан в этанол 4)Этанол в диэтиловый эфир?
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения : 1)Этиловый эфир муравьиной кислоты в этанол 2)Этанол в хлорэтан 3)Хлорэтан в этанол 4)Этанол в диэтиловый эфир.
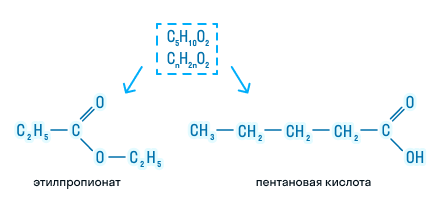
А)Реакции этерификации между муравьиной кислоты и этаноломб)Реакции гидролиза этилого эфира пентановой кислоты?
А)Реакции этерификации между муравьиной кислоты и этанолом
б)Реакции гидролиза этилого эфира пентановой кислоты.
Реакций получения данных веществ : = O
CH3 — CH2 — C — O — CH2 — CH3.
Какая реакция называется реакцией этерификации?
Какая реакция называется реакцией этерификации?
Составьте уравнение химической реакции получения абрикосовой эссенции из масляной кислоты и этанола.
Напишите уравнения реакций этерификации между метановой кислотой и 2 — метилпропанолом — 1?
Напишите уравнения реакций этерификации между метановой кислотой и 2 — метилпропанолом — 1.
Запишите качественные реакции на этанол, уксусную кислоту и муравьиный альдегид?
Запишите качественные реакции на этанол, уксусную кислоту и муравьиный альдегид.
Помогите с реакцией муравьиной кислоты с этанолом, нужно уравнение?
Помогите с реакцией муравьиной кислоты с этанолом, нужно уравнение.
Напишите следующие уравнения реакций : а) этерификации этанола и муравьиной кислоты, б) щелочного гидролиза этилового эфира масляной кислоты, в) гидролиза метилового эфира пропионовой кислоты, г) восс?
Напишите следующие уравнения реакций : а) этерификации этанола и муравьиной кислоты, б) щелочного гидролиза этилового эфира масляной кислоты, в) гидролиза метилового эфира пропионовой кислоты, г) восстановления изопропилового эфира пропионовой кислоты.
Вопрос Напишите пожалуйста уравнение реакции этерификации муравьиной кислоты с этанолом?, расположенный на этой странице сайта, относится к категории Химия и соответствует программе для 10 — 11 классов. Если ответ не удовлетворяет в полной мере, найдите с помощью автоматического поиска похожие вопросы, из этой же категории, или сформулируйте вопрос по-своему. Для этого ключевые фразы введите в строку поиска, нажав на кнопку, расположенную вверху страницы. Воспользуйтесь также подсказками посетителей, оставившими комментарии под вопросом.
FeCl3 + NaOH = FeOH + NaCl3 K2CO3 + HNO3 = K2NO3 + H2CO3 BaCl2 + Na2SO4 = BaSO4 + NaCl2.
Селен назван в честь Луны.
HCl ; H2SO4 ; — кислоты ; Cu(NO3)2 ; FeCl3 ; — соли ; Na2O ; BaO ; Mg(OH)2 — основные оксиды ; СО2 — кислотный оксид ; KOH — основание( гидроксид калия).
Ответ второй и четвертый.
BaCl2 + 2H2O — > Cl2 + H2 + Ba(OH)2 Ba(OH)2 + H2SO4 — > BaSO4 + 2H2O.
Рассчитывается по числу молекул. Здесь будет 5 ионов.
CO2 + H2O H2CO3 (реакция обратимая, так как кислота неустойчива) Не уверена.
Сложные эфиры: способы получения и свойства
Сложные эфиры: способы получения, химические и физические свойства, строение.
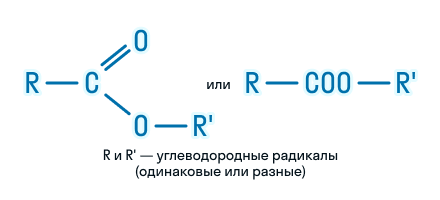
| Сложные эфиры – это органические вещества, в молекулах которых углеводородные радикалы соединены через карбоксильную группу -СОО-, а именно R1-COOH-R2. |
Общая формула предельных сложных эфиров: СnH2nO2
Классификация сложных эфиров
По числу карбоксильных групп:
- сложные эфиры одноосновных карбоновых кислот — содержат одну карбоксильную группу -СОО-. Общая формула CnH2nO2.
| Например, метилформиат |
- сложные эфиры многоатомных спиртов — содержат две и более карбоксильные группы -СОО-.
| Например, тристеарат глицерина |
- Сложные эфиры многоосновных органических кислот.
Например, общая формула сложных эфиров двухосновных карбоновых кислот CnH2n-2O4
Номенклатура сложных эфиров
В названии сложного эфира сначала указывают алкильную группу, связанную с кислородом, затем кислоту, заменяя суффикс в названии кислоты (-овая кислота) на суффикс -оат.
| Название сложного эфира | Тривиальное название | Формула эфира |
| Метилметаноат | Метилформиат | HCOOCH3 |
| Этилметаноат | Этилформиат | HCOOC2H5 |
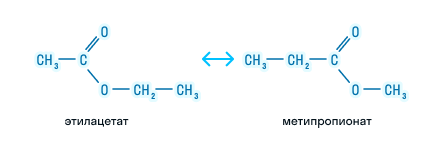
| Метилэтаноат | Метилацетат | CH3COOCH3 |
| Этилэтаноат | Этилацетат | CH3COOC2H5 |
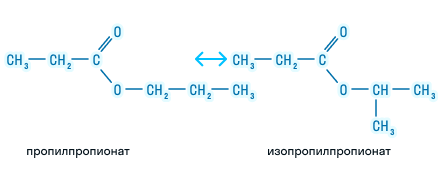
| Пропилэтаноат | Пропилацетат | CH3COOCH2CH2CH3 |
Химические свойства сложных эфиров
| Сложные эфиры устойчивы в нейтральной среде, но легко разлагаются при нагревании в присутствии кислот или в присутствии щелочей. |
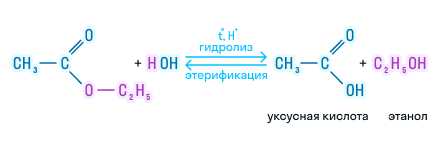
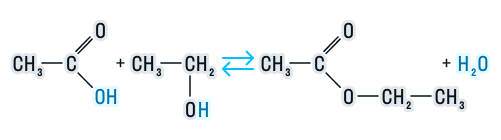
В присутствии кислот гидролиз сложных эфиров протекает как реакция, обратная этерификации. при гидролизе сложных эфиров образуются спирты и карбоновые кислоты.
R-COO-R’ + H2O = R-COOH + R’-OH
Например , при гидролизе метилацетата образуются уксусная кислота и метанол.
При щелочном гидролизе сложных эфиров образуются соли карбоновых кислот и спирты.
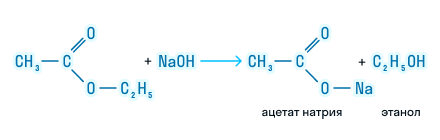
Например , при щелочном гидролизе этилформиата образуются этанол и формиат натрия:
При щелочном гидролизе этилацетата образуются ацетат и этанол:
Щелочной гидролиз сложных эфиров — реакция, имеющая промышленное значение. Гидролиз жиров в присутствии оснований — древнейший способ получения мыла. Первые способы получения мыла связаны со смешиванием жира с золой. Один из основных компонентов животного жира — тристеарат глицерина. В щелочной среде тристеарат глицерина разлагается на глицерин и соль стеариновой кислоты:
2. Переэтерификация
Переэтерификация — это реакция превращения одного сложного эфира в другой под действием соответствующих спиртов в присутствии катализатора (кислоты или основания)
R-COO-CH3 + R’-OH = R-COOR’ + CH3-OH
3.Восстановление сложных эфиров
Сложные эфиры восстанавливаются с разрывом связи С-О карбоксильной группы. При этом образуется смесь спиртов.
| Например, этилбензоат восстанавливается литийалюминийгидридом до бензилового спирта и этанола |
Получение сложных эфиров
1. Этерификация карбоновых кислот спиртами
Карбоновые кислоты вступают в реакции с одноатомными и многоатомными спиртами с образованием сложных эфиров.
| Например, этанол реагирует с уксусной кислотой с образованием этилацетата (этилового эфира уксусной кислоты): |
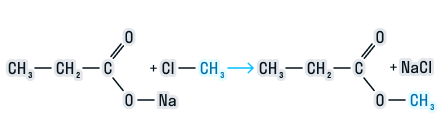
2. Соли карбоновых кислот с галогеналканами
При взаимодействии солей карбоновых кислот с галогеналканами образуются сложные эфиры.
Сложные эфиры
О чем эта статья:
Для начала дадим определение и разберемся, почему эти эфиры — сложные.
Сложные эфиры или эсте́ры (от древнегреческого αἰθήρ — «эфир») — это класс соединений на основе неорганических (минеральных) или органических (карбоновых) одно- или многоосновных кислот, у которых атом водорода в гидроксогруппе замещен на радикал. Эпитет «сложные» они получили для того, чтобы их не путали с простыми эфирами — производными спиртов.
Общая формула сложных эфиров выглядит так:
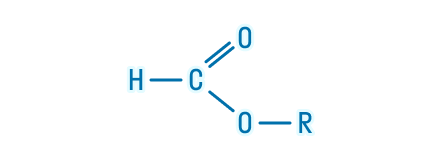
Однако представители сложных эфиров муравьиной кислоты выглядят иначе. Для них общая формула приобретает такой вид:
Номенклатура сложных эфиров
Теперь поговорим о том, как называть представителей данного класса. Различают два способа, позволяющие назвать сложные эфиры: по систематической номенклатуре (ИЮПАК) или по рациональной номенклатуре. Рассмотрим оба варианта.
По номенклатуре ИЮПАК название строится следующим образом:
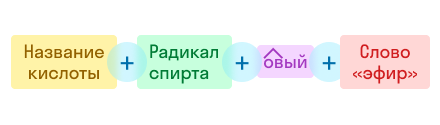
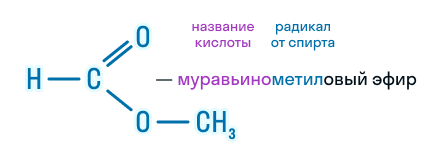
По рациональной номенклатуре название строится так:
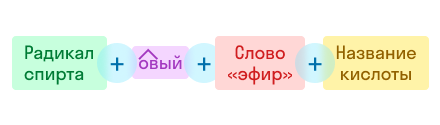
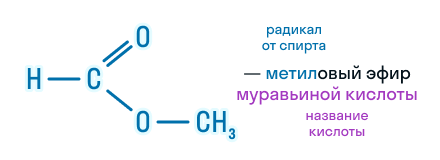
По этой же номенклатуре эфиры можно называть, используя четыре слова: радикал спирта + слово «эфир» + название кислоты + слово «кислота». Например, муравьинометиловый эфир можно иначе назвать метиловый эфир муравьиной кислоты:
Изомерия сложных эфиров
Возможна ли изомерия для сложных эфиров? Давайте разбираться.
Возможна изомерия углеродного скелета у радикала кислоты и радикала спирта при наличии трех и более углеродных атомов.
Изомерия положения функциональной группы:
Межклассовая изомерия также определяется общей формулой органических соединений. Например:
Физические свойства сложных эфиров
Агрегатное состояние сложного эфира напрямую зависит от молекулярной массы образующих его кислоты и спирта. Так, например, сложные эфиры низших и средних гомологов являются летучими жидкостями с характерным запахом. Чаще всего у них фруктовые или плодовые ароматы. Сложные эфиры хуже растворяются в воде, чем образующие их кислоты и спирты. Чем больше атомов углерода в составе сложного эфира, тем хуже его растворимость в воде.
Эфиры высших карбоновых кислот и высших одноатомных первичных спиртов — основа природного воска. Например, известный пчелиный воск — это сложный эфир пальмитиновой кислоты (C15H31COOH) и мирицилового спирта (С31H63OH).
Химические свойства сложных эфиров
Сложные эфиры подвергаются гидролизу (разложению под действием воды), который бывает двух видов: в кислой среде и в щелочной. Рассмотрим каждый из этих видов.
В кислой среде реакция протекает следующим образом:
Эта реакция обратима, так как образующиеся в процессе кислота и спирт подвергаются взаимодействию с образованием этого же сложного эфира. Обратная реакция имеет название реакция этерификации.
Щелочной гидролиз или реакция омыления:
Этот вид гидролиза протекает необратимо, так как образовавшаяся в ходе реакции соль не может реагировать со спиртом.
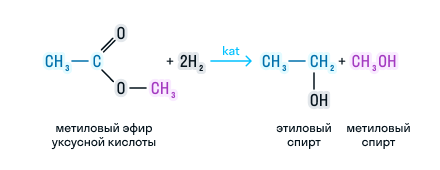
Сложные эфиры можно восстановить водородом в присутствии катализатора до двух спиртов. Причем один из спиртов будет иметь в составе столько атомов углерода, сколько было в кислоте, а во втором спирте количество углерода будет соответствовать исходному спирту. Рассмотрим на примере:
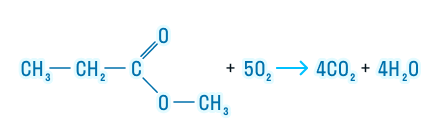
Эфиры подвергаются полному окислению, то есть горят с образованием углекислого газа и воды:
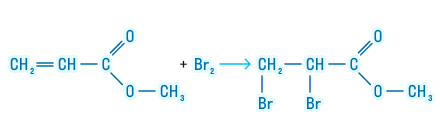
Следующее химическое свойство относится только к тем сложным эфирам, которые образованы непредельной карбоновой кислотой. Сложные эфиры таких кислот могут подвергаться галогенированию. Посмотрим, как происходит эта реакция:
Способы получения сложных эфиров
Реакция обратимая, поэтому требуется либо избыток одного из реагентов, либо отгонка образующегося сложного эфира, чтобы предотвратить обратную реакцию гидролиза.
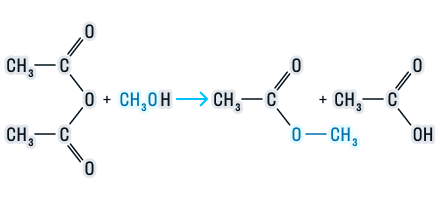
Взаимодействие ангидрида карбоновой кислоты со спиртом с образованием сложного эфира и карбоновой кислоты.
Взаимодействие солей карбоновых кислот с галогеналканами.
Нахождение сложных эфиров в природе и применение
Сложные эфиры широко представлены в природе, но их количество минимально. Они участвуют в процессах, которые протекают в живых организмах, а также являются компонентами аромата ряда растений.
Некоторые эфиры получают искусственным способом. Например, за грушевый вкус в лимонаде отвечает уксусноизоамиловый эфир, а за яблочный — изовалерианоэтиловый эфир.
Помимо пищевой промышленности, сложные эфиры применяют в качестве растворителей для приготовления лаков, а также как пластификаторы для приготовления пластических масс.
Сложные эфиры на основе ароматических спиртов нашли применение в парфюмерной промышленности.
http://chemege.ru/slozhnye-efiry/
http://skysmart.ru/articles/chemistry/slozhnye-efiry