Взаимодействие этилена с бромной водой
Наличие кратной связи в молекуле этилена можно определить пропусканием этилена через раствор брома Br2 в воде (бромной воды) жёлтого цвета. Бромная вода быстро обесцвечивается. Бром присоединяется к этилену, при этом разрушается двойная связь.
Так при помощи бромной воды можно определить, что этилен — непредельный углеводород.
Реакция этилена с раствором перманганата калия
Наличие кратной связи вмолекуле этилена можно определить пропусканием этилена через подкисленный раствор перманганата калия KMnO4 розового цвета. В процессе реакции этилен будет окисляться до двухатомного спирта — этиленгликоля, при этом происходит обесцвечивание раствора перманганата калия.
Эта реакция является качественной реакцией на двойную связь.
Практ. 1
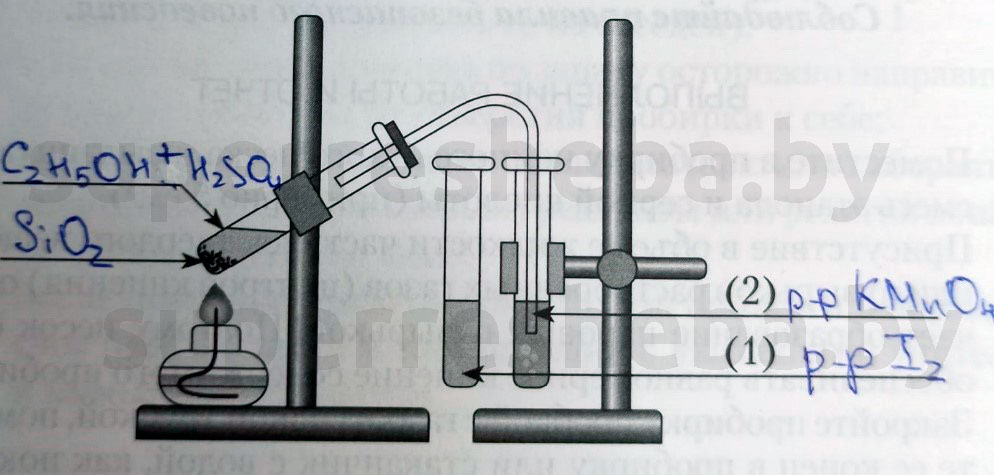
Напишите над стрелками формулы или названия веществ в пробирках.
Объясните явления, которые наблюдаются в процессе получения этилена.
В процессе получения мы наблюдали появление пузырьков газа и обесцвечивание растворов иода и перманганата калия. (Причины обесцвечивания приведены далее).
Приведите уравнение реакции получения этилена.
+ ° C 2 H 4 ↑ + H 2 O .
Объясните явления, наблюдаемые при пропускании этилена в пробирки с растворами иода (1) и перманганата калия (2).
В процессе получения этилена мы наблюдали обесцвечивание растворов иода и перманганата калия, потому что образовывались бесцветные продукты реакции. Раствор перманганата обесцвечивался, т.к. в ходе реакции перманганат переходил в щелочь и оксид марганца (IV), а раствора иода – потому что молекулы иода встраивались в молекулу этилена.
Приведите уравнения реакции этилена с раствором иода.
Приведите схему реакции этилена с раствором K M n O 4 \mathrm
Приведите уравнение реакции горения этилена.
1. Напишите, благодаря наличию какого структурного фрагмента в молекулах алкенов они вступают в реакции с иодной и бромной водой. К какому типу относятся данные реакции?
Алкены вступают в реакции с иодной и бромной водой благодаря наличию двойной связи. Эти реакции относятся к реакциям присоединения.
2. В каких условиях реагируют с бромом алканы? К какому типу относится реакция алканов с бромом?
Алканы реагируют с бромом на свету. Это реакция замещения.
3. Сравните отношение к бромной воде алканов и алкенов. Можно ли различить этан и этен при помощи бромной воды?
Да, можно. При пропускании этана через бромную воду раствор брома не будет обесцвечиваться, а при пропускании этена — будет.
Уравнение реакции этилена с бромной водой
FOR-DLE.ru — Всё для твоего DLE 😉
Привет, я Стас ! Я занимаюсь так называемой «вёрсткой» шаблонов под DataLife Engine.
На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх.
Раньше я занимался простой вёрсткой одностраничных, новостных и т.п. шаблонов на HTML, Bootstrap. Однажды увидев сайты на DLE решил склеить пару шаблонов и выложить их в интернет. В итоге эта парочка шаблонов набрала неплохую популярность и хорошие отзывы, и я решил создать отдельный проект.
Кроме шаблонов я так же буду выкладывать полезную информацию для DataLife Engin и «статейки» для веб мастеров. Так же данный проект будет очень полезен для новичков и для тех, кто хочет правильно содержать свой сайт на DataLife Engine. Надеюсь моя работа вам понравится и вы поддержите этот проект. Как легко и удобно следить за обновлениями на сайте?
Достаточно просто зарегистрироваться на сайте, и уведомления о каждой новой публикации будут приходить на вашу электронную почту!
Задание 1
Возможно ли протекание окисления без восстановления? Почему? Невозможно, т.к. это противоположные взаимосвязанные процессы: при окислительно-восстановительных реакциях происходит переход электронов от восстановителя к окислителю.
Задание 2
Какие из четырёх типов реакций: соединения, разложения, замещения и обмена ― относятся к окислительно-восстановительным не относятся к окислительно-восстановительным могут быть и теми, и другими? Подтвердите своё мнение уравнениями соответствующих реакций. К окислительно-восстановительным относятся все реакции замещения, а также те реакции соединения и разложения, в которых участвует хотя бы одно простое вещество.
Zn 0 + H +1 Cl = Zn +2 Cl2 + H2 0 ↑
S +4 O2 -2 + O2 0 = S +6 O3 -2
2K +1 Cl +5 O3 -2 MnO2 ⟶ 2K +1 Cl -1 + O2 0
Задание 3
Почему аммиак проявляет только восстановительные свойства, а азотная кислота – только окислительные? Азот в аммиаке находится в минимальной степени окисления -3, а азот в азотной кислоте ― в максимальной степени окисления +5
Задание 4
Рассчитайте степени окисления элементов в веществах: H2SO4, H2SO3, Al2(SO4)3, Ca3(PO4)2, H4P2O7, C2H2, C6H6, HCHO.
Ответ: H2 +1 S +6 O 4 −2 , H2 +1 S +4 O3 −2 , Al2 +3 (S +6 O4 −2 )3, Ca3 +2 (P +5 O4 −2 )2, H4 +1 P2 +5 O7 −2 , C2 −1 H2 +1 , C6 −1 H6 +1 , H +1 C 0 H +1 O −2
Соединение H2SO4. Степень окисления водорода +1, а кислорода -2. В соединении H 2SO4 обозначим степень окисления серы через х: H 2 +1 S х O4 -2 , принимая во внимание свойство электронейтральности вещества, получим уравнение: 2•1+х+4 •(-2) =0, отсюда имеем х=8-2=6. Степень окисления серы равна +6.
Соединение H2SO3. Степень окисления водорода +1, а кислорода -2. В соединении H 2SO3 обозначим степень окисления серы через х: H 2 +1 S х O3 -2 , принимая во внимание свойство электронейтральности вещества, получим уравнение: 2•1+х+3 •(-2) =0, отсюда имеем х=6-2=4. Степень окисления серы равна +4.
Соединение Al2(SO4)3. Степень окисления алюминия +3, а кислорода -2. В соединении Al2(SO4)3 обозначим степень окисления серы через х: Al 2 +3 (S х O4 -2 )3, принимая во внимание свойство электронейтральности вещества, получим уравнение: 2•3+ 3 • х+12 •(-2) =0, отсюда имеем х=(24-6):3=6. Степень окисления серы равна +6.
Соединение Ca3(PO4)2. Степень окисления кальция +2, а кислорода -2. В соединении Ca3(PO4)2 обозначим степень окисления фосфора через х: Ca3 +2 (P х O4 -2 )2, принимая во внимание свойство электронейтральности вещества, получим уравнение: 2•3+2 • х+8 •(-2) =0, отсюда имеем х=(16-6):2=5. Степень окисления фосфора равна +5.
Соединение H4P2O7. Степень окисления водорода +1, а кислорода -2. В соединении H4P2O7 обозначим степень окисления фосфора через х: H4 +1 P2 х O7 -2 , принимая во внимание свойство электронейтральности вещества, получим уравнение: 4•1+2 • х+7 •(-2) =0, отсюда имеем х=(14-4):2=5. Степень окисления фосфора равна +5.
Соединение C2H2. Степень окисления водорода +1. В соединении C2H2 обозначим степень окисления углерода через х: C2 х H2 +1 , принимая во внимание свойство электронейтральности вещества, получим уравнение: 2 • х+2 •1 =0, отсюда имеем х=-2:2=-1. Степень окисления углерода равна -1.
Соединение C6H6. Степень окисления водорода +1. В соединении C6H6 обозначим степень окисления углерода через х: C6 х H6 +1 , принимая во внимание свойство электронейтральности вещества, получим уравнение: 6 • х+6 •1 =0, отсюда имеем х=-6:6=-1. Степень окисления углерода равна -1.
Соединение HCHO. Степень окисления водорода +1 , а кислорода -2. В соединении HCHO обозначим степень окисления углерода через х: H +1 C х H +1 O-2, принимая во внимание свойство электронейтральности вещества, получим уравнение: 1+ х+1-2=0, отсюда имеем х=1-1=0. Степень окисления углерода равна 0.
Задание 5
Методом электронного баланса уравняйте окислительно-восстановительные реакции, схемы которых:
а) Al + CuCl2 ⟶ AlCl3 + Cu
Al 0 + Cu +2 Cl2 ⟶ Al +3 Cl3 + 3Cu 0
Cu +2 +2ē ⟶ Cu 0 |2|6|3 ― процесс восстановления
Al 0 -3ē ⟶ Al +3 |3| |2 ― процесс окисления
Проводим вертикальную черту и пишем за ней число электронов, которые присоединили и отдали атомы меди и алюминия. Находим наименьшее общее кратное для чисел 2 и 3. Это число 6, которое записываем за второй вертикальной чертой посередине, и поделив его поочередно на 2 и 3, записываем результат за третьей чертой в строках, касающихся элементов меди и алюминия. Множители 3 и 2 являются искомыми коэффициентами. Поскольку элементы изменили степень окисления полностью (в правой части схемы эти элементы ни в одном веществе не проявляют такую же степень окисления, как в исходном веществе) и одинаковыми являются индексы этих элементов в формуле исходного вещества и продукта реакции, поэтому коэффициент 3 ставим перед формулами двух соединений меди (CuCl2, Cu) и коэффициент 2 — перед формулами двух соединений алюминия (Al, AlCl3).
2Al + 3CuCl2 = 2AlCl3 + 3Cu
В приведённой реакции алюминий — восстановитель, а хлорид меди (II) (за счёт атомов меди в степени окисления +2) — окислитель.
б) NH3 + CuO ⟶ N2 + H2O + Cu,
N -3 H3 + Cu +2 O ⟶ N2 0 + H2O + Cu 0
Cu +2 +2ē ⟶ Cu 0 |2|6|3 ― процесс восстановления
2N -3 -6ē ⟶ N2 0 |6| |1 ― процесс окисления
Проводим вертикальную черту и пишем за ней число электронов, которые присоединили и отдали атомы меди и азота. Находим наименьшее общее кратное для чисел 2 и 6. Это число 6, которое записываем за второй вертикальной чертой посередине, и поделив его поочередно на 2 и 6, записываем результат за третьей чертой в строках, касающихся элементов меди и азота. Множители 3 и 1 являются искомыми коэффициентами. Поскольку элементы изменили степень окисления полностью (в правой части схемы эти элементы ни в одном веществе не проявляют такую же степень окисления, как в исходном веществе) и одинаковыми являются индексы элемента меди в формуле исходного вещества и продукта реакции, поэтому ставим коэффициент 3 перед формулами двух соединений меди (CuO, Cu), а разными являются коэффициенты азота — коэффициент 1 (относится к двум атомам азота) перед формулой азота N2.
NH3 + 3CuO ⟶ N2 + H2O + 3Cu
Подбираем коэффициенты для остальных соединений. Получим уравнение:
2NH3 + 3CuO = N2 + 3H2O + 3Cu
в) KClO3 + S ⟶ KCl + SO2
KCl +5 O3 + S 0 ⟶ KCl -1 + S +4 O2
Cl +5 +6ē ⟶ Cl -1 |6|12|2 ― процесс восстановления
S 0 -4ē ⟶ S +4 |4| |3 ― процесс окисления
Проводим вертикальную черту и пишем за ней число электронов, которые присоединили и отдали атомы хлора и серы. Находим наименьшее общее кратное для чисел 6 и 4. Это число 12, которое записываем за второй вертикальной чертой посередине, и поделив его поочередно на 6 и 4, записываем результат за третьей чертой в строках, касающихся элементов хлора и серы. Множители 2 и 3 являются искомыми коэффициентами. Поскольку элементы изменили степень окисления полностью (в правой части схемы эти элементы ни в одном веществе не проявляют такую же степень окисления, как в исходном веществе) и одинаковыми являются индексы этих элементов в формуле исходного вещества и продукта реакции, поэтому коэффициент 2 ставим перед формулами двух соединений хлора (KClO3, KCl) и коэффициент 3 — перед формулами двух соединений серы (S, SO2).
2KClO3 + 3S = 2KCl + 3SO2
г) H2SO4 (конц.) + Zn ⟶ ZnSO4 + H2S + H2O
H2S +6 O4 + Zn 0 ⟶ Zn +2 S +6 O4 + H2S -2 + H2O
S +6 +8ē ⟶ S -2 |8|8|1 ― процесс восстановления
Zn 0 -2ē ⟶ Zn +2 |2| |4 ― процесс окисления
Проводим вертикальную черту и пишем за ней число электронов, которые присоединили и отдали атомы серы и цинка. Находим наименьшее общее кратное для чисел 8 и 2. Это число 8, которое записываем за второй вертикальной чертой посередине, и поделив его поочередно на 8 и 2, записываем результат за третьей чертой в строках, касающихся элементов серы и цинка. Множители 1 и 4 являются искомыми коэффициентами. Поскольку элемент цинк изменил степень окисления полностью (в правой части схемы этот элемент ни в одном веществе не проявляет такую же степень окисления, как в исходном веществе) и одинаковыми являются индексы этого элемента в формуле исходного вещества и продукта реакции, поэтому ставим коэффициент 4 перед формулами двух соединений цинка (Zn, ZnSO4). Поскольку элемент сера изменил степень окисления не полностью, поэтому ставим коэффициент 1 только перед формулой сероводорода H2S:
H2SO4 (конц.) + 4Zn ⟶ 4ZnSO4 + H2S↑ + H2O
Подбираем коэффициенты для остальных соединений. Получим уравнение:
5H2SO4 (конц.) + 4Zn = 4ZnSO4 + H2S↑ + 4H2O
Задание 6
Дайте характеристику реакции цинка с соляной кислотой по всем возможным признакам классификации реакций.
Zn + 2HCl ⟶ ZnCl2 + H2↑
Реакция замещения, экзотермическая, необратимая, гетерогенная, некаталитическая, окислительно-восстановительная .
Задание 7
Рассмотрите взаимодействие этилена с бромной водой с позиции окисления-восстановления.
C2H4 + Br2 = C2H4Br2
C2 +2 H4 + Br2 0 ⟶ C2 +3 H4Br2 -1
C +2 +1ē ⟶ C +3 |1|х 2 ― процесс восстановления
Br2 0 -2ē ⟶ 2Br -1 |2|х 1 ― процесс окисления
Проводим вертикальную черту и пишем за ней число электронов, которые присоединили и отдали атомы углерода и брома. Находим наименьшее общее кратное для чисел 1 и 2 ― это число 2 и, поделив его поочередно на 1 и 2, записываем результат за второй чертой в строках, касающихся элементов углерода и брома. Множители 2 и 1 являются искомыми множителями. Сложим левые и правые части уравнений полуреакций, умножив их на дополнительные множители 2 и 1:
2C +2 + 2ē + Br2 0 — 2ē ⟶ 2C +3 + 2Br -1
2C +2 + Br2 0 ⟶ 2C +3 + 2Br -1
Эти коэффициенты переносим в уравнение реакции (имея в виду, что в формулах C2H4 и C2H4Br2 уже указаны два атома углерода и два атома брома).
В приведённой реакции бром — восстановитель, а этилен (за счёт атомов углерода в степени окисления +2) — окислитель.
http://superresheba.by/resh/54116
http://gdz.cool/h11_gos_2019/1295-h11_gos_2019____14.html