Процесс гликолиза его реакции, аэробный и анаэробный (Таблица, схема)
Гликолиз — процесс окисления глюкозы, при котором из одной молекулы глюкозы образуются две молекулы пировиноградной кислоты, не является мембранозависимым процессом. Он происходит в цитоплазме. Однако ферменты гликолиза связаны со структурами цитоскелета. Суть гликолиза состоит в том, что молекула глюкозы (C6H12O6) без участия кислорода распадается на две молекулы пировиноградной кислоты (СН3СОСООН). При этом окисление идет за счет отщепления от молекулы глюкозы четырех атомов водорода, связывающихся со сложным органическим веществом НАД с получением двух молекул НАД•Н. Выделяющаяся при этом энергия запасается (40% от общего количества) в виде макроэргических связей двух молекул АТФ. 60% энергии выделяется в виде тепла. При последующем окислении НАД•Н получается еще 6 молекул АТФ. Таким образом, полный энергетический выход гликолиза в анаэробных условиях составляет 8 молекул АТФ.
Аэробный процесс гликолиза (10 реакций), уравнение (с образованием пирувата):
Анаэробный процесс гликолиза (11 реакций), уравнение (с образованием лактата):
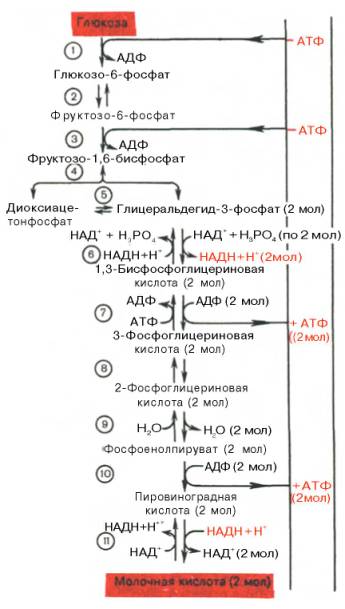
Схема процесса гликолиза и его реакции
На схеме в рамках обозначены исходные субстраты и конечные продукты гликолиза, цифрами в скобках — число молекул.
ATP (АТФ) — это аденозинтрифосфорная кислота, универсальный источник энергии
ADP (АДФ) — это аденозиндифосфат, нуклеотид, участвует в энергетическом обмене
NAD (НАД) — никотинамидадениндинуклеотидфосфата
NADH (НАД•Н) — востановленная форма NAD
Таблица процесс гликолиза его реакции
Для распада и частичного окисления молекулы глюкозы требуется протекание 11 сложных последовательных реакций.
Ферменты, Активаторы, ингибиторы
Подготовительная стадия гликолиза
Стадия активации глюкозы проходит в 5 реакций, в ходе которых 1 молекула гексозы (глюкозы) расщепляется на 2 молекулы триоз-глицеральдегидфосфата
1. Необратимая реакция фосфорилирования глюкозы
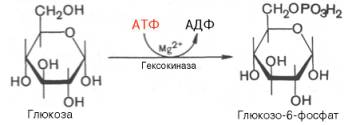
Процесс гликолиза начинается с фосфорилирования глюкозы за счет АТФ — первая реакция. Это первая пусковая реакция гликолиза. Ее результатом является глюкозо-6-фосфат, имеющий отрицательный заряд. В гликолизе может участвовать не только глюкоза, но и другие гексозы (фруктоза), но в результате фосфорилирования и активации все равно образуется глюкозо-6-фосфат.
Ингибиторы: глюкозо-6-Ф, фосфоенолпируват.
2. Обратимая реакция изомеризации глюкозо-6-фосфата
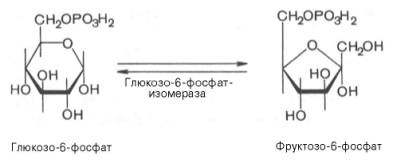
Во второй реакции происходит изомеризация (внутримолекулярные перестройки) глюкозо-6-фосфата во фруктозо-6-фосфат.
3. Необратимая реакция фосфорилирования фруктозо-6-фосфата (ключевая стадия гликолиза)
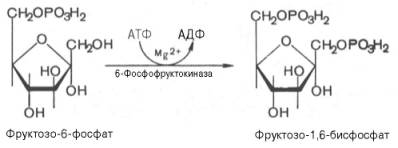
В третьей реакции происходит фосфорилирование (присоединение остатка ортофосфорной кислоты) фруктозо-6-фосфата с образованием фруктозо-1,6-дифосфата. При этом затрачивается еще одна молекула АТФ (уже вторая) — это вторая пусковая реакция гликолиза. Она идет в присутствии Mg2 + и является необратимой, так как сопровождается масштабным уменьшением свободной энергии.
Ингибиторы: АТФ, цитрат, НАДН.
4. Обратимая реакция дихотомического расщепления фруктозо-1,6-дифосфата
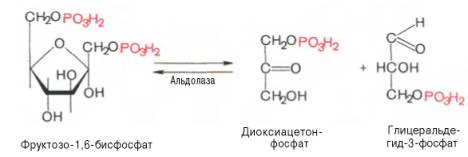
В четвертой реакции гликолиза происходит расщепление фруктозо-1,6-дифосфата на две молекулы глицеральдегид-3-фосфата.
5. Обратимая реакция изомеризации дигидроксиацетона-3-фосфат в глицеральдегид-3-фосфат
В пятой реакции происходит изомеризация полученных триозофосфатов. На этом заканчивается первая стадия гликолиза.
Стадия генерации АТФ
Проходит в 6 реакций (или 5), в ходе которых энергия окислительных реакций трансформируется в химическую энергию АТФ (субстратное фосфорилирование).
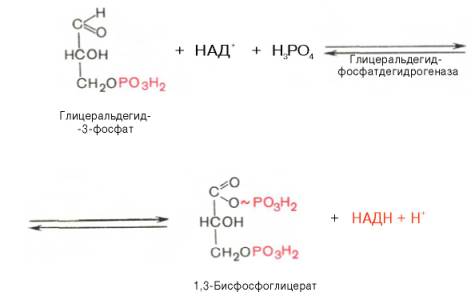
6. Окисление глицеральдегид-3-фосфата до 1,3-дифосфоглицерата (реакция гликолитической оксиредукции)
В шестой реакции происходит окисление альдегидной группы до карбоксильной. Выделившийся Н+ акцептируется NAD, который восстанавливается до NADH. Освобождающаяся энергия затрачивается для образования высокоэнергетической связи 1,3-бифосфоглицерата (1,3-бифосфоглицериновая кислота).
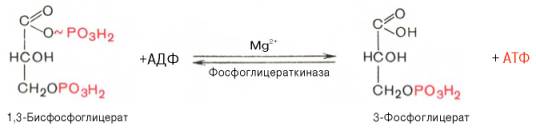
7. Субстратное фосфорилирование АДФ (7)
В седьмой реакции фосфорильная группа 1,3-бифосфоглицерата переносится на ADP, в результате чего образуется АТР (напоминаем, что следует иметь в виду две параллельные цепи реакций, с участием двух молекул триоз, образовавшихся из одной молекулы гексозы, следовательно, синтезируется не одна, а две молекулы АТР).
8. Реакция изомеризации 3-фосфоглицерата в 2-фосфоглицерат
В восьмой реакции гликолиза происходит перенос фосфатной группы с третьего атома углерода на второй. В результате образуется 2-фосфоглицерат (2-фосфоглицериновая кислота).
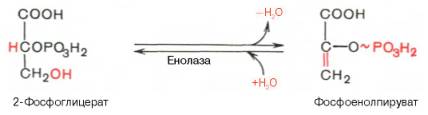
9. Реакция енолизации
Девятая реакция сопровождается внутримолекулярными окислительно-восстановительными процессами, в результате которых образуется фосфоенолпируват (фосфоенолпировиноградная кислота) с высокоэнергетической связью во втором атоме углерода и отщепляется молекула воды
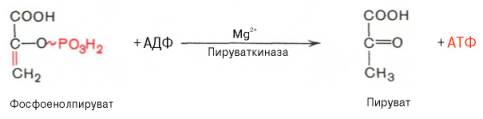
10. Реакция субстратного фосфорилирования
В ходе десятой реакции фосфорильная группа переносится на ADP. При этом синтезируется АТР и пируват (пировиноградная кислота). Эта реакция также необратима, поскольку высокоэкзергонична.
11. Реакция обратимого восстановления пировиноградной кислоты до молочной кислоты (в анаэробных условиях)
Если после гликолиза следует аэробное расщепление, пируват мигрирует в матрикс митохондрий, где, взаимодействуя с коэнзимом-А, участвует в образовании ацетил-СоА. В анаэробных условиях пируват при участии NADH восстанавливается до лактата (молочной кислоты), который при этом является конечным продуктом гликолиза. Затем в аэробных условиях лактат может обратно превратиться в пируват и окислиться в митохондриях.
_______________
Источник информации:
1. Биология для поступающих в вузы / Г.Л. Билич, В.А. Крыжановский. — 2008.
2. Биология в таблицах и схемах / Спб. — 2004.
3. Биохимия в схемах и таблицах / И. В. Семак — Минск — 2011.
ГЛИКОЛИЗ
Гликолиз (от греч. glycys – сладкий и lysis – растворение, распад) – это последовательность ферментативных реакций, приводящих к превращению глюкозы в пируват с одновременным образованием АТФ.
При аэробных условиях пируват проникает в митохондрии, где полностью окисляется до СО2 и Н2О. Если содержание кислорода недостаточно, как это может иметь место в активно сокращающейся мышце, пируват превращается в лактат.
Итак, гликолиз – не только главный путь утилизации глюкозы в клетках, но и уникальный путь, поскольку он может использовать кислород, если
последний доступен (аэробные условия), но может протекать и в отсутствие кислорода (анаэробные условия).
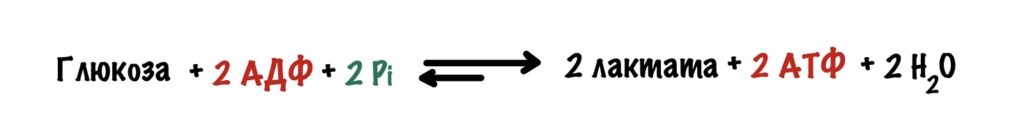
Анаэробный гликолиз – сложный ферментативный процесс распада глюкозы, протекающий в тканях человека и животных без потребления кислорода. Конечным продуктом гликолиза является молочная кислота. В процессе гликолиза образуется АТФ. Суммарное уравнение гликолиза можно представить следующим образом:
В анаэробных условиях гликолиз – единственный процесс в животном организме, поставляющий энергию. Именно благодаря гликолизу организм человека и животных определенный период может осуществлять ряд физиологических функций в условиях недостаточности кислорода. В тех случаях, когда гликолиз протекает в присутствии кислорода, говорят об аэробном гликолизе .
Последовательность реакций анаэробного гликолиза, так же как и их промежуточные продукты, хорошо изучена. Процесс гликолиза катализируется одиннадцатью ферментами, большинство из которых выделено в гомогенном, клисталлическом или высокоочищенном виде и свойства которых достаточно известны. Заметим, что гликолиз протекает в гиало-плазме (цитозоле) клетки.
Первой ферментативной реакцией гликолиза является фосфорилирование, т.е. перенос остатка ортофосфата на глюкозу за счет АТФ. Реакция катализируется ферментом гексокиназой:
Образование глюкозо-6-фосфата в гексокиназной реакции сопровождается освобождением значительного количества свободной энергии системы и может считаться практически необратимым процессом.
Наиболее важным свойством гексокиназы является ее ингибирование глюкозо-6-фосфатом, т.е. последний служит одновременно и продуктом реакции, и аллостерическим ингибитором.
Фермент гексокиназа способен катализировать фосфорилирование не только D-глюкозы, но и других гексоз, в частности D-фруктозы, D-маннозы и т.д. В печени, кроме гексокиназы, существует фермент глюкокиназа, который катализирует фосфорилирование только D-глюкозы. В мышечной ткани этот фермент отсутствует (подробнее см. главу 16).
Второй реакцией гликолиза является превращение глюкозо-6-фос-фата под действием фермента глюкозо-6-фосфатизомеразы во фруктозо-6-фосфат:
Эта реакция протекает легко в обоих направлениях, и для нее не требуется каких-либо кофакторов.
Третья реакция катализируется ферментом фосфофруктокиназой; образовавшийся фруктозо-6-фосфат вновь фосфорилируется за счет второй молекулы АТФ:
Данная реакция аналогично гексокиназной практически необратима, протекает в присутствии ионов магния и является наиболее медленно текущей реакцией гликолиза. Фактически эта реакция определяет скорость гликолиза в целом.
Фосфофруктокиназа относится к числу аллостерических ферментов. Она ингибируется АТФ и стимулируется АМФ . При значительных величинах отношения АТФ/АМФ активность фосфофруктокиназы угнетается и гликолиз замедляется. Напротив, при снижении этого коэффициента интенсивность гликолиза повышается. Так, в неработающей мышце активность фосфофруктокиназы низкая, а концентрация АТФ относительно высокая. Во время работы мышцы происходит интенсивное потребление АТФ и активность фосфофруктокиназы повышается, что приводит к усилению процесса гликолиза.
Четвертую реакцию гликолиза катализирует фермент альдолаза. Под влиянием этого фермента фруктозо-1,6-бисфосфат расщепляется на две фосфотриозы:
Эта реакция обратима. В зависимости от температуры равновесие устанавливается на различном уровне. При повышении температуры реакция сдвигается в сторону большего образования триозофосфатов (дигидро-ксиацетонфосфата и глицеральдегид-3-фосфата).
Пятая реакция – это реакция изомеризации триозофосфатов. Катализируется ферментом триозофосфатизомеразой:
Равновесие данной изомеразной реакции сдвинуто в сторону дигид-роксиацетонфосфата: 95% дигидроксиацетонфосфата и около 5% глице-ральдегид-3-фосфата. В последующие реакции гликолиза может непосредственно включаться только один из двух образующихся триозофосфатов, а именно глицеральдегид-3-фосфат. Вследствие этого по мере потребления в ходе дальнейших превращений альдегидной формы фосфотриозы ди-гидроксиацетонфосфат превращается в глицеральдегид-3-фосфат.
Образованием глицеральдегид-3-фосфата как бы завершается первая стадия гликолиза. Вторая стадия – наиболее сложная и важная. Она включает окислительно-восстановительную реакцию (реакция гликолитической оксидоредукции), сопряженную с субстратным фосфорилированием, в процессе которого образуется АТФ.
В результате шестой реакции глицеральдегид-3-фосфат в присутствии фермента глицеральдегидфосфатдегидрогеназы, кофермента НАД и неорганического фосфата подвергается своеобразному окислению с образованием 1,3-бисфосфоглицериновой кислоты и восстановленной формы НАД (НАДН). Эта реакция блокируется йод- или бромацетатом, протекает в несколько этапов:
1,3-Бисфосфоглицерат представляет собой высокоэнергетическое соединение (макроэргическая связь условно обозначена знаком «тильда»
). Механизм действия глицеральдегидфосфатдегидрогеназы сводится к следующему: в присутствии неорганического фосфата НАД + выступает как акцептор водорода, отщепляющегося от глицеральдегид-3-фосфата. В процессе образования НАДН глицеральдегид-3-фосфат связывается с молекулой фермента за счет SH-групп последнего. Образовавшаяся связь богата энергией, но она непрочная и расщепляется под влиянием неорганического фосфата, при этом образуется 1,3-бисфосфоглицериновая кислота.
Седьмая реакция катализируется фосфоглицераткиназой, при этом происходит передача богатого энергией фосфатного остатка (фосфатной группы в положении 1) на АДФ с образованием АТФ и 3-фосфогли-цериновой кислоты (3-фосфоглицерат):
Таким образом, благодаря действию двух ферментов (глицеральде-гидфосфатдегидрогеназы и фосфоглицераткиназы) энергия, высвобождающаяся при окислении альдегидной группы глицеральдегид-3-фосфата до карбоксильной группы, запасается в форме энергии АТФ. В отличие от окислительного фосфорилирования образование АТФ из высокоэнергетических соединений называется субстратным фосфорилированием.
Восьмая реакция сопровождается внутримолекулярным переносом оставшейся фосфатной группы, и 3-фосфоглицериновая кислота превращается в 2-фосфоглицериновую кислоту (2-фосфоглицерат).
Реакция легкообратима, протекает в присутствии ионов Mg 2+ . Кофактором фермента является также 2,3-бисфосфоглицериновая кислота аналогично тому, как в фосфоглюкомутазной реакции роль кофактора выполняет глюкозо-1,6-бисфосфат:
Девятая реакция катализируется ферментом енолазой, при этом 2-фосфоглицериновая кислота в результате отщепления молекулы воды переходит в фосфоенолпировиноградную кислоту (фосфоенолпируват), а фосфатная связь в положении 2 становится высокоэргической:
Енолаза активируется двухвалентными катионами Mg 2+ или Мn 2+ и ингибируется фторидом.
Десятая реакция характеризуется разрывом высокоэргической связи и переносом фосфатного остатка от фосфоенолпирувата на АДФ (субстратное фосфорилирование). Катализируется ферментом пируваткиназой:
Для действия пируваткиназы необходимы ионы Mg 2+ , а также одновалентные катионы щелочных металлов (К + или др.). Внутри клетки реакция является практически необратимой.
В результате одиннадцатой реакции происходит восстановление пировиноградной кислоты и образуется молочная кислота. Реакция протекает при участии фермента лактатдегидрогеназы и кофермента НАДН, образовавшегося в шестой реакции:
Последовательность протекающих при гликолизе реакций представлена на рис. 10.3.
Рис. 10.3. Последовательность реакций гликолиза.
1 — гексокиназа; 2 — фосфоглюкоизоме-раза; 3 — фосфофруктокиназа; 4 — альдо-лаза; 5 — триозофосфатизомераза; 6 — гли-церальдегидфосфатдегидрогеназа; 7 -фосфоглицераткиназа; 8 — фосфоглицеромутаза; 9 — енолаза; 10 — пируватки-наза; 11 — лактатдегидрогеназа.
Реакция восстановления пирувата завершает внутренний окислительно-восстановительный цикл гликолиза. НАД + при этом играет роль промежуточного переносчика водорода от глицеральдегид-3-фосфата (6-я реакция) на пировиноградную кислоту (11-я реакция), при этом сам он регенерируется и вновь может участвовать в циклическом процессе, получившем название гликолитический оксидоредукции.
Биологическое значение процесса гликолиза заключается прежде всего в образовании богатых энергией фосфорных соединений. На первых стадиях гликолиза затрачиваются 2 молекулы АТФ (гексокиназная и фосфофрук-токиназная реакции). На последующих образуются 4 молекулы АТФ (фосфоглицераткиназная и пируваткиназная реакции). Таким образом, энергетическая эффективность гликолиза в анаэробных условиях составляет 2 молекулы АТФ на одну молекулу глюкозы.
Как отмечалось, основной реакцией, лимитирующей скорость гликолиза, является фосфофруктокиназная. Вторая реакция, лимитирующая скорость и регулирующая гликолиз – гексокиназная реакция. Кроме того, контроль гликолиза осуществляется также ЛДГ и ее изоферментами.
В тканях с аэробным метаболизмом (ткани сердца, почек и др.) преобладают изоферменты ЛДГ1 и ЛДГ2 (см. главу 4). Эти изоферменты инги-бируются даже небольшими концентрациями пирувата, что препятствует образованию молочной кислоты и способствует более полному окислению пирувата (точнее, ацетил-КоА) в цикле трикарбоновых кислот.
В тканях человека, в значительной степени использующих энергию гликолиза (например, скелетные мышцы), главными изоферментами являются ЛДГ5 и ЛДГ4. Активность ЛДГ5 максимальна при тех концентрациях пирувата, которые ингибируют ЛДГ1. Преобладание изоферментов ЛДГ4 и ЛДГ5 обусловливает интенсивный анаэробный гликолиз с быстрым превращением пирувата в молочную кислоту.
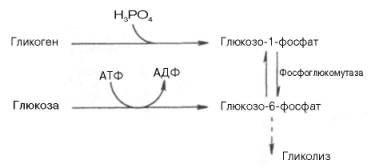
Как отмечалось, процесс анаэробного распада гликогена получил название гликогенолиза. Вовлечение D-глюкозных единиц гликогена в процесс гликолиза происходит при участии 2 ферментов – фосфорилазы а и фосфо-глюкомутазы. Образовавшийся в результате фосфоглюкомутазной реакции глюкозо-6-фосфат может включаться в процесс гликолиза. После образования глюкозо-6-фосфата дальнейшие пути гликолиза и гликогенолиза полностью совпадают:
В процессе гликогенолиза в виде макроэргических соединений накапливаются не две, а три молекулы АТФ (АТФ не тратится на образование глюкозо-6-фосфата). Кажется, что энергетическая эффективность глико-генолиза выглядит несколько более высокой по сравнению с процессом гликолиза, но эта эффективность реализуется только при наличии активной фосфорилазы а. Следует иметь в виду, что в процессе активации фосфо-рилазы b расходуется АТФ (см. рис. 10.2).
Гликолиз и его субстраты
Гликолиз — это катаболизм глюкозы до двух молекул пировиноградной кислоты. Не слишком понятное определение, но сейчас попытаемся прояснить его.
Катаболизм — это окисление молекулы до более простой/простых с выделением энергии. Наша молекула — глюкоза. А энергия выделяется в виде АТФ и тепла. В химических связях глюкозы запасено много энергии, которая может быть использована организмом. Если мы будем окислять глюкозу до талого, то получим углекислый газ и воду. И кучу энергии! Но это нужно сделать с умом.
Представьте, что мы просто спалим глюкозу в один этап. Так мы получим углекислый газ и воду, да ещё вот такое количество энергии. Это горение молекулы.
В нашем организме такой реакции нет. Это экзотермическая реакция. В ней вся энергия выделяется в виде тепла, а не идёт на синтез полезной батарейки — молекулы АТФ. Если бы так было в организме, то вряд ли наши клетки долго прожили. У них бы быстро случилось профессиональное выгорание.
Организм делает умнее и удобнее. Он постепенно окисляет молекулу глюкозы до углекислого газа и воды — делит окисление на несколько стадий. А стадии делит на реакции. Так молекула глюкозы окисляется до промежуточных продуктов. В ходе этого выделяется энергия, которая запасается в виде АТФ. Часть энергии рассеивается — выделяется тепло.
Весь этот процесс называется катаболизмом глюкозы. Он состоит из гликолиза и общего пути катаболизма.
Гликолиз это первая стадия катаболизма. В ходе него выделяется немного энергии в виде АТФ, но что важнее — мы получаем две молекулы пирувата. Пируват та же пировиноградная кислота. Просто в растворе кислота диссоциирует, а название её иона — пируват.
Почему пируват, а не другая молекула?
Наш организм получает энергию из белков, жиров и углеводов. Можно подумать, что для каждого класса молекул существует отдельный способ вытащить из него энергию. Но это не так. Зачем делать печку для каждого вида дров, если можно сделать одну общую для всех? Таким вопросом задались клетки нашего организма и решили, что лучше сделать одну печь. Эта печь — общий путь катаболизма.
Общий путь катаболизма включает превращение пирувата в ацетил-коэнзим А, цикл трикарбоновых кислот и окислительное фосфорилирование. Видите? Он начинается с пирувата. Потому что:
Пируват объединяет катаболизм белков, жиров и углеводов.
Клетки умнее, чем кажутся. Они решили, что можно сделать не только одну печь, но и один вид дров. Они окисляют белки, жиры и углеводы до одной молекулы — ацетил-коэнзим А. И пируват — это его предшественник. Их отделяет всего одна реакция, поэтому если мы посмотрим на все виды обмена, то увидим такое.
В ходе общего пути катаболизма образуется огромное количество молекул АТФ. Куда больше, чем при гликолизе.
Теперь мы поняли, что гликолиз — это первый этап катаболизма глюкозы. В ходе него образуется немного энергии в виде АТФ. Но что важнее — гликолиз готовит дрова для печи. Или пируват для общего пути катаболизма, как тебе больше нравится.
Гликолиз — это первый этап катаболизма глюкозы
У гликолиза есть и другое название — дихотомическое расщепление глюкозы. Это название заключает главный смысл гликолиза: в ходе него происходит деление молекулы глюкозы надвое.
Этапы гликолиза
Гликолиз идёт в цитоплазме всех клеток нашего организма. Прочитай это ещё раз. Он состоит из двух этапов: подготовительного и энергетического. Мне кажется, что подготовительный этап можно разделить на два шага. Так будет удобнее для понимания.
- Первый шаг. Глюкоза фосфорилируется с затратами двух молекул АТФ — образуется фруктозо-1,6-бисфосфат.
- Второй шаг. Расщепление фруктозо-1,6-бисфосфата с образованием двух молекул фосфотриоз.
На энергетическом этапе из каждой фосфотриозы образуется пируват. На этом этапе образуются 4 молекулы АТФ и 2 молекулы НАДH.
Кажется, что я вас слишком быстро окунул в тему. Не бойтесь, дальше всё будет понятнее. Если что, то нам даже не придётся зубрить все десять реакций. Да-да, их всего десять. Мы выведем всё логически. Нам нужно знать только формулу молекулы глюкозы и пирувата. С чего начинаем и к чему идём. В глюкозе шесть атомов углерода, а в пирувате всего три. Поэтому сначала нужно превратить глюкозу (гексозу) в триозу. За этим и нужен подготовительный этап.
У большинства ферментов название будет по субстратам. Знаем субстрат и продукт реакции — можем назвать фермент. Если хорошо знаем их классы.
Подготовительный этап гликолиза
В нём пять реакций. В процессе поймёте, почему лучше разделить его на два шага.
Первый шаг подготовительного этапа
Наша задача на этом шаге — получить фруктозо-1,6-фосфат.
Первая реакция. Мы начинаем с глюкозы. Она попадает в клетку с помощью глюкозного транспортёра (ГЛЮТ). Проблема в том, что этот транспортёр работает в обе стороны. ГЛЮТ может загонять глюкозу в клетку, а может выкидывать её. Всё зависит от градиента концентрации между кровью и клеткой. Так не пойдёт!
Ещё нам нужно увеличить реакционную способность глюкозы, потому что ей дальше придётся вступать в реакции. Убьём двух зайцев с помощью фосфорилирования! Для этого нам понадобится фермент — гексокиназа/глюкокиназа и молекула АТФ. Глюкокиназа действует в печени, а гексокиназа в других тканях — это изоферменты. Между ними есть отличия, о которых можно прочитать здесь.
В ходе реакции мы получаем глюкозо-6-фосфат. У него больше реакционная способность, чем у глюкозы. А ещё он не может вылететь из клетки — для него нет переносчика в клеточной мембране. Мы загнали глюкозу в ловушку и сделали её менее стабильной.
Для этой реакции нужен кофактор — ион магния. У АТФ огромный отрицательный заряд -4. Из-за этого её трудно загнать в активный центр фермента. Но при присоединении магния заряд уменьшается до -2. Теперь ей легче попасть в активный центр.
Эта реакция необратима, потому что мы затратили энергию макроэргической связи АТФ.
Вторая реакция. Мы превратим глюкозо-6-фосфат в фруктозо-6-фосфат. Зачем? Это пока секрет, но доверьтесь мне — дальше всё станет ясно! Фосфогексоизомераза катализирует эту реакцию.
Реакция идёт в несколько этапов. Сначала фосфогексоизомераза раскрывает циклическую форму глюкозо-6-фосфата — переводит его в линейную. Далее образуется линейная форма фруктозо-6-фосфата. Линейная форма фруктозо-6-фосфата быстро переходит циклическую. Такая форма более стабильна.
Эта реакция обратима
Третья реакция. Из-за того, что прошлая реакция обратима, мы можем опять получить глюкозо-6-фосфат. А он отправится на другие процессы — пентозофосфатный путь, синтез гликогена и всё такое. Нужно закрепить наш успех — отделить молекулу от других процессов. Прицепим ещё одну фосфатную группу к молекуле. Для этого нужна киназа — фосфофруктокиназа — и молекула АТФ. Получаем фруктозо-1,6-бисфосфат.
Клетка опять убила двух зайцев. Отделила гликолиз от других процессов через необратимую реакцию фосфорилирования. И увеличила реакционную способность молекулы. На фруктозо-1,6-бисфосфате суммарный заряд -4. Это слишком много — такая молекула не сможет долго оставаться без изменений.
Этим заканчивается первый шаг подготовительного этапа. В нём произошло несколько важных вещей. Клетка поймала глюкозу в ловушку — теперь она не сможет пройти через биологическую мембрану. С помощью образования фруктозо-1,6-бисфосфата гликолиз отделился от других клеточных процессов. Клетка увеличила реакционную способность глюкозы, превратив её в нестабильный фруктозо-1,6-бисфосфат. На эти важные процессы клетка не поскупилась и потратила две молекулы АТФ.
Как-то даже парадоксально: клетка хочет получить энергию, но при этом тратит её.
Второй шаг подготовительного этапа
Наша задача на этом шаге — получить фосфотриозы.
Четвёртая реакция. Начнём двигаться к образованию пирувата. А в нём все-таки три углеродных атома, а не шесть. Для этого расщепим фруктозо-1,6-бисфосфат с помощью фермента альдолазы. Этот фермент относится к классу лиаз.
Альдолаза раскрывает циклическую форму фруктозо-1,6-бисфосфата. Она действует на середину молекулы — образуется две триозы: дигидроксиацетонфосфат и глицеральдегид-3-фосфат. Если мы знаем формулу фруктозы, то легко можем написать эти продукты. Одна триоза будет кетонной, а другая альдегидной.
В этой реакции кроется причина превращения глюкозо-6-фосфата в фруктозо-6-фосфат. Это тот, который образовался во время второй реакции. Представьте, что мы забили на превращение глюкозо-6-фосфата. И просто отправили его на альдолазную реакцию. Мы бы не получили две триозы. Дело в том, что альдолаза действует через один атом углерода, у которого находится двойная связь.
Все реакции начиная с четвёртой и до десятой будут обратимые. Поэтому я дальше не буду заострять на этом внимание. А может и буду, кто знает)))
Пятая реакция. Хоть мы и получили две триозы, но не каждая может пойти дальше по пути гликолиза. Глицеральдегид-3-фосфат может, а вот дигидроксиацетонфосфат — нет. Нам нужна альдегидная группа для следующих реакций гликолиза. Если внимательно посмотреть на эти молекулы, то можно сказать: «Да они почти одинаковые, может превратим одну в другую?»
Это можно сделать! С помощью фермента триозофосфатизомеразы. Он переводит дигидроксиацетонфосфат в глицеральдегид-3-фосфат. Давайте я переверну молекулу дигидроксиацетонфосфата. Так будет понятнее.
При этой реакции устанавливается константа равновесия. Возьмём за сто процентов количество молекул дигидроксиацетонфосфата (ДГАФ) и глицеральдегид-3-фосфата. 96 % молекул будут в виде ДГАФ, и только 4 % виде глицеральдегид-3-фосфата. Но это не проблема, потому что глицеральдегид-3-фосфат постепенно тратится на реакции гликолиза. Количество его молекул уменьшается. Нужно поддержать константу равновесия, поэтому ДГАФ изомеризуется. Так постепенно ДГАФ превращается в глицеральдегид-3-фосфат.
Смысл второго шага подготовительного этапа — образовать две молекулы глицеральдегид-3-фосфата. Он может превратиться в пируват — нашу конечную цель.
Получается, что в ходе подготовительного этапа клетка затратила две молекулы АТФ, но при этом получила две молекулы глицеральдегид-3-фосфата. На следующем этапе из глицеральдегид-3-фосфата будет образовываться АТФ. Ведь клетка не глупышка. Она не будет тратить энергию просто так.
Энергетический этап гликолиза
Время получать молекулы АТФ из наших глицеральдегид-3-фосфатов. Дальше будут реакции с одним глицеральдегид-3-фосфатом. Но помните о том, что их два. Позже мы всё удвоим, но не стоит выбрасывать это из головы.
Откуда взять энергию для получения АТФ в этой молекуле?
Можно подумать, что фосфатная группа у третьего атома будет участвовать в синтезе АТФ. Но это не так — пока не так. Для того, чтобы синтезировать АТФ из АДФ нужно разрушить ковалентную связь, но необычную. Она должна быть макроэргической.
Макроэргическая связь — это связь, при гидролизе которой выделяется большое количество энергии. Эта энергия используется для присоединения фосфатной группы к молекуле АДФ — мы получаем АТФ. Этот процесс называется субстратное фосфорилирование.
Есть и другое фосфорилирование — окислительное. Там для синтеза АТФ будет использоваться градиент концентрации протонов. Но мы поговорим об этом подробнее, когда доберёмся до дыхательной цепи. Пока что остановимся на субстратном.
Не каждая связь будет макроэргической. Чаще всего эти связи есть в ангидридах фосфорных и карбоновых кислот. Ангидрид состоит из двух кислотных остатков, которые соединены через атом кислорода. Давайте посмотрим на молекулу АТФ — в ней две макроэргических связи.
И это как раз фосфорный ангидрид — в нём соединены три фосфорных остатка. Два из них — это ангидриды. Теперь вы догадались, что мы сделаем с глицеральдегид-3-фосфатом. Превратим его в ангидрид!
Шестая реакция. Ангидридная группа будет на первом атоме углерода, а не на третьем. Катализирует реакцию — глицеральдегидфосфатдегидрогеназа. Раз это дегидрогеназа, то нам понадобится кофермент. Здесь им будет НАД + . Он будет присоединять протон водорода и электроны от альдегидной группы. Альдегидная группа окисляется до карбоновой кислоты, но к ней тут же присоединяется неорганический фосфат.
Получился смешанный ангидрид фосфорной и карбоновой кислот — 1,3-бисфосфоглицерат. Ура, у нас есть макроэргическая связь.
У этой реакции есть плюсы и минусы. Плюсы:
- На синтез макроэргической связи затрачивается неорганический фосфат. А не молекула АТФ.
- В ходе реакции мы получаем восстановленный кофермент — НАДH.
А о минусе мы поговорим ниже.
Седьмая реакция. Время получить молекулу АТФ. В этом нам поможет фермент — фосфоглицераткиназа. Она катализирует разрыв макроэргической связи в 1,3-бисфосфоглицерате. Энергия разрыва этой связи идёт на присоединение фосфорной группы к АДФ — образованию макроэргической связи. Получаем АТФ и 3-фосфоглицерат. Это и есть субстратное фосфорилирование.
Фермент назван по обратной реакции. Потому что АТФ находится справа. Все киназы получают название в зависимости от того, где находится АТФ. Эта реакция обратима, потому что с двух сторон есть макроэргические связи — нет резкого изменения свободной энергии. Такое изменение было в первой и третьей реакциях, но не здесь.
Восьмая реакция. В 3-фосфоглицерате ещё остаётся фосфатная группа. Она связана с третим атомом углерода с помощью ковалентной связи. Попробуем превратить эту связь в макроэргическую. Для этого придётся перенести фосфатную группу на второй атом углерода. Катализирует реакцию фосфоглицератмутаза.
Реакция протекает в два этапа: вначале фосфоглицератмутаза отдаёт фосфатную группу 3-фосфоглицерату — образуется 2,3-бисфофоглицерат. Потом фосфоглицератмутаза забирает фосфатную группу с третьего атома углерода. В клетке образуется 2-фосфоглицерат. Зачем я про это рассказываю? Потому что вы уже встречались с этой молекулой. 2,3-бисфосфоглицерат снижает сродство гемоглобина к кислороду. Вспомнили? Ну да ладно, сейчас не об этом.
Девятая реакция. У нас не получится превратить 2-фосфоглицерат в ангидрид, но есть другой вариант. Для этого нам понадобится фермент — енолаза. Она занимается отщеплением воды от молекулы с образованием двойной связи по месту разрыва — класс лиазы. Образуется фосфоенолпируват.
Эта реакция увеличивает энергетический потенциал молекулы — в ней появляется енолфосфатная связь. Это макроэргическая связь. Фосфоенолпируват теперь может отдать фосфорную группу молекуле АДФ в следующей реакции.
Десятая реакция. Её катализирует фермент пируваткиназа. Гидролиз макроэргической связи приводит к высвобождению энергии, которая идёт на присоединение фосфорной группы к АДФ. Образуется АТФ и пируват. И снова субстратное фосфорилирование.
Опять фермент назван по обратной реакции. Но есть ли вообще тут обратная реакция? Если есть, то почему я нарисовал стрелочку в одну сторону. Дело в том, что пируват может находиться в енольной или кетонной формах. Это зависит от положения двойной связи.
После отщепления фосфорной группы образуется енольная форма. Но эта форма менее стабильна, чем кетонная. Поэтому быстро происходит таутомерия — переход изомеров друг в друга. Образуется стабильная кето-форма пирувата. За счёт этого реакция становится необратимой!
На этом энергетический этап гликолиза заканчивается. Да и сам гликолиз тоже.
Сделаем выводы
Давайте посмотрим на общую схему гликолиза. Всего три реакции из десяти необратимы: первая, третья и десятая.
Почему они необратимы? В этих трёх реакциях происходит значительное изменение свободной энергии. Если сказать проще, то при первой, третьей и десятой реакции выделяется большое количество энергии. Это экзотермические реакции. Поэтому для того, чтобы повернуть эти реакции в обратную сторону нужно затратить энергию. Это невозможно при физиологических клеточных условиях.
Другие семь реакций обратимы. В них свободная энергия меняется незначительно. Некоторые из этих реакций экзотермические, а некоторые эндотермические. При физиологических условиях в клетке можно легко провести реакции в другую сторону. Достаточно ферментов, которые снизят энергию активации этой реакции.
Это полезно, потому что иногда клетка хочет синтезировать глюкозу из продуктов гликолиза. Всё зависит от условий внутри клетки. Катаболизм глюкозы и её синтез работают по типу выключателя. Когда клетка включает синтез, то отключается распад. И наоборот. Синтез глюкозы из продуктов гликолиза и других молекул — это глюконеогенез. Но я отвлёкся, давайте вернёмся к гликолизу.
На подготовительном этапе мы затратили две молекулы АТФ для активации глюкозы — первая и третья реакция. В конце этапа у нас есть две молекулы глицеральдегид-3-фосфата. Дальше эти две молекулы вступят в энергетический этап.
В энергетическом этапе из каждой молекулы глицеральдегид-3-фосфата мы получили две молекулы АТФ. Первую в седьмой реакции, а вторую в десятой реакции. Обе были получены с помощью субстратного фосфорилирования. Так как молекул глицеральдегид-3-фосфата две, то всего мы получили четыре молекулы АТФ.
Общий выхлоп гликолиза (пока что) = получено на энергетическом этапе (АТФ) — затрачено на подготовительном этапе (АТФ) = 4-2 = 2 молекулы АТФ. Как то не густо….
Но ещё мы получили две молекулы пирувата, которые отправятся в цикл трикарбоновых кислот (ЦТК). А потом и в дыхательную цепь. Для этого две молекулы пирувата переносятся в митохондрию, где находятся ЦТК и дыхательная цепь. Там из пирувата, через серию реакций, образуются молекулы АТФ.
Ах да, есть ещё две важные молекулы, которые были получены в ходе гликолиза. Это 2 НАДH. Они образовались в шестой реакции, и я обещал вам рассказать про её минусы. Время выполнять обещание.
Значение НАДH для гликолиза
Эту реакцию катализирует глицеральдегидфосфатдегидрогеназа. Она может работать только при условии, что в её активном центре находится НАД + . НАД + принимает на себя два электрона и протон водорода от глицеральдегид-3-фосфата. После этого НАДH покидает активный центр фермента вместе со своей добычей. В активный центр фермента попадает следующий НАД + . И тут возможны два варианта:
- В цитоплазме есть НАД + . Он залетает в активный центр фермента и реакция идёт снова. И так по кругу.
- В цитоплазме нет НАД + , но избыток НАДH. Из-за этого шестая реакция останавливается, а с ней и весь гликолиз. Клетка не может получить пируват, ей такое не нравится.
Но у клетки есть выход из этой ситуации. Нужно просто восстановить количество НАД + . А для этого нужно окислить НАДH. И это можно сделать двумя способами. Перенести его протон водорода и электроны в митохондрию, где они отправятся в дыхательную цепь. Либо же оставить протон и электроны в цитоплазме, но для этого придётся пожертвовать молекулами пирувата — превратить его в лактат.
Тут нужно поговорить об аэробном и анаэробном гликолизе. Я не стал пихать их в начало статьи для того, чтобы разобраться с ними сейчас.
Аэробный гликолиз
Дыхательная цепь находится в митохондриях. НАДH не может проникнуть через двойную биологическую мембрану. Это можно сделать с помощью челночных механизмов (подробнее здесь). Челночные механизмы окисляют НАДH до НАД + — при этом он остаётся в цитоплазме. А его протон и два электрона переносятся внутрь митохондрии. Ещё для этого используется протон водорода из цитоплазмы, но их там не мало — от цитоплазмы не убудет. После этого НАД + присоединяется к активному центру глицеральдегидфосфатдегидрогеназы.
Челночные механизмы нужны не только для того, чтобы окислить НАДH. После того, как протоны и электроны были перенесены в митохондрию, они попадают в дыхательную цепь. Там из них синтезируется три или пять молекул АТФ. Это зависит от челночного механизма, который был использован клеткой.
Вы можете найти инфу, что в в ходе гликолиза синтезируется восемь молекул АТФ. Потому что каждый НАДH идёт на образование трёх молекул АТФ. Но если говорить строго, то из каждого НАДH может синтезироваться только 2,5 молекулы. Наверное, они округляют или пользуются старыми данными. Так что тут вам решать. Я считаю по 2,5 молекулы, поэтому:
Общий выход аэробного гликолиза: пять или семь молекул АТФ и две молекулы пирувата. Количество АТФ зависит от челночного механизма
Уравнение аэробного гликолиза:
Но что случится, если дыхательная цепь прекратит свою работу?
Анаэробный гликолиз
При анаэробном гликолизе челночные механизмы останавливаются. Это случается при недостатке кислорода (ого!) — дыхательная цепь перестает работать. В митохондрии накапливаются протоны и электроны. Для наших уже просто не хватает места.
Но клетка делает кое-что интересное. Она превращает пируват в лактат с помощью лактатдегидрогеназы. Фермент использует НАДH и протон водорода на эту реакцию. Далее он присоединяет их к пирувату. Та-дам! Клетка получает НАД + и лактат. НАД + снова идёт в шестую реакцию.
Выхлоп энергии здесь намного меньше — всего две молекулы АТФ. Протон и электроны с НАДН не отправляются в митохондрию, а значит мы не получим дополнительные три или пять молекул АТФ. Пируват не отправляется в ЦТК, а превращается в лактат. В общем, невыгодно как-то. Клетка слишком много теряет на этом.
Общий выход анаэробного гликолиза: две молекулы АТФ и две молекулы лактата
Уравнение анаэробного гликолиза:
Зачем тогда нужен анаэробный гликолиз? Некоторые клетки не могут получать энергию по-другому. Вот у эритроцитов просто нет митохондрий, поэтому единственный вариант получить энергию — анаэробный гликолиз.
Ещё он протекает в мышцах при резкой физической нагрузке. Представьте, что мы побежали за автобусом. У нас небольшой запас кислорода в мышцах — в виде миоглобина. Он сгорит очень быстро, а мышцам нужна энергия. Запускается анаэробный гликолиз с образованием лактата. Потом к мышцам увеличивается кровоток — переход на аэробный гликолиз.
С мышцами бывает и другая ситуация. Они частенько сокращаются, а это иногда приводит к сдавлению сосудов. Кровоток снижается, а энергию на сокращения где-то брать нужно. Снова включается анаэробный гликолиз. Так что анаэробный гликолиз незаменимая штука для эритроцитов и мышц.
Опухоли тоже пользуются гликолизом, но это не хорошая инфа. А так анаэробный гликолиз больше характерен для бактерий: клостридий и других облигатных анаэробов.
Но вернёмся к нашему организму. В мышцах лактат не лежит просто так, а отправляется в кровь. Там он циркулирует, пока не попадёт в печень или почки. Зачем? Эти органы могут превратить лактат в глюкозу с помощью глюконеогенеза. В них идёт обратная реакция, которую катализирует лактатдегидрогеназа — образование пирувата из лактата. Далее пируват вступает в глюконеогенез — через серию реакций образуется глюкоза. Печень/почки отправляют её в кровь. Дальше глюкоза попадёт в другие клетки, где будет использована на их нужды. Часть глюкозы снова окажется в мышцах, где из неё опять образуется лактат. Цикличненько. У этого цикла есть своё название — цикл Кори.
Другие субстраты гликолиза
Только что мы разобрали гликолиз на примере глюкозы. Она попадает в клетку из крови, а потом фосфорилируется. И так далее. Но откуда она там взялась? Есть два варианта:
Мы сытно поели, и в ЖКТ началось пищеварение. Большая часть полисахаридов и дисахаридов состоит из глюкозы. Глюкоза попадёт из кишечника в кровь, а потом в клетку. Там глюкоза будет использоваться для синтеза АТФ — гликолиза, либо запасаться в виде гликогена. Она может использоваться и для других процессов, но пока не будем запариваться.
Второй вариант — образование глюкозы из гликогена.
Гликоген
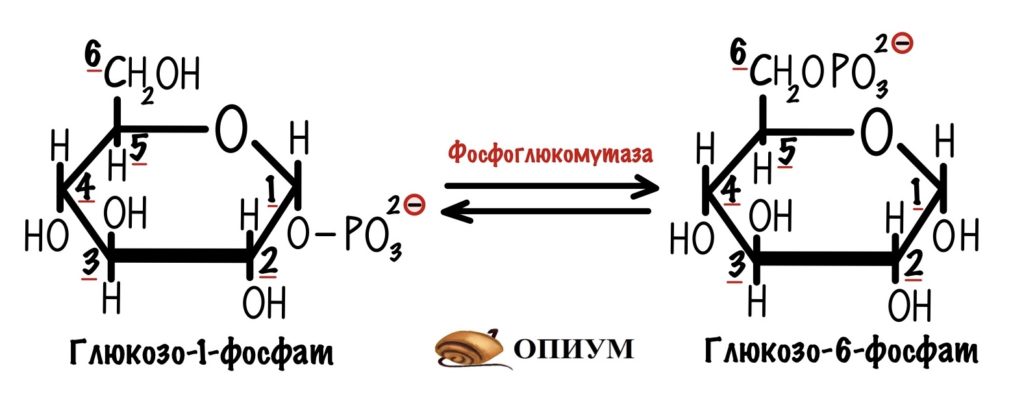
В мышцах и печени можно получить молекулу глюкозо-6-фосфата, продукт первой реакции, по-другому. Через разрушение гликогена — гликогенолиз. Под действием гликогенфосфорилазы от гликогена отщепляется молекула глюкозы. Эта реакция идёт с помощью фосфоролизиса — альфа-1-4-гликозидная связь разрушается с участием неорганического фосфата. Клетка получает глюкозо-1-фосфат и гликоген, в котором меньше на одну молекулу глюкозы.
Далее глюкозо-1-фосфат превращается в глюкозо-6-фосфат с помощью фермента фосфоглюкомутазы. А вот и наш глюкозо-6-фосфат, который можно запихнуть в гликолиз.
Но такая тема работает только в мышечной ткани — глюкозо-6-фосфат идёт на гликолиз. В печени глюкозо-6-фосфат превратится в глюкозу с помощью глюкозо-6-фосфатазы. Из клеток печени она пойдёт в кровь. Так происходит между приёмами пищи, когда падает уровень глюкозы в крови. Печень заботится об уровне глюкозы в крови между приёмами пищи, поэтому она не использует глюкозу самостоятельно. Но давайте вернёмся к пищеварению.
При пищеварении мы получали не только глюкозу, но и другие моносахариды: фруктозу и галактозу. Можно ли их отправить в гликолиз? А давайте посмотрим.
Фруктоза
Фруктоза образуется при гидролизе сахарозы во время пищеварения. Сахароза — это дисахарид, который состоит из глюкозы и фруктозы. В начале пути глюкозы и фруктозы схожи. Фруктоза тоже всасывается в кишечнике, а потом попадает в кровь. Оттуда фруктоза захватывается клетками. А дальше начинаются отличия. Фруктоза может вступать в гликолиз двумя разными путями.
Первый путь. Фруктоза фосфорилируется с помощью гексокиназы. Фосфорная группа присоединяется к шестому атому углерода. При этом затрачивается молекула АТФ.
Удобно, клетка получила продукт второй реакции гликолиза. Даже не нужно проводить изомеризацию. Можно сразу фосфорилировать фруктозо-6-фосфат фосфофруктокиназой.
Второй путь. Фруктоза фосфорилируется с помощью фруктокиназы. Фосфорилирование идёт по первому атому углерода, а не шестому. Уже можно не писать, что на это тратится молекула АТФ?
Дальше клетка превращает фруктоза-6-фосфат в две триозы. Очень похоже на четвертую реакцию гликолиза, но только одна будет фосфотриозой. Фермент тоже называется альдолазой, но с приставкой — фруктозо-1-фосфатальдолаза.
Дигидроксиацетонфосфат может пойти на гликолиз через изомерию. Триозофосфатизомераза превращает его в глицеральдегид-3-фосфат. Далее он вступает в гликолиз.
Глицеральдегид в гликолиз не отправить. Сначала нужно прицепить к нему фосфатную группу. Катализирует реакцию — триозокиназа. Получаем ещё один глицеральдегид-3-фосфат.
Оба глицеральдегид-3-фосфата попадают на энергетический этап гликолиза. Очень похоже на классический гликолиз. Просто он идёт немного в обход. При этом оба пути одинаковы в энергетическом плане — клетка тратит на них две молекулы АТФ.
Галактоза
Галактоза образуется при гидролизе лактозы. Лактоза — это дисахарид, который состоит из галактозы и глюкозы. Галактоза всасывается из кишечника, а потом попадает в клетку. Ну и куда же без фосфорилирования. Ведь нужно загнать галактозу в ловушку и увеличить её реакционную способность. Фермент галактозокиназа фософрилирует первый атом углерода.
Дальше идёт вот такой интересный цикл:
В итоге мы получаем глюкозо-1-фосфат, который можно превратить в глюкозо-6-фосфат с помощью фосфоглюкомутазы. Где мы уже встречались с УДФ-глюкозой? Да, в синтезе гликогена.
Вот общая табличка со всеми субстратами гликолиза.
Регуляцию гликолиза и глюконеогенеза разбираем здесь.
Хочешь задать вопрос, похвалить или наговорить гадостей? Тогда залетай в телегу. Там ты сможешь предложить новый формат или разбор темы. А если серьёзно, то эти статьи пишутся для вас, поэтому мне важна обратная связь.
http://xumuk.ru/biologhim/145.html
http://opiumedu.ru/bihomiya/glikoliz-substraty-dlya-glikoliza/