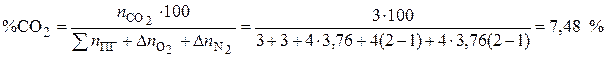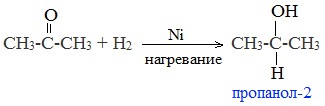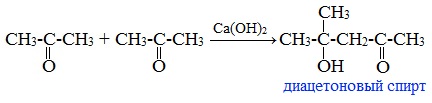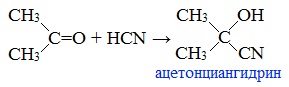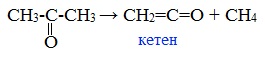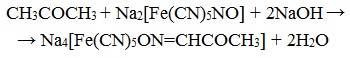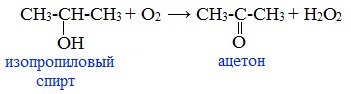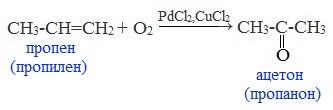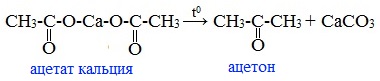Решение. Сгорает индивидуальное химическое соединение в конденсированном состоянии
Сгорает индивидуальное химическое соединение в конденсированном состоянии.
1. Составляем уравнение реакции горения ацетона в воздухе:
2. Объём воздуха, необходимый для сгорания 1 кг ацетона, рассчитываем по формуле (7), учитывая при этом, что масса одного киломоля ацетона составляет 58 кг/кмоль:
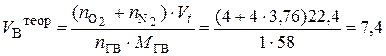
3. Действительный объём воздуха, пошедшего на сгорание 1 кг ацетона, рассчитывается с учётом коэффициента избытка воздуха a:

4. Избыток воздуха составит:
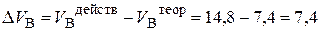
5. Теоретический объём продуктов горения рассчитываем по формуле (14):

6. Действительный объём продуктов горения составит:
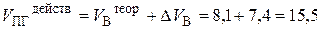
7. Объём воздуха, теоретически необходимого для сгорания 100 кг ацетона, составит соответственно 740 м 3 (7,4 × 100), при этом выделится 1 550 м 3 продуктов сгорания.
8. Процентное содержание углекислого газа рассчитывается по формуле, %
Ответ: При сгорании 100 кг ацетона объём воздуха при нормальных условиях составит 1480 м 3 , а объём продуктов горения – 1550 м 3 , процентное содержание углекислого газа в продуктах горения составило 7,48 %.
Примечание.Если в процессе горения были заданы условия, отличные от нормальных (Т¹273 К, Р¹101,3 кПа), то объём продуктов горения и воздуха рассчитывается с учётом объёма, который занимает один кмоль газа при заданной температуре:

где Р0 =101,3 кПа; Т0 = 273 К; Т и Р заданные температура и давление.
ПРИМЕР:Рассчитать количество толуола (С7Н8), которое сгорело в закрытом помещении объёмом 100 м 3 , если содержание кислорода в продуктах горения составило 12 %. Условия нормальные.
Уравнение горения ацетона?
Химия | 10 — 11 классы
Уравнение горения ацетона.
C3H6O + 4O2 — > ; 3CO2 + 3H2O.
Составьте реакцию горения ацетона и пропаналя?
Составьте реакцию горения ацетона и пропаналя.
Химическая формула ацетона С3Н6О?
Химическая формула ацетона С3Н6О.
а) из атомов каких элементов состоит ацетон
б) число атомов в составе его молекулы
в) молекулярную массу ацетона и массовую долю ацетона
Общее уравнение горения аренов?
Общее уравнение горения аренов.
Уравнение реакции горения гексана?
Уравнение реакции горения гексана?
Химическая формула ацетона С3Н6О укажитеа) из атомов каких элементов состоит ацетонб)число атомов в его составев)относительную молекулярную массу ацетона?
Химическая формула ацетона С3Н6О укажите
а) из атомов каких элементов состоит ацетон
б)число атомов в его составе
в)относительную молекулярную массу ацетона.
Уравнение горения циклобутана)))?
Уравнение горения циклобутана))).
Напишите уравнение — горение полипропилена?
Напишите уравнение — горение полипропилена.
Уравнение реакции горения серы?
Уравнение реакции горения серы.
Химическая формула ацетона C6H3O?
Химическая формула ацетона C6H3O.
Укажите : из атомов каких элементов состоит ацетон, число атомов в составе его молекулы, относительную молекулярную массу ацетона.
Пж помогите сотавить уравнения образования воды при горении водорода, метана CH4, сероводорода H2S и ацетона C3H6O?
Пж помогите сотавить уравнения образования воды при горении водорода, метана CH4, сероводорода H2S и ацетона C3H6O!
Вы перешли к вопросу Уравнение горения ацетона?. Он относится к категории Химия, для 10 — 11 классов. Здесь размещен ответ по заданным параметрам. Если этот вариант ответа не полностью вас удовлетворяет, то с помощью автоматического умного поиска можно найти другие вопросы по этой же теме, в категории Химия. В случае если ответы на похожие вопросы не раскрывают в полном объеме необходимую информацию, то воспользуйтесь кнопкой в верхней части сайта и сформулируйте свой вопрос иначе. Также на этой странице вы сможете ознакомиться с вариантами ответов пользователей.
CaCO3 + 2HNO3 — — >Ca(NO3)2 + H2O + CO2↑.
Реакция идёт до образования газа СО2 : CaCO3 + HNO3 — — — — — > Ca(NO3)2 + H2O + CO2.
Сначала определяем в какой группе и периоде находится элемент Cr — 4 — й период, 6 — я группа. Периоды — количество энергетических электронов ; их будет 4 52 Cr ) ) ) ) 24 2 8 8 6 Почти у всех элементов на 1 — ом и на 2 — ом уровнях получается по 2 ..
Mg + S — > MgS Mg + H2O→Mg(OH)2 + H2 Mg + Cl2→MgCl2 JiOH + H2SO4 — не знаю Na + O2→Na2O Na2SO4 + KOH — не знаю.
Mg + S — > MgS Mg + 2H2O — > Mg(OH)2 + H2 (при высокой температуре) Mg + Cl2 — > MgCl2 2LiOH + H2SO4 — > Li2SO4 + 2H2O 4Na + O2 — > 2Na2O Na2SO4 + KOH — > реакция не идёт.
Mr(NaBr) = 23 + 80 = 103 Mr(Cu(NO3)2) = 64 + 14 * 2 + 16 * 6 = 188.
1)CH4 + Br2 — — — — (hv) — — — — >CH3Br 2)2CH3Br + Na — — — — — — — — — — >CH3 — CH3 + 2NaBr 3)CH3 — CH3 — — — — — — >CH2 = CH2 + H2 4)CH2 = CH2 — — — — >CH(тр. Связь)CH + H2 5)3CH(тр. Связь)CH — — — — >C6H6.
16, 7 г Пусть масса воды М, масса соли в растворе м. Тогда в первом случае 4% раствора имеем 0, 04 = м / (М + м), отсюда получаем, что м = М / 24. Поскольку м + М = 250 г. , то подставив сюда значение м получим для М : М = 240 г. , тогда м = 10 г..
Ответ : А и С (D) Порядковый номер показывает число протонов и число электронов.
1)L = n \ N * 100% (5 / 100) * 100% = 5% (80 / 100) * 100% = 80% 2)Чтобы ты понял( — а), сильными электролитами считаются те, у которых связь между атомами слаба, которые больше разлагаются на ионы. Это кислоты (не все), соли, щелочи. Серная кислот..
Уравнение реакции горения ацетона в кислороде
Ацетон — простейший представитель насыщенных кетонов.
Физические свойства
Ацетон (пропанон-2, диметилкетон) СН3-СО-СН3 — летучая бесцветная жидкость с характерным запахом и температурой кипения 56 0 С.

Он хорошо растворяет многие органические вещества (жиры, смолы, ацетилцеллюлозу, воск, резину и др.), поэтому является незаменимым растворителем в быту и в лакокрасочной промышленности.
Ацетон встречается в организме человека. Он является промежуточным продуктом обмена веществ. Незначительное количество ацетона, образующееся в организме человека в результате метаболических реакций, выводится вместе с мочой. У больных диабетом следы ацетона можно обнаружить в выдыхаемом воздухе.
Один из простейших и в то же время важнейших из кетонов — ацетон — впервые выявлен в 1595 году немецким химиком Андреасом Либавием в процессе сухой перегонки ацетата свинца. Однако точно определить его природу и химический состав удалось только в 1832 году Жану-Батисту Дюма и Юстусу фон Либиху. До 1914 года ацетон получали практически исключительно коксованием древесины.
Токсичность ацетона
Ацетон обладает возбуждающим и наркотическим действием, поражает центральную нервную систему. Ацетон способен накапливаться в организме, т.к. медленно выводится из организма. Он может поступать в организм с вдыхаемым воздухом, а также через пищевой канал и кожу.
После поступления ацетона в кровь часть его переходит в головной мозг, селезенку, печень, поджелудочную железу, почки, легкие и сердце. Содержание ацетона в указанных органах несколько меньшее, чем в крови.
При вдыхании паров ацетона происходит кислородное голодание мозга. Поэтому, в помещениях, в которых происходит испарение ацетона, создается опасность отравления при вдыхании его паров.
Химические свойства
Ацетон является одним из наиболее реакционноспособных кетонов.
Ацетон, как и все кетоны, не дает реакции «серебряного зеркала», не полимеризуется. В этом его отличие от альдегидов.
1. Гидрирование (восстановление)
При тех же условиях, что и формальдегид, ацетон присоединят водород:
Водород присоединяется вследствие разрыва двойной связи карбонильной группы.
2. Взаимодействие с гидросульфитом натрия
Ацетон один из немногих кетонов образует бисульфитное соединение:
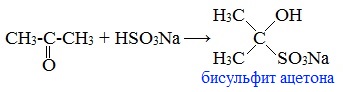
Под действием щелочей ацетон вступает в альдольную самоконденсацию, с образованием «ацетонового» (диацетонового) спирта:
4. Взаимодействие с синильной кислотой
Одной из наиболее важных реакций ацетона является присоединение к нему синильной кислоты с образованием ацетонциангидрина:
5. Пиролиз ацетона
При нагревании выше 500 0 C ацетон распадается на кетен и метан:
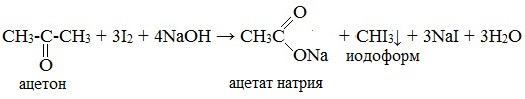
6. Галоформная реакция (иодоформная реакция, или проба Люголя)
Качественная реакция на ацетон!
При взаимодействии ацетона с избытком йода в щелочной среде образуется йодоформ – желтое вещество с характерным запахом:
Аналогичные реакции идут с хлором и бромом, но только реакция с йодом приводит к нерастворимому йодоформу.
7. Взаимодействие с нитропруссидом натрия
Качественная реакция на ацетон!
Ацетон с нитропруссидом натрия в щелочной среде дает интенсивно-красную окраску . При подкислении уксусной кислотой CH3COOH окраска переходит в красно-фиолетовую :
Йодоформная реакция и реакция с нитропруссидом натрия используются для обнаружения ацетона в моче при сахарном диабете.
Получение
Ацетон получают в больших количествах различными методами: при сухой перегонке дерева, разложением ацетата кальция, окислением пропена, «кумольным» способом, окислением изопропилового спирта, гидратацией ацетилена водяным паром.
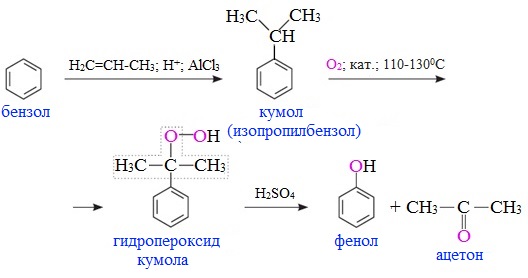
1.Кумольный способ
Данный способ получения фенола основан на окислении кумола (изопропилбензола). В качестве исходных продуктов используют бензол и пропилен.
Процесс протекает в три стадии. На первой стадии бензол алкилируется пропеном с получением кумола, на второй и третьей (реакция Удриса-Сергеева) полученный кумол окисляется кислородом воздуха до гидропероксида, который при действии серной кислоты разлагается на фенол и ацетон:
Окисление кумола — экономически выгодный метод, так как позволяет получить наряду с фенолом другой важный продукт — ацетон (на 1 кг фенола приходится 0,6 кг ацетона). В настоящее время этот метод наиболее широко используется в промышленности и позволяет производить более 80% синтетического фенола.
2. Окисление изопропилового спирта
Ацетон получают в больших количествах при окислении изопропилового спирта:
В качестве катализатора применяется медь, серебро, никель, платина и др. Воздух, насыщенный парами изопропилового спирта, пропускают над тонким слоем катализатора при температуре 400-650 0 С.
Если процесс окисления протекает в жидкой фазе, то, как побочный продукт образуется пероксид водорода:
3. Каталитическое окисление пропена кислородом воздуха
В промышленности ацетон получают прямым окислением пропена в жидкой фазе в присутствии катализатора — смеси PdCl2 и CuCl2 при температуре 100 0 C:
4. Брожение крахмала
Незначительное значение имеет метод брожения крахмала под действием бактерий с образованием ацетона и бутанола. Метод характеризуется малыми выходами.
5. Пиролиз ацетата кальция
Ацетон можно получить пиролизом ацетата кальция:
6. Гидратация ацетилена водяным паром
Реакция протекает при 400-460 0 С над катализатором, содержащим оксиды железа и марганца:
Применение
В качестве растворителя ацетон используется в производстве красок, лаков и олифы, резины, пластмасс, красителей, взрывчатых веществ, а также в фотографии.
Ацетон применяется в производство искусственного шелка и синтетической кожи, в производстве смазочных масел, бездымного пороха, кинопленки.
В химической промышленности ацетон является промежуточным химическим соединением при производстве многих химикатов, таких как кетен, уксусный ангидрид, бисфенол А, метилметакрилат, хлороформ, изофорон, йодоформ, витамин С.
Метилметакрилат применяется, главным образом, в виде листов пластика, порошков для литья и формовки, поверхностных покрытий, эмульсионных полимеров, волокон, чернил и пленок.
Метилметакрилат также применяется в производстве материалов, известных под названием плексигласа или люцита. Они используются в зубных протезах, твердых контактных линзах, и клеях.
Метилметакрилат – мономер для синтеза полиметилметакрилата («органическое сырье»).
http://himia.my-dict.ru/q/1398962_uravnenie-gorenia-acetona/
http://himija-online.ru/organicheskaya-ximiya/aldegidy-i-ketony/aceton-predstavitel-ketonov.html