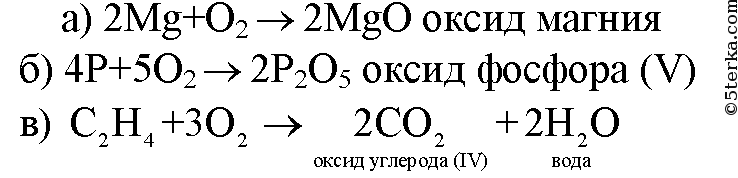Реакция горения бора , кремния , этана C2H6?
Химия | 5 — 9 классы
Реакция горения бора , кремния , этана C2H6.
2C2H6 + 7O2 = 4CO2 + 6H2O.
Помогите составить уравнение реакции горения диоксида кремния?
Помогите составить уравнение реакции горения диоксида кремния.
Написать уравнения реакций взаимодействия этана с хлором, азотной кислотой, горения?
Написать уравнения реакций взаимодействия этана с хлором, азотной кислотой, горения.
Указать название продукта.
Каков характер пламени при горении этана?
Каков характер пламени при горении этана.
Реакция характерна и для этилена и для этана1) горение2) присоединение хлора3) присоединение брома4)полимеризация?
Реакция характерна и для этилена и для этана
2) присоединение хлора
3) присоединение брома
Уравнение реакции горения кремния в кислороде?
Уравнение реакции горения кремния в кислороде.
Сколько неспаренных электронов у кремния и бора?
Сколько неспаренных электронов у кремния и бора?
Напишити пожалоста реакции горения этана (C2H6) в кислороде ?
Напишити пожалоста реакции горения этана (C2H6) в кислороде .
Ответ дайте в виде суммы коэффициентов в уравнения реакции?
Ответьте пожалуйста ?
1)Составить уравнение реакций замещение метана.
2)Уравнение реакции горения этана.
Определить объем израсходовавшего кислорода в реакции горения кислорода в реакции 25 г этана?
Определить объем израсходовавшего кислорода в реакции горения кислорода в реакции 25 г этана.
Горение водородного соединения кремния (уравнение)?
Горение водородного соединения кремния (уравнение).
Вы зашли на страницу вопроса Реакция горения бора , кремния , этана C2H6?, который относится к категории Химия. По уровню сложности вопрос соответствует учебной программе для учащихся 5 — 9 классов. В этой же категории вы найдете ответ и на другие, похожие вопросы по теме, найти который можно с помощью автоматической системы «умный поиск». Интересную информацию можно найти в комментариях-ответах пользователей, с которыми есть обратная связь для обсуждения темы. Если предложенные варианты ответов не удовлетворяют, создайте свой вариант запроса в верхней строке.
Ответ — Г ) Ar , тк слева на право радиус уменьшается.
HF фтороводородная плавиковая фторидHCl хлороводородная соляная хлоридHBr бромоводородная бромидHI иодоводородная иодидH2S сероводородная сульфидH2SO3 сернистая сульфитH2SO4 серная сульфатH2CO3 угольная карбонатH2SiO3 кремниевая силикатHNO3 азотная н..
K2CO3 = 39 * 2 + 12 + 16 * 3 = 138г / моль Na2SO4 = 23 * 2 + 32 + 16 * 4 = 142г / моль.
LiCl — хлорид лития ; NaBr — бромид натрия ; KCl — хлорид калия.
Карбонат магния в — вует с соляной к — той, обменная р — ция. Получается хлорид магния, вода и углекислый газ. MgCO3 + 2HCl = MgCl2 + H2CO3 (не устойчивая к — та распадается на H2O и CO2) Магний стоит во второй группе, щелочно — земельный металл Во..
MgCO3 + 2HCl = MgCl2 + CO2 + H2O Исходные вещества перед знаком равно, продукты реакции — после. Классификационная группа Mg — элемент второй подгруппы, Cl — Принадлежит к17 — й группепериодической таблицы, Н — первая группа главная подгруппа.
С5H12 = = C2H6 + C3H6.
А) HCI M (HCI) = Ar (H) + Ar (CI) = 1 + 35. 5 = 36. 5(молекулярная масса) Mr (HCI) = 36. 5 г / моль (молярная масса) W (H) = (Ar(H) * 1) : (Mr(HCI)) = 1 / 36. 5 = 0. 0274 = 2. 74 % W(Cl) = (Ar(CI) * 1) : (Mr(HCI)) = 35. 5 / 36. 5 = 0. 9726 =..
145 мм = 0, 145 м 1, 5 км = 1500 м 2 км = 2000 м 32 м = 32 м.
Тема II. Работа 1. Получение и свойства кислорода. Вариант 3
Вопросы:
1. Напишите уравнения реакций горения в кислороде: а) фосфора; б) магния; в) этилена С2H4 (углерод в образующемся оксиде четырехвалентен). Назовите продукты реакций.
2. Перечислите известные вам области применения кислорода. Укажите, на каких свойствах кислорода они основаны.
3. Рассчитайте количество вещества и массу кислорода, образующегося при разложении 24,5 г хлората калия KClO3.
Уравнение реакции: 2KClO3 = 2KCl + 3O2↑
Решения и ответы:

задача №3
к главе «Тема II. Кислород. Оксиды. Горение. Работа 1. Получение и свойства кислорода».
http://5terka.com/node/11266