Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Формула нитробензола: физические и химические свойстваЧто такое нитробензол? Это органическое соединение, которое представляет собой ароматическое ядро и присоединенную к нему нитрогруппу. По внешнему виду, в зависимости от температуры, — это ярко-желтые кристаллы или маслянистая жидкость. Имеет миндальных запах. Токсичен. Структурная формула нитробензолаНитрогруппа — это очень сильный акцептор электронной плотности. Поэтому молекула нитробензола обладает отрицательным индуктивным и отрицательным мезомерным эффектом. Нитрогруппа довольно сильно притягивает на себя электронную плотность ароматического ядра, дезактивируя его. Электрофильные реагенты уже не так сильно притягиваются к ядру, и потому нитробензол не так активно вступает в подобные реакции. Чтобы напрямую присоединить к нитробензолу еще одну нитрогруппу, необходимы очень жесткие условия, гораздо более жесткие, чем при синтезе мононитробензола. Тоже самое касается галогенов, сульфогруппы и др.
Из структурной формулы нитробензола видно, что одна связь азота с кислородом одинарная, а другая — двойная. Но на самом деле, из-за мезомерного эффекта, они обе равнозначны и имеют одинаковую длину 0,123 нм.
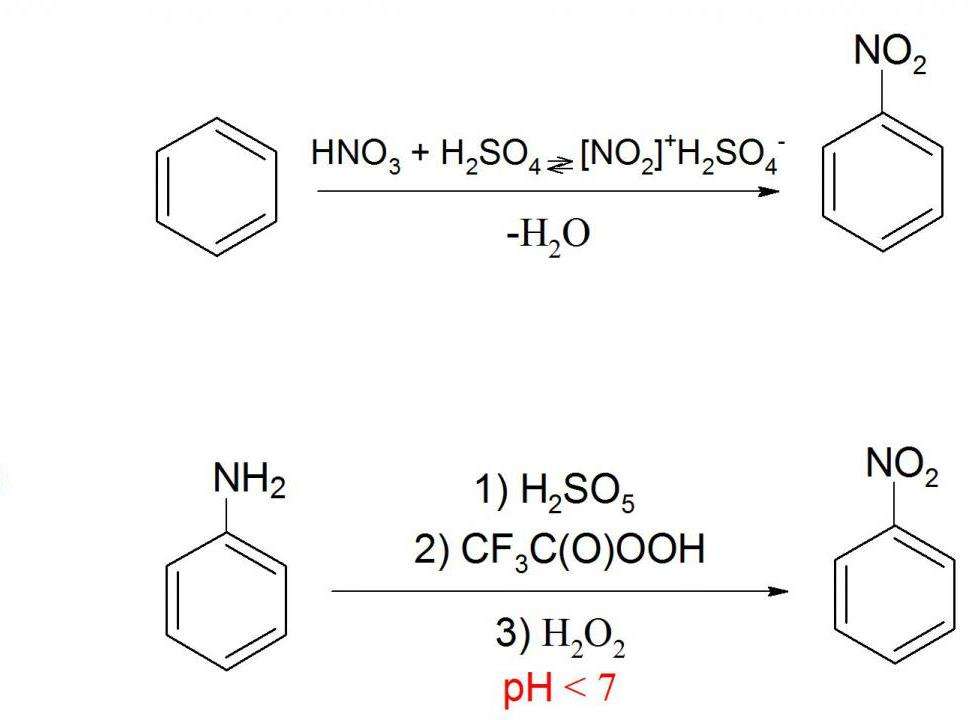
Получение нитробензола в промышленностиНитробензол — важный промежуточный продукт в синтезе многих веществ. Поэтому его производят в промышленных масштабах. Основной способ получения нитробензола — это нитрование бензола. Обычно для этого используют нитрующую смесь (смесь концентрированных серной и азотной кислоты). Реакцию ведут 45 минут при температуре примерно 50 °C. Выход нитробензола составляет 98 %. Именно поэтому данный способ в основном применяют в промышленности. Для его реализации существуют специальные установки как периодического, так и непрерывного типа. На 1995 г производство нитробензола в США составляло 748 000 тонн в год. Нитрование бензола можно также вести просто концентрированной азотной кислотой, но в таком случае выход продукта будет ниже.
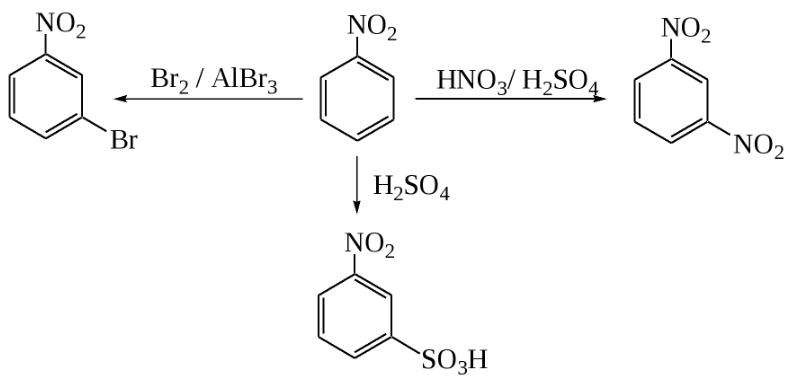
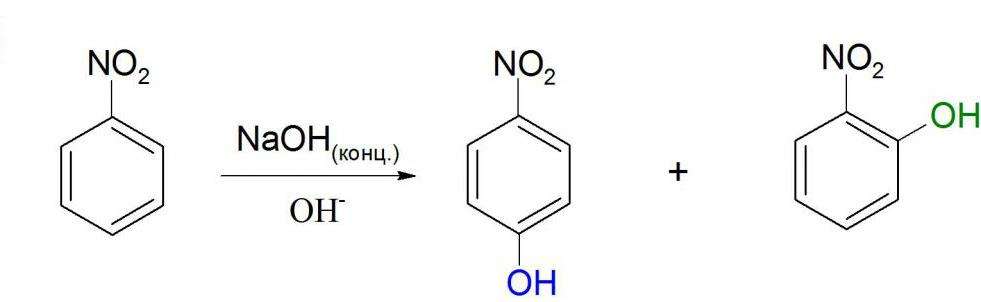
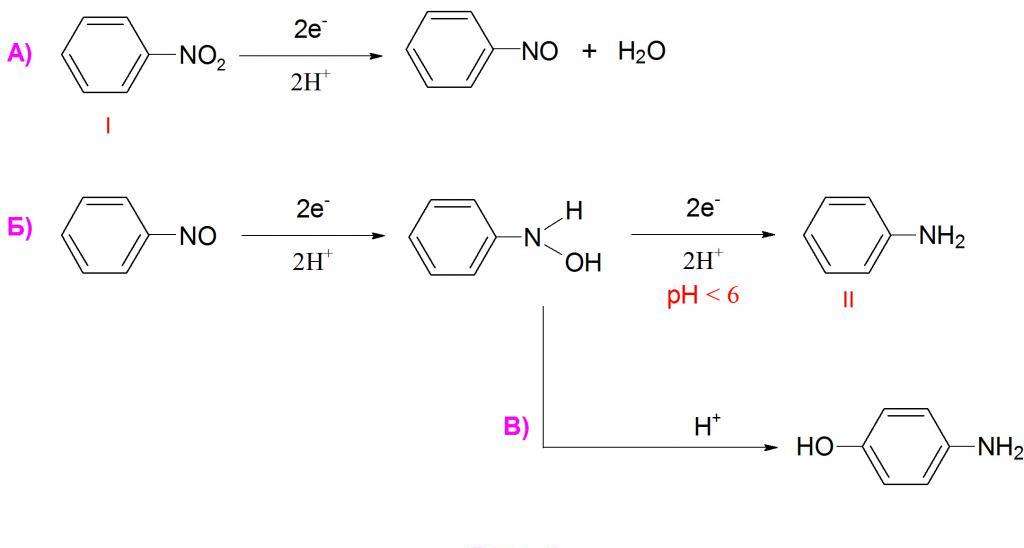
Получение нитробензола в лабораторииСуществует еще один способ получения нитробензола. В качестве сырья здесь используется анилин (аминобензол), который окисляют пероксисоединениями. Благодаря этому аминогруппа заменяется на нитрогруппу. Но в ходе этой реакции образуется несколько побочных продуктов, что мешает эффективно использовать данный способ в промышленности. Тем более, нитробензол в основном и используют для синтеза анилина, поэтому применять анилин для производства нитробензола не имеет смысла. Физические свойстваПри комнатной температуре нитробензол представляет из себя бесцветную маслянистую жидкость с запахом горького миндаля. При температуре 5,8 °C она затвердевает, превращаясь в желтые кристаллы. При 211 °C нитробензол кипит, а при 482 °C самовоспламеняется. Данное вещество, почти как любое ароматическое соединение, нерастворимо в воде, зато хорошо растворимо в органических соединениях, особенно в бензоле. Также он может перегоняться водяным паром. Электрофильное замещениеДля нитробензола, как и для любого арена, характерны реакции электрофильного замещения в ядро, хотя они и несколько затруднены по сравнению с бензолом из-за влияния нитрогруппы. Так, из нитробензола можно получить динитробензол путем дальнейшего нитрования смесью азотной и серой кислот при повышенной температуре. Полученный продукт будет преимущественно (93 %) состоять из мета-динитробензола. Возможно даже получение тринитробензола прямым путем. Но для этого необходимо использовать еще более жесткие условия, а также трехфтористый бор. Точно так же нитробензол может сульфироваться. Для этого используют очень сильный сульфирующий реагент — олеум (раствор оксида серы VI в серной кислоте). Температура реакционной смеси должна составлять не менее 80 °C. Еще одна реакция электрофильного замещения — прямое галогенирование. В качестве катализаторов используют сильные кислоты Льюиса (хлорид алюминия, трехфтористый бор и др.), а также повышенную температуру. Нуклеофильное замещениеКак видно из структурной формулы, нитробензол может вступать в реакции с сильными электронодонорными соединениями. Это возможно из-за влияния нитрогруппы. Примером такой реакции может служить взаимодействие с концентрированными или твердыми гидроксидами щелочных металлов. Но в этой реакции не образуется нитробензол натрия. Химическая формула нитробензола предполагает скорее присоединение гидроксильной группы в ядро, т. е. образование нитрофенола. Но происходит это только при достаточно жестких условиях. Подобная реакция протекает и с магнийорганическими соединениями. Углеводородный радикал присоединяется к ядру в орто- или пара- положения к нитрогруппе. Побочным процессом в этом случае является восстановление нитрогруппы до аминогруппы. Реакции нуклеофильного замещения идут проще, если нитрогрупп несколько, так как они еще сильнее будут оттягивать на себя электронную плотность ядра. Реакция восстановленияКак известно, нитросоединения могут восстанавливаться до аминов. Не является исключением и нитробензол, формула которого предполагает возможность этой реакции. Она часто применяется в промышленности для синтеза анилина. Но нитробензол может давать и очень много других продуктов восстановления. Чаще всего используют восстановление атомарным водородом в момент его выделения, т. е. в реакционной смеси проводят реакцию взаимодействия кислоты с металлом, и выделяющийся водород вступает в реакцию с нитробензолом. Обычно при таком взаимодействии получается анилин. Если на нитробензол подействовать цинковой пылью в растворе хлорида аммония, то продуктом реакции будет являться N-фенилгидроксиламин. Это соединение довольно легко может быть восстановлено стандартным способом до анилина, либо же окислено обратно в нитробензол сильным окислителем. Восстановление также может вестись в газовой фазе молекулярным водородом в присутствии платины, палладия или никеля. В этом случае также получается анилин, но существует вероятность восстановления самого бензольного ядра, что зачастую нежелательно. Иногда также применяют такой катализатор, как никель Ренея. Он представляет из себя пористый никель, насыщенный водородом и содержащий 15 % алюминия. При восстановлении нитробензола алкоголятами калия или натрия образуется азоксибензол. Если использовать более сильные восстановители в щелочной среде, то получается азобензол. Эта реакция также довольно важна, так как с ее помощью синтезируют некоторые красители. Азобензол может быть подвергнут дальнейшему восстановлению в щелочной среде до образования гидразобензола. Изначально восстановление нитробензола проводилось сульфидом аммония. Этот способ в 1842 г предложил Зинин Н. Н., поэтому реакция носит его имя. Но в настоящий момент ее уже редко применяют на практике из-за низкого выхода. ПрименениеСам по себе нитробензол применяют очень редко, только как селективный растворитель (например, для эфиров целлюлозы) или мягкий окислитель. Иногда его добавляют в полировочные растворы для металлов. Почти весь производимый нитробензол используется для синтеза других полезных веществ (например, анилина), которые, в свою очередь, используются для синтеза лекарственных препаратов, красителей, полимеров, взрывчатых веществ и др. ОпасностьИз-за своих физических и химических свойств, нитробензол — очень опасное соединение. Он имеет третий уровень опасности для здоровья из четырех по стандарту NFPA 704. Помимо того, что он может попасть в организм при дыхании или через слизистые оболочки, он также всасывается через кожу. При отравлении большой концентрацией нитробензола человек может потерять сознание и умереть. При небольших концентрациях симптомами отравления являются недомогание, головокружение, шум в ушах, тошнота и рвота. Особенность отравления нитробензолом — высокая скорость заражения. Симптомы проявляются очень быстро: нарушаются рефлексы, кровь приобретает темно-бурый цвет из-за образования в ней метгемоглобина. Иногда могут присутствовать высыпания на коже. Концентрация, достаточная для отправления, очень мала, хотя точных данных по смертельной дозе нет. В специальной литературе часто встречается информация, что 1-2 капли нитробензола хватает, чтобы убить человека. ЛечениеПри отравлении нитробензолом пострадавшего необходимо немедленно удалить из токсичной зоны и избавить его от зараженной одежды. Тело омывают теплой водой с мылом, чтобы удалить нитробензол с кожи. Каждые 15 минут пострадавшему делают ингаляцию карбогеном. При легких отравлениях необходимо принимать цистамин, пиридоксин или липоевую кислоту. В более тяжелых случаях рекомендуется использовать метиленовую синь или хромосмон внутривенно. При отравлении нитробезнолом через рот необходимо немедленно вызывать рвоту и промыть желудок теплой водой. Противопоказано принимать какой-либо жир, в том числе и молоко. Химические свойства ареновАрены (ароматические углеводороды) – это непредельные (ненасыщенные) циклические углеводороды, молекулы которых содержат устойчивые циклические группы атомов (бензольные ядра) с замкнутой системой сопряженных связей. Общая формула: CnH2n–6 при n ≥ 6. Химические свойства ареновАрены – непредельные углеводороды, молекулы которых содержат три двойных связи и цикл. Но из-за эффекта сопряжения свойства аренов отличаются от свойств других непредельных углеводородов. Для ароматических углеводородов характерны реакции:
Ароматическая система бензола устойчива к действию окислителей. Однако гомологи бензола окисляются под действием перманганата калия и других окислителей. 1. Реакции присоединенияБензол присоединяет хлор на свету и водород при нагревании в присутствии катализатора. 1.1. ГидрированиеБензол присоединяет водород при нагревании и под давлением в присутствии металлических катализаторов (Ni, Pt и др.). При гидрировании бензола образуется циклогексан: При гидрировании гомологов образуются производные циклоалканы. При нагревании толуола с водородом под давлением и в присутствии катализатора образуется метилциклогексан: 1.2. Хлорирование ареновПрисоединение хлора к бензолу протекает по радикальному механизму при высокой температуре, под действием ультрафиолетового излучения. При хлорировании бензола на свету образуется 1,2,3,4,5,6-гексахлорциклогексан (гексахлоран). Гексахлоран – пестицид, использовался для борьбы с вредными насекомыми. В настоящее время использование гексахлорана запрещено. Гомологи бензола не присоединяют хлор. Если гомолог бензола реагирует с хлором или бромом на свету или при высокой температуре (300°C), то происходит замещение атомов водорода в боковом алкильном заместителе, а не в ароматическом кольце.
2. Реакции замещения
2.1. ГалогенированиеБензол и его гомологи вступают в реакции замещения с галогенами (хлор, бром) в присутствии катализаторов (AlCl3, FeBr3). При взаимодействии с хлором на катализаторе AlCl3 образуется хлорбензол: Ароматические углеводороды взаимодействуют с бромом при нагревании и в присутствии катализатора – FeBr3 . Также в качестве катализатора можно использовать металлическое железо. Бром реагирует с железом с образованием бромида железа (III), который катализирует процесс бромирования бензола:
Мета-хлортолуол образуется в незначительном количестве. При взаимодействии гомологов бензола с галогенами на свету или при высокой температуре (300 о С) происходит замещение водорода не в бензольном кольце, а в боковом углеводородном радикале.
Например, при хлорировании этилбензола: 2.2. НитрованиеБензол реагирует с концентрированной азотной кислотой в присутствии концентрированной серной кислоты (нитрующая смесь). При этом образуется нитробензол:
Толуол реагирует с концентрированной азотной кислотой в присутствии концентрированной серной кислоты. В продуктах реакции мы указываем либо о-нитротолуол: Нитрование толуола может протекать и с замещением трех атомов водорода. При этом образуется 2,4,6-тринитротолуол (тротил, тол): 2.3. Алкилирование ароматических углеводородов
2.4. Сульфирование ароматических углеводородовБензол реагирует при нагревании с концентрированной серной кислотой или раствором SO3 в серной кислоте (олеум) с образованием бензолсульфокислоты: 3. Окисление ареновБензол устойчив к действию даже сильных окислителей. Но гомологи бензола окисляются под действием сильных окислителей. Бензол и его гомологи горят. 3.1. Полное окисление – горениеПри горении бензола и его гомологов образуются углекислый газ и вода. Реакция горения аренов сопровождается выделением большого количества теплоты. Уравнение сгорания аренов в общем виде: При горении ароматических углеводородов в недостатке кислорода может образоваться угарный газ СО или сажа С. Бензол и его гомологи горят на воздухе коптящим пламенем. Бензол и его гомологи образуют с воздухом и кислородом взрывоопасные смеси. 3.2. О кисление гомологов бензолаГомологи бензола легко окисляются перманганатом и дихроматом калия в кислой или нейтральной среде при нагревании. При этом происходит окисление всех связей у атома углерода, соседнего с бензольным кольцом, кроме связи этого атома углерода с бензольным кольцом. Толуол окисляется перманганатом калия в серной кислоте с образованием бензойной кислоты: Если окисление толуола идёт в нейтральном растворе при нагревании, то образуется соль бензойной кислоты – бензоат калия: Таким образом, толуол обесцвечивает подкисленный раствор перманганата калия при нагревании.
Более длинные радикалы окисляются до бензойной кислоты и карбоновой кислоты: При окислении пропилбензола образуются бензойная и уксусная кислоты: Изопропилбензол окисляется перманганатом калия в кислой среде до бензойной кислоты и углекислого газа: 4. Ориентирующее действие заместителей в бензольном кольцеЕсли в бензольном кольце имеются заместители, не только алкильные, но и содержащие другие атомы (гидроксил, аминогруппа, нитрогруппа и т.п.), то реакции замещения атомов водорода в ароматической системе протекают строго определенным образом, в соответствии с характером влияния заместителя на ароматическую π-систему.
Типы заместителей в бензольном кольце
В уравнении реакции в качестве продукта записывается либо орто-толуол, либо пара-толуол.
5. Особенности свойств стиролаСтирол (винилбензол, фенилэтилен) – это производное бензола, которое имеет в своем составе двойную связь в боковом заместителе. Общая формула гомологического ряда стирола: CnH2n-8.
Стирол присоединяет водород, кислород, галогены, галогеноводороды и воду в соответствии с правилом Марковникова.
При полимеризации стирола образуется полистирол: Как и алкены, стирол окисляется водным раствором перманганата калия при обычных условиях. Обесцвечивание водного раствора перманганата калия — качественная реакция на стирол: При жестком окислении стирола перманганатом калия в кислой среде (серная кислота) разрывается двойная связь и образуется бензойная кислота и углекислый газ: При окислении стирола перманганатом калия в нейтральной среде при нагревании также разрывается двойная связь и образуется соль бензойной кислоты и карбонат: источники: http://1ku.ru/obrazovanie/20868-formula-nitrobenzola-fizicheskie-i-ximicheskie-svojstva/ http://chemege.ru/ximicheskie-svojstva-areny/ |

 Вам будет интересно: Математика: действия с дробями. Действия с десятичными и обыкновенными дробями
Вам будет интересно: Математика: действия с дробями. Действия с десятичными и обыкновенными дробями Вам будет интересно: Единое водное пространство, разделяющее материки
Вам будет интересно: Единое водное пространство, разделяющее материки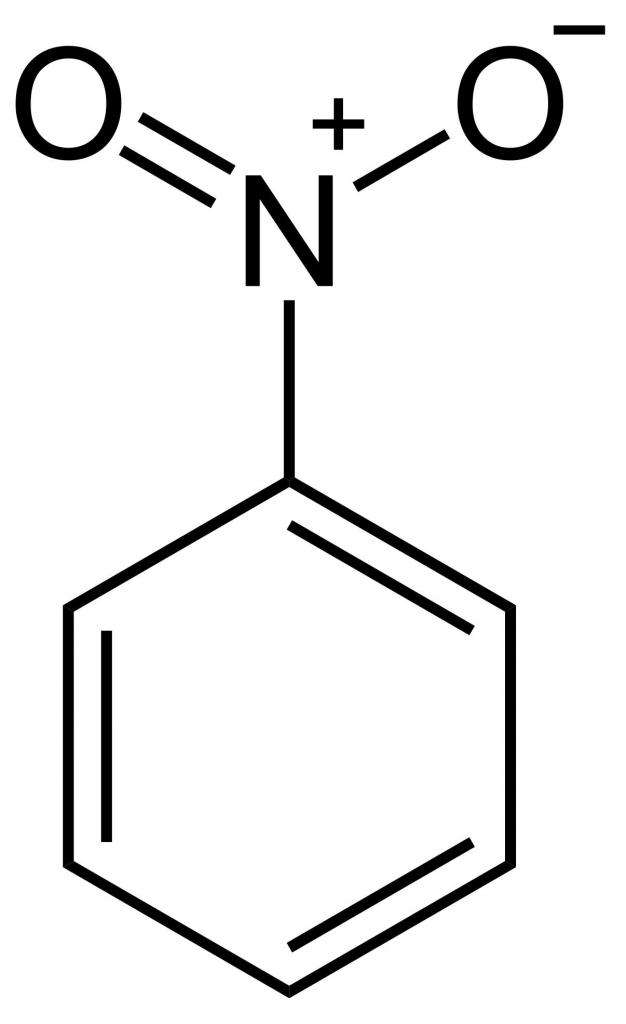
 Вам будет интересно: Какое уравнение не имеет корней? Примеры уравнений
Вам будет интересно: Какое уравнение не имеет корней? Примеры уравнений