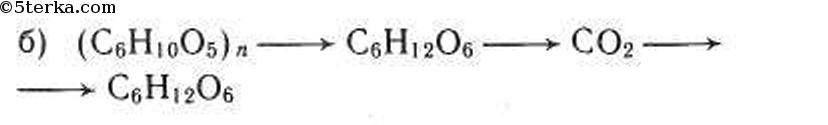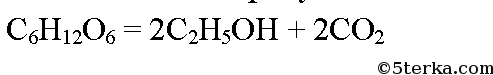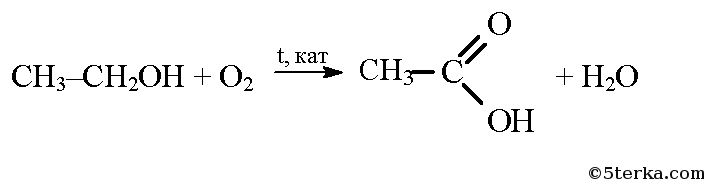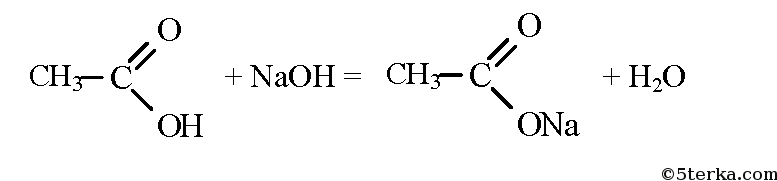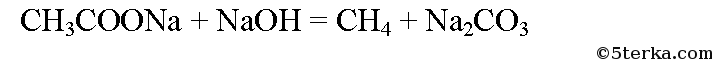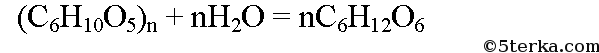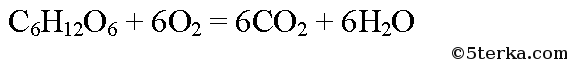Напишите уравнения реакций метан → X1 → X2 → X3 → X2 → уксусная кислота
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,296
- гуманитарные 33,622
- юридические 17,900
- школьный раздел 607,211
- разное 16,830
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Метан: способы получения и свойства
Метан CH4 – это предельный углеводород, содержащий один атом углерода в углеродной цепи. Бесцветный газ без вкуса и запаха, легче воды, нерастворим в воде и не смешивается с ней.
Гомологический ряд метана
Все алканы — вещества, схожие по физическим и химическим свойствам, и отличающиеся на одну или несколько групп –СН2– друг от друга. Такие вещества называются гомологами, а ряд веществ, являющихся гомологами, называют гомологическим рядом.
Самый первый представитель гомологического ряда алканов – метан CH4, или Н–СH2–H.
Продолжить гомологический ряд можно, последовательно добавляя группу –СН2– в углеводородную цепь алкана.
| Название алкана | Формула алкана |
| Метан | CH4 |
| Этан | C2H6 |
| Пропан | C3H8 |
| Бутан | C4H10 |
| Пентан | C5H12 |
| Гексан | C6H14 |
| Гептан | C7H16 |
| Октан | C8H18 |
| Нонан | C9H20 |
| Декан | C10H22 |
Общая формула гомологического ряда алканов CnH2n+2.
Первые четыре члена гомологического ряда алканов – газы, C5–C17 – жидкости, начиная с C18 – твердые вещества.
Строение метана
В молекуле метана встречаются связи C–H. Связь C–H ковалентная слабополярная. Это одинарная σ-связь. Атом углерода в метане образует четыре σ-связи. Следовательно, гибридизация атома углерода в молекуле метана– sp 3 :
При образовании связи С–H происходит перекрывание sp 3 -гибридной орбитали атома углерода и s-орбитали атома водорода:
Четыре sp 3 -гибридные орбитали атома углерода взаимно отталкиваются, и располагаются в пространстве так, чтобы угол между орбиталями был максимально возможным.
Поэтому четыре гибридные орбитали углерода в алканах направлены в пространстве под углом 109 о 28′ друг к другу:
Это соответствует тетраэдрическому строению молекулы.
| Например, в молекуле метана CH4 атомы водорода располагаются в пространстве в вершинах тетраэдра, центром которого является атом углерода |
Изомерия метана
Для метана не характерно наличие изомеров – ни структурных (изомерия углеродного скелета, положения заместителей), ни пространственных.
Химические свойства метана
Метан – предельный углеводород, поэтому он не может вступать в реакции присоединения.
Для метана характерны реакции:
Разрыв слабо-полярных связей С – Н протекает только по гомолитическому механизму с образованием свободных радикалов.
Поэтому для метана характерны только радикальные реакции.
Метан устойчив к действию сильных окислителей (KMnO4, K2Cr2O7 и др.), не реагирует с концентрированными кислотами, щелочами, бромной водой.
1. Реакции замещения
Для метана характерны реакции радикального замещение.
1.1. Галогенирование
Метан реагирует с хлором и бромом на свету или при нагревании.
При хлорировании метана сначала образуется хлорметан:
Хлорметан может взаимодействовать с хлором и дальше с образованием дихлорметана, трихлорметана и тетрахлорметана:
| Химическая активность хлора выше, чем активность брома, поэтому хлорирование протекает быстро и неизбирательно. |
Бромирование протекает более медленно.
Реакции замещения в алканах протекают по свободнорадикальному механизму.
Свободные радикалы R∙ – это атомы или группы связанных между собой атомов, которые содержат неспаренный электрон.
Первая стадия. Инициирование цепи.
Под действием кванта света или при нагревании молекула галогена разрывается на два радикала:
Свободные радикалы – очень активные частицы, которые стремятся образовать связь с каким-либо другим атомом.
Вторая стадия. Развитие цепи.
Радикал галогена взаимодействует с молекулой алкана и отрывает от него водород.
При этом образуется промежуточная частица – алкильный радикал, который в свою очередь взаимодействует с новой нераспавшейся молекулой хлора:
Третья стадия. Обрыв цепи.
При протекании цепного процесса рано или поздно радикалы сталкиваются с радикалами, образуя молекулы, радикальный процесс обрывается.
Могут столкнуться как одинаковые, так и разные радикалы, в том числе два метильных радикала:
1.2. Нитрование метана
Метан взаимодействует с разбавленной азотной кислотой по радикальному механизму, при нагревании до 140 о С и под давлением. Атом водорода в метане замещается на нитрогруппу NO2.
Например. При нитровании метана образуется преимущественно нитрометан:2. Реакции разложения метана (д егидрирование, пиролиз)При медленном и длительном нагревании до 1500 о С метан разлагается до простых веществ: Если процесс нагревания метана проводить очень быстро (примерно 0,01 с), то происходит межмолекулярное дегидрирование и образуется ацетилен: Пиролиз метана – промышленный способ получения ацетилена. 3. Окисление метанаАлканы – малополярные соединения, поэтому при обычных условиях они не окисляются даже сильными окислителями (перманганат калия, хромат или дихромат калия и др.). 3.1. Полное окисление – горениеАлканы горят с образованием углекислого газа и воды. Реакция горения алканов сопровождается выделением большого количества теплоты. Уравнение сгорания алканов в общем виде: При горении алканов в недостатке кислорода может образоваться угарный газ СО или сажа С. Промышленное значение имеет реакция окисления метана кислородом до простого вещества – углерода: Эта реакция используется для получения сажи. 3.2. Каталитическое окисление
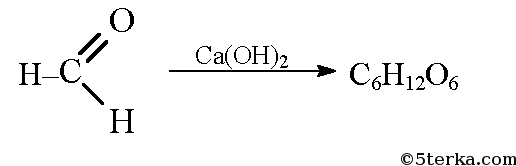
Продукт реакции – так называемый «синтез-газ». Получение метана1. Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца)Это один из лабораторных способов получения алканов. При этом происходит удвоение углеродного скелета. Реакция больше подходит для получения симметричных алканов. Получить таким образом метан нельзя. 2. Водный или кислотный гидролиз карбида алюминияЭтот способ получения используется в лаборатории для получения метана. 3. Декарбоксилирование солей карбоновых кислот (реакция Дюма)Реакция Дюма — это взаимодействие солей карбоновых кислот с щелочами при сплавлении. R–COONa + NaOH → R–H + Na2CO3 Декарбоксилирование — это отщепление (элиминирование) молекулы углекислого газа из карбоксильной группы (-COOH) или органической кислоты или карбоксилатной группы (-COOMe) соли органической кислоты. При взаимодействии ацетата натрия с гидроксидом натрия при сплавлении образуется метан и карбонат натрия: 4. Синтез Фишера-ТропшаИз синтез-газа (смесь угарного газа и водорода) при определенных условиях (катализатор, температура и давление) можно получить различные углеводороды: Это промышленный процесс получения алканов. Синтезом Фишера-Тропша можно получить метан: 5. Получение метана в промышленностиВ промышленности метан получают из нефти, каменного угля, природного и попутного газа . При переработке нефти используют ректификацию, крекинг и другие способы. Уравнение реакции метана с уксусной кислотойПолучают в три этапа: Формула уксусной кислоты СН3СООН Если ответ по предмету Химия отсутствует или он оказался неправильным, то попробуй воспользоваться поиском других ответов во всей базе сайта. а) При окислении метана в присутствии катализатора образуется мета-наль (формальдегид): В присутствии гидроксида кальция из метаналя образуется смесь углеводов, в том числе глюкоза: При спиртовом брожении глюкозы образуется этиловый спирт: При окислении этилового спирта в присутствии катализатора образуется уксусная кислота: Из уксусной кислоты в две стадии можно получить метан. При взаимодействии уксусной кислоты и гидроксида натрия образуется натриевая соль уксусной кислоты — ацетат натрия. При сильном нагревании ацетата натрия с твердым гидроксидом натрия выделяется метан: При гидролизе крахмала образуется глюкоза. Уравнение реакции: При сжигании глюкозы образуется оксид углерода (IV): Превращение оксида углерода в глюкозу осуществимо только в клетках растений, содержащих хлорофилл, в процессе фотосинтеза: Уксусная кислота – вещество с химической формулой СН3СООН. Она относится к классу карбоновых кислот, обширно распространена в природе. Являясь продуктом брожения, знаменита человеку издавна. Представляет собою бесцветную жидкость с характерным и крайне крутым запахом. Хорошо смешивается с водой. Как получают уксусную кислоту ? Инструкция1. Методов ее приобретения дюже много. Их использование зависит, раньше каждого, от экономической производительности. По этой причине теперь теснее не применяются обширно распространенные раньше методы, такие, как окисление уксусного альдегида либо типичного бутана. Их давным-давно вытеснил метод карбонилирования метилового спирта окисью углерода (угарным газом), происходящий по дальнейшей схеме:СН3ОН + СО = СН3СООНОн крайне распространен до сего времени. 2. Уксусную кислоту дозволено получать и из метана . Ниже приведены методы поэтапно. CH4 + Cl2 = CH3Сl + HCl (Образуются хлорметан и хлороводород). 2CH3Cl + 2Na = C2H6 + 2NaCl ( «Реакция Вюрца», с образованием этана и хлористого натрия). C2H6 + Cl2 = C2H5Cl + HCl (Образуются хлорэтан и хлороводород). C2H5Cl + Cl2 = C2H4Cl2 + HCl (Образуются дихлорэтан и хлороводород). C2H4Cl2 + Cl2 = C2H3Cl3 + HCl (Образуются трихлорэтан и хлороводород). C2H3Cl3 + 3NaOH = CH3COOH + H2O + 3NaCl (Образуется уксусная кислота). 2CH4 = C2H4 + 2H2 (образуются этилен и водород). C2H4 + H2O = C2H5OH (гидратацией этилена получаем этиловый спирт). 3. Также существуют и другие способы: C2H5OH + CuO = CH3COH + Cu + H2O (этиловый спирт, восстанавливая медь из ее оксида, превращается в уксусный альдегид). 2CH3COH + O2 = 2CH3COOH (окислением уксусного альдегида, получаем уксусную кислоту). 2CH4 = C2H2 + 3H2 (образуются ацетилен и водород). C2H2 + H2O = CH3COH (гидратацией ацетилена получаем уксусный альдегид, т.н. «Реакция Кучерова»). 2CH3COH + O2 = 2CH3COOH (Как в предыдущем примере, окислением уксусного альдегида получаем уксусную кислоту). Еще с глубокой древности люди знали и применяли уксусную кислоту не только в пище, но даже и в медицине. Для ее создания вовсе не нужно было заниматься наукой, что–то постигать, открывать, проводить эксперименты, довольно было примитивно позабыть закрыть крышкой бутылку какого-либо слабенького винца. Вино примитивно скисало под действием уксусного грибка, находящегося в воздухе, и превращалось в уксус. Вам понадобится
Инструкция1. В промышленности уксусная кислота получается окислением ацетальдегида, но ее дозволено получить и перегонкой древесины. Необходимо взять древесные щепки (отличнее будет если древесина содержит минимальное число смолы) и разместить их в дистиллятор (вернее перегонный куб), а позже начать нагрев. В начале процесса будет выдаваться дым, а позднее в приемнике дистиллятора начнет скапливаться жидкость, приемник не должен быть герметичным, дабы не возрастало давление, т.к. не все газы конденсируются. Перегонка ведется до того момента, пока не обуглится древесина. 2. Позже заключения перегонки даем жидкости отстояться, позже жидкость расслаивается на две фазы: смола и прозрачный раствор. Отфильтровываем раствор и вновь перегоняем. Приблизительно при 80 градусах Цельсия отгоняется немножко жидкости, это в основном метанол (дюже ядовит) и немножко ацетона. Когда отгонится каждый метанол, температуру повышаем и отгоняем раствор уксусной кислоты с водой, а в остатке остаются смолы. Дальше к раствору кислоты понемногу добавляем сообщи, до тех пор, пока не исчезнет кислотность среды (пока раствор не перестанет окрашивать лакмусовую бумагу в алый цвет). Кислота взаимодействует с известью и получается ацетат кальция. Дальше, данный ацетат смешиваем с концентрированной серной кислотой, происходит обменная реакция с образованием прочной уксусной кислоты, тем же методом отгоняем с подмогой дистилляции уксусную кислоту , а в остатке остается сернокислая кальциевая соль. 3. Но в приготовлении пищи отменнее каждого применять уксус настоящий, на данный случай существует восхитительный рецепт яблочного уксуса. Надобно измельчить яблоки и залить их теплой водой (кипяченой), расчет ведется так, приблизительно 0,5 литра воды на 400 грамм яблок. На всякий литр воды надобно 100 грамм сахара и 10 грамм хлебных дрожжей. Все это дело удерживаем в открытой емкости, в темном месте. Раза три в день нужно помешивать раствор, но это только первые 10 – 12 суток. После этого, эту массу необходимо отжать, а сока процедив слить в банку либо кастрюлю. После этого на всякий литр сока добавить еще 100 грамм сахара. Кастрюлю закрывают и хранят в тепле. Для того, дабы получился добротный уксус его надобно выдерживать от 40 до 60 суток. Видео по теме Обратите внимание! Полезный совет Этилен – это горючий газ, он владеет слабым запахом. Этилен применяют в производстве гидролизного этилового спирта, этиленгликоля (основная часть тосола), стирола, полиэтилена и многого иного. Получают его при помощи пиролиза (нагревания без доступа воздуха) нефтяных фракций, скажем прямогонного бензина и т.п. Но существуют методы приобретения этилена без применения нефтепродуктов. Вам понадобится
Инструкция1. В емкость из жаропрочного материала разместите немножко оксида алюминия и закройте ее крышкой с двумя газоотводными трубками, одну из которых разместите в пробирку с концентрированной серной кислотой. Нагрейте емкость на газовой горелке, температура оксида алюминия должна быть приблизительно, от 350 до 500 градусов. 2. Дальше, в отдельную пробирку налейте немножко чистого этилового спирта. Закройте пробирку пробкой с газоотводной трубкой и нагрейте ее на спиртовой горелке. Газоотводную трубку объедините с емкостью, в которой находится оксид алюминия. При нагревании спирт начнет испаряться, проходя по газоотводу, попадет в емкость с оксидом алюминия, а при высокой температуре на оксиде алюминия будет протекать дегидратация, т.е. отщепление воды от молекул спирта. Из емкости будет выходить этилен с водяным паром и не прореагировавший спирт в газообразном состоянии. Эта смесь попадет в пробирку с серной кислотой, которая служит для обезвоживания смеси. 3. Смешайте этиловый спирт и концентрированную серную кислоту. Произойдет реакция с образованием кислого этилового эфира. Нагрейте смесь, при нагревании произойдет процесс дегидратации спирта с выделением этилена. Видео по теме Обратите внимание! Этан – один из зачастую встречающихся в природе газов. Это органическое вещество, которое наравне с метаном входит в состав нефти и природного газа. Из него получают этилен, тот, что, в свою очередь, является сырьем для приобретения уксусной кислоты, этилового спирта, винилацетата ряда других веществ. В качестве начального материала для приобретения этана обыкновенно применяется метан. Инструкция1. Как метан, так и этан относятся к классу органических соединений, называемых алканами. Они, в свою очередь, являются частными случаями предельных углеводородов. Углеводороды представляют собой органические соединения, молекулы которых состоят, как и следует из их наименования, из атомов углерода и водорода.Метан является первым поверенным гомологического ряда алканов. Дальше за ним следуют этан, пропан , бутан и ряд других веществ. Формулы предельных углеводородов выражаются дальнейшим образом: CnH2n+2. Метан и этан между собой являются гомологами. Так именуются вещества, идентичные по химическим свойствам, но различные по составу, и, следственно, физическим свойствам. Состав гомологов отличается на CH2-группу. 2. Существует два основных метода приобретения этана из метана . 1-й из них заключается в использовании реакции Вюрца, открытой в 1870 году. Данная реакция основана на взаимодействии галогенопроизводных предельных углеводородов с металлическим натрием. В частности, она может быть осуществлена в отношении хлорметана . Для упрощения хода реакции нужно добавить к этому соединению натрий. Он вступит в реакцию с молекулами хлора. Натрий присоединит к себе молекулы хлора, в итоге чего получится этан:CH3—CH3хлорметан?-2NaCl?C2H6Для того, дабы получить этан, следует заранее подготовить хлорметан. Он получается путем нагрева метана и хлора до 400 градусов. Позже этого, проводят реакцию Вюрца как показано выше. 3. 2-й метод является многоступенчатым. Сначала метан окисляют до ацетилена, а после этого ацетилен гидрируют до этана. Окисление метана до ацетилена проходит дальнейшим образом:4CH4+4O2?CH?CH+CO2+CO+5H2O+2H2Далее приступают к гидрированию ацетилена. В итоге двойного гидрирования окончательным продуктом реакции становится этан:CH3?CH3?CH2=CH2?C2H6 (Гидрирование по водородному радикалу H2)Невзирая на то, что этан почаще каждого получают несколько иными методами -это способ все равно изредка используется, исключительно когда начальным веществом может быть только метан. Метан и этан -газы одного класса и одной группы, следственно одно из иного легко получить. Обратите внимание! Хлорэтан (другие наименования – хлористый этил, этилхлорид) представляет собою бесцветный газ, имеет химическую формулу C2Н5Cl. Смешивается с этиловым спиртом и диэтиловым эфиром, примерно не смешивается с водой. Каким образом дозволено получить это вещество? Инструкция1. Существует два основных индустриальных способа синтеза хлорэтана :1) Путем гидрохлорирования этилена (этена).2) Путем хлорирования этана. 2. В текущее время больше многообещающим и экономически обоснованным признан 2-й метод. Реакция протекает таким образом: С2Н6 + Cl2 = C2H5Cl + HCl 3. Как и любая стандартная реакция галогенирования алканов, она протекает по т.н. «радикальному механизму». Для того, дабы инициировать ее предисловие, смесь: алкан (в данном случае, этан) – галоген (в данном случае, хлор) нужно подвергнуть насыщенному ультрафиолетовому облучению. 4. Под действием света молекула хлора распадается на радикалы. Эти радикалы здесь же вступают во взаимодействие с молекулами этана, забирая у них атом водорода, в итоге этого образуются этильные радикалы •С2Н5, которые, в свою очередь, разрушают молекулы хлора, образуя новые радикалы. То есть происходит так сказать «цепная реакция». 5. Возрастание температуры увеличивает скорость хлорирования этана. Впрочем от того что также нарастает «выход» других хлорсодержащих производных этана, что неугодно, эту реакцию проводят при низких температурах, для максимально допустимого приобретения целевого продукта. Полезный совет Видео по теме Полезный совет источники: http://chemege.ru/metan/ http://piteika.com/zavisimosti/kak-poluchit-metan-iz-uksusnoj-kisloty.html |

















 Решебник по химии за 10 класс (Г.Е.Рудзитис, Ф.Г.Фельдман, 2000 год),
Решебник по химии за 10 класс (Г.Е.Рудзитис, Ф.Г.Фельдман, 2000 год),