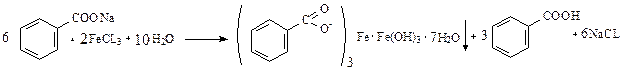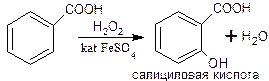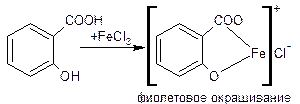Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Подлинность. 1. ФС УФ-спектр водного раствора натрия бензоата в области 220-300 нм должен иметь максимум поглощения при 226±2 нм.1. ФС УФ-спектр водного раствора натрия бензоата в области 220-300 нм должен иметь максимум поглощения при 226±2 нм. 2. ФС. Реакция солеобразования с солями тяжелых металлов (с FеСl3). Реакция на бензоат-ион. Кислоту предварительно переводят в натриевую соль. Проводится в нейтральной среде, т.к. в кислой среде осадок комплексной соли растворяется (поэтому кислоту предварительно растворяют в 0,1н NаОН), а в щелочной – выпадает бурый осадок Fе(ОН)3. Эффект реакции — образование труднорастворимой комплексной соли железа окрашенной в розовато-желтый цвет (телесный цвет). бензойная кислота экв. осадок розовато-желтого цвета 3. ФС температура плавлениябензойной кислоты.В натрия бензоате её получают, обработав препарат азотной кислотой, определяют температуру плавления выпавшей в осадок бензойной кислоты. 4.ФССоль натрия, внесенная в бесцветное пламя, окрашивает его в желтый цвет (катион натрия). Не фармакопейные реакции: 5. с Н2О2 в присутствии катализатора FеSО4 из бензойной образуется салициловая кислота и последующее добавление FеСl3 вызывает появление фиолетового окрашивания, а не розовато-желтого. 6.С CuSO4в нейтральной среде образуется осадок соли меди сине-зеленого цвета. При последующем добавлении хлороформа, слой хлороформа окрашивается в голубой цвет, водный – обесцвечивается (экстракция продукта реакции, т.к. неполярное соединение). осадок сине-зелёноro цвета 7. В нейтральной среде при добавлении к раствору АgNO3образуется осадок белого цвета. C6H5COOАg↓. Бензоат натрия структура, свойства, синтез, использование и рискибензоат натрия представляет собой органическую соль, химическая формула которой C6H5COONa. Это произведено или произведено реакцией нейтрализации между бензойной кислотой и гидроксидом натрия. В результате получается белое твердое вещество (нижнее изображение), растворимое в воде и разлагающееся при нагревании до 120 ° C.. Эту соль можно найти в природе в различных фруктах и других частях овощей, таких как: черника, слива, изюм, корица, гвоздика и яблоки. Это также метаболит водорослей и растений. Бензоат натрия не накапливается в организме, так как быстро соединяется с аминокислотой глицин с образованием гиппуровой кислоты, которая свободно выводится с мочой.. Это соединение используется с пищевым консервантом, его действие более эффективно при кислотном pH. Это связано с наличием органических кислот, которые дают пище pH, подходящий для действия бензоата натрия; который, как таковой, заканчивается протонированием в бензойную кислоту. Эта соль также используется для лечения наследственных метаболических нарушений цикла мочевины, что приводит к накоплению промежуточного метаболита, для которого фермент, который обрабатывает его, является дефицитным.. Международная программа по химической безопасности не обнаружила вредного воздействия бензоата натрия на человека при потреблении от 647 до 825 мг / кг массы тела.. Однако сообщалось, что бензоат натрия может вызывать псевдоаллергические реакции и обострять симптомы у пациентов с частыми приступами крапивницы и астмы..
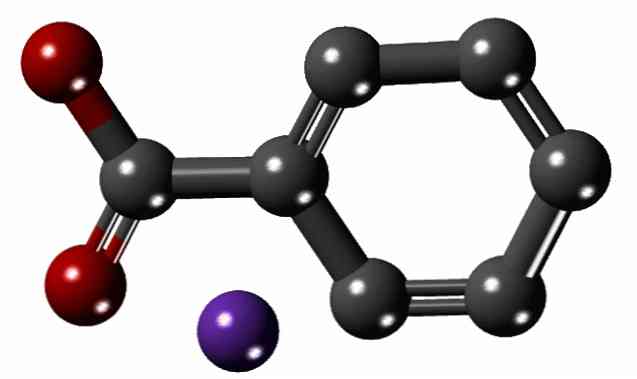
Структура бензоата натрияНа верхнем изображении показана структура бензоата натрия с моделью сфер и стержней. Ароматическое кольцо видно невооруженным глазом, с карбоксилатной группой -COO — , связано с ним (что из красных сфер); а последний, в свою очередь, электростатически притягивает катион Na + (фиолетовая сфера). Поскольку разница в размерах между двумя ионами велика (сравните на изображении), неудивительно, что ретикулярная энергия кристаллов бензоата натрия низкая. Это приводит к тому, что их кристаллы имеют естественную тенденцию растворяться в полярных растворителях или подвергаться ряду химических реакций.. C6H5COO — Он может принимать два водородных мостика из двух молекул воды, что способствует его гидратации. Между тем, На + Он также заканчивается сольватированной водой, преодолевая электростатические силы, которые удерживают его вместе с C6H5COO — . Итак, эта соль состоит из ионов C6H5COO — и на + , которые расположены упорядоченным образом, чтобы построить кристаллы. В литературе нет информации о его кристаллической структуре, поэтому неизвестно, какой тип элементарной ячейки для этой соли. свойстваХимические названия-Натриевая соль бензойной кислоты Физическое описаниеБелые гранулы или кристаллический порошок. Бесцветный кристаллический порошок. источники: http://helpiks.org/5-7132.html http://ru.thpanorama.com/articles/qumica/benzoato-de-sodio-estructura-propiedades-sntesis-usos-y-riesgos.html |