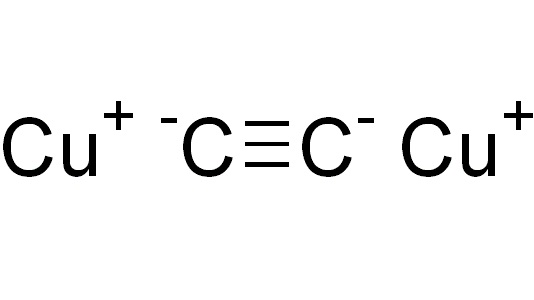Ацетиленид меди(I): получение и свойства
Ацетиленид меди является металлорганическим бинарным соединением. Данная формула известна науке по крайней мере с 1856 года. В кристаллах образует моногидрат с формулой Cu2C2×H2O. Термически неустойчив, при нагревании взрывается.
Строение
Ацетиленид меди является бинарным соединением. Можно условно выделить в нем отрицательно заряженную часть — анион C 2− 2, и положительно заряженную — катионы меди Cu + . На самом деле такое деление условно: в соединении есть лишь доля ионной связи, хотя она больше по сравнению со связью H-C≡. Но и указанная связь имеет очень сильную полярность (как для ковалентной) из-за того, что атом углерода с тройной связью находится в sp-гибридизации — его относительная электроотрицательность больше, чем в гибридизациях sp 3 (одинарная связь) или sp 2 (двойная связь). Именно это позволяет углероду в ацетилене сравнительно легко отщеплять от себя атом водорода и замещать его атомом металла, то есть проявлять свойства, присущие кислотам.
Получение
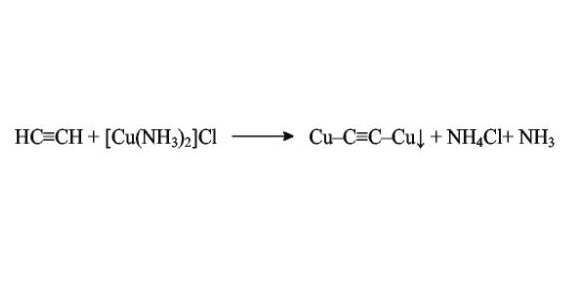
Наиболее распространенный способ получения ацетиленида меди в лаборатории — пропускание газообразного ацетилена сквозь аммиачный раствор хлорида меди(I). В результате образуется нерастворимый осадок ацетиленида красноватого цвета.
Вместо хлорида меди(I) также можно использовать ее гидроксид Cu2O. В обоих случаях важно то, что фактически реакция идет с аммиачным комплексом меди.
Физические свойства
Ацетиленид меди в чистом виде — темные красно-коричневые кристаллы. На самом деле это моногидрат — в осадке каждой молекуле ацетиленида соответствует одна молекула воды (записывается в виде Cu2C2×H2O). Сухой ацетиленид меди взрывоопасен: может сдетонировать при нагревании (он менее термически устойчив, чем ацетиленид серебра), а также при механическом воздействии, например при ударе.
По этому поводу существует предположение, что медные трубы на химических производствах несут большую опасность, так как при длительной эксплуатации внутри образовывается ацетиленид, который потом может привести к сильному взрыву. Особенно это актуально для области нефтехимии, где медь, а также ее ацетилениды используются также и в качестве катализаторов, что повышает уровень риска.
Химические свойства
Мы уже говорили о том, что углерод с тройной связью в ацетилене гораздо более электроотрицателен, чем, например, углерод со связью двойной (как в этилене) или одинарной (в этане). Способность ацетилена реагировать с некоторыми металлами, отдавая ион водорода и замещая его ионом металла (например, реакция образования ацетиленида натрия при взаимодействии ацетилена с металлическим натрием) подтверждает это. Мы называем эту способность ацетилена одним из кислотных свойств в соответствии с теорией Бренстеда — Лоури: согласно ей, кислотность вещества определяется его способностью отщепить от себя протон. Кислотность ацетилена (в ацетилениде меди также) можно рассмотреть относительно аммиака и воды: при взаимодействии амида металла с ацетиленом образуется ацетиленид и аммиак. То есть ацетилен отдает протон, что характеризует его как более сильную, чем аммиак, кислоту. В случае с водой ацетиленид меди разлагается, образуя ацетилен — он принимает протон воды, показывая себя менее сильной кислотой, чем вода. Так, в относительном ряде кислотности (по Бренстеду — Лоури) ацетилен является слабой кислотой, находясь где-то между водой и аммиаком.
Ацетиленид меди(I) неустойчив: в воде (как нам уже известно) и в растворах кислот он разлагается с выделением газа ацетилена и красно-коричневого осадка — оксида меди(I) или белого осадка хлорида меди(I) в случае разбавления раствором соляной кислоты.
Чтобы избежать взрыва, разложение ацетиленида проводят аккуратным нагреванием во влажном виде в присутствии сильной минеральной кислоты, например разбавленной азотной.
Использование
Реакция образования ацетиленида меди(I) может быть качественной для обнаружения терминальных (с тройной связью на конце) алкинов. Индикатором является выпадения нерастворимого красно-коричневого осадка ацетиленида.
На крупнотоннажном производстве — например, в нефтехимии — ацетиленид меди(I) не используется, поскольку взрывоопасен и неустойчив в воде. Однако с ним связаны несколько специфичных реакций в так называемом тонком синтезе.
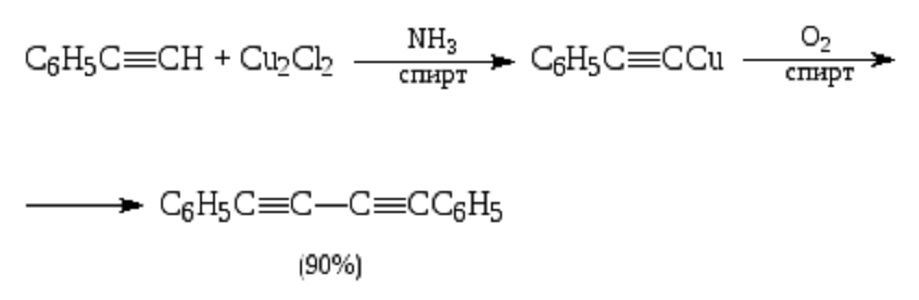
Ацетиленид меди(I) также может использоваться в качестве нуклеофильного реагента в органическом синтезе. В частности, важную роль он играет в процессе синтеза полиинов — соединений с несколькими чередующимися тройными и одинарными связями. Ацетилениды меди(I) в спиртовом растворе окисляются кислородом воздуха, конденсируясь с образованием диинов. Это реакция Глазера — Эллингтона, открытая в 1870 году и позже усовершенствованная. Медь(I) здесь играет роль катализатора, так как сама в процессе не расходуется.
Позже вместо кислорода в качестве окислителя был предложен гексацианоферрат(III) калия.
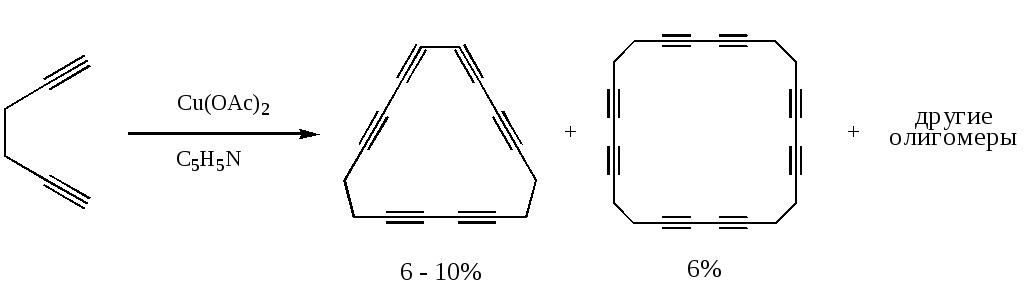
Эллингтон усовершенствовал метод получения полиинов. Вместо изначально вводившихся в раствор алкинов и солей меди(I), например хлорида он предложил брать ацетат меди(II), который окислял бы алкин в среде уже другого органического растворителя — пиридина — при температуре 60-70 °С.
Такая модификация позволила получать из диинов гораздо более крупные и устойчивые молекулы — макроциклы.
Ацетиленид меди (I)
| Ацетиленид меди (I) | |
|---|---|
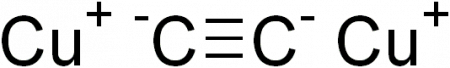 | |
| Систематическое наименование | Ацетиленид меди (I) |
| Традиционные названия | Углеродистая медь; карбид меди |
| Хим. формула | Cu2C2 |
| Состояние | кристаллы |
| Молярная масса | 151,11 г/моль |
| Рег. номер CAS | 1117-94-8 |
| PubChem | 19021056 |
| SMILES | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Ацетиленид меди (I) — бинарное неорганическое соединение меди и углерода, химическая формула Cu2C2 красно-коричневые, иногда черные кристаллы. В сухом виде кристаллы детонируют при ударе или нагреве. При детонации в отсутствие кислорода не образуется газообразных веществ. Известен моногидрат соединения состава Cu2C2·H2O.
Содержание
Получение
Образуется в виде осадка при пропускании ацетилена в аммиачные растворы солей меди (I).
Эта реакция используется для качественного обнаружения ацетилена.
Химические свойства
Разлагается под действием кислот. В сухом виде взрывоопасен.
Синтез хлорида меди (I). Получение ацетиленида серебра и ацетиленида меди (I).
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
МУНИЦИПАЛЬНОЕ ОБЩЕОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ СРЕДНЯЯ ОБЩЕОБРАЗОВАТЕЛЬНАЯ ШКОЛА с. ОКТЯБРЬСКОЕ
СТЕРЛИТАМАКСКОГО РАЙОНА РЕСПУБЛИКИ БАШКОРТОСТАН
Секция: Мир химии
Номинация: Учёные будущего
Получение ацетиленида серебра и ацетиленида меди
Выполнила: Лукманова Ангелина, ученица 11 класса МОБУ СОШ
Научный руководитель: Исхакова Р.У., учитель химии МОБУ СОШ
Получение ацетиленида серебра и ацетиленида меди
получение ацетиленида серебра;
получение ацетиленида меди;
доказать свойства веществ.
Оборудование: колба, делительная воронка, воронка Бюхнера, газоотводная трубка, стакан, штатив, фильтровальная бумага, штатив с пробирками, ложечка.
Химикаты: гидрат аммиака ( NH 4 OH ), нитрат серебра ( AgNO 3 ), карбид кальция ( CaC 2 ), вода, хлорид меди ( CuCl ).
Получение ацетиленида серебра
Подготовка оборудования и химикатов.
Получение аммиачного раствора оксида серебра.
Наполнили на четверть пробирку гидратом аммиака. Добавили столько же оксида серебра. Перемешали. Получили аммиачный раствор оксида серебра.
Закрепили колбу в штативе. Газоотводную трубку опустили в пробирку с аммиачным раствором оксидом серебра.
В колбу насыпали 15 грамм карбида кальция. Плотно закрыли. В делительную воронку приливали воду до образования ацетилена.
Получение ацетиленида серебра.
Пройдя через газоотводную трубку, ацетилен провзаимодействовал с аммиачным раствором оксида серебра. В результате чего образовался чёрный осадок-ацетиленид серебра.
Фильтрование и сушка.
Осадок отфильтровали. Затем высушили.
Ацетиленид серебра- очень неустойчивое взрывчатое вещество.
Провели проверку : поднесли горящую спичку к 2 граммам ацетиленида серебра. Произошёл взрыв.
Получение ацетиленида меди
Подготовка оборудования и химикатов.
Получение аммиачного раствора хлорида меди.
Наполнили на четверть пробирку гидратом аммиака. Добавили 10 грамм хлорида меди ( I ). Перемешали до растворения. Получили аммиачный раствор хлорида меди.
Закрепили колбу в штативе. Газоотводную трубку опустили в пробирку с аммиачным раствором хлорида меди ( I ).
Получение ацетиленида меди.
В колбу насыпали 15 грамм карбида кальция. Плотно закрыли. В делительную воронку приливали воду до образования ацетилена.
Пройдя через газоотводную трубку, ацетилен провзаимодействовал с аммиачным раствором хлорида меди ( I ). В результате чего образовался красный осадок-ацетиленид меди.
Фильтрование и сушка.
Осадок отфильтровали. Затем высушили.
Ацетиленид меди — очень неустойчивое взрывчатое вещество.
Провели проверку: поднесли горящую спичку к 2 граммам ацетиленида меди. Произошёл взрыв.
Проблемы в ходе опыта
Может возникнуть проблема с хлоридом меди ( I ): если он получен не в чистом виде, тогда при его добавлении в гидрат аммиака он растворится не полностью. Чтобы решить эту проблему, нужно отфильтровать раствор.
Был получен ацетиленид серебра-очень неустойчивое взрывчатое вещество.
Был получен ацетиленид меди-очень неустойчивое взрывчатое вещество.
Репетитор по химии/ под ред. А.С. Егорова. – Изд. 41-е – Ростов н/Д: Феникс,2014. – 762, [1] с. : ил. – (Абитуриент).
Курс повышения квалификации
Дистанционное обучение как современный формат преподавания
- Сейчас обучается 925 человек из 80 регионов
Курс повышения квалификации
Педагогическая деятельность в контексте профессионального стандарта педагога и ФГОС
- Курс добавлен 23.11.2021
- Сейчас обучается 35 человек из 23 регионов
Курс повышения квалификации
Инструменты онлайн-обучения на примере программ Zoom, Skype, Microsoft Teams, Bandicam
- Курс добавлен 31.01.2022
- Сейчас обучается 24 человека из 14 регионов
Ищем педагогов в команду «Инфоурок»
Дистанционные курсы для педагогов
«Взбодрись! Нейрогимнастика для успешной учёбы и комфортной жизни»
Свидетельство и скидка на обучение каждому участнику
Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
5 575 996 материалов в базе
Самые массовые международные дистанционные
Школьные Инфоконкурсы 2022
33 конкурса для учеников 1–11 классов и дошкольников от проекта «Инфоурок»
Другие материалы
- 10.01.2016
- 3376
- 11
- 10.01.2016
- 6620
- 20
- 09.01.2016
- 16334
- 96
- 09.01.2016
- 1119
- 3
- 09.01.2016
- 1394
- 0
- 09.01.2016
- 807
- 0
- 09.01.2016
- 4418
- 19
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Добавить в избранное
- 10.01.2016 4058
- DOCX 26.8 кбайт
- 5 скачиваний
- Оцените материал:
Настоящий материал опубликован пользователем Исхакова Руфина Ураловна. Инфоурок является информационным посредником и предоставляет пользователям возможность размещать на сайте методические материалы. Всю ответственность за опубликованные материалы, содержащиеся в них сведения, а также за соблюдение авторских прав несут пользователи, загрузившие материал на сайт
Если Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с сайта, Вы можете оставить жалобу на материал.
Автор материала
- На сайте: 7 лет и 3 месяца
- Подписчики: 3
- Всего просмотров: 332433
- Всего материалов: 79
Московский институт профессиональной
переподготовки и повышения
квалификации педагогов
Дистанционные курсы
для педагогов
663 курса от 690 рублей
Выбрать курс со скидкой
Выдаём документы
установленного образца!
Учителя о ЕГЭ: секреты успешной подготовки
Время чтения: 11 минут
В школах Хабаровского края введут уроки спортивной борьбы
Время чтения: 1 минута
Тринадцатилетняя школьница из Индии разработала приложение против буллинга
Время чтения: 1 минута
Полный перевод школ на дистанционное обучение не планируется
Время чтения: 1 минута
Приемная кампания в вузах начнется 20 июня
Время чтения: 1 минута
В Воронеже продлили удаленное обучение для учеников 5-11-х классов
Время чтения: 1 минута
Инфоурок стал резидентом Сколково
Время чтения: 2 минуты
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
http://chem.ru/acetilenid-medi-i.html
http://infourok.ru/sintez-hlorida-medi-i-poluchenie-acetilenida-serebra-i-acetilenida-medi-i-747728.html