Please wait.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 6e283ed23d239769 • Your IP : 85.95.188.35 • Performance & security by Cloudflare
Цистеин: формула и описание вещества
Все белки нашего организма построены из аминокислот. Белков в организме огромное множество, а кирпичиков — аминокислот, из которых они состоят, всего 20. Таким образом, белки отличаются друг от друга набором аминокислот и их последовательностью. Цистеин является одной из этих 20 аминокислот.
Цистеин — что это такое?
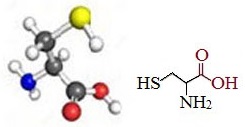
Цистеин — алифатическая серосодержащая аминокислота. Алифатическая — содержащая только насыщенные связи. Как и у любой аминокислоты, формула цистеина включает карбоксильную (-СООН) и аминогруппу (-NH2), а также уникальную тиоловую (-SH). В состав тиоловой (другое название — сульфгидрильной) группы входит атом серы и атом водорода.
Молекулярная химическая формула цистеина — С3Н7NO2S. Молекулярная масса — 121.
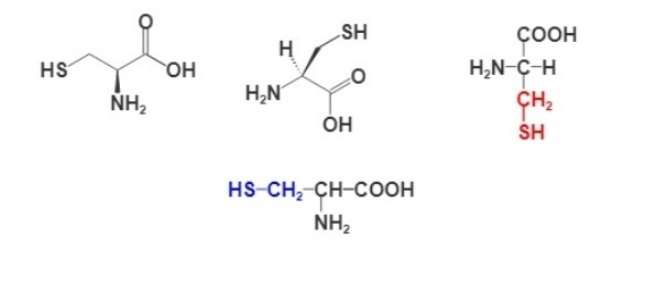
Формула аминокислоты цистеина
Для изображения строения аминокислот используют разные формулы. Ниже представлены несколько вариантов написания структурной формулы цистеина.
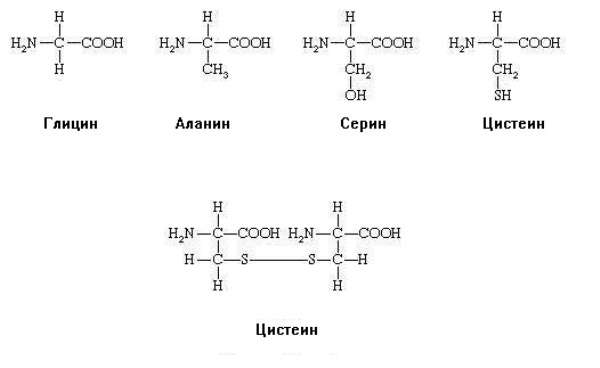
Все аминокислоты имеют амино- и карбоксильную группы, присоединенные к α-углеродному атому, и отличаются только строением радикала, присоединенному к этому же атому углерода. Например, ниже представлены структурные формулы аланина, цистеина и глицина, серина а также цистина.

Все аминокислоты имеют одинаковый остов и разные радикалы. Именно строение радикала лежит в основе квалификации аминокислот и определяет свойства самой молекулы. У цистеина формула радикала — СН2-SH. Этот радикал относится к группе полярных незаряженных, гидрофильных. Это значит, что участки белка, содержащие цистеин, могут присоединять воду (гидратироваться) и взаимодействовать при помощи водородных связей с другими участками белка, также содержащими аминокислоты с гидрофильными группами.
Цистеин содержит уникальную тиоловую группу
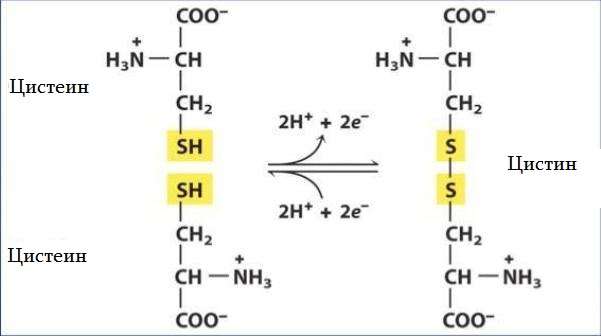
Цистеин — уникальная аминокислота. Она единственная среди 20 природных аминокислот содержит тиоловую (-HS) группу. Тиоловые группы могут подвергаться окислительным и восстановительным реакциям. При окислении тиоловой группы цистеина образуется цистин — аминокислота, представляющая собой два цистеиновых остатка, соединенных дисульфидной связью. Реакция обратима — восстановление дисульфидной связи регенерирует две молекулы цистеина. Дисульфидные связи цистина имеют решающее значение для определения структур многих белков.

Окисление тиоловой группы цистеина приводит к образованию дисульфидной связи с другим тиолом, в ходе дальнейшего окисления образуются сульфиновые и сульфоновые кислоты.
Благодаря способности вступать в окислительно-восстановительные реакции, цистеин обладает антиоксидантными свойствами.
Цистеин — компонент белков
Аминокислоты, входящие в состав белков, называют протеиногенными. Как уже было сказано, их 20, и цистеин — один из них. Для формирования первичной структуры белка аминокислоты соединяются между собой в длинную цепь. Соединение идет за счет групп остова аминокислот, радикалы в этом не участвуют. Связь между аминокислотами образуется за счет карбоксильной группы одной аминокислоты и аминогруппы другой аминокислоты. Связь, образованная таким образом, между двумя аминокислотами, называется пептидной.
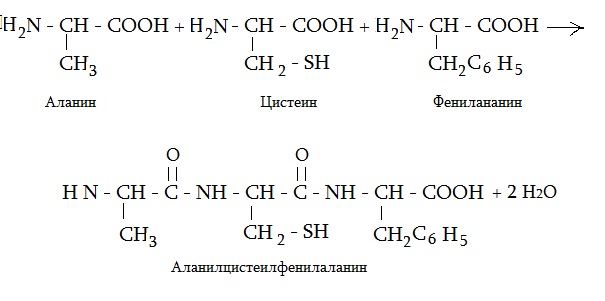
На рисунке представлена формула трипептида аланин цистеин фенилаланин и схема его образования.
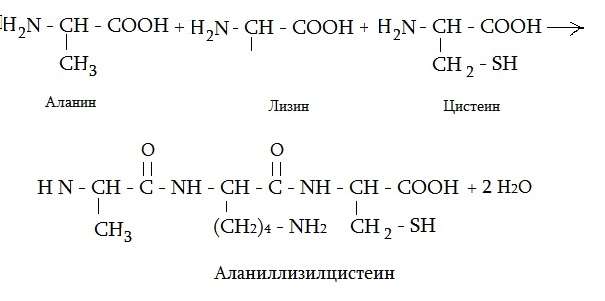
Самым мелким пептидом в организме является глутатион, в состав которого входят всего две аминокислоты, в том числе и цистеин. Две аминокислоты, соединенные между собой, называют дипептидом, три — трипептидом. Приведем еще формулу трипептида из аланина, лизина и цистеина.
Вещества, содержащие от 10 до 40 аминокислот, называют полипептидами. В состав собственно белков входит более 40 аминокислотных остатков. Цистеин входит в состав многих пептидов и белков, например, инсулина.
Источники цистеина
Ежедневно человек должен потреблять 4,1 мг цистеина на 1 кг веса. То есть в организм человека с массой 70 кг должно поступать 287 мг этой аминокислоты в день.
Часть цистеина может синтезироваться в организме, часть поступает с пищей. Ниже приведен список продуктов, содержащих максимальное количество аминокислоты.
| Содержание цистеина в продуктах | |
| Продукт | Содержание цистеина в 100 г продукта, мг |
| Соевые продукты | 638 |
| Говядина и баранина | 460 |
| Семена (подсолнечника, арбуза, кунжута, льна, тыквы) и орехи (фисташки, кедровые) | 451 |
| Куриное мясо | 423 |
| Овес и овсяные отруби | 408 |
| Свинина | 388 |
| Рыба (тунец, лосось, окунь, скумбрия, палтус) и моллюски (мидии, креветки) | 335 |
| Сыр, молочные продукты и яйца | 292 |
| Бобовые (нут, бобы, фасоль, чечевица) | 127 |
| Крупы (гречка, ячмень, рис) | 120 |
Кроме того, цистеин содержится в красном перце, чесноке, луке, в темных листовых овощах — брюссельской капусте, брокколи.
Производят пищевые добавки, например, L-цистеин гидрохлорид, N-ацетилцистеин. Второй обладает большей растворимостью и легче усваивается организмом.
В промышленности L-цистеин получают гидролизом из перьев птиц, щетины и человеческих волос. Производится более дорогой синтетический L-цистеин, подходящий под мусульманские и еврейские пищевые правила (в соответствии с религиозными аспектами).
Синтез цистеина в организме
Цистеин, наряду с тирозином, относится к условно заменимым аминокислотам. Это значит, что они могут синтезироваться в организме, но только из незаменимых аминокислот: цистеин из метионина, тирозин из фенилаланина.
Для синтеза цистеина необходимы две аминокислоты — незаменимая метионин и заменимая серин. Метионин является донором атома серы. Цистеин синтезируется из гомоцистеина в ходе двух реакций, катализируемых пиридоксальфосфатом. Генетические нарушения, а также недостаток витаминов В9 (фолиевой кислоты), В6 и В12 приводят к нарушению использования фермента, гомоцистеин превращается не в цистеин, а в гомоцистин. Это вещество накапливается в организме, вызывая заболевание, сопровождающееся катарактой, остеопорозом, умственной отсталостью.
Синтез в организме может быть недостаточен у пожилых людей и младенцев, лиц с некоторыми метаболическими заболеваниями, страдающих синдромом мальабсорбции.
Реакции синтеза цистеина
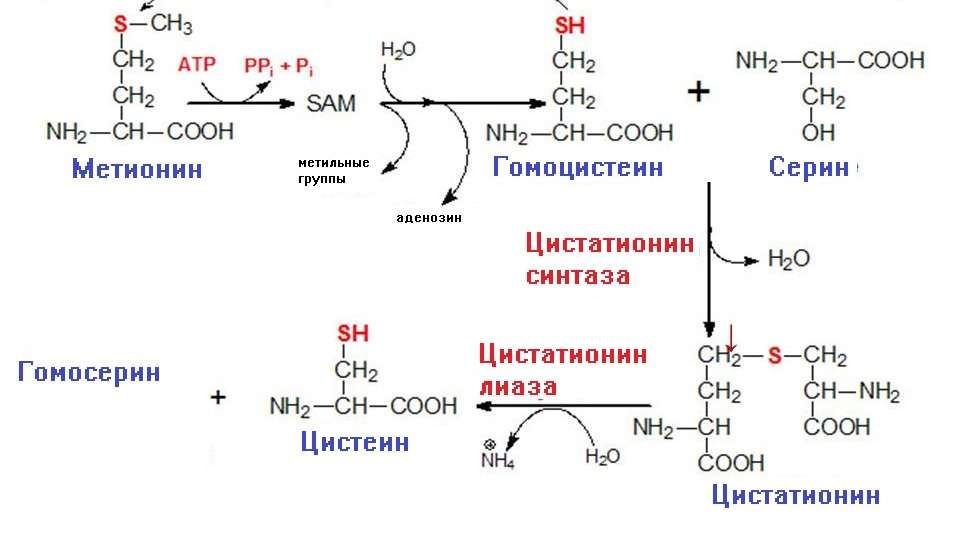
В организме животного цистеин синтезируется непосредственно из серина, а источником серы является метионин. Метионин превращается в гомоцистеин через промежуточные вещества S-AM и S-АГ. S-аденозилметионин — активная форма метионина, образуется соединением АТФ и метионина. Выступает донором метильной группы в реакциях синтеза различных соединений: цистеина, адреналина, ацетилхолина, лецитина, карнитина.
В результате трансметилирования S-AM превращается в S-аденозилгомоцистеин (S-АГ). Последний в ходе гидролиза образует аденозин и гомоцистеин. Гомоцистеин соединяется с серином с участием фермента цистатионин-β-синтазы с образованием тиоэфирного цистатионина. Цистатионин превращается в цистеин и α-кетобутират под действием фермента цистатионин-γ-лиазы.
У растений и бактерий синтез происходит иначе. Источником серы для синтеза цистеина могут выступать разные вещества, даже сероводород.
Биологическая роль цистеина
За счет тиоловой группы (-HS) в составе формулы цистеина, в белках формируются дисульфидные связи, называемые дисульфидными мостиками. Дисульфидные связи — ковалентные, сильные. Они образуются между двумя молекулами цистеина в составе белка. Могут образовываться внутрицепочечные мостики в пределах одной полипептидной цепочки, и межцепочечные — между отдельными цепями белка. Например, в структуре инсулина имеют место оба вида мостиков. Эти связи обеспечивают поддержание третичной и четвертичной структуры белка.
Дисульфидные связи содержат в основном внеклеточные белки. Например, этот вид связи имеет большое значение в стабилизации структуры инсулина, иммуноглобулинов и пищеварительных ферментов. Белки, содержащие множество дисульфидных мостиков, более устойчивы к тепловой денатурации, что позволяет им поддерживать свою активность в более экстремальных условиях.
Особенности формулы цистеина обеспечивают ему антиоксидантные свойства. Цистеин играет роль антиоксиданта, вступая в реакции окисления-восстановления. Тиоловая группа имеет высокое сродство к тяжелым металлам, поэтому белки, содержащие цистеин, связывают металлы, такие как ртуть, свинец и кадмий. В составе белка рК цистеина такой, что это обеспечивает нахождение аминокислоты в реактивной тиолятной форме, то есть цистеин легко отдает HS-анион.
Цистеин является важным источником серы в метаболизме.
Функции цистеина
За счет наличия тиоловой группы, легко вступающей в реакции, цистеин участвует в разнообразных процессах в организме и выполняет многие функции.
Применение цистеина
Цистеин нашел широкое применение в медицинской, фармацевтической, пищевой промышленности.
Цистеин часто используют при лечении различных заболеваний:

Кроме того, цистеин ускоряет выздоровление после операций и ожогов, активизирует лейкоциты.
Цистеин ускоряет сжигание жиров и построение мышечной ткани, поэтому его часто применяют спортсмены.
Аминокислота применяется как ароматизатор. Цистеин является зарегистрированной пищевой добавкой Е920.
Уравнение реакции образования цистеина из цистеина
Цистеин — условно заменимая алифатическая α-аминокислота.
Цистеин — серусодержащая аминокислота, так как для ее синтеза необходим атом серы, источником которого служит незаменимая аминокислота метионин.
Так же для синтеза цистеина в организме необходима еще одна аминокислота — серин (источник углеродного скелета), а также АТФ и витамин В6.
Цистеин — 2-амино-3-меркаптопропановая кислота или α-амино-β-тиопропионовая кислота.
Цистеин (Цис, Cys, С) имеет химическую формулу HO2CCH (NH2) CH2SH.
Цистеин впервые выделен в виде цистина К. Мернером в 1899 из рога.
Суточная потребность в цистеине составляет 2-3 грамма.
Физические свойства
Цистеин представляет собой бесцветные кристаллы, легко растворимые в воде. Температура плавления 178 0 С.
Пути метаболизма цистеина
Цистеин является чрезвычайно важной аминокислотой в связи с тем, что это единственный источник органической серы для клеток организма. В результате реакций метаболизма эта сера переходит в состав других серусодержащих веществ – фосфоаденозинфосфосерная кислота (ФАФС), коэнзим А, глутатион, сульфированные производные углеводов.
Биологическая роль
Цистеин может находиться в составе белка в двух формах: либо в форме цистеина, либо в форме дипептида — цистина, который представляет собой комплекс из двух молекул цистеина, ковалентно связанных друг с другом при помощи дисульфидного мостика.
Благодаря этому свойству цистеин выполняет важную функцию по стабилизации структуры белковой молекулы.
Цистеин играет ключевую роль в формировании инсулина и иммуноглобулинов (антител).
Цистеин входит в состав белков и пептидов, играет важную роль в процессах формирования тканей кожи.
Цистеин обладает антиоксидантными свойствами.
Участвует в процессе биологической детоксикации при отравлении токсическими веществами (разлагает и удаляет токсины из организма).
Цистеин участвует в биосинтезе цистина, глутатиона, таурина и кофермента А.
Цистеин является предшественником глутатиона — вещества, оказывающего защитное действие на клетки печени и головного мозга от повреждения алкоголем, некоторыми лекарственными препаратами и токсическими веществами, содержащимися в сигаретном дыме.
Цистеин входит в состав альфа-кератина, основного белка ногтей, кожи и волос. Он способствует формированию коллагена и улучшает эластичность и текстуру кожи.
Цистеин способствует пищеварению, участвуя в процессах переаминирования.
Белки, содержащие цистеин, такие как металлотионеин, способны связывать такие металлы, как ртуть, свинец и кадмий.
Цистеин участвует в синтезе таурина в животных тканях. Таурин необходим для синтеза парных желчных кислот в печени. Кроме того, он очень важен в клетках как антиоксидант.
Цистеин участвует в обмене веществ хрусталика глаза. Изменения, происходящие при катаракте, связаны с нарушением содержания в хрусталике этой аминокислоты.
Характерная особенность цистеина – его способность подвергаться в составе молекулы белка самопроизвольному окислению с образованием остатков цистина.
Хотя цистеин классифицируется как заменимая аминокислота, в редких случаях он может быть жизненно важен для младенцев, пожилых людей и лиц с заболеванием, которое возникает вследствие нарушения пищеварительно-транспортной функции тонкой кишки, что приводит к метаболическим расстройствам.
В нормальных физиологических условиях, при наличии достаточного количества доступного метионина, цистеин может быть синтезирован в организме человека. Цистеин катаболизируется в желудочно-кишечном тракте и плазме крови.
Природные источники
Цистеин содержится в большинстве продуктов с высоким содержанием белка.
Животные источники: мясо (свинина, курица, индейка, утка), яйца, молоко, сывороточный протеин, рикотта, творог, йогурт.
Растительные источники: красный перец, чеснок, лук, брокколи, брюссельская капуста, овес, мюсли, зародыши пшеницы, проросшая чечевица, горох, соя, рис.
Области применения
Цистеин является исходным сырьем в пищевой, фармацевтической и медицинской промышленности.
Очень часто цистеин используется для создания запахов. Например, в результате взаимодействия цистеина с сахаром можно ощутить ярко выраженный запах мяса.
Цистеин также используется в качестве технологической добавки в кулинарии для выпечки. В качестве пищевой добавки цистеин обозначается как Е920.
Цистеин используется как средство для перманентной завивки волос, так как он способен разрушать дисульфидные связи кератина волос.
Цистеин растворяется лучше, чем цистин, и быстрее утилизируется в организме, поэтому его чаще используют в комплексном лечении различных заболеваний.
Цистеин необходим при ревматоидном артрите, заболеваниях артерий, раке.
Он ускоряет выздоровление после операций, ожогов, связывает тяжелые металлы и растворимое железо.
Цистеин ускоряет сжигание жиров и образование мышечной ткани.
Цистеин обладает способностью разрушать слизь в дыхательных путях, благодаря этому его часто применяют при бронхитах и эмфиземе легких. Он ускоряет процессы выздоровления при заболеваниях органов дыхания и играет важную роль в активизации лейкоцитов и лимфоцитов.
Цистеин помогает обезвреживать некоторые токсические вещества и защищает организм от повреждающего действия радиации.
Он представляет собой один из самых мощных антиоксидантов, при этом его антиоксидантное действие усиливается при одновременном приеме витамина С и селена.
Цистеин был предложен в качестве профилактического средства негативным эффектам алкоголя, в том числе повреждений печени и похмелья.
Он противодействует ядовитому воздействию ацетальдегида, основного побочного продукта метаболизма алкоголя и отвечает за большинство отрицательных последствий и долгосрочных повреждений, связанных с употреблением алкоголя (но не отменяет непосредственного эффекта опьянения).
В результате метаболизма цистеина ацетальдегид превращается в относительно безвредную уксусную кислоту.
Цистеин применяется для задержки развития катаракты и просветления хрусталика, при начальных формах возрастной, миопатической, лучевой и контузионной катаракты.
Отмечено сильное противовирусное, противоопухолевое (цитотоксическое) и противовоспалительное действие цистеина.
Цистеин помогает уменьшить отрицательные последствия химио- и лучевой терапии.
При цистинурии, редком генетическом состоянии, приводящем к образованию цистиновых камней, принимать цистеин нельзя.
Сахарный диабет также является противопоказанием для назначения цистеина.
http://1ku.ru/obrazovanie/27978-cistein-formula-i-opisanie-veshhestva/
http://himija-online.ru/organicheskaya-ximiya/aminokisloty/cistein.html