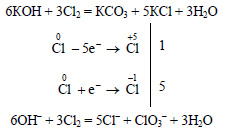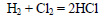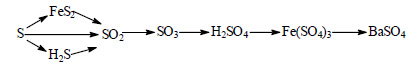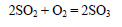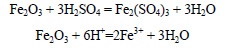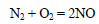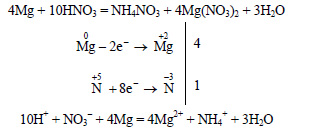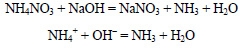Хлорид калия: способы получения и химические свойства
Хлорид калия KCl — соль щелочного металла калия и хлороводородной кислоты. Белое вещество, плавится и кипит без разложения. Умеренно растворяется в воде.
Относительная молекулярная масса Mr = 74,55; относительная плотность для тв. и ж. состояния d = 1, 984; tпл = 770º C; tкип = 1430º C;
Способ получения
1. Хлорид калия можно получить путем взаимодействия калия и разбавленной хлороводородной кислоты, образуются хлорид калия и газ водород:
2K + 2HCl = 2KCl + H2↑.
2. При комнатной температуре, в результате взаимодействия калия и хлора, образуется хлорид калия:
2K + Cl2 = 2KCl
3. Концентрированный раствор гидроксида калия реагирует с концентрированным раствором хлорида аммония при кипении. При этом образуются хлорид калия, газ аммиак и вода:
4. Разбавленная хлороводородная кислота реагирует с гидроксидом калия . Взаимодействие хлороводородной кислоты с гидроксидом калия приводит к образованию хлорида калия и воды:
KOH + HCl = KCl + H2O
5. В результате взаимодействия сульфата калия и хлорида бария образуется сульфат бария и хлорид калия:
6. Карбонат калия взаимодействует с разбавленной соляной кислотой , образуя хлорид калия, углекислый газ и воду:
Качественная реакция
Качественная реакция на хлорид калия — взаимодействие его с нитратом серебра, в результате реакции происходит образование белого творожного осадка:
1. При взаимодействии с нитратом серебра , хлорид калия образует нитрат калия и осадок хлорид серебра:
KCl + AgNO3 = KNO3 + AgCl↓
Химические свойства
1. Хлорид калия вступает в реакцию со многими сложными веществами :
1.1. Хлорид калия взаимодействует с кислотами :
Хлорид калия в твердом состоянии при кипении реагирует с концентрированной серной кислотой с образованием сульфата калия и газа хлороводорода:
1.2. Хлорид калия способен вступать в реакцию с многими солями :
1.2.1. Твердый хлорид калия реагирует с концентрированной и горячей серной кислотой и твердым перманганатом калия . Взаимодействие хлорида калия с перманганатом калия и серной кислотой приводит к образованию сульфата марганца, сульфата калия, газа хлора и воды:
1.2.2. Хлорид калия взаимодействует с гидросульфатом калия при температуре 450–700º C . При этом образуются сульфат калия и хлороводородная кислота:
1.2.3. При взаимодействии концентрированного раствора хлорида калия и насыщенного перхлората натрия выделяются перхлорат калия и хлорид натрия:
KCl + NaClO4 = KClO4↓ + NaCl
Уравнение реакции оксида хлора с гидроксидом калия
Напишите формулу высшего оксида хлора. Известно, что при взаимодействии с водой он образует хлорную кислоту HClO4. Будет ли этот оксид реагировать с раствором гидроксида калия? Напишите уравнение реакции.
Высший оксид хлора сначала будет реагировать с водой раствора, а образовавшаяся хлорная кислота будет реагировать с гидроксидом калия:
Cl2O7 + H2O ⟶ 2HClO4
HClO4 + KOH ⟶ KClO4 + H2O
Составьте уравнения реакций, при помощи которых молено осуществить следующие превращения:
Уравнения реакций, если это возможно, составьте в полном и сокращенном ионном виде
Ответ:
а) При реакции хлора с гидроксидом кальция образуется смесь хлорида кальция и гипохлорита кальция:
При реакции хлора с горячим раствором гидроксида калия образуется хлорат калия:
Хлорат калия является сильным окислителем, при его реакции с соляной кислотой выделяется хлор:
Хлор реагирует с водородом с образованием хлороводорода:
При реакции хлороводорода с гидроксидом кальция образуется хлорид кальция:
При реакции раствора хлорида кальция с раствором нитрата серебра в осадок выпадает хлорид серебра:
При реакции хлора с железом при нагревании образуется хлорид железа (III):
При реакции раствора хлорида железа (III) с раствором гексацианоферрата (II) калия (желтая кровяная соль) образуется осадок гексацианоферрата (II) железа (III), так называемая берлинская лазурь:
При реакции серы с железом при нагревании можно получить дисульфид железа FeS2:
Сера реагирует при нагревании с водородом с образованием сероводорода:
При окислении дисульфида железа образуется оксид серы (IV):
Оксид серы (IV) образуется также при сжигании серы или сероводорода:
При окислении оксида серы (IV) кислородом в присутствии катализатора и при повышенной температуре образуется оксид серы (VI) (триоксид серы, серный ангидрид):
Триоксид серы бурно реагирует с водой с образованием серной кислоты:
При реакции серной кислоты с оксидом железа (111) образуется сульфат железа (III):
При реакции сульфата железа (III) с хлоридом бария выпадает осадок сульфата бария:
Азот реагирует с кислородом в условиях электрического разряда с образованием оксида азота (II):
В присутствии катализатора азот реагирует с водородом с образованием аммиака:
При окислении аммиака кислородом в присутствии катализатора образуется оксид азота (II):
Оксид азота (II) окисляется кислородом в оксид азота (IV):
Оксид азота (IV) реагирует в присутствии кислорода с водой с образованием азотной кислоты:
При реакции 30%-ной азотной кислоты с медью выделяется оксид азота (II):
При реакции разбавленной (15%-ной) азотной кислоты с цинком выделяется оксид азота (I):
При реакции сильно разбавленной (5%-ной) азотной кислоты с магнием образуется нитрат аммония:
При действии щелочи на нитрат аммония выделяется аммиак:

задача №11
к главе «Глава VI. Неметаллы».
http://gomolog.ru/reshebniki/8-klass/eremin-2019/43/4.html
http://5terka.com/node/161