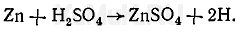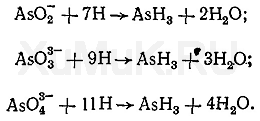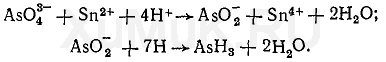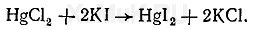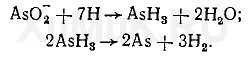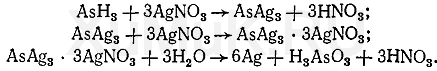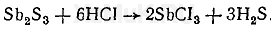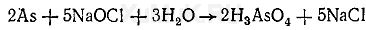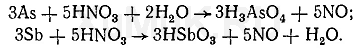Химические свойства мышьяка
Мышьяк является неметаллом, образует соединения, подобные по его химическим свойствам. Однако, наряду с неметаллическими свойствами, мышьяк проявляет и металлические. На воздухе при обычных условиях мышьяк слегка окисляется с поверхности. Ни в воде, ни в органических растворителях мышьяк и его аналоги нерастворимы.
Мышьяк химически активен. На воздухе при нормальной температуре даже компактный (плавленый) металлический мышьяк легко окисляется, при нагревании порошкообразный мышьяк воспламеняется и горит голубым пламенем с образованием оксида As2O3. Известен также термически менее устойчивый нелетучий оксид As2O5.
При нагревании (в отсутствие воздуха) As возгоняется (температура возгонки 615 о С). Пар состоит из молекул As4 с ничтожной (порядка 0,03%) примесью молекул As2.
Мышьяк относится к группе элементов окислителей-восстановителей. При действии сильных восстановителей он проявляет окислительные свойства. Так, при действии металлов и водорода в момент выделения он способен давать соответствующие металлические и водородистые соединения:
При действии сильных окислителей мышьяк переходит в трех- или пятивалентное состояние. Например, при накаливании на воздухе мышьяк, окисляясь кислородом, сгорает и образует белый дым – оксид мышьяка (III) As2O3:
Устойчивые формы оксида мышьяка в газовой фазе – сесквиоксид (мышьяковистый ангидрид) As2O3 и его димер As4O6. До 300 о С основная форма в газовой фазе – димер, выше этой температуры он заметно диссоциирован, а при температурах выше 1800 о С газообразный оксид состоит практически из мономерных молекул As2O3.
Газообразная смесь As4O6 и As2O3 образуется при горении As в кислороде, при окислительном обжиге сульфидных минералов As, например арсенопирита, руд цветных металлов и полимерных руд.
При конденсации пара As2O3 (As4O6) выше 310 о С образуется стекловидная форма As2O3. При конденсации пара ниже 310 о С образуется бесцветная поликристаллическая кубическая модификация арсенолит. Все формы As2O3 хорошо растворимы в кислотах и щелочах.
Оксид As(V) (мышьяковый ангидрид) As2O5 – бесцветные кристаллы ромбической сингонии. При нагревании As2O5 диссоциирует на As4O6 (газ) и О2. Получают As2O5 обезвоживанием концентрированных растворов H3AsO4 с последующим прокаливанием образующихся гидратов.
Известен оксид As2O4, получаемый спеканием As2O3 и As2O5 при 280 о С в присутствии паров воды. Известен также газообразный монооксид AsO, образующийся при электрическом разряде в парах триоксида As при пониженном давлении.
При растворении в воде As2O5 образует существующие только в растворе ортомышьяковистую H3AsO3, или As(OH)3, и метамышьяковистую HAsO2, или AsO(OH), кислоты, обладающие амфотерными, преимущественно кислыми, свойствами.
По отношению к кислотам мышьяк ведет себя следующим образом:
— с соляной кислотой мышьяк не реагирует, но в присутствии кислорода образуется трихлорид мышьяка AsCl3:
— разбавленная азотная кислота при нагревании окисляет мышьяк до ортомышьяковистой кислоты H3AsO3, а концентрированная азотная кислота – до ортомышьякой кислоты H3AsO4:
Ортомышьяковая кислота (мышьяковая кислота) H3AsO4*0.5H2O – бесцветные кристаллы; температура плавления – 36 о С (с разложением); растворима в воде (88% по массе при 20 о С); гигроскопична; в водных растворах – трехосновная кислота; при нагревании около 100 о С теряет воду, превращаясь в пиромышьяковую кислоту H4As5O7, при более высоких температурах переходит в метамышьяковую кислоту HAsO3. Получают окислением As или As2O3 концентрированной HNO3. Она легкорастворимая в воде и по силе приблизительно равна фосфорной.
Окислительные свойства мышьяковой кислоты заметно проявляются лишь в кислой среде. Мышьяковая кислота способна окислить HI до I2 по обратимым реакциям:
Ортомышьяковистая кислота (мышьяковистая кислота) H3AsO3 существует только в водном растворе; слабая кислота; получают растворением As2O3 в воде; промежуточный продукт при получении арсенитов (III) и других соединений.
— концентрированная серная кислота реагирует с мышьяком по следующему уравнению c образованием ортомышьяковистой кислоты:
— растворы щелочей в отсутствие кислорода с мышьяком не реагируют. При кипячении мышьяка со щелочами он окисляется в соли мышьяковистой кислоты H3AsO3. При сплавлении со щелочами образуется арсин (мышьяковистый водород) AsH3 и арсенаты (III). Применяют AsH3
для легирования полупроводниковых материалов мышьяком, для получения As высокой чистоты.
Известны неустойчивые высшие арсины: диарсин As2H4, разлагается уже при -100 о С; триарсин As3H5.
Металлический мышьяк легко взаимодействует с галогенами, давая летучие галогениды AsHal3:
AsCl3 – бесцветная маслянистая жидкость, дымящаяся на воздухе, при застывании образует кристаллы с перламутровым блеском.
C F2 образует также и AsF5 — пентафторид – бесцветный газ, растворимый в воде и растворах щелочей (с небольшим количеством тепла), в диэтиловом эфире, этаноле и бензоле.
Порошкообразный мышьяк самовоспламеняется в среде F2 и Cl2.
С S, Se и Te мышьяк образует соответствующие халькогениды:
сульфиды — As2S5, As2S3 ( в природе – минерал аурипигмент), As4S4 (минерал реальгар) и As4S3 (минерал диморфит); селениды – As2Se3 и As4Se4; теллурид – As2Te3. Халькогениды мышьяка устойчивы на воздухе, не растворимы в воде, хорошо растворимы в растворах щелочей, при нагревании – в HNO3. Обладают полупроводниковыми свойствами, прозрачны в ИК области спектра.
С большинством металлов дает металлические соединения – арсениды. Галлия арсенид и индия арсенид – важные полупроводниковые соединения.
Известны многочисленные мышьякорганические соединения. Мышьякорганические соединения содержат связь As-C. Иногда к мышьякорганическим соединениям относят все органические соединения, содержащие As, например эфиры мышьяковистой кислоты (RO)3As и мышьяковой кислоты (RO)3AsO. Наиболее многочисленная группа мышьякорганических соединений – производные As с координационным числом 3. К ней относятся органоарсины RnAsH3-n, тетраорганодиарсины R2As-AsR2, циклические и линейные полиарганоарсины (RAs)n, а также органоарсонистые и диарганоарсинистые кислоты и их производные RnAsX3-n (X= OH, SH, Hal, OR’, NR2’ и др.). Большинство мышьякорганических соединений – жидкости, полиорганоарсины и органические кислоты As – твердые вещества, CH3AsH2 и CF3AsH2 – газы. Эти соединения, как правило, растворимы в органических растворителях, ограничено растворимы в воде, в отсутствие кислорода и влаги сравнительно устойчивы. Некоторые тетраорганодиарсины на воздухе воспламеняются.
Мышьяк
Его природные соединения необычайно красивы. Это сульфиды – красный реальгар As4S4 и золотисто-жёлтый аурипигмент As2S3, которые упоминаются уже античными авторами. Алхимики считали, что мышьяк является составной частью всех металлов. Особое отношение к мышьяку в Средние века объясняется не только тем, что многие его соединения ядовиты, но также и способностью этого элемента «превращать медь в серебро». Когда в расплавленную медь добавляют мышьяк, она приобретает белый цвет, становясь похожей на серебро. Выделение мышьяка в виде простого вещества традиционно связывают с именем теолога и алхимика XIII в. Альберта Великого. Русское название элемента – это, по-видимому, искаженное «мышиный яд», «мышь-яд». Латинское Arsenicum происходит от греческого наименования сернистых соединений мышьяка. «Арсеникон» по-гречески означает «сильный», «мужественный» — такую дань благоговения воздали древние исключительно ядовитым соединениям мышьяка.

Как и фосфор, мышьяк существует в виде нескольких аллотропных модификаций, из которых наиболее устойчив серый мышьяк – твердое вещество серого цвета с металлическим блеском, построенное наподобие черного фосфора. Когда мышьяк сгорает на воздухе, образуется оксид As2O3, известный еще алхимиками под названием «белый мышьяк». Это ангидрид слабой мышьяковистой кислоты H3AsO3. Её медная соль (арсенит меди) очень долго использовалась как зеленая краска – зелень Шееле CuHAsO3. В старину белый мышьяк был весьма «популярным» ядом, смертельная доза его для человека составляет 20 – 300 мг. Например, галицкий князь Дмитрий Шемяка, по приказу которого в 1446 г. ослепили великого князя московского Василия II, был отравлен именно соединениями мышьяка. Это доказано химическими методами при изучении останков князя в 80-х годах XX столетия. Несмотря на ядовитость, белый мышьяк до сих пор применяют в стоматологии.
Некоторые соединения мышьяка находят широкое применение в электронике. Так, германий при введении в него небольшого количества мышьяка становится полупроводником n-типа. Среди полупроводниковых материалов большое распространение получил арсенид галлия GaAs. На его основе выполняют многие элементы микросхем, фотодиодов, транзисторов, солнечных батарей.

Химические свойства
В воде мышьяк нерастворим. На воздухе при комнатной температуре он окисляется очень медленно, при накаливании же сгорает, образуя белый оксид As2O3 и распространяя характерный чесночный запах. При высокой температуре мышьяк непосредственно соединяется со многими элементами. Сильные окислители переводят его в мышьяковую кислоту, напрмер:
В соединениях мышьяк проявляет степени окисления +5, +3 и -3.
Мышьяковистый водород AsH3, или арсин, представляет собой бесцветный, очень ядовитый газ с характерным чесночным запахом, малорастворимый в воде. Арсин образуется при восстановлении водородом в момент выделения всех соединений мышьяка. Например:
Арсин сравнительно нестоек и при нагревании легко разлагается на водород и свободный мышьяк. Это свойство арсина используется для открытия мышьяка в различных веществах. На анализируемое вещество действуют восстановителем и, если в нем содержится какое-либо соединение мышьяка или мышьяк в свободном состоянии, то образуется AsH3. Далее продукты восстановления нагревают, арсин разлагается, а выделяющийся мышьяк образует на холодных частях прибора характерный черный блестящий налет, называемый «мышьяковым зеркалом».

Оксид мышьяка (III) As2O3 образуется при сгорании мышьяка на воздухе или при прокаливании мышьяковых руд. Он довольно плохо растворим в воде. При растворении происходит присоединение воды к оксиду мышьяка (III) и образуется мышьяковистая кислота:
В свободном состоянии эта кислота не получена и известна только в водных растворах. При действии на As2O3 щелочей получаются соли мышьяковистой кислоты – арсениты. Например:
Соединения мышьяка (III) проявляют восстановительные свойства; при их окислении получают соединения мышьяка (V).
Мышьяковая кислота H3AsO4 при обычных условиях находится в твердом состоянии; она хорошо растворима в воде. По силе мышьяковая кислота почти равна фосфорной. Соли ее – арсенаты – очень похожи на соответствующие фосфаты. Известны также мета- и пиромышьяковая кислоты. При прокаливании мышьяковой кислоты получается оксид мышьяка (V), или мышьяковый ангидрид, As2O5 в виде белой стеклообразной массы.
Кислотные свойства мышьяковой кислоты выражены значительно сильнее, чем у мышьяковистой. Будучи трёхосновной она образует средние (арсенаты) и кислые (гидро- и дигидроарсенаты), например, Na3AsO4, Na2HAsO4, NaH2AsO4. В кислой среде мышьяковая кислота и арсенаты проявляют свойства окислителей.
Скачать:
Скачать бесплатно реферат на тему: «Мышьяк» Мышьяк.docx (238 Загрузок)
Скачать рефераты по другим темам можно здесь
*на изображении записи минерал красный реальгар
§ 19. СОЕДИНЕНИЯ МЫШЬЯКА
Применение и токсичность соединений мышьяка. Соединения мышьяка относятся к числу веществ, проявляющих сильное токсическое действие на организм людей и животных. Отмечены случаи отравлений ангидридом мышьяковистой кислоты, арсе-нитами, арсенатами, хлоридом мышьяка (III), мышьяковистым водородом, органическими препаратами мышьяка и др.
Ангидрид мышьяковистой кислоты применяется в медицине, в сельском хозяйстве (как инсектицид), в стекольной и кожевенной промышленностях. Арсениты и арсенаты некоторых металлов применяются в качестве ядохимикатов. Сюда относится парижская (швейнфуртская) зелень (см. гл. VI, § 18). Определенное токсикологическое значение имеют органические соединения мышьяка, применяемые в медицине (новарсенол, осарсол и др.). Известны случаи отравлений мышьяковистым водородом. Очень токсичными являются боевые отравляющие вещества (люизит, адамсит и др.), содержащие мышьяк. Соединения пятивалентного мышьяка в организме превращаются в более токсичные соединения трехвалентного мышьяка. Определенное количество мышьяка содержится в тканях организма как составная их часть (см. табл. 7).
Водорастворимые соединения мышьяка хорошо всасываются из пищевого канала. Пыль, содержащая ангидрид мышьяковистой кислоты, мышьяксодержащие ядохимикаты, попадая в организм через дыхательные пути, действует на ферменты, содержащие сульфгидрильные группы. Это приводит к торможению обменных процессов в организме. В ряде случаев под влиянием соединений мышьяка наступает паралич капилляров. Некоторые соединения мышьяка оказывают некротизирующее действие. Это свойство ангидрида мышьяковистой кислоты используется в зубоврачебной практике. Поступивший в организм мышьяковистый водород проникает преимущественно в эритроциты, в результате чего наступает их гемолиз. Это приводит к закупорке почечных канальцев, возникновению желтухи и т. д. Мышьяк способен кумулироваться в организме.
При остром отравлении соединениями мышьяка они накапливаются в основном в паренхиматозных органах, а при хронических отравлениях — в костях и ороговевших тканях (покровы кожи, ногти, волосы и др.).
Мышьяк выводится из организма через почки с мочой, кишки и через некоторые железы. Выделение мышьяка из организма происходит медленно, чем и обусловлена возможность его кумуляции. В экскрементах мышьяк еще можно обнаружить через несколько недель, а в трупном материале — и через несколько лет после смерти.
Исследование минерализатоз на наличие соединений мышьяка
Применяемые в химико-токсикологическом анализе методы обнаружения мышьяка основаны на переведении его в мышьяковистый водород и на последующем определении мышьяковистого водорода при помощи реакции Зангер — Блека, реакции с раствором диэтилдитиокарбамата серебра в пиридине и реакции Марша. При всех этих реакциях из соединений мышьяка выделяется летучий и очень ядовитый мышьяковистый водород. Поэтому при выполнении всех перечисленных выше реакций на мышьяк требуется предосторожность.
Две первые реакции являются предварительными. При их отрицательном результате дальнейшее исследование минерализата на наличие мышьяка не производится. При положительном результате указанных реакций на мышьяк дополнительно выполняют реакцию Марша.
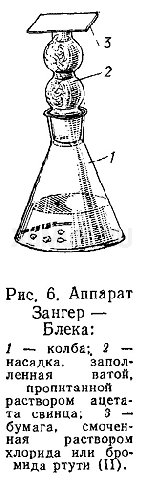
Реакция Зангер — Блека основана на восстановлении соединений мышьяка до мышьяковистого водорода, который затем на фильтровальной бумаге реагирует с хлоридом или бромидом ртути (II). Реакция выполняется в специальном приборе (рис. 6).
Восстановление соединений мышьяка производится водородом в момент его выделения, который получают при взаимодействии металлического цинка с серной кислотой:
Металлический цинк и серная кислота, применяемые для получения водорода, не должны содержать мышьяка. Реакция между металлическим цинком и серной кислотой протекает медленно.
Для ее ускорения применяют так называемый «купрированный» цинк (цинк, поверхность которого покрыта сульфатом меди).
Водород, образовавшийся при взаимодействии серной кислоты и цинка, восстанавливает соединения мышьяка до AsH 3 :
Скорость восстановления соединений трех-и пятивалентного мышьяка (арсенитов и арсена-тов) водородом неодинаковая. Арсениты восстанавливаются водородом легче, чем арсенаты. Поэтому вначале производят восстановление арсенатов в арсениты водородом в присутствии солей железа (II) или олова (II), затем арсениты восстанавливаются водородом с образованием мышьяковистого водорода:
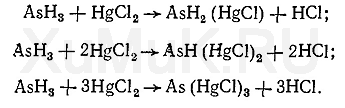
Образовавшийся мышьяковистый водород реагирует с хлоридом или бромидом ртути (II), которыми пропитана фильтровальная бумага. При реакции образуется ряд окрашенных соединений, которые располагаются на бумаге в виде желтых или коричневых пятен.
После обработки бумаги слабым раствором иодида калия вся бумага (кроме пятна, содержащего указанные соединения мышьяка) приобретает красноватую окраску, обусловленную переходом хлорида или бромида ртути в иодид этого металла:
При дальнейшей обработке бумаги концентрированным раствором иодида калия бумага обесцвечивается (образуется K 2 [HgI 4 ]), а пятно, содержащее соединения мышьяка AsH 2 (HgCl), AsH(HgCl) 2, As(HgCl) 3, остается желтым или коричневым.
Реакции Зангер — Блека мешает сероводород, который может образоваться при взаимодействии водорода с серной кислотой: H 2 SO 4 + 8Н —> H 2 S + 4Н 2 О.
Реакции Зангер — Блека также мешают соединения, ионы которых восстанавливаются водородом.
Сереводород, выделившийся при взаимодействии водорода с серной кислотой, на фильтровальной бумаге реагирует с хлоридом или бромидом ртути (II). В результате этой реакции образуется черного цвета сульфид ртути, который маскирует окраску пятен, содержащих соединения мышьяка. Для связывания сероводорода применяют вату, пропитанную раствором ацетата свинца:
Выполнение реакции. В колбу аппарата Зангер — Блека вносят 2 мл минерализата, 10 мл 4 н. раствора серной кислоты, 5 мл воды и 1 мл 10 %-го раствора хлорида олова (II) в 50 %-й серной или соляной кислоте. Затем в колбу аппарата вносят 2 г мелких гранул «купрированного» цинка. Колбу аппарата закрывают насадкой, в которую вложена бумага, пропитанная хлоридом или бромидом ртути (II), а ниже вставлен тампон ваты, пропитанный ацетатом свинца. Аппарат оставляют на время, необходимое для образования на бумаге буровато-коричневого пятна. При наличии больших количеств мышьяка в пробе это пятно может появиться через несколько минут. При малых количествах мышьяка в минерализате пятно появляется через 30—45 мин. Если и через 45 мин не появится пятно, то бумагу опускают в 3 %-й водный раствор иодида калия. При этом бумага приобретает красноватую окраску. Затем бумагу опускают в насыщенный раствор иодида калия. При наличии мышьяка в минерализате на бумаге остается желтое или коричневое пятно, а вокруг него исчезает красноватая окраска. Предел обнаружения: 0,1 мкг мышьяка в пробе. Граница обнаружения: 0,01 мг мышьяка в 100 г биологического материала.
Приготовление «купрированного» цинка (см. Приложение 1, реактив 61).
Приготовление бумаги, пропитанной раствором хлорида или бромида ртути (III) (см. Приложение 1, реактив 7).
Приготовление ваты, пропитанной раствором ацетата свинца (см. Приложение 1, реактив 8).
Реакция с раствором диэтилдитиокарбамата серебра в пиридине. При выполнений этой реакции находящиеся в минерализате соединения мышьяка восстанавливают до мышьяковистого водорода, который собирают в пробирку (приемник), содержащую свежеприготовленный раствор диэтилдитиокарбамата серебра в пиридине. Раствор диэтилдитиокарбамата серебра в пиридине не должен содержать влаги. При наличии мышьяка в минерализате раствор диэтилдитиокарбамата серебра приобретает устойчивую красно-фиолетовую окраску. Химизм этой реакции не выяснен.
Обнаружению мышьяка при помощи этой реакции мешают соединения сурьмы, которые тоже реагируют с указанным реактивом и дают оранжево-красную окраску. Сурьма дает эту реакцию тогда, когда содержание ее в 100 г биологического материала составляет 0,5 мг и выше.
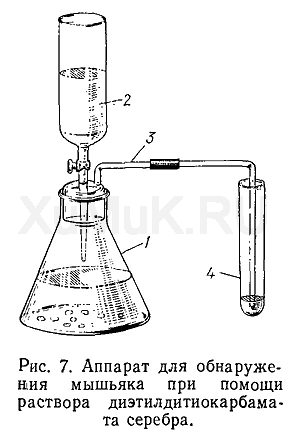
Восстановление соединений мышьяка при этой реакции происходит под влиянием водорода, условия получения которого подробно приведены при описании реакции Зангер — Блека. Реакцию соединений мышьяка с диэтилдитиокарбаматом серебра выполняют в специальном аппарате (см. рис. 7).
Выполнение реакции. В колбу 1 аппарата вместимостью 50 мл вносят 2 г мелких гранул «купрированного» цинка, не содержащего мышьяка. Колбу закрывают притертой пробкой, в которую впаяна цилиндрическая воронка 2 с краном и отводная трубка 3. В цилиндрическую воронку вносят 10 мл минерализата, 5 мл воды, 1 мл 10 %-го раствора хлорида олова (II) в 50 %-м растворе серной или соляной кислоты. Конец отводной трубки опускают в приемник 4, в который наливают 1 мл 0,5%-го раствора диэтилдитикарбамата серебра в пиридине.
После указанной выше подготовки прибора в цилиндрической воронке открывают кран и постепенно (в течение 10—15 мин) вливают ее содержимое в колбу аппарата, содержащую «купрированный» цинк. Как только закончится вытекание жидкости из воронки, ее ополаскивают 5 мл 4 н. раствором серной кислоты, которую тоже вливают в колбу с «купрированным» цинком, и наблюдают изменение окраски раствора диэтилдитиокарбамата серебра в пиридине. При наличии мышьяка в исследуемом минерализате содержимое пробирки (приемника) приобретает розовую или красно-фиолетовую окраску. В зависимости от количества мышьяка в пробирке окраска жидкости появляется через 4—45 мин.
Предел обнаружения: 0,5 мкг мышьяка в 1 мл минерализата. Граница обнаружения: 0,01 мг мышьяка в 100 г биологического материала.
Приготовление раствора диэтилдитиокарбамата серебра в пи ридине (см. Приложение 1, реактив 15).
Реакция Марша основана на восстановлении соединений мышьяка водородом в момент его выделения и на последующем термическом разложении образовавшегося при этом мышьяковистого водорода:
Мышьяк, образовавшийся при термическом разложении мышьяковистого водорода, откладывается на стенках восстановительной трубки аппарата Марша в виде налета («мышьякового зеркала»).
Реакция Марша является наиболее доказательной из всех реакций, рекомендованных для обнаружения мышьяка в различных объектах. Она не только позволяет обнаружить малые количества мышьяка, но и отличить его от сурьмы.
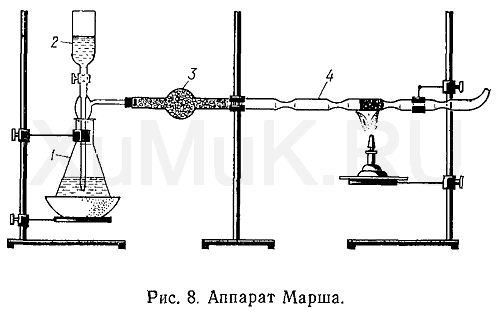
Реакцию Марша выполняют в специальном аппарате (рис. 8), который состоит из колбы 1, капельной воронки 2, хлор кальциевой трубки 3 и восстановительной трубки 4. Отверстие колбы аппарата Марша имеет пришлифованную поверхность и закрывается пришлифованной пробкой, в которую впаяны капельная воронка и отводная трубка. Восстановительная трубка аппарата Марша изготовляется из тугоплавкого стекла (диаметр 4 мм) или кварца. В нескольких местах этой трубки имеются сужения (диаметр 1,5 мм), а конец ее согнут почти под прямым углом и вытянут в острие. Между отводной и восстановительной трубками помещается хлоркальциевая трубка, заполненная безводным хлоридом кальция, предназначенным для осушивания газов, выходящих из колбы аппарата. Колбу, хлоркальциевую и восстановительную трубки соединяют друг с другом (стык в стык) при помощи кусочков резинового шланга. Собранный таким образом аппарат Марша должен быть герметичным.
Определение мышьяка с помощью реакции Марша выполняют в три этапа. Вначале проверяют реактивы на отсутствие в них мышьяка, затем определяют мышьяк в исследуемом растворе и, наконец, проверяют подлинность налета, образовавшегося в восстановительной трубке.
1. Проверка чистоты реактивов. Прежде чем приступить к обнаружению мышьяка в исследуемом растворе, необходимо убедиться в том, что применяемые для этой цели реактивы («купрированный» цинк и серная кислота) не содержат мышьяка.
С этой целью в колбу аппарата Марша вносят 10 г мелких гранул «купрированного» цинка, колбу закрывают пробкой с вмонтированными капельной воронкой и отводной трубкой. В капельную воронку вносят 30 мл 10 %-го раствора серной кислоты, которую небольшими порциями (по 4—5 мл) приливают к «купрированному» цинку, находящемуся в колбе аппарата Марша. Всегда необходимо оставлять в капельной воронке 8—10 мл раствора серной кислоты, которая препятствует проникновению воздуха извне в аппарат Марша. Попадание воздуха в аппарат Марша через капельную воронку может быть причиной взрыва этого аппарата при нагревании восстановительной трубки или при зажигании выходящих из нее газов.
Через 20—25 мин после начала выделения водорода проверяют полноту вытеснения воздуха водородом из аппарата Марша. Для этого над выходным отверстием восстановительной трубки аппарата держат опрокинутую узкую пробирку. Через 4—5 мин эту пробирку закрывают пальцем и, не переворачивая ее, относят подальше от аппарата Марша. К отверстию пробирки подносят зажженную спичку для воспламенения водорода. Если водород полностью вытеснил воздух из пробирки, то при зажигании водорода не будет ощущаться даже незначительного взрыва (треска). Если воздух из аппарата вытеснен не полностью, через аппарат продолжают пропускать водород до вытеснения им воздуха. Полноту вытеснения воздуха водородом проверяют через каждые 4—5 мин.
После полного удаления воздуха из прибора приступают к проверке наличия мышьяка в реактивах (серной кислоте и «купрированном» цинке).
2. Определение наличия мышьяка в реактивах. Для этой цели можно применить несколько способов.
Зажигают водород, выходящий из отверстия восстановительной трубки аппарата Марша. При наличии мышьяка в реактивах пламя приобретает синеватую окраску. Эту пробу можно производить только тогда, когда из аппарата Марша полностью вытеснен воздух водородом. При наличии хотя бы следов воздуха в аппарате во время зажигания газов, выходящих из трубки, может произойти взрыв .
Восстановительную трубку аппарата Марша перед одним из сужений обвертывают куском металлической сетки (для равномерного нагревания), а находящееся за сеткой сужение трубки обвертывают мокрым фитилем из марли. Один конец фитиля погружают в чашку с водой, а второй — в стакан для стекания жидкости. После этого расширенную часть трубки, обвернутую металлической сеткой, нагревают до слабого красного каления. Если в реактивах содержится мышьяк, то через некоторое время в охлажденной суженной части восстановительной трубки появляется темный налет с металлическим блеском (свободный мышьяк). Обычно проверку наличия металлического налета в трубке производят через час после начала нагревания восстановительной трубки.
Если перечисленные выше опыты будут положительными, то делают вывод, что серная кислота или «купрированный» цинк, применявшиеся для получения водорода, непригодны для дальнейших исследований на наличие мышьяка. Только при отрицательных результатах опытов на наличие мышьяка серную кислоту и «купрированный» цинк можно применять для определения соединений этого элемента в минерализатах и в других объектах.
3. Исследование минерализата. В колбу аппарата Марша вносят 10 г «купрированного» цинка, не содержащего мышьяка, а в капельную воронку наливают 30 мл 4 н. раствора серной кислоты, которая тоже не содержит мышьяка. Из капельной воронки небольшими порциями (по 4—5 мл) несколько раз приливают 4 н. раствор серной кислоты к цинку. Сразу прибавлять большие объемы раствора серной кислоты к цинку не следует, так как это вызовет бурную реакцию, в результате которой часть серной кислоты может восстановиться до сероводорода, который при нагревании восстановительной трубки будет образовывать налет серы. Также следует помнить, что в капельной воронке всегда должен оставаться небольшой объем раствора серной кислоты для предупреждения попадания воздуха в прибор через эту воронку.
Спустя 15—20 мин после начала взаимодействия цинка с серной кислотой проверяют полноту вытеснения воздуха из аппарата Марша водородом, как указано выше. После полного вытеснения воздуха из аппарата Марша в капельную воронку, в которой еще остался небольшой объем раствора серной кислоты, вносят 20 мл минерализата и 2 мл 10%-го раствора хлорида олова (II) в 50 %-м растворе серной кислоты. Содержимое капельной воронки в течение 30—40 мин небольшими порциями вливают в колбу аппарата Марша и равномерно нагревают расширенную часть восстановительной трубки (перед сужением). Одновременно с этим при помощи фитиля из марли охлаждают суженную часть восстановительной трубки, расположенную за местом нагревания. Через 20—30 мин после начала нагревания восстановительной трубки проверяют наличие мышьяка в исследуемой пробе минерализата. С этой целью проводят ряд наблюдений и опытов.
1. Проверяют наличие налета в восстановительной трубке аппарата Марша. Наличие налета, его внешний вид и место расположения в восстановительной трубке может указывать на наличие мышьяка в пробе.
2. Зажигают водород, выходящий из трубки аппарата Марша. При наличии мышьяка в микерализате пламя приобретает сине-
ватую окраску. Зажигание водорода производят только после вытеснения им воздуха из аппарата. Если из аппарата не пол ностью вытеснен воздух, то может быть взрыв.
3. В указанное пламя вносят холодные фарфоровые крышки или фарфоровые пластинки. Если в минерализате содержатся соединения мышьяка, то на холодных фарфоровых крышках или пластинках отложится буро-сероватый налет.
4. Восстановительную трубку аппарат Марша осторожно поворачивают на 180°, а затем конец ее погружают в 5 %-й раствор нитрата серебра, слабо подщелоченный аммиаком. Если в выходящем из аппарата токе газов содержится мышьяковистый водород, то указанный раствор потемнеет в результате образования металлического серебра:
Выделившаяся при этих реакциях азотная кислота связывается аммиаком.
В течение первых 20—30 мин с начала реакции в аппарате Марша результаты перечисленных опытов и наблюдений могут быть положительными только при наличии относительно больших количеств мышьяка в минерализате. При малых количествах мышьяка в минерализате за указанное время налет его в восстановительной трубке не образуется. В связи с этим исследование минерализата на наличие мышьяка в аппарате Марша продолжают в течение часа. Если в восстановительной трубке аппарата Марша образуется налет, то его подвергают дальнейшему исследованию на наличие мышьяка.
Исследование налета. Образование налета в восстановительной трубке является одним из важных доказательств наличия мышьяка в минерализате. Однако в восстановительной трубке могут давать налеты и другие вещества (сурьма, селен, сера, уголь).
Налеты мышьяка можно отличить от налетов других веществ по окраске и по расположению их в восстановительной трубке. Налет мышьяка имеет буровато-серую окраску с металлическим блеском, налет сурьмы — матово-черный, налет селена — серый, а налет серы — желтоватый или слегка бурый.
При несоблюдении условий разрушения биологического материала в минерализатах могут быть органические вещества, которые откладываются в восстановительной трубке в виде черного налета (уголь). Налет мышьяка откладывается в суженной части восстановительной трубки сразу же за местом ее нагревания, а налет сурьмы образуется по обе стороны от места нагревания восстановительной трубки. Это объясняется тем, что сурьмянистый водород (SbH 3 ) при нагревании разлагается легче, чем мышьяковистый водород. Кроме этого, сурьма менее летуча, чем мышьяк.
Для дальнейшего исследования налетов, образовавшихся в восстановительной трубке, ее отсоединяют от аппарата Марша и выполняют ряд опытов. Восстановительную трубку в области расположения налета нагревают. При этом происходит окисление отложившихся в трубке веществ. Налеты угля и серы исчезают из трубки, так как при их окислении образуются газообразные продукты (оксид серы (IV) или оксид углерода (IV). Налеты мышьяка и сурьмы окисляются и откладываются в виде оксидов в холодных местах восстановительной трубки. Оксид мышьяка имеет форму октаэдров, а оксид сурьмы аморфный. Образование кристаллов, имеющих форму октаэдров, является одним из важнейших доказательств наличия мышьяка в минерализате.
При пропускании сероводорода через восстановительную трубку, содержащую оксиды мышьяка или сурьмы, образуются сульфиды, отличающиеся друг от друга окраской. Сульфид мышьяка имеет желтую окраску, а сульфид сурьмы — красную или черную. При действии концентрированной соляной кислоты окраска сульфида мышьяка не изменяется, а сульфид сурьмы обесцвечивается:
Налеты мышьяка, которые образуются в восстановительной трубке, растворяются в свежеприготовленном растворе гипохлорита натрия:
Отложившиеся в восстановительной трубке налеты мышьяка и сурьмы могут быть использованы для обнаружения этих веществ при помощи микрокристаллоскопических реакций. При обработке этих налетов несколькими каплями концентрированной азотной кислоты они растворяются с образованием мышьяковой и метасурьмяной кислот:
Полученные растворы указанных кислот наносят на предметные стекла, а затем осторожно выпаривают досуха. На сухие остатки наносят по капле 5 н. раствора соляной кислоты и по кристаллику хлорида цезия. В присутствии сурьмы образуются бесцветные кристаллы в виде многогранников. Соединения мышьяка с этим реактивом не дают кристаллов. Если к указанному раствору прибавить кристаллик хлорида цезия и кристаллик иодида калия, то мышьяк дает красно-оранжевый осадок.
http://al-himik.ru/myshjak/
http://xumuk.ru/toxicchem/141.html