Кислоты и щёлочи

И получается такое вещество, которое не относится ни к кислотам, ни к щелочам. Оно не способно вызывать ожоги. Но это будет только при правильной пропорции кислоты и щёлочи (иногда для верности пользуются фенолфталеином, он окрашивает щёлочь в слегка фиолетовый цвет).
Кислота и щёлочи — это как две противоположности. Но они очень важны при изготовлении таких вещей как: удобрения, пластик, мыла, моющие средства, красок, бумаги и даже взрывчаток. Это далеко не весь список.
Что такое кислота
Кислота — это и есть что-то кислое, оно характеризуется кислым вкусом. Кислота содержится в уксусе – уксусная кислота, в лимоне – лимонная кислота, в молоке – молочная кислота, в желудке – соляная кислота и т.п. Но это всё так называемые слабые кислоты, помимо них существуют кислоты с большей концентрацией (серная, синильная кислоты и т.д. хотя этот учёный пробовал). Они гораздо опаснее для человека и пробовать их не рекомендуется никому. Они способны разъесть одежду, кожу, вызвать тяжёлый ожог на коже, разъесть бетон и другие вещества. Например, соляная кислота нам нужна для того, чтобы желудок быстрее переваривал пищу, а также для уничтожения большинства вредных бактерий, которые приходят вместе с пищей.
Что такое щелочь?
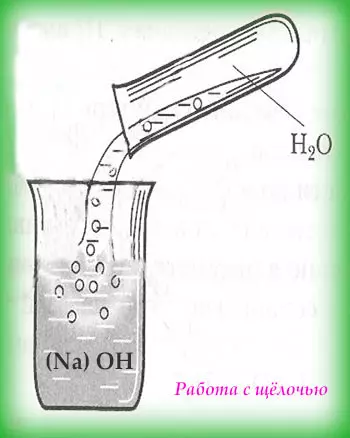
Щелочь — это те вещества, которые хорошо растворяются в воде. При этом реакция сопровождается с выделением тепла, с увеличением температуры. Если щёлочь сравнивать с кислотой, то на ощупь она намного «мыльнее», то есть скользкая. Вообще, щёлочи не сильно отстают от кислот по разъеданию и по силе. Они также могут с лёгкостью разъесть древесину, пластик, одежду и тому подобное.
Кстати, из щёлочей делают мыло, стекло, бумагу, ткань и это не весь список. Щёлочь можно найти у себя на кухне, ну или в магазине под названием пищевая сода. Кстати, пищевая сода это очень хороший помощник всем домохозяйкам.
Кислоты и щёлочи – отличия
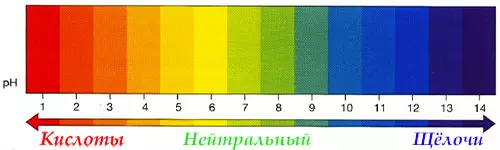
Кислоты и щёлочи отличают по показателям pH (шкала pH). Ниже Вы видите картинку – это специальная шкала, на которой имеются числа от 0 и до 14. Нулём обозначают самые сильные кислоты, а четырнадцатью – самую сильную щёлочь. Но какая же середина между этими числами? Может быть 5, может быть 7, а может быть 10? Серединой принято считать число 7 (нейтральное положение). То есть числа до 7 — это все кислоты, а больше 7 — это щёлочи.
pH продуктов
Сильные кислоты и слабые кислоты
Есть некоторые кислоты, которые мы можем употреблять, в то время как работа с другими предполагает строгие меры безопасности.
Сильные кислоты — это те, которые полностью диссоциируют или ионизируются в водных растворах.
Один из способов визуализировать, как отличить слабые и сильные кислоты, по аналогии с игроками в регби:
- сильная кислота является игроком, который бросает мяч, как только он его получает;
- слабая кислота, как игрок , который получает мяч и бежит с ним.
Примеры сильных кислот
Среди известных сильных кислот выделяют:
- HCl соляная кислота,
- серная кислота H 2 SO 4 ,
- азотная кислота HNO 3
- хлорная кислота HClO 4
- фторантимоновая кислота H [SbF 6 ]
Примеры слабых кислот
Обычно кислоты органических соединений известны как слабые:
- уксусная кислота H 3 CCOOH,
- масляная или бутановая кислота H 7 C 3 COOH (органическая кислота в масле),
- лимонная кислота или 2-гидрокси кислота 1,2,3-трикарбоксилпропан C 6 H 8 O 7,
- молочная кислота или 2-гидроксипропановая кислота H 6 C 3 O 3 .
Показатель кислотности растворов рН, механизм действия
Именно для этой шкалы разработаны специальные индикаторы — лакмусы. Это обычная полоска, которая реагирует на среду. В кислотной среде она окрашивается в красный цвет, а в щелочной среде – в синий цвет. Она необходима не только в химии, но и в быту.
Например, если у Вас есть аквариум, то немаловажную роль играет кислотность воды. От неё зависит вся жизнь аквариума. К примеру, показатель кислотности воды для аквариумных рыбок колеблется от 5 до 9 рН. Если будет больше или меньше, то рыбка будет чувствовать себя не комфортно, а может и вовсе умереть. Всё тоже самое и с растениями для аквариумов.
Работа с кислотами и щёлочами
Работа с кислотами и щёлочами требует большой внимательности и осторожности. Ведь при попадании на кожу они вызывают сильные ожоги. Старайтесь работать в проветриваемом помещении. Вдыхать пары щёлочей и кислот также не рекомендуется. Для личной безопасности стоит воспользоваться очками, перчатками и специальной одеждой, чтобы не повредить глаза, руки и любимую одёжку.
При работе с кислотами следует помнить, что сначала вливают кислоту в раствор (воду), а не наоборот. В противном случае произойдёт бурная реакция, которая сопровождается брызгами. А сам процесс добавления кислоты в раствор следует делать очень медленно, при этом контролировать степень нагрева сосуда и обязательно добавлять кислоту по стенкам сосуда.
При работе со щёлочами первым следует добавлять понемногу щёлочь. К тому же запрещено пользоваться стеклянной посудой, рекомендуют фарфоровую или специальную посуду.
При химической обработке металлов (оксидирование, анодирование, травление и др.) погружать в раствор и вынимать из раствора изделие следует с помощью специальных приспособлений или инструментов, но никак не руками, даже если они в резиновых перчатках. Кстати, щёлочь входит в состав некоторых батареек.
Запомните, что при химических ожогах кожи поражённое место нужно промыть сильной струёй проточной воды. И окончательно нейтрализовать: от кислот — 3%-ным раствором питьевой соды, а щёлочь — 1%-ным раствором уксусной кислоты.
Реакция гидроксида натрия с соляной кислотой
Повесть о Ромео и Джульетте со счастливым финалом
Ни на одной карте мира вы не найдете страны под названием Химия. Но она существует, и жизнь в ней протекает не менее насыщенно (а иногда и более интересно), чем в любой другой стране. К примеру, самая известная история любви всех веков и народов там заканчивается очень счастливо. Но давайте по порядку, ведь нам предстоит очень многое: познакомиться с химическими Монтекки и Капулетти, выбрать лучшего свидетеля реакции гидроксида натрия и соляной кислоты, слетать в космос, посетить самый лучший ресторан мира, заглянуть на концерт ансамбля песни и пляски Черноморского флота и многое другое.
Для начала заглянем в химическую лабораторию.
Если здесь чтут технику безопасности, то щелочи и их растворы хранятся строго отдельно от кислот и их растворов. Это химические Монтекки и Капулетти: оба семейства агрессивны и находятся в непримиримой вражде. Если они столкнутся без присмотра Химика, жди беды! Да и ученого они не жалуют: так и норовят обжечь или отравить. Поэтому при общении с ними Химик защищается как может: работает в вытяжном шкафу, надевает халат, фартук, перчатки, спецобувь и даже очки или защитный щиток.
И надо же такому случиться, чтобы прекрасный юноша Гидроксид натрия из рода Щелочей влюбился в обворожительную девушку по имени Соляная Кислота из семейства Кислот! Чтобы понять полноту трагедии, давайте поближе познакомимся и узнаем характеры гидроксида натрия и соляной кислоты.
Гидроксид натрия
Химическая формула — NaOH. Является одной из самых распространенных щелочей, известен также как каустическая сода.
Физические свойства
Твердый белый или чуть желтоватый порошок. Гигроскопичен, разъедает многие материалы и органические вещества: бумагу, кожу и даже некоторые металлы, растворяется в воде, этиловом и метиловом спиртах.
Химические свойства
Это сильное химическое основание, взаимодействует с:
- кислотами;
- амфотерными оксидами;
- амфотерными гидроксидами;
- солями в растворе;
- неметаллами;
- галогенами;
- металлами;
- эфирами, амидами и алкилгалогенидами;
- многоатомными спиртами.
Области применения
Гидроксид натрия используется в самых различных отраслях:
- в химической промышленности;
- при нефтепереработке;
- в целлюлозно-бумажной промышленности;
- для устранения засора в трубах;
- в гражданской обороне (нейтрализующее вещество);
- в пищевой промышленности: для очистки овощей и фруктов от корочки; в производстве шоколада и какао; для размягчения маслин и окрашивания их в темный цвет;
- в косметологии (для удаления ороговевших участков кожи);
- в быту.
Теперь познакомимся поближе с соляной кислотой.
Соляная кислота
Химическая формула — HCl. Сильная минеральная одноосновная бескислородная кислота.
Физические свойства
Бесцветная прозрачная едкая жидкость, дымящаяся на воздухе. Максимальная концентрация при 200 °С равна 38%, плотность такого раствора — 1,19 г/см³. Если высококонцентрированная кислота вызывает сильные ожоги кожи, слизистых оболочек и глаз, а вот в концентрации около 0,5 % она присутствует в желудке человека.
Химические свойства
Это сильная кислота, взаимодействует с:
• металлами; • гидроксидами металлов; • оксидами металлов; • солями металлов; • сильными окислителями; • аммиаком.
Качественная реакция на соляную кислоту и ее соли – взаимодействие с нитратом серебра.
Область применения
Соляная кислота используется в:
- в гидрометаллургии и гальванопластике;
- в химической промышленности;
- в пищевой промышленности (пищевая добавка Е507);
- в медицине (при пониженной кислотности в желудке).
И вот решил Химик подружить два непримиримых рода и повенчать влюбленных: сделать всё, чтоб состоялась реакция гидроксида натрия с соляной кислотой. В свидетели с невестой-кислотой пошел индикатор Фенолфталеин. Как только сбудется реакция с гидроксидом, бесцветный индикатор от радости станет малиновым. Несмотря на то что агрессивными были гидроксид натрия и соляная кислота, какая реакция получилась хорошая!
Напишем уравнение этой реакции:
HCl + NaOH = NaCl + H₂O + Q
Соляная кислота и гидроксид натрия> взаимодействуют, в результате чего образуются соль и вода и выделяется тепло.
Как видим, в результате взаимодействия двух агрессивнейших соединений получилась поваренная соль и вода — безобиднейшие и даже полезные для человека соединения. Примирились-таки два враждующих рода и перестали быть злыми и опасными.
А чтобы оценить по достоинству продукты реакции, давайте сядем в ракету и устремимся в космос. Взгляните на нашу Землю со стороны. Не зря ее называют голубой планетой, ведь 71% ее поверхности занимают моря и океаны, то есть вода, один из продуктов нашей реакции. Хотя отметим, справедливости ради, что только 1% от этого количества пригоден к употреблению.
А теперь заглянем в самый лучший ресторан, какой — вы решите сами. Не ограничивайте себя в фантазиях, ведь в пределах нашей истории возможно всё! Давайте пройдем на кухню и спросим шеф-повара, без каких двух продуктов он не смог бы обойтись. И поверьте, он назовет не икру, трюфели или пармезан — он выберет соль и воду, поскольку без этих простых компонентов не приготовишь ни одно блюдо.
Наши продукты реакции входят в состав соединения, которое вы найдете и дома в супе или рассоле, и в морской воде. Об этом соединении поет ансамбль песни и пляски Черноморского флота «Эх! Соленая вода, ветер на просторе, полюбили навсегда голубое море!» А теперь присмотримся повнимательней и определим, какая же это реакция гидроксида натрия и соляной кислоты с точки зрения классификации химических реакций.
Определение вида химической реакции соляной кислоты с гидроксидом натрия.
1. По числу и состоянию исходных и образующихся веществ, это реакция обмена.
Другими словами, количество веществ, вступивших в реакцию, равно количеству веществ, получившихся в результате. Просто произошел обмен ионами. Чтобы увидеть это, напишем уравнение реакции в ионном виде:
H⁺ + Cl⁻ + Na⁺ + OH⁻ = Na⁺+Cl⁻ + H₂O
Следуя сюжету нашей повести, жених с невестой обменялись своим личным имуществом: бери, мол, мне для тебя ничего не жалко. Узнать больше об их «приданном» вы можете здесь.
2. По типу взаимодействующих веществ, это реакция нейтрализации:
3. По агрегатному состоянию веществ, эта реакция является гомогенной.
Вещества, вступающие в реакцию, находятся в одинаковом агрегатном состоянии — в растворе.
4. По направлению протекания реакции, она необратимая.
Реакция протекает до конца, то есть до полного расхода реагирующих веществ.
5. По тепловому эффекту — экзотермическая. Другими словами, церемония венчания прошла в теплой атмосфере. Реакция сопровождается тепловым эффектом, выделяется 57,3 кДж тепловой энергии.
6. Реакция не является окислительно-восстановительной: степени окисления атомов в ходе реакции не изменились.
H⁺Cl⁻ + Na⁺O₂⁻H⁺ = Na⁺Cl⁻ + H₂⁺ O₂⁻
Подведем итоги. У нашей любовной истории счастливый финал: любящие сердца из двух непримиримых семейств воссоединились.
Взаимодействовали агрессивные гидроксид натрия, соляная кислота, реакция же в результате дала нам очень полезные продукты, воспетые в искусстве.
Какая всё-таки замечательная наука − химия. Благодаря реакции кислоты со щелочью мы смогли изменить финал самой печальной трагедии и превратить ее в счастливый роман!
Please wait.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 6e0833084f370c71 • Your IP : 85.95.188.35 • Performance & security by Cloudflare
http://melscience.com/RU-ru/articles/reakciya-gidroksida-natriya-s-solyanoj-kislotoj/
http://gomolog.ru/reshebniki/8-klass/eremin-2019/36/lab-18.html