Урок-обобщение по теме «Серебро и его соединения». 11-й класс
Разделы: Химия
Класс: 11
Цель урока:
Задачи урока:
- Серебро – химический элемент.
- История происхождения серебра.
- Нахождение в природе.
- Физические свойства серебра.
- Химические свойства серебра:
- Взаимодействие с простыми веществами.
- Взаимодействие со сложными веществами.
- Химические свойства соединений серебра со степенью окисления +1.
- Получение серебра.
- Применение серебра.
- Закрепление.
- Домашнее задание.
Ход урока
При подготовке к уроку учащиеся класса получают задание по анализу отдельных вопросов и делятся на экспертные группы: “историки”, “геологи”, “физики”, “химики – теоретики”, “химики – экспериментаторы”, “технологи”, “врачи”.
1. Серебро – химический элемент.
Учитель: На основании положения атома серебра в периодической системе дайте характеристику как типичному d-элементу.
Ученик: Серебро – химический элемент с порядковым номером 47, номер периода 5, большой, нечетный 7 ряд, номер группы 1, побочная подгруппа, d-элемент, металл, электронная конфигурация [Кr]4d 10 5s 1 .
Учащиеся на доске изображают электронно-графическую формулу атома серебра, отмечают характерные степени окисления: 0, +1; отмечая признаки проскокa электронов, о возможности проявления степеней окисления +2, +3.
2. История происхождения серебра (сообщение учащегося их группы “историков”).
Серебро известно человечеству с древнейших времен. Это связано с тем, что в свое время серебро, равно как золото, часто встречалось в самородном виде – его не приходилось выплавлять из руд. Это предопределило довольно сильное присутствие серебра в культурных традициях различных народов. В Ассирии и Вавилоне серебро считалось священным металлом и являлось символом Луны. В средние века серебро и его соединения были очень популярны среди алхимиков. На русском “серебро”, на немецком “зильбер”, на английском “сильвер” – эти слова восходят к древнеиндийскому слову “сарпа”, которым обозначили Луну и Серп – древнейшее орудие земледельца. Латынское слово “аргентум” означает “белое”. С середины 18 века серебро становится традиционным материалом для изготовления посуды. Кроме того, серебро и по сей день используется для чеканки монет.
3. Нахождение в природе (сообщение учащегося из группы “геологов”).
- Определенная часть благородных и цветных металлов встречаются в природе в самородной форме. Известны и документально подтверждены факты нахождения не просто больших, а огромных самородков серебра. Так, например, в 1447г. на руднике “Святой Георгий” был обнаружен самородок серебра весом 20 т. Глыбу серебра размером 1х1х2,2 м выволокли из горной выработки, устроили на ней праздничный обед, а затем раскололи и взвесили. В Дании, в музее Копенгагена, находится самородок весом 254 кг, обнаруженный в 1666 г. на норвежском руднике Конгсберг.
- В настоящее время в здании парламента Канады хранится одна из добытых на месторождении Кобальт самородных пластин серебра, получившая за свои размеры название “серебряный тротуар”, она имела длину около 30 м и содержала 20 т серебра.
- Известны более 50 природных минералов серебра; в них серебро связано с серой, селеном, теллуром или галогенами, из которых важное промышленное значение имеют лишь 15-20, в том числе: самородное серебро; электрум (золото-серебро); кюстелит (серебро-золото); аргентит Ag2S (серебро-сера).
Серебро встречается в природе в самородном состоянии и в виде соединений. Серебро– редкий элемент; в земной коре его почти в тысячу раз меньше, чем меди и его содержание составляет 7х10 -6 весовых процента (золота в 20 раз меньше), по распространенности серебро на 67-месте среди элементов. Серебром богаты страны Центральной Европы ( Чехии, Германии, Австрии, Испании, Франции, Англии), Южной Америки (Перу, Чили, Мексики, Боливии), Канады.
4. Физические свойства серебра.
Учитель: Какова кристаллическая решетка серебра? Исходя из этого, назовите известные Вам физические свойства серебра, отмечая самые привлекательные из них.
Сообщение учащегося из группы “физиков”: Серебро – довольно тяжелый ( его плотность 10,5 г/см 3 ) металл белого цвета, сравнительно мягкий, ковкий, пластичный (1 г его можно вытянуть в проволоку длиной до 2 км), тугоплавкий (температура плавления 1235,1?С). Имеет высокую отражательную способность (во время ВОВ при штурме Берлина войсками Первого и Белорусского фронта 143 прожектора огромной светосилы ослепили гитлеровцев в их оборонительной полосе, и это способствовало быстрому исходу операции) и самые высокие показатели электропроводности и теплопроводности среди всех металлов. Серебро легко сплавляется со многими металлами; небольшие добавки меди делают его более твердым, годным для изготовления различных изделий.
Не стоит забывать и о “фамильном серебре”: ковкость, пластичность, бактерицидность делали посуду предметом роскоши. Это был символ достатка и респектабельности. В этом никто не мог переплюнуть графа Орлова, фаворита Екатерины Великой. Его респектабельность состояла из 3275 серебряных предметов, на изготовление которых более 2 тонн серебра.
5. Химические свойства серебра.
a. Взаимодействие с простыми веществами
Учитель: Какова химическая активность серебра по положению в электрохимическом ряду напряжения металлов?
Учитель: С какими простыми веществами реагирует серебро?
В работу включаются учащиеся из группы “химиков – теоретиков”.
На доске составляются левые части уравнений химических реакций; учащиеся в духе соревнования дописывают правую часть уравнений.
4Ag + O2—> 2Ag2O (при обычных условиях с кислородом реакция не идет)
Учитель: Что происходит с серебром во время грозы?
Учитель: Почему серебряные изделия чернеют на воздухе и на кожном покрове?
2Ag + S—> Ag2S (черный осадок)
Серебро также темнеет при продолжительном контакте с белком и кожей нездорового человека, отсюда и поверье о том, что серебро обладает даром предвидеть тяжелое заболевание своего хозяина. Чёрное вещество на серебре – это окись серебра и сульфид серебра в разных пропорциях.
Учитель: Почему при работе с галогенами нужно снимать серебряные изделия?
2Ag + Cl2—> 2AgCl (серебро хорошо реагирует с галогенами)
b. Взаимодействие со сложными веществами
Учитель: Возможно ли протекание следующих уравнений химических реакций:
Ответ: Серебро – благородный металл (находится в ряду напряжений металлов после водорода, с разбавленными растворами кислот, кроме HNO3, реакция не идет)
Учитель: Составьте уравнения следующих реакций (на доске представляется схема левой части уравнений):
Учитель: Возможно ли протекание следующих уравнений химических реакций:
Ag +CuSO4 —> (реакция не протекает, так как атом серебра в электрохимическом ряду напряжений металлов находится после атома меди).
Вывод: Серебро – малоактивный металл (электродный потенциал равен 0), восстановительные свойства выражены слабо.
c. Химические свойства соединений серебра со степенью окисления +1
1) Взаимодействие с неорганическими веществами
Учитель: Как из нитрата серебра можно получить оксид серебра (I)
Ag2 O – оксид серебра – твердое вещество темно–коричнего цвета. Проявляет амфотерные свойства
AgNO3 нитрат серебра (ляпис) – кристаллы белого цвета. Самая известная соль элемента №47. Обладает прижигающим и вяжущим действием. На коже оставляет след.
Учитель: Какие ионы можно определять с помощью раствора нитрата серебра AgNO3 ? (Приложение 1).
AgNO3 + NaГ —> Ag Г + NaNO3; Г=Cl, Г=Br, Г=J, 
Учащиеся составляют уравнения химических реакций качественного анализа в молекулярном ионном видах с указанием цвета осадков.
Группа химиков-экспериментаторов осуществляет качественный анализ, результаты исследований представляет вниманию класса.
Учитель: Какие изменения происходят с соединениями серебра со степенью окисления +1 при термическом разложении?
Разложение AgBr используется в фотоделе:
Учитель: В чем проявляются основные свойства 
Учитель: Какие свойства имеют соединения Ag +1 с точки зрения ОВР?
Окислительные свойства 
Учитель: Соединения Ag +1 – комплексообразователи.
Соединения Ag +1 легко восстанавливаются до Ag 0 :
Но хлорид серебра не растворяется даже в концентрированной азотной кислоте.
2) Взаимодействие аммиачного раствора оксида серебра (I) с органическими веществами.
Учитель: Как можно качественно обнаружить концевую тройную связь у алкинов?
Ответ: Концевую тройную связь у алкинов можно обнаружить с помощью аммиачного раствора оксида серебра (I). При этом с ацетиленом образуется взрывчатое вещество ацетитиленида серебра (I) темно-серого цвета, применяемое в военном деле для взрывных работ.
Данная реакция не характерна для алкинов с положением тройной связи в других позициях: реакция не идет с бутином-2.
Учитель: Какие функциональные группы у кислородсодержащих органических соединений можно качественно обнаружить с помощью аммиачного раствора оксида серебра (I)?
Ответ: C помощью аммиачного раствора оксида серебра (I) определяется альдегидная группа у альдегидов, моносахаридов (глюкозы), дисахаридов: восстанавливающихся сахаров– лактозы и мальтозы. При этом идет реакция “серебряного зеркала” с выпадением блестящего зеркального налета (использовалась для производства зеркал), где 
Учитель: В двух пробирках находятся растворы муравьиной и уксусной кислот. Как экспериментально можно обнаружить данные кислоты?
Ответ: Оба раствора кислот является бесцветными жидкостями со специфическим запахом, изменяют цвет лакмуса в красный, метилоранжа – розовый. Под действием соды – вскипают. Но у муравьиной кислоты в результате внутренней перегруппировки атомов имеется альдегидная группа. Поэтому единственной карбоновой кислоте характерна реакция “серебряного зеркала”.
Выводы:
6. Получение серебра (выступает группа “технологов”).
Поскольку месторождения серебра редки и выработаны, его получают из руд таких металлов, как медь и свинец, в которых всегда содержится примесь серебра:
1) Пирометаллургический способ получения серебра.
Серебро выделяют из неочищенного свинца. Сначала к свинцу добавляют жидкий цинк, который не смешивается со свинцом, но дает прочные интерметаллиды с серебром: Ag2Zn3, Ag2Zn5. В жидком свинце эти интерметаллиды не растворяются, а всплывают на поверхность (образуется серебристая поверхность). Ее снимают, удаляют Zn перегонкой, а свинец удаляют в виде оксида:
Далее серебро очищается электролитически.
2) Серебро получают в виде побочного продукта при переработке медных руд. При очистке электролизом “черновой меди” в электролит (раствор CuSO4) переходят примеси металлов, стоящих в ряду напряжений до меди, а в осадок (шлам) выпадает Ag, Au, платиновые металлы и т.д.– металлы, стоящие в ряду напряжений до меди.
7. Применение серебра.
Учитель: На основании изученных физико-химических свойств серебра и его соединений выделите наиболее важные отрасли применения серебра.
Ответ:
Серебро используется в качестве катализатора в фильтрах противогазов.
Ацетиленид серебра (карбид) изредка применяется как мощное инициирующее взрывчатое вещество (детонаторы).
Серебро зарегистрировано в качестве пищевой добавки Е174.
Еще более эффективно действует слабый раствор комплексного соединения серебра с аммиаком, применяющийся в медицине под названием аммарген (производное от слов “аммиак” и “аргентум”). Нитраты серебра в виде раствора аммаргена широко применяются для промывания ран или слизистой оболочки при различных воспалительных состояниях, а также используются в изготовлении различных антибактериальных средств.
Физиологическое действие (выступает группа “врачей”).
Обычно серебро поступает с водой и пищей в ничтожно малых количествах– всего 7 микрограммов в сутки. И при этом такое явление, как дефицит серебра, пока нигде не описано.Серебро не относится к жизненно важным биоэлементам. Серебро – это тяжелый металл. Пить воду с ионами серебра не стоит. Серебро – клеточный яд. Постоянное употребление серебра даже в малых дозах может вызвать хроническое заболевание, связанное с повышенным содержанием серебра в организме – аргирию (аргентоз, аргироз). ПДК для серебра – 50 мкг/л. При длительном употреблении может возникать поражение почек, неврологические расстройства, нарушение пищеварения, головные боли и хроническая усталость. При попадании в организм больших доз растворимых солей серебра наступает острое отравление, сопровождающееся некрозом слизистой желудочно-кишечного тракта. Первая помощь при отравлении – промывание желудка раствором хлорида натрия, при этом образуется нерастворимый хлорид серебра, который и выводится из организма. Ион Ag + , попадая на тело, вызывает ожог.
Химические свойства серебра
В твердом серебре растворимость кислорода мала, поэтому при затвердевании расплавленного серебра происходит выделение растворенного в нем кислорода, сопровождающееся иногда разбрызгиванием металла.
С водородом, азотом и углеродом серебро непосредственно не взаимодействует. Фосфор действует на серебро лишь при температуре красного каления с образованием фосфидов.
При нагревании с серой серебро легко образует сульфид Ag2S. Это же соединение получается при действии на серебро газообразной серы, выделяющейся при термической диссоциации некоторых сульфидов (пирита, пирротина, халькопирита), и при нагреве металла в контакте с этими сульфидами. При воздействии сероводорода поверхность серебра покрывается черной пленкой Ag2S. Процесс медленно идет уже в обычных условиях и является причиной постепенного потемнения серебянных изделий.
Серебро взаимодействует также со свободными хлором, бромом и иодом с образованием соответствующих галогенидов. Эти процессы медленно протекают, даже при обычных температурах и ускоряются в присутствии влаги, при нагревании и под действием света.
Электродный потенциал серебра в водных растворах высок :
Ag → Ag⁺ + е, φ0 = + 0,799В
Поэтому, как и золото, серебро не вытесняет водород из водных растворов кислот, устойчиво по отношению к щелочам. Однако в отличие от золота оно растворяется в кислотах, являющихся достаточно сильными окислителями, например, в азотной и концентрированной серной. Подобно золоту, серебро легко взаимодействует с царской водкой и насыщенной хлором соляной кислотой, но при этом оно остается в нерастворимом остатке вследствие образования малорастворимого хлорида AgCl.
Такие различия в поведении золота и серебра часто используют для разделения этих металлов. Тонкодисперсное серебро в контакте с кислородом воздуха растворяется в разбавленной серной кислоте. Подобно золоту, серебро растворяется также в насыщенных воздухом водных растворах цианидов щелочных и щелочноземельных металлов, в водном растворе тиомочевины в присутствии солей железа (III).
Соединения серебра
В подавляющем большинстве своих соединений серебро имеет степень окисления (+1). Соединения с более высокой степенью окисления серебра (+2 и +3) сравнительно малочисленны и практического значения не имеют.
Оксид серебра Ag2О
Черно-коричневого цвета может быть получен введением щелочи в раствор, содержащий ионы Ag⁺. Вначале, по-видимому, образуется гидроксид, тотчас переходящий в оксид:
2AgOH = Ag2O + Н2О.
Хотя оксид серебра — малорастворимое в воде соединение, его водная суспензия имеет четко выраженную основную реакцию, поэтому соли серебра в водных растворах не гидролизуются и дают нейтральную реакцию. При нагревании до 185—190°С Ag2О разлагается на элементы. Перекись водорода легко восстанавливается Ag2О уже при комнатной температуре:
В водном растворе аммиака Ag2О растворяется с образованием комплексного соединения:
При стоянии из раствора осаждается чрезвычайно взрывчатый даже во влажном состоянии осадок нитрида серебра Ag3N (гремучее серебро).
Галогениды серебра
Малорастворимые соединения. Исключение составляет лишь легкорастворимый фторид AgF. Хлорид AgCl, бромид AgBr и иодид AgI выпадают в осадок при введении в раствор, содержащий ионы Ag⁺ (например, раствор AgNO3), ионов Сl⁻, Вr⁻ и I⁻. Их произведения растворимости составляют соответственно 1,8 • 10⁻¹º (AgCI), 5,3 • 10⁻¹³ (AgBr) и 8,3 •10⁻¹⁷ (AgI).
В гидрометаллургии и аффинаже благородных металлов широко используют прием осаждения серебра в виде хлорида, осуществляемый введением в серебросодержащие растворы NaCl или НСl. Хлорид серебра плавится при 455°С. Температура кипения AgCl 1550°С, но заметное улетучивание наблюдается уже при температуре выше 1000 °с.
Ионы серебра образуют прочные комплексы с целым рядом ионов и молекул (CN⁻, S2O²3⁻, SO²3⁻ Cl⁻, NH3, CS(NH2)2 и т.д.). Благодаря этому практически нерастворимый в воде AgCl легко растворяется в водных растворах цианистого калия, тиосульфата и сульфита натрия, аммиака, например:
AgCl + 2CN⁻ = Ag (CN)F + Сl⁻;
AgCl + 2S2C²3⁻ = Ag (S2O2)³2⁻ + Сl⁻;
AgCl + 2NH4OH = Ag(NH3)2+ + Сl⁻ + 2H2O.
Вследствие образования комплексов с ионами Сl³⁻ хлорид серебра заметно растворим также в концентрированных соляной кислоте и растворах других хлоридов:
AgCl + Сl⁻ = AgCl⁻ 2.
Например, в концентрированном растворе NaCl растворимость хлорида серебра составляет 6,7•10³⁻моль/л (0,72 г/л Ag) против 1,3•10⁻⁵ в воде. Концентрированные растворы NaCl использовали ранее для выщелачивания серебра из огарков хлорирующего обжига.
Таким образом при введении хлор-ионов в серебросодержащие растворы концентрация серебра вначале падает (образование AgCl), а затем начинает возрастать (в ре-зультате комплексообразования). Поэтому для достижения полноты осаждения серебра следует избегать большого избытка ионов хлора.
Электроотрицательными металлами (цинком, железом) .хлорид серебра, взятый в виде суспензии в разбавленной серной кислоте, легко восстанавливается до металла. Этот простой прием получения металлического серебра из его хлорида широко применяют в аффинажном производстве.
Бромид серебра AgBr похож по своим свойствам на AgCl. Он растворим в аммиачных, тиосульфатных, сульфитных и цианистых растворах, легко восстанавливается до металла.
Иодид AgI
Наименее растворимый из галогенидов серебра, поэтому в отличие от AgCl и AgBr он не растворим в аммиачных растворах, но растворим в присутствии ионов CN⁻ и S2O²3⁻ , с которыми серебро образует более прочные, нежели с аммиаком, комплексы. Заметной растворимостью AgI обладает также в концентрированных растворах иодидов щелочных металлов, что объясняется образованием комплексных ионов AgI⁻2.
Весьма характерной и важной особенностью труднорастворимых галогенидов серебра является их светочувст-вительность, заключающаяся в том, что под действием света они разлагаются на металлическое серебро и свободный галоид:
Это свойство галоидных солей серебра лежит в основе их применения для производства фотоматериалов — светочувствительных пленок, пластинок и бумаги. Светочувствительность галидов серебра возрастает в ряду AgI
К галогенидам серебра очень близок по своим свойствам цианид AgCN. Он выпадает в виде белого осадка при добавлении к раствору, содержащему ионы Ag⁺, раствора цианида щелочного металла (без избытка). Подобно галогенидам серебра, AgCN практически нерастворим в воде (произведение растворимости 2.3•10⁻¹⁶) и разбавленных кислотах, но растворим в аммиачных, тиосульфатных и цианистых растворах, вследствие образования соответствующих комплексных соединений. В отличие от галогенидов цианид серебра под действием света не разлагается.
Нитрат серебра
Из других соединений серебра большое практическое значение имеют нитрат и сульфат серебра.
Нитрат серебра AgNО3 получают действием азотной кислоты на металлическое серебро:
3Ag + 4HNO3 = 3AgNО3 + NO + 2H2О.
Нитрат серебpa представляет собой бесцветные негигроскопичные кристаллы, плавящиеся при 208,5 °С ; при температуре выше 350 °С термически разлагается. AgNО3 очень легко растворяется в воде. При 20 °С его растворимость составляет 222 г на 100 г воды, при 100 °С она возрастает до 952 г на 100 г.
В присутствии органических веществ нитрат серебра чернеет вследствие частичного восстановления до металла.
Нитрат серебра — технически наиболее важное соединение этого металла. Эта соль служит исходным продуктом для приготовления остальных соединений серебра. Водный раствор AgNO3 используют в качестве электролита при электролитическом рафинировании серебра.
Сульфат серебра Ag2SO4
Может быть получен растворением металлического серебра в горячей концентрированной серной кислоте:
2Ag + 2H2SO4 = Ag2SO4 + SO2 + 2Н2O.
Сульфат серебра образует бесцветные кристаллы, плавящиеся при 660°С. При температуре выше 1000°С термически разлагается. Растворимость Ag2SO4 в воде невелика, при 25°С она составляет 0,80 г на 100 г воды. В концентрированной серной кислоте растворимость значительно выше вследствие образования более растворимого бисульфата AgHSO4.
Сульфид серебра Ag2S — наиболее трудно растворимая соль этого металла (произведение растворимости 6.3• 10⁻⁵º). Он выпадает в виде черного осадка при пропускании сероводорода через растворы солей серебра. Образование Ag2S происходит также при действии H2S на металлическое серебро в присутствии влаги и кислорода воздуха;
4Ag + 2H2S + O2 = 2Ag2S + 2Н2O
Как было отмечено, этот процесс является причиной потемнения серебряных изделий при длительном хранении. Сульфид серебра можно получить также непосредственно из элементов, нагревая металлическое серебро с элементарной серой.
В цианистых растворах Ag2S растворяется в результате образования комплексного соединения:
Ag2S + 4CN⁻ ⇄ 2Ag(CN)⁻2 + S²⁻
Эта реакция обратима, протеканию ее слева направо способствует повышение концентрации иновов CN⁻ и удаление ионов S²⁻ окислением их кислородом продуваемого воздуха.
С разбавленными минеральными кислотами Ag2S не взаимодействует. Концентрированная серная и азотная кислота окисляют сульфид серебра до сульфата. При нагревании в атмосфере воздуха Ag2S разлагается с образованием металлического серебра и диоксида серы:
Ag2S + О2 = 2Ag + SО2
Из ранее упоминавшихся комплексных соединений серебра наибольший интерес для гидрометаллургии этого металла представляют хорошо растворимые комплексные цианистые соединения калия, натрия и кальция. Подобно аналогичным соединениям золота, комплексные цианиды серебра образуются при растворении металлического серебра в растворе соответствующего цианида при доступе кислорода воздуха:
4Ag + 8CN⁻ + О2 + 2Н2О = 4Ag(CN)7 + 4ОН⁻
Эта реакция, как и аналогичная реакция с золотом, лежит в основе процесса цианирования.
Как и золото, серебро растворяется в водных растворах тиомочевины в присутствии солей Fe(III),образуя комплексные катионы Ag[CS(NH2)2]⁺2
Статья на тему химические свойства серебра
Похожие страницы:
Понравилась статья поделись ей
Leave a Comment
Для отправки комментария вам необходимо авторизоваться.
Серебро (Ag)
Серебро известно человеку с древности, что связано, в первую очередь с тем, что оно встречается в природе в виде самородков.
Серебро является одним из самых распространенных в земной коре благородных металлов — содержание серебра в земной коре составляет 7·10 -6 по массе, наиболее богаты серебром глинистые сланцы (1 г на тонну). Современной науке известно порядка 60 минералов, в состав которых входит серебро.
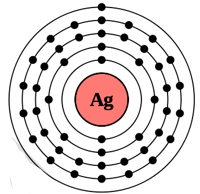
Рис. Строение атома серебра.
Электронная конфигурация атома серебра — 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4d 10 5s 1 (см. Электронная структура атомов). Серебро является химически неактивным металлом.
Физические свойства серебра:
- блестящий мягкий металл белого цвета;
- обладает хорошей пластичностью;
- имеет среди всех металлов самую высокую теплопроводность и электропроводность.
Химические свойства серебра:
- при н. у. не реагирует с кислородом, при нагревании до 170°C покрывается оксидной пленкой: 4Ag + O2 = 2Ag2O;
- не реагирует с водой, щелочными растворами;
- с концентрированной серной кислотой реагирует при нагревании: 2Ag + 2H2SO4 = Ag2SO4 + SO2 + 2H2O;
- легко реагирует с азотной кислотой, как разбавленной, так и концентрированной: Ag + 2HNO3(конц.) = AgNO3 + NO2 + H2O.
Применение серебра:
- для получения сплавов с другими металлами;
- в производстве аккумуляторов большой емкости;
- в ювелирном деле;
- в чеканке монет;
- в качестве катализатора химических процессов.
Наиболее распространенные соединения серебра:
- оксид серебра Ag2O;
- гидроксид серебра AgOH;
- галогениды AgCl, AgBr, AgI — применяются в производстве кино- и фотопленки;
- нитрат серебра AgNO3 — растворимое в воде соединение, применяется в фотографии, для серебрения зеркал, для получения других соединений серебра.
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
http://znaesh-kak.com/q/s/%D1%85%D0%B8%D0%BC%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B5-%D1%81%D0%B2%D0%BE%D0%B9%D1%81%D1%82%D0%B2%D0%B0-%D1%81%D0%B5%D1%80%D0%B5%D0%B1%D1%80%D0%B0
http://prosto-o-slognom.ru/chimia/512_serebro_Ag.html










