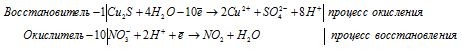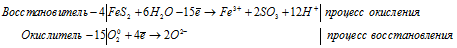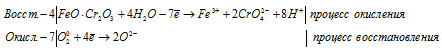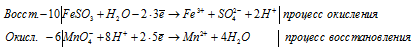Please wait.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 6e0bcd88cce01607 • Your IP : 85.95.188.35 • Performance & security by Cloudflare
Оксид серы (IV)
Оксид серы (IV) – это кислотный оксид . Бесцветный газ с резким запахом, хорошо растворимый в воде.
Cпособы получения оксида серы (IV)
1. Сжигание серы на воздухе :
2. Горение сульфидов и сероводорода:
2CuS + 3O2 → 2SO2 + 2CuO
3. Взаимодействие сульфитов с более сильными кислотами:
Например , сульфит натрия взаимодействует с серной кислотой:
4. Обработка концентрированной серной кислотой неактивных металлов.
Например , взаимодействие меди с концентрированной серной кислотой:
Химические свойства оксида серы (IV)
Оксид серы (IV) – это типичный кислотный оксид. За счет серы в степени окисления +4 проявляет свойства окислителя и восстановителя .
1. Как кислотный оксид, сернистый газ реагирует с щелочами и оксидами щелочных и щелочноземельных металлов .
Например , оксид серы (IV) реагирует с гидроксидом натрия. При этом образуется либо кислая соль (при избытке сернистого газа), либо средняя соль (при избытке щелочи):
SO2(изб) + NaOH → NaHSO3
Еще пример : оксид серы (IV) реагирует с основным оксидом натрия:
2. При взаимодействии с водой S O2 образует сернистую кислоту. Реакция обратимая, т.к. сернистая кислота в водном растворе в значительной степени распадается на оксид и воду.
3. Наиболее ярко выражены восстановительные свойства SO2. При взаимодействии с окислителями степень окисления серы повышается.
Например , оксид серы окисляется кислородом на катализаторе в жестких условиях. Реакция также сильно обратимая:
Сернистый ангидрид обесцвечивает бромную воду:
Азотная кислота очень легко окисляет сернистый газ:
Озон также окисляет оксид серы (IV):
Качественная реакция на сернистый газ и на сульфит-ион – обесцвечивание раствора перманганата калия:
Оксид свинца (IV) также окисляет сернистый газ:
4. В присутствии сильных восстановителей SO2 способен проявлять окислительные свойства.
Например , при взаимодействии с сероводородом сернистый газ восстанавливается до молекулярной серы:
Оксид серы (IV) окисляет угарный газ и углерод:
SO2 + 2CO → 2СО2 + S
Составление ионно-молекулярной формы процесса окисления-восстановления с двумя окисляющимися элементами
После приведения членов обеих частей уравнения, получим:
Добавив в обе части равенства соответствующее количество ионов Н+ и NO3-, получим молекулярную форму процесса
4FeS2 + 15O2 0 + 24Н2О = 4Fe 3+ + 8SO3 + 48H + + 30O 2- .
Сорок восемь ионов водорода и двадцать четыре иона кислорода, соединяясь образуют двадцать четыре молекулы воды, получим:
После приведения членов обеих частей уравнения, получим:
Уравнение в молекулярной форме имеет вид:
4FeO . Cr2O3 + 7O2 0 + 16H2O = 4Fe 3+ + 8CrO4 2- + 14H + + 10O 2-
После приведения членов обеих частей уравнения, получим:
Так как в качестве исходного продукта в систему введён карбонат калия, то, подставив его в уравнение, получим:
Для получения полного уравнения после уравнивания калия получим:
4FeO . Cr 2 O 3 + 7O 2 0 + 2H 2 O + 8K 2 CO 3 = 4Fe 3+ + 8K 2 CrO 4 + 4H + + 8CO3 2-
С учётом того, что одним из продуктов реакции является углекислый газ, получим окончательную ионно-молекулярную форму уравнения реакции:
Уравнение в молекулярной форме будет имеет вид:
10FeSO3 + 6MnO4 — + 48H + + 10H2O = 10Fe 3+ + 6Mn 2+ + 10SO4 2- + 20H + + 24H2O
После приведения членов в обеих частях уравнения получим:
10FeSO3 + 6MnO4 — + 28H + = 10Fe 3+ + 6Mn 2+ + 10SO4 2- + 14H2O
Молекулярная форма имеет вид:
В данном процессе восстановитель содержит два окисляющихся элемента. Так FeSO3 содержит атом железа, который увеличивает свою степень окисления от +2 до +3, а атом серы от +4 до +6. При составлении уравнения электронно-ионного баланса число отданных электронов умножаем на 2, для того, чтобы привести к чётному значению числа атомов железа, серы и кислорода в формуле вещества Fe2(SO4)3.
http://chemege.ru/oksid-sery-iv/
http://buzani.ru/zadachi/khimiya-glinka/1218-vosstanovitel-s-dvumya-okislyayushchimisya-elementami-zadacha-636