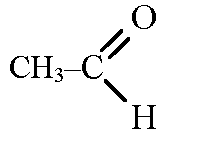
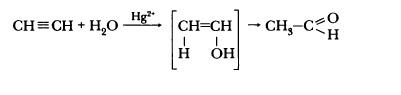Этанол: химические свойства и получение
Этанол C2H5OH или CH3CH2OH, этиловый спирт – это органическое вещество, предельный одноатомный спирт .
Общая формула предельных нециклических одноатомных спиртов: CnH2n+2O.
Строение этанола
В молекулах спиртов, помимо связей С–С и С–Н, присутствуют ковалентные полярные химические связи О–Н и С–О.
| Электроотрицательность кислорода (ЭО = 3,5) больше электроотрицательности водорода (ЭО = 2,1) и углерода (ЭО = 2,4). |
Электронная плотность обеих связей смещена к более электроотрицательному атому кислорода:
| Атом кислорода в спиртах находится в состоянии sp 3 -гибридизации. |
В образовании химических связей с атомами C и H участвуют две 2sp 3 -гибридные орбитали, а еще две 2sp 3 -гибридные орбитали заняты неподеленными электронными парами атома кислорода.
Поэтому валентный угол C–О–H близок к тетраэдрическому и составляет почти 108 о .
Водородные связи и физические свойства спиртов
Спирты образуют межмолекулярные водородные связи. Водородные связи вызывают притяжение и ассоциацию молекул спиртов:
Поэтому этанол – жидкость с относительно высокой температурой кипения (температура кипения этанола +78 о С).
Водородные связи образуются не только между молекулами спиртов, но и между молекулами спиртов и воды. Поэтому спирты очень хорошо растворимы в воде. Молекулы спиртов в воде гидратируются:
| Чем больше углеводородный радикал, тем меньше растворимость спирта в воде. Чем больше ОН-групп в спирте, тем больше растворимость в воде. |
Этанол смешивается с водой в любых соотношениях.
Изомерия спиртов
Структурная изомерия
Для этанола характерна структурная изомерия – межклассовая изомерия.
Межклассовые изомеры — это вещества разных классов с различным строением, но одинаковым составом. Спирты являются межклассовыми изомерами с простыми эфирами. Общая формула и спиртов, и простых эфиров — CnH2n+2О.
| Например. Межклассовые изомеры с общей формулой С2Н6О этиловый спирт СН3–CH2–OH и диметиловый эфир CH3–O–CH3 |
| Этиловый спирт | Диметиловый эфир |
| СН3–CH2–OH | CH3–O–CH3 |
Химические свойства этанола
Спирты – органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
1. Кислотные свойства
| Спирты – неэлектролиты, в водном растворе не диссоциируют на ионы; кислотные свойства у них выражены слабее, чем у воды. |
1.1. Взаимодействие с раствором щелочей
При взаимодействии этанола с растворами щелочей реакция практически не идет, т. к. образующийся алкоголят почти полностью гидролизуется водой.
Равновесие в этой реакции так сильно сдвинуто влево, что прямая реакция не идет. Поэтому этанол не взаимодействуют с растворами щелочей.
1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
Этанол взаимодействует с активными металлами (щелочными и щелочноземельными).
| Например, этанол взаимодействует с калием с образованием этилата калия и водорода . |
Алкоголяты под действием воды полностью гидролизуются с выделением спирта и гидроксида металла.
| Например, этилат калия разлагается водой: |
2. Реакции замещения группы ОН
2.1. Взаимодействие с галогеноводородами
При взаимодействии спиртов с галогеноводородами группа ОН замещается на галоген и образуется галогеналкан.
| Например, этанол реагирует с бромоводородом. |
2.2. Взаимодействие с аммиаком
Гидроксогруппу спиртов можно заместить на аминогруппу при нагревании спирта с аммиаком на катализаторе.
| Например, при взаимодействии этанола с аммиаком образуется этиламин. |
2.3. Этерификация (образование сложных эфиров)
Одноатомные и многоатомные спирты вступают в реакции с карбоновыми кислотами, образуя сложные эфиры.
| Например, этанол реагирует с уксусной кислотой с образованием этилацетата (этилового эфира уксусной кислоты): |
2.4. Взаимодействие с кислотами-гидроксидами
Спирты взаимодействуют и с неорганическими кислотами, например, азотной или серной.
| Например, при взаимодействии этанола с азотной кислотой образуется сложный эфир этилнитрат : |
3. Реакции замещения группы ОН
В присутствии концентрированной серной кислоты от спиртов отщепляется вода. Процесс дегидратации протекает по двум возможным направлениям: внутримолекулярная дегидратация и межмолекулярная дегидратация.
3.1. Внутримолекулярная дегидратация
При высокой температуре (больше 140 о С) происходит внутримолекулярная дегидратация и образуется соответствующий алкен.
| Например, из этанола под действием концентрированной серной кислоты при температуре выше 140 градусов образуется этилен: |
В качестве катализатора этой реакции также используют оксид алюминия.
3.2. Межмолекулярная дегидратация
При низкой температуре (меньше 140 о С) происходит межмолекулярная дегидратация по механизму нуклеофильного замещения: ОН-группа в одной молекуле спирта замещается на группу OR другой молекулы. Продуктом реакции является простой эфир.
| Например, при дегидратации этанола при температуре до 140 о С образуется диэтиловый эфир: |
4. Окисление этанола
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
В зависимости от интенсивности и условий окисление можно условно разделить на каталитическое, мягкое и жесткое.
| При окислении первичных спиртов они последовательно превращаются сначала в альдегиды, а потом в карбоновые кислоты. Глубина окисления зависит от окислителя. Первичный спирт → альдегид → карбоновая кислота |
Типичные окислители — оксид меди (II), перманганат калия KMnO4, K2Cr2O7, кислород в присутствии катализатора.
4.1. Окисление оксидом меди (II)
Cпирты можно окислить оксидом меди (II) при нагревании. При этом медь восстанавливается до простого вещества.
| Например, этанол окисляется оксидом меди до уксусного альдегида |
4.2. Окисление кислородом в присутствии катализатора
Cпирты можно окислить кислородом в присутствии катализатора (медь, оксид хрома (III) и др.).
4.3. Жесткое окисление
При жестком окислении под действием перманганатов или соединений хрома (VI) первичные спирты окисляются до карбоновых кислот.
| Например, при взаимодействии этанола с перманганатом калия в серной кислоте образуется уксусная кислота |
4.4. Горение спиртов
Образуются углекислый газ и вода и выделяется большое количество теплоты.
| Например, уравнение сгорания этанола: |
5. Дегидрирование этанола
При нагревании спиртов в присутствии медного катализатора протекает реакция дегидрирования.
| Например, при дегидрировании этанола образуется этаналь |
Получение этанола
1. Щелочной гидролиз галогеналканов
При взаимодействии галогеналканов с водным раствором щелочей образуются спирты. Атом галогена в галогеналкане замещается на гидроксогруппу.
| Например, при нагревании хлорэтана с водным раствором гидроксида натрия образуется этанол |
2. Гидратация алкенов
Гидратация (присоединение воды) алкенов протекает в присутствии минеральных кислот. При присоединении воды к алкенам образуются спирты.
| Например, при взаимодействии этилена с водой образуется этиловый спирт. |
3. Гидрирование карбонильных соединений
Присоединение водорода к альдегидам и кетонам протекает при нагревании в присутствии катализатора. При гидрировании альдегидов образуются первичные спирты, при гидрировании кетонов — вторичные спирты, а из формальдегида образуется метанол.
| Например, при гидрировании этаналя образуется этанол |
4. Получение этанола спиртовым брожением глюкозы
Для глюкозы характерно ферментативное брожение, то есть распад молекул на части под действием ферментов. Один из вариантов — спиртовое брожение.
Уравнение реакций этанола на этаналь
Он хорошо растворим в воде, спирте и эфире.
Рис. 1. Строение молекулы этаналя.
Таблица 1. Физические свойства этаналя.
Плотность (0 o С), г/см 3
Температура плавления, o С
Температура кипения, o С
Получение этаналя
Наиболее популярным способом получения этаналя является окисление этанола:
Кроме этого используются и другие реакции:
- пиролиз кальциевый (бариевых) солей карбоновых кислот:
- гидратация ацетилена и его гомологов (реакция Кучерова)
- каталитическое окисление ацетилена
Химические свойства этаналя
Типичные реакции, характерные для этаналя – реакции нуклеофильного присоединения. Все они протекают преимущественно с расщеплением:
- p-связи в карбонильной группе
— присоединение синильной кислоты
— присоединение гидросульфита натрия
- связи С-Н в карбонильной группе
— окисление аммиачным раствором оксида серебра (реакция «серебряного зеркала») – качественная реакция
— окисление гидроксидом меди (II)
Применение этаналя
Этаналь используется в основном для производства уксусной кислоты и в качестве исходного сырья для синтеза многих органических соединений. Кроме этого этаналь и его производные идут на изготовление некоторых лекарств.
Примеры решения задач
| Задание | Эквимолекулярная смесь ацетилена и этаналя полностью реагирует с 69,6 г Ag2O, растворенного в аммиаке. Определите состав исходной смеси. |
| Решение | Запишем уравнения реакций, указанных в условии задачи: |
Рассчитаем количество вещества оксида серебра (I):
n(Ag2O) = 69,6 / 232 = 2,6 моль.
По уравнению (2) количество вещества этаналя будет равно 0,15 моль. По условию задачи смесь эквимолекулярна, следовательно, ацетилена тоже будет 0,15 моль.
Найдем массы веществ, составляющих смесь:
M(HC≡CH) = 26 г/моль;
m(HC≡CH) = 0,15× 26 = 3,9 г;
| Задание | При каталитическом гидрировании 55 г этаналя образовалась карбоновая кислота. Рассчитайте какая масса кислоты была получена. |
| Решение | Запишем уравнение реакции каталитического окисления этаналя: |
Вычислим количество вещества этаналя (молярная масса равна 44 г/моль):
n(CH3-C(O)H) = 55 / 44 = 1,25 моль.
Согласно уравнению реакции n(CH3-C(O)H) : n(CH3-COOH) = 1:1, т.е.
Тогда масса уксусной кислоты будет равна (молярная масса – 60 г/моль):
6. Взаимодействие этанола с натрием является
А эндотермических реакцией В реакцией присоединения
Б реакцией замещения Г оборотной реакцией
7. Глицерол есть
А ненасыщенным трехатомных спиртом
Б насыщенным одноатомного спиртом
В одним из продуктов гидролиза тристеарин
Г одним из продуктов гидролиза метилетаноату
8. Глицерол отличается от этанола тем, что
А реагирует с натрием В вступает в реакцию полного окисления
Б реагирует с меди (II) гидроксидом Г вступает в реакции этерификации
9. Фенол отличается от метанола тем, что
А легко окисляется на воздухе В не имеет характерного запаха Б не реагирует с щелочными металлами Г является сильной кислотой
10. Метановая кислота отличается от етановои тем, что
А вступает в реакцию «серебряного зеркала»
Б не реагирует с магнием
В не имеет характерного запаха
Г образует белый осадок под действием бромной воды
11. Зпомиж веществ, формулы которых приведены, укажите ту, в которой кислотные свойства выражены сильнее.
А СН3СООН Б НСООН В С6Н5ОН Г Н2СО3
12. Зпомиж веществ, формулы которых приведены, укажите ту, в которой кислотные свойства
выражены слабое.
А СН3СООН Б НСООН В С6Н5ОН Г Н2СО3
13. Метилетаноат изомерный
А пропаналя В пропан1,2диолу
Б пропан2олу Г пропан кислоте
14. Проанализируйте утверждение.
И. Одним из продуктов щелочного гидролиза тристеарин есть мыло.
ИИ. Одним из продуктов щелочного гидролиза тристеарин является глицерин. Определите, есть ли между ними правильные.
А верно лишь И В оба правильные Б верно лишь ИИ Г нет правильных
15. Конечным продуктом гидролиза крахмала является
А фруктоза Б глюкоза В декстрин Г сахароза
16. Проанализируйте утверждение.
И. Жиры по своей природе эфирами.
ИИ. Одним из продуктов гидролиза любого эфира является глицерин. Определите, есть ли между ними правильные.
А верно лишь И Б верно лишь ИИ В оба правильные Г нет правильных
17. Проанализируйте утверждение.
И. Одним из продуктов щелочного гидролиза тристеарин есть маргарин.
ИИ. Одним из продуктов щелочного гидролиза тристеарин является стеариновая кислота. Определите, есть ли между ними правильные.
А верно лишь И Б верно лишь ИИ В оба правильные Г нет правильных
18. Проанализируйте утверждение.
И. Сок спелого яблока от сока незрелого можно отличить, используя аммоний ачний раствор аргентум (И) оксида.
ИИ. Сок спелого яблока от сока незрелого можно отличить, используя водно спиртовой раствор йода.
Определите, есть ли между ними правильные.
А верно лишь И В оба правильные
Б верно лишь ИИ Г нет правильных
19. Молекулярная формула насыщенного одноатомного спирта — это
А С3Н8О2 Б С5Н12 В С2Н4О2 Г С3Н4О
20. Укажите вещество, в молекуле которого нет карбонильной группы.
А метановая кислота Б формальдегид В етанова кислота Г этаналь
21. Укажите вещество, которое восстанавливает серебро аммиачные раствора аргентум (И) оксида.
А сахароза Б этанол В крахмал Г этаналь
22. Сколько из среды приведенных веществ — метановая кислота, водород, магний, меди (II)
гидроксид — реагирует с этаналя?
А1Б2В3Г4
23. Водородные связи не образуются между молекулами
А воды Б этанола В глицерина Г этаналя
24. моносахаридов является
А глюкоза Б сахароза В крахмал Г целлюлоза
25. Для скольких веществ из среды приведенных — крахмал, сахароза, глюкоза, целлюлоза — возможная реакция гидролиза?
А1Б2В3Г4
26. Для скольких веществ из среды приведенных — триолеин, тристеарин, етилетаноат, фи
нол — возможная реакция гидролиза?
А1Б2В3Г4
27. Для скольких веществ из среды приведенных — этаналь, триолеин, тристеарин, пропа
наль — возможная реакция гидрирования?
А1Б2В3Г4
28. Для скольких веществ из среды приведенных — фенол, триолеин, тристеарин, этанол —
возможна реакция со щелочью?
А1Б2В3Г4
29. Для скольких веществ из среды приведенных — фенол, триолеин, тристеарин, сахароза — возможна реакция с бромной водой?
А1 Б2 В3 Г4
30. Сколько веществ из среды приведенных — фенол, крахмал, глицерин, целлюлоза — под
действием водноспиртового раствора йода приобретают синего цвета? А1 Б2 В3 Г4
Как из этанола получить этаналь?! (напишите наблюдение и реакцию)
- Попроси больше объяснений
- Следить
- Отметить нарушение
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. источники: http://piteika.com/zavisimosti/vzaimodejstvie-jetanalja-s-jetanolom.html http://acetyl.ru/o/a21i.php |