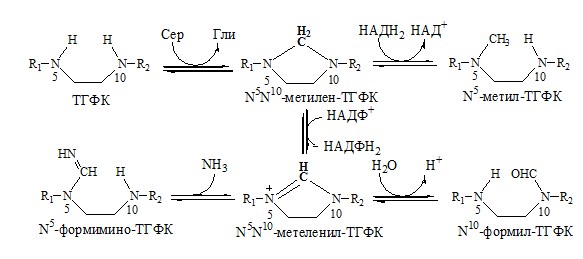
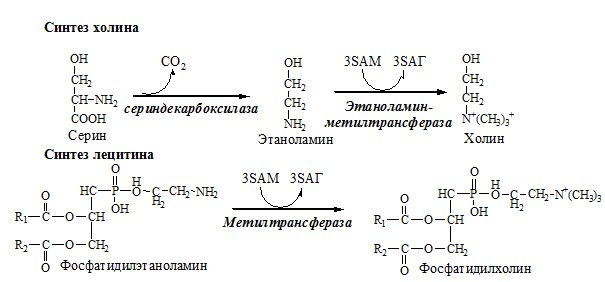
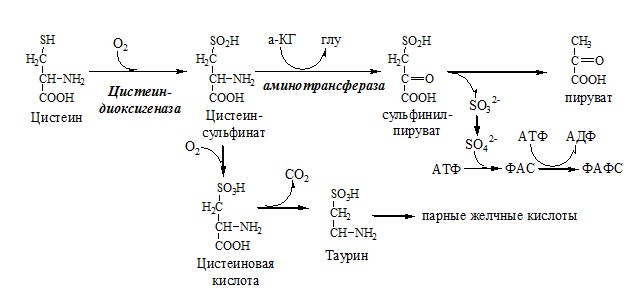
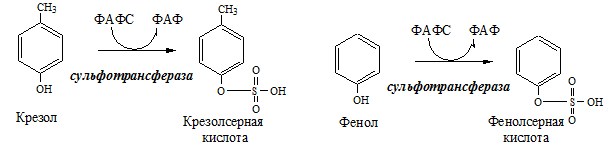
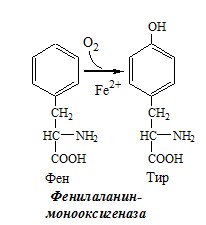
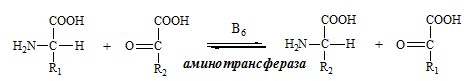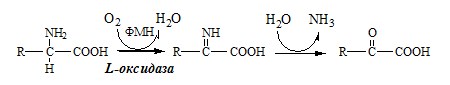БИОХИМИЯ УЧЕБНИК ДЛЯ ВУЗОВ — Е. С. Северина — 2004
РАЗДЕЛ 9. ОБМЕН И ФУНКЦИИ АМИНОКИСЛОТ
V. Обмен аммиака
А. Источники аммиака в клетках
Катаболизм аминокислот в тканях происходит постоянно со скоростью -100 г/сут. При этом в результате дезаминирования аминокислот освобождается большое количество аммиака. Значительно меньшие количества его образуются при дезаминировании биогенных аминов и нуклеотидов. Основные источники аммиака в клетках представлены в табл. 9-3.
Таблица 9-3. Основные источники аммиака
Непрямое дезаминирование (основной путь дезаминирования аминокислот)
Окислительное дезаминирование глутамата
Неокислительное дезаминирование Гис, Сер, Тре
Окислительное дезаминирование аминокислот (малозначимый путь дезаминирования)
Оксидаза L-аминокислот, FМN
Окислительное дезаминирование (путь инактивации биогенных аминов)
Интенсивно работающая мышца
Часть аммиака образуется в кишечнике в результате действия бактерий на пищевые белки (гниение белков в кишечнике) и поступает в кровь воротной вены. Концентрация аммиака в крови воротной вены существенно больше, чем в общем кровотоке. В печени задерживается большое количество аммиака, что поддерживает низкое содержание его в крови. Концентрация аммиака в крови в норме редко превышает 0,4 — 0,7 мг/л (или 25 — 40 мкмоль/л). В крови и цитозоле клеток при физиологических значениях pH аммиак переходит в ион аммония — NН4 + , количество неионизированного NН3 невелико (
Аммиак — токсичное соединение. Даже небольшое повышение его концентрации оказывает неблагоприятное действие на организм, и прежде всего на ЦНС. Так, повышение концентрации аммиака в мозге до 0,6 ммоль вызывает судороги. К симптомам гипераммониемии относят тремор, нечленораздельную речь, тошноту, рвоту, головокружение, судорожные припадки, потерю сознания. В тяжёлых случаях развивается кома с летальным исходом.
Механизм токсического действия аммиака на мозг и организм в целом, очевидно, связан с действием его на несколько функциональных систем.
✵ Аммиак легко проникает через мембраны в клетки и в митохондриях сдвигает реакцию, катализируемую глутаматдегидрогеназой, в сторону образования глутамата:
α-Кетоглутарат + NADH + Н + + NН3 —> Глутамат + NAD + .
Уменьшение концентрации α-кетоглутарата вызывает: угнетение обмена аминокислот (реакции транса- минирования) и, следовательно, синтеза из них нейромедиаторов (ацетилхолина, дофамина и др.); гипоэнергетическое состояние в результате снижения скорости ЦТК.
Недостаточность α-кетоглутарата приводит к снижению концентрации метаболитов ЦТК, что вызывает ускорение реакции синтеза оксалоацетата из пирувата, сопровождающейся интенсивным потреблением СO2. Усиленное образование и потребление диоксида углерода при гипераммониемии особенно характерны для клеток головного мозга.
✵ Повышение концентрации аммиака в крови сдвигает pH в щелочную сторону (вызывает алкалоз). Это, в свою очередь, увеличивает сродство гемоглобина к кислороду, что приводит к гипоксии тканей, накоплению СO2 и гипоэнергетическому состоянию, от которого главным образом страдает головной мозг.
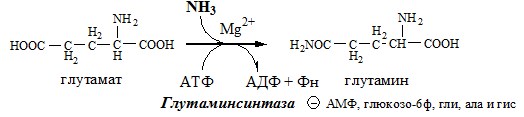
✵ Высокие концентрации аммиака стимулируют синтез глутамина из глутамата в нервной ткани (при участии глутаминсинтетазы):
Глутамат + NН3 + АТФ —> Глутамин + АДФ + Н3РO4.
Накопление глутамина в клетках нейроглии приводит к повышению осмотического давления в них, набуханию астроцитов и в больших концентрациях может вызвать отёк мозга. Снижение концентрации глутамата нарушает обмен аминокислот и нейромедиаторов, в частности синтез y-аминомасляной кислоты (ГАМК), основного тормозного медиатора. При недостатке ГАМК и других медиаторов нарушается проведение нервного импульса, возникают судороги.
✵ Ион NН4 + практически не проникает через цитоплазматические и митохондриальные мембраны. Избыток иона аммония в крови способен нарушать трансмембранный перенос одновалентных катионов Na + и К + , конкурируя с ними за ионные каналы, что также влияет на проведение нервных импульсов.
Б. Связывание (обезжиривание) аммиака
Высокая интенсивность процессов дезаминирования аминокислот в тканях и очень низкий уровень аммиака в крови свидетельствуют о том, что в клетках активно происходит связывание аммиака с образованием нетоксичных соединений, которые выводятся из организма с мочой. Эти реакции можно считать реакциями обезвреживания аммиака. В разных тканях и органах обнаружено несколько типов таких реакций.
Основной реакцией связывания аммиака, протекающей во всех тканях организма, является синтез глутамина под действием глутамин- синтетазы:
Глутаминсинтетаза локализована в митохондриях клеток, для работы фермента необходим кофактор — ионы Мg 2+ . Глутаминсинтетаза — один из основных регуляторных ферментов обмена аминокислот и аллостерически ингибируется АМФ, глюкозо-6-фосфатом, а также Гли, Ала и Гис.
Глутамин легко транспортируется через клеточные мембраны путём облегчённой диффузии (для глутамата возможен только активный транспорт) и поступает из тканей в кровь. Основными тканями-поставщиками глутамина служат мышцы, мозг и печень. С током крови глутамин транспортируется в кишечник и почки.
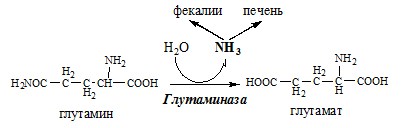
В клетках кишечника под действием фермента глутаминазы происходит гидролитическое освобождение амидного азота в виде аммиака:
Образовавшийся в реакции глутамат подвергается трансаминированию с пируватом. α-Аминогруппа глутаминовой кислоты переносится в состав аланина (рис. 9-10). Большие количества аланина поступают из кишечника в кровь воротной вены и поглощаются печенью. Около 5% образовавшегося аммиака удаляется в составе фекалий, небольшая часть через воротную вену попадает в печень, остальные
90% выводятся почками.
Рис. 9-10. Метаболизм азота глутамина в кишечнике.
В почках также происходит гидролиз глутамина под действием глутаминазы с образованием аммиака. Этот процесс является одним из механизмов регуляции кислотно-щелочного равновесия в организме и сохранения важнейших катионов для поддержания осмотического давления. Глутаминаза почек значительно индуцируется при ацидозе, образующийся аммиак нейтрализует кислые продукты обмена и в виде аммонийных солей экскретируется с мочой (рис. 9-11). Эта реакция защищает организм от излишней потери ионов Na + и К + , которые также могут использоваться для выведения анионов и утрачиваться. При алкалозе количество глутаминазы в почках снижается.
Рис. 9-11. Метаболизм амидного азота глутамина в почках.
В почках образуется и выводится около 0,5 г солей аммония в сутки.
Высокий уровень глутамина в крови и лёгкость его поступления в клетки обусловливают использование глутамина во многих анаболических процессах. Глутамин —основной донор азота в организме. Амидный азот глутамина используется для синтеза пуриновых и пиримидиновых нуклеотидов, аспарагина, аминосахаров и других соединений (рис. 9-12).
Рис. 9-12. Пути использования глутамина в организме.
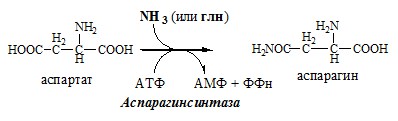
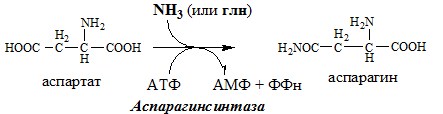
Ещё одной реакцией обезвреживания аммиака в тканях можно считать синтез аспарагина под действием аспарагинсинтетазы.
Существуют 2 изоформы этого фермента — глутаминзависимая и аммиакзависимая, которые используют разные доноры амидных групп. Первая функционирует в животных клетках, вторая преобладает в бактериальных клетках, но присутствует и у животных. Однако такой путь обезвреживания аммиака в клетках человека используется редко и к тому же требует больших энергетических затрат (энергию двух макроэргических связей), чем синтез глутамина.
Наиболее значительные количества аммиака обезвреживаются в печени путём синтеза мочевины. В первой реакции процесса аммиак связывается с диоксидом углерода с образованием карбамоилфосфата, при этом затрачиваются 2 молекулы АТФ. Реакция происходит в митохондриях гепатоцитов под действием фермента карбамоилфосфатсинтетазы I. Карбамоилфосфатсинтетаза II локализована в цитозоле клеток всех тканей и участвует в синтезе пиримидиновых нуклеотидов (см. раздел 10). Карбамоилфосфат затем включается в орнитиновый цикл и используется для синтеза мочевины.
В мозге и некоторых других органах может протекать восстановительное аминирование α-кетоглутарата под действием глутаматдегидрогеназы, катализирующей обратимую реакцию. Однако этот путь обезвреживания аммиака в тканях используется слабо, так как глутаматдегидрогеназа катализирует преимущественно реакцию дезаминирования глутамата. Хотя, если учитывать последующее образование глутамина, реакция выгодна для клеток, так как способствует связыванию сразу 2 молекул NH3.
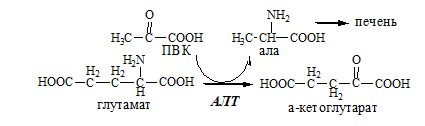
Из мышц и кишечника избыток аммиака выводится преимущественно в виде аланина. Этот механизм необходим, так как активность глутаматдегидрогеназы в мышцах невелика и непрямое дезаминирование аминокислот малоэффективно. Поэтому в мышцах существует ещё один путь выведения азота. Образование аланина в этих органах можно представить следующей схемой (см. схему ниже).
Аминогруппы разных аминокислот посредством реакций трансаминирования переносятся на пируват, основным источником которого служит процесс окисления глюкозы.
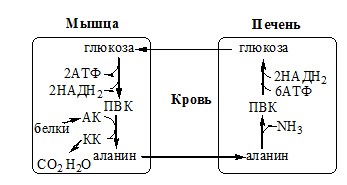
Мышцы выделяют особенно много аланина в силу их большой массы, активного потребления глюкозы при физической работе, а также потому, что часть энергии они получают за счёт распада аминокислот. Образовавшийся аланин поступает в печень, где подвергается непрямому дезаминированию. Выделившийся аммиак обезвреживается, а пируват включается в глюконеогенез. Глюкоза из печени поступает в ткани и там, в процессе гликолиза, опять окисляется до пирувата (рис. 9-13).
Образование аланина в мышцах, его перенос в печень и перенос глюкозы, синтезированной в печени, обратно в мышцы составляют глюкозо- аланиновый цикл, работа которого сопряжена с работой глюкозо-лактатного цикла (см. раздел 7).
Рис. 9-13. Глюкозо-аланиновый цикл.
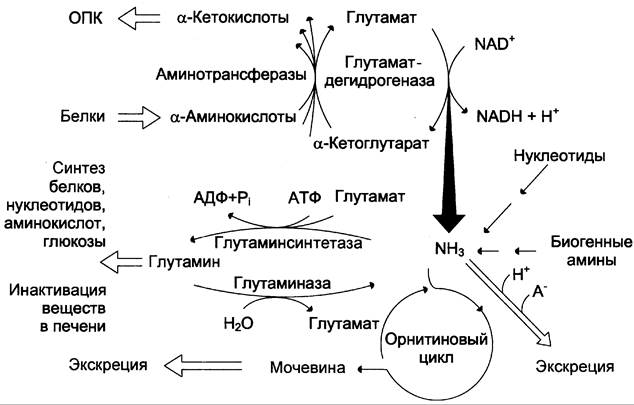
Совокупность основных процессов обмена аммиака в организме представлена на рис. 9-14. Доминирующими ферментами в обмене аммиака служат глутаматдегидрогеназа и глутаминсинтетаза.
Рис. 9-14. Обмен аммиака. Основной источник аммиака — аминокислоты. Большая часть образовавшегося аммиака обезвреживается в орнитиновом цикле в печени и выделяется в виде мочевины. Основной реакцией обезвреживания аммиака в тканях является синтез глутамина, который затем используется в анаболических процессах и для обезвреживания веществ в печени. Ферменты глутаматдегидрогеназа и глутаминсинтетаза являются регуляторными и обусловливают скорость процессов образования и обезвреживания аммиака.
В. Орнитиновый цикл
Мочевина — основной конечный продукт азотистого обмена, в составе которого из организма выделяется до 90% всего выводимого азота (рис. 9-15). Экскреция мочевины в норме составляет
Рис. 9-15. Количество азотсодержащих веществ в моче (%) при нормальном белковом питании.
При повышении количества потребляемых с пищей белков экскреция мочевины увеличивается. Мочевина синтезируется только в печени, что было установлено ещё в опытах И. П. Павлова. Поражение печени и нарушение синтеза мочевины приводят к повышению содержания в крови и тканях аммиака и аминокислот (в первую очередь, глутамина и аланина).
В 40-х годах XX века немецкие биохимики Г. Кребс и К. Гензелейт установили, что синтез мочевины представляет собой циклический процесс, состоящий из нескольких стадий, ключевым соединением которого, замыкающим цикл, является орнитин. Поэтому процесс синтеза мочевины получил название «орнитиновый цикл», или «цикл Кребса—Гензелейта».
1. Реакции синтеза мочевины
Мочевина (карбамид) — полный амид угольной кислоты — содержит 2 атома азота.
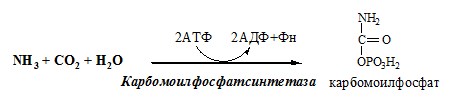
Источником одного из них является аммиак, который в печени связывается с диоксидом углерода с образованием карбамоилфосфата под действием карбамоилфосфатсинтетазы I (см. схему А).
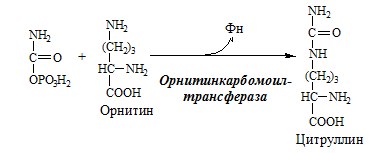
Далее под действием орнитин-карбамоил- трансферазы карбамоильная группа карбамоилфосфата переносится на α-аминокислоту орнитин, и образуется другая α-аминокислота — цитруллин (см. схему Б).
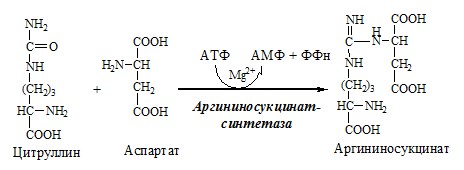
В следующей реакции аргининосукцинатсин- тетаза связывает цитруллин с аспартатом и образует аргининосукцинат (аргининоянтарную кислоту). Этот фермент нуждается в ионах Мg 2+ . В реакции затрачивается 1 моль АТФ, но используется энергия двух макроэргических связей. Аспартат — источник второго атома азота мочевины (см. схему А).
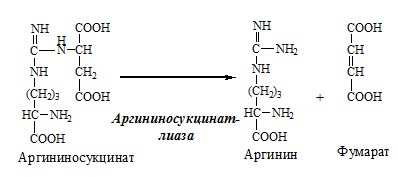
Далее фермент аргининосукцинатлиаза (аргининосукциназа) расщепляет аргининосукцинат на аргинин и фумарат, при этом аминогруппа аспартата оказывается в молекуле аргинина (см. схему Б ниже).
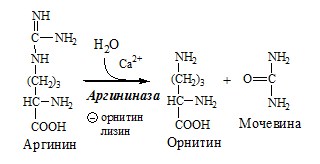
Аргинин подвергается гидролизу под действием аргиназы, при этом образуются орнитин и мочевина. Кофакторами аргиназы являются ионы Са 2+ или Мn 2+ . Высокие концентрации орнитина и лизина, являющихся структурными аналогами аргинина, подавляют активность этого фермента:
Образующийся орнитин взаимодействует с новой молекулой карбамоилфосфата, и цикл замыкается.
Первые две реакции процесса происходят в митохондриях гепатоцитов. Затем цитруллин, являющийся продуктом этих реакций, транспортируется в цитозоль, где и осуществляются дальнейшие превращения (рис. 9-16).
Рис. 9-16. Орнитиновый цикл Кребса-Гензелейта. Окислительное дезаминирование глутамата происходит в митохондриях. Ферменты орнитинового цикла распределены между митохондриями и цитозолем. Поэтому необходим трансмембранный перенос глутамата, цитруллина и орнитина с помощью специфических транслоказ. На схеме показаны пути включения азота двух разных аминокислот (аминокислота 1 и аминокислота 2) в молекулу мочевины: • одна аминогруппа — в виде аммиака в матриксе митохондрии; • вторую аминогруппу поставляет аспартат цитозоля.
Суммарное уравнение синтеза мочевины:
Аммиак, используемый карбамоилфосфатсинтетазой I, поставляется в печень с кровью воротной вены. Роль других источников, в том числе окислительного дезаминирования глутаминовой кислоты в печени, существенно меньше.
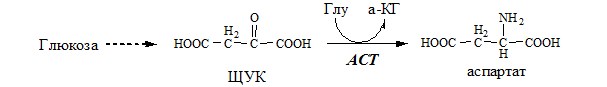
Аспартат, необходимый для синтеза аргининосукцината, образуется в печени путём транс-аминирования аланина с оксалоацетатом. Аланин поступает главным образом из мышц и клеток кишечника. Источником оксалоацетата, необходимого для этой реакции, можно считать превращение фумарата, образующегося в реакциях орнитинового цикла. Фумарат в результате двух реакций цитратного цикла превращается в оксалоацетат, из которого путём трансаминирования образуется аспартат (рис. 9-17). Таким образом, с орнитиновым циклом сопряжён цикл регенерации аспартата из фумарата. Пируват, образующийся в этом цикле из аланина, используется для глюконеогенеза.
Рис. 9-17. Цикл регенерации аспартата, сопряжённый с орнитиновым циклом.
Ещё одним источником аспартата для орнитинового цикла является трансаминирование глутамата с оксалоацетатом.
2. Энергетический баланс процесса
В реакциях орнитинового цикла расходуются четыре макроэргических связи трёх молекул АТФ на каждый оборот цикла. Однако процесс превращения аминокислот в безазотистые остатки и мочевину имеет пути компенсации энергозатрат:
✵ при включении фумарата в ЦТК на стадии дегидрирования малата образуется NАDН, который обеспечивает синтез 3 молекул АТФ (рис. 9-18);
✵ при окислительном дезаминировании глутамата в разных органах также образуется NАDН, соответственно — ещё 3 молекулы АТФ.
Затраты энергии происходят также и при трансмембранном переносе веществ, связанном с синтезом и экскрецией мочевины (рис. 9-18). Первые две реакции орнитинового цикла происходят в митохондриях, а последующие три — в цитозоле. Цитруллин, образующийся в митохондрии, должен быть перенесён в цитозоль, а орнитин, образующийся в цитозоле, необходимо транспортировать в митохондрию. Кроме того, в почках перенос мочевины из крови в мочу происходит путём активного транспорта за счёт градиента ионов натрия, создаваемого К + , Na + -АТФ-азой, что тоже сопряжено с энергозатратами.
Рис. 9-18. Взаимосвязь орнитинового цикла и общего пути катаболизма. Фумарат, образующийся в результате расщепления аргининосукцината, превращается в малат, который затем переносится в митохондрии, включается в ЦТК и дегидрируется с образованием оксалоацетата. Эта реакция сопровождается выделением 3 молекул АТФ, которые и компенсируют затраты энергии на синтез одной молекулы мочевины.
Полный набор ферментов орнитинового цикла есть только в гепатоцитах. Отдельные же ферменты орнитинового цикла обнаруживаются не только в печени, но и в других клетках. В энтероцитах, например, имеется карбамоилфосфат- синтетаза I и орнитинкарбамоилтрансфераза, следовательно, может синтезироваться цитрул
лин. В почках обнаружены аргининосукцинат- синтетаза и аргининосукцинатлиаза. Цитруллин, образовавшийся в энтероцитах, может поступать в почки и превращаться там в аргинин, который переносится в печень и гидролизуется аргиназой. Активность этих рассеянных по разным органам ферментов значительно ниже, чем в печени.
3. Биологическая роль орнитинового цикла Кребса—Гензелейта
Орнитиновый цикл в печени выполняет 2 функции:
✵ превращение азота аминокислот в мочевину, которая экскретируется и предотвращает накопление токсичных продуктов, главным образом аммиака;
✵ синтез аргинина и пополнение его фонда в организме.
Регуляторные стадии процесса — синтез карбамоилфосфата, синтез цитруллина и заключительная стадия, катализируемая аргиназой. Эффективность работы орнитинового цикла при нормальном питании человека и умеренных физических нагрузках составляет примерно 60% его мощности. Запас мощности необходим для избежания гипераммониемии при изменениях количества белка в пище. Увеличение скорости синтеза мочевины происходит при длительной физической работе или длительном голодании, которое сопровождается распадом тканевых белков. Некоторые патологические состояния, характеризующиеся интенсивным распадом белков тканей (сахарный диабет и др.), также сопровождаются активацией орнитинового цикла.
При избыточном белковом питании количество ферментов орнитинового цикла в печени увеличивается, что приводит к интенсификации синтеза мочевины.
Нарушение реакций обезвреживания аммиака может вызвать повышение содержания аммиака в крови — гипераммониемию, что оказывает токсическое действие на организм. Причинами гипераммониемии могут выступать как генетический дефект ферментов орнитинового цикла в печени, так и вторичное поражение печени в результате цирроза, гепатита и других заболеваний. Известны пять наследственных заболеваний, обусловленных дефектом пяти ферментов орнитинового цйкла (табл. 9-4).
Таблица 9-4. Наследственные нарушения орнитинового цикла и основные их проявления
Гипераммониемия, тип I
Карбамоил- фосфат- синтетаза I
В течение 24-48 ч после рождения кома, смерть
Гипераммониемия, тип II
Сцепленный с Х-хромосомой
Гипотония, снижение толерантности к белкам
Гипераммониемия тяжёлая у новорождённых.
У взрослых — после белковой нагрузки
Гипераммониемия, атаксия, судороги, выпадение волос
Аргининосукцинат, Глн, Ала, Лиз
В литературе описаны случаи всех этих довольно редких энзимопатий, среди которых отмечено больше всего случаев гипераммониемии II типа.
Нарушение орнитинового цикла наблюдается при гепатитах различной этиологии и некоторых других вирусных заболеваниях. Например, установлено, что вирусы гриппа и других острых респираторных вирусных инфекций снижают активность карбамоилфосфатсинтетазы I. При циррозе и других заболеваниях печени также часто наблюдают гипераммониемию.
Снижение активности какого-либо фермента синтеза мочевины приводит к накоплению в крови субстрата данного фермента и его предшественников. Так, при дефекте аргининосукцинатсинтетазы повышается содержание цитруллина (цитруллинемия); при дефекте аргиназы — концентрация аргинина, аргининосукцината, цитруллина и т. д. При гипераммониемиях I и II типа вследствие дефекта орнитинкарбамоилтрансферазы происходит накопление карбамоилфосфата в митохондриях и выход его в цитозоль. Это вызывает увеличение скорости синтеза пиримидиновых нуклеотидов (вследствие активации карбамоилфосфатсинтетазы II), что приводит к накоплению оротата, уридина и урацила и выведению их с мочой. Содержание всех метаболитов повышается, и состояние больных ухудшается при увеличении количества белков в пище. Тяжесть течения заболевания зависит также от степени снижения активности ферментов.
Все нарушения орнитинового цикла приводят к значительному повышению в крови концентрации аммиака, глутамина и аланина.
Гипераммониемия сопровождается появлением следующих симптомов:
✵ тошнота, повторяющаяся рвота;
✵ потеря сознания, отёк мозга (в тяжёлых случаях);
✵ отставание умственного развития (при хронической врождённой форме).
Все симптомы гипераммониемии — проявление действия аммиака на ЦНС (см. выше подраздел IV, Б).
Для диагностики различных типов гипераммониемии производят определение содержания аммиака в крови, метаболитов орнитинового цикла в крови и моче, активности фермента в биоптатах печени.
Основной диагностический признак — повышение концентрации аммиака в крови. Содержание аммиака в крови может достигать 6000 мкмоль/л (в норме — 60 мкмоль/л). Однако в большинстве хронических случаев уровень аммиака может повышаться только после белковой нагрузки или в течение острых осложнённых заболеваний.
Лечение больных с различными дефектами орнитинового цикла в основном направлено на снижение концентрации аммиака в крови за счёт малобелковой диеты, введения кетоаналогов аминокислот в рацион и стимуляцию выведения аммиака в обход нарушенных реакций:
✵ путём связывания и выведения NН3 в составе фенилацетилглутамина и гиппуровой кислоты;
✵ повышением концентрации промежуточных метаболитов цикла (аргинина, цитруллина, глутамата), образующихся вне блокируемых реакций (рис. 9-19).
Рис. 9-19. Пути выведения аммиака при включении в диету глутамата и фенилацетата (А), бензоата (Б), цитруллина и аргинина (В). На рисунке обозначены ферментные блоки: 1 — дефект карбамоилфосфатсинтетазы I; 2 — дефект орнитинкарбамоилтрансферазы; 3 — дефект аргининосукцинатлиазы.
Вводимый больным с дефектом карбамоил- фосфатсинтетазы I в качестве пищевой добавки фенилацетат в результате его конъюгации с глутамином образует фенилацетилглутамин, который экскретируется почками. Состояние больных при этом улучшается, так как происходит активация синтеза глутамина и снижение концентрации аммиака в крови (рис. 9-19, А).
Аналогичное действие оказывает введение бензоата, который связывает молекулу глицина. Образующаяся гиппуровая кислота выводится с мочой (рис. 9-19, Б). В составе гиппурата происходит выделение азота из организма. Недостаток глицина компенсируется либо путём синтеза его из серина, либо за счёт образования из NH3 и СO2 в реакции, катализируемой глицинсинтетазой. При этом образование глицина сопровождается связыванием одной молекулы аммиака.
При гипераммониемии II типа (дефект орнитинкарбамоилтрансферазы) введение больших доз цитруллина стимулирует синтез мочевины из аспартата (рис. 9-19, В), что также приводит к выведению азота из организма. Введение больших доз аргинина при аргининосукцинатурии (дефект аргининосукцинатлиазы) стимулирует регенерацию орнитина и выведение азота в составе цитруллина и аргининосукцината.
Г. Обмен аммиака и аминокислот между органами и тканями
В катаболизме аминокислот и образовании аммиака участвуют многие ткани. В клетках происходит связывание аммиака. Из организма азот выводится почками в виде двух конечных продуктов азотистого обмена — аммонийных солей (
0,5 г/сут), которые образуются в почках, и мочевины (
25 г/сут), которая содержит до 90% выводимого азота. Синтез мочевины происходит в печени в орнитиновом цикле, причём на образование 1 моля мочевины используется 1 моль аммиака и 1 моль аспарагиновой кислоты. Таким образом, для синтеза 25 г мочевины в сутки затрачивается 6,3 г аммиака и 50 г аспартата. Для доставки азота в печень должны интенсивно функционировать специальные механизмы.
Транспорт азота из тканей в печень происходит, в основном, в составе 3 соединений: глутамина, аланина, аммиака (небольшое количество в несвязанном виде).
Кроме глутамина и аланина, в крови присутствуют и другие свободные аминокислоты, причём содержание их и направление транспорта зависят от приёма пищи и использования эндогенных белков. Наибольшее количество свободных аминокислот поступает из мышц и кишечника, причём до 50% составляют аланин и глутамин. Существует направленный поток аминокислот из этих тканей в печень, который усиливается в абсорбтивный период при белковом питании.
Основное количество глутамина поставляют в кровь мышцы и мозг. Из кровеносного русла его поглощают печень и почки, где он подвергается действию глутаминазы. Почки —основной источник серина и частично аланина, которые сорбируются из плазмы печенью. Головной мозг, в отличие от всех других тканей, способен поглощать и окислять большие количества аминокислот с разветвлённой боковой цепью (валин, лейцин, изолейцин).
После приёма пищи из кишечника в плазму крови поступает много аминокислот, причём преобладают аминокислоты с разветвлённой боковой цепью (до 20% от общего количества), которые затем поглощаются, в основном, печенью, мышцами и мозгом (рис. 9-20). В мышцах происходит усиленный катаболизм этих аминокислот, причём они выступают основными донорами аминогруппы в синтезе аланина из пирувата (см. выше «глюкозо-аланиновый цикл»).
Рис. 9-20. Обмен аминокислот между тканями и органами в абсорбтивном периоде. В абсорбтивный период основным источником свободных аминокислот служит кишечник. Большую часть поступивших аминокислот составляют гидрофобные аминокислоты с разветвлённой цепью. Экзогенные полярные аминокислоты из воротной вены сорбируются и используются в основном печенью. Разветвлённые аминокислоты поглощаются из кровотока клетками мозга или мышц.
В постабсорбтивном периоде основными источниками свободных аминокислот служат мышцы. Они поставляют в основном аланин и глутамин (рис. 9-21). Аланин поглощается печенью, глутамин — кишечником и почками. В кишечнике азот глутамина переносится в аланин или серин и в их составе транспортируется в печень, где активируется процесс глюконеогенеза. Интенсивность глюконеогенеза из этих аминокислот намного выше, чем из всех других. Таким образом, аланин и серин — основные гликогенные аминокислоты. Аминокислоты с разветвлённой боковой цепью (валин, лейцин, изолейцин и др.), которые освобождаются из мышц, направляются в мозг, где окисляются и служат важным источником энергии.
Рис. 9-21. Обмен аминокислот между тканями и органами в постабсорбтивном периоде. В постабсорбтивный период свободные аминокислоты поступают преимущественно из мышц, в которых усиливается катаболизм белков. Аминокислоты используются в глюконеогенезе в печени. В крови повышен уровень аланина, серина и глутамина.
Биологическая библиотека — материалы для студентов, учителей, учеников и их родителей.
Наш сайт не претендует на авторство размещенных материалов. Мы только конвертируем в удобный формат материалы, которые находятся в открытом доступе и присланные нашими посетителями.
Если вы являетесь обладателем авторского права на любой размещенный у нас материал и намерены удалить его или получить ссылки на место коммерческого размещения материалов, обратитесь для согласования к администратору сайта.
Разрешается копировать материалы с обязательной гипертекстовой ссылкой на сайт, будьте благодарными мы затратили много усилий чтобы привести информацию в удобный вид.
© 2018-2022 Все права на дизайн сайта принадлежат С.Є.А.
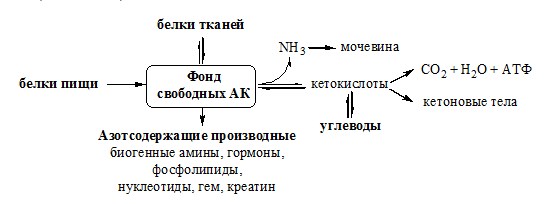
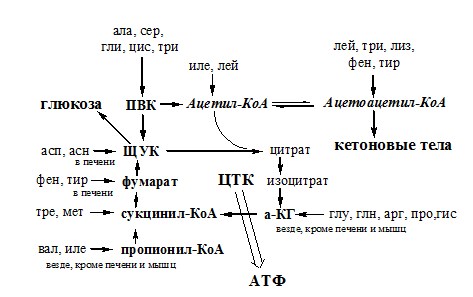
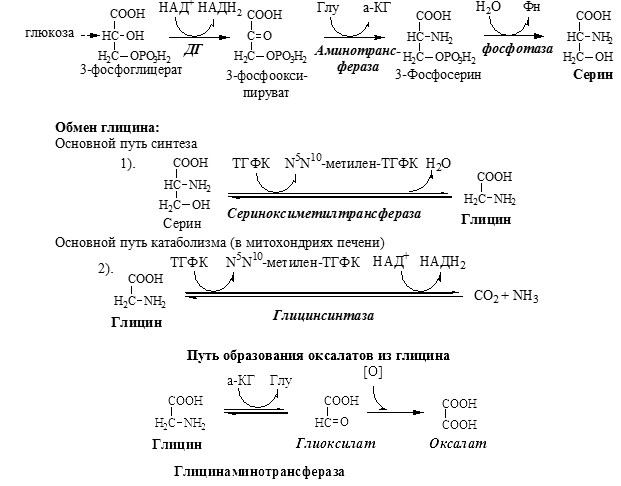
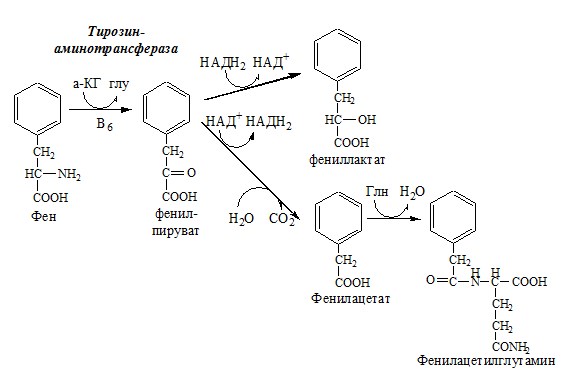
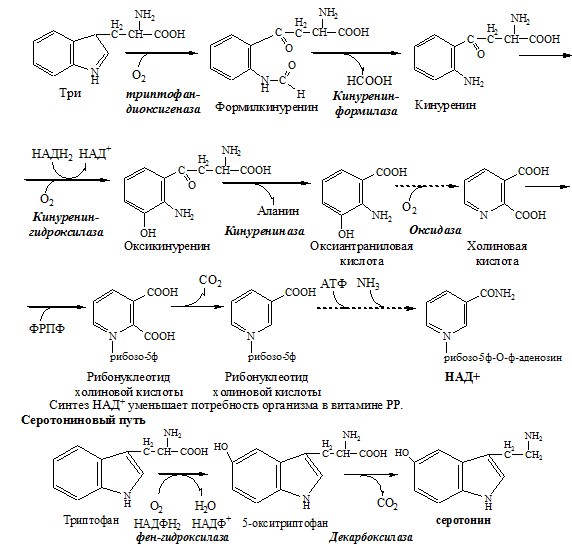
Общие пути распада аминокислот
Часть аминокислот подвергается распаду и превращается в конечные продукты: С02, Н20 и NH3.
Распад начинается с реакций, общих для большинства аминокислот. К ним относятся:
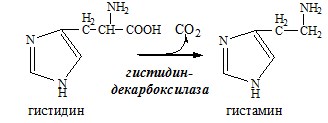
а) декарбоксилирование — отщепление от аминокислот карбоксильной группы в виде углекислого газа:
Это превращение аминокислот обычно протекает с очень низкой скоростью и аминов образуется мало. Но некоторые амины, находясь в очень низкой концентрации, обладают высокой биологической активностью и влияют на различные функции организма. Примером такого амина является гистамин, образующийся из аминокислоты гистидина.
б) дезаминирование — отщепление аминогруппы в виде NH3. У человека дезаминирование аминокислот идет окислительным путем:
Дезаминирование аминокислот также протекает с низкой скоростью. И только одна аминокислота – глутаминовая – дезаминируется с высокой скоростьювследствие наличияв организме активного фермента, вызывающего дезаминирование только этой аминокислоты.
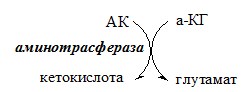
в) трансаминирование (переамииирование) — реакция между аминокислотами и а-кетокислотами. В ходе этой реакции ее участники обмениваются функциональными группами, в результате чего аминокислота превращается в а-кетокислоту, а кетокислота становится аминокислотой:
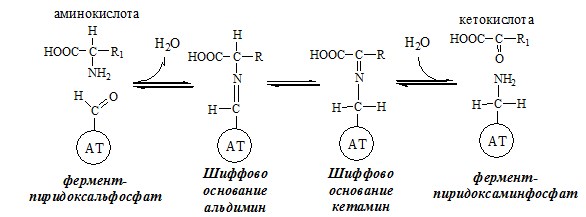
Трансаминированию подвергаются все аминокислоты. В этой реакции участвует кофермент — фосфопиридоксаль, для образования которого необходим витамин В6 — пиридоксин.
Трансаминирование — это главное превращение аминокислот в организме, так как его скорость значительно выше, чем у реакций декарбоксилирования и дезаминирования.
Трансаминирование выполняет две основные функции:
а) за счет трансаминирования одни аминокислоты могут превращаться в другие. При этом общее количество аминокислот не меняется, но изменяется соотношение между ними. С пищей в организм поступают чужеродные белки, у которых аминокислоты находятся в иных пропорциях по сравнению с белками организма. Путем трансаминирования происходит корректировка аминокислотного состава организма.
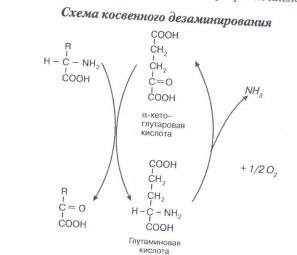
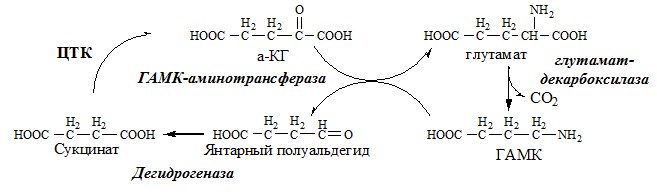
б) является составной частью косвенного (непрямого) дезаминирования аминокислот — процесса, с которого начинается распад большинства аминокислот. На первой стадии этого процесса аминокислоты вступают в реакцию трансаминирования с а-кетоглутаровой кислотой (а-кетокислота). Аминокислоты при этом превращаются в а- кетокислоты, а а-кетоглутаровая кислота переходит в глутаминовую кислоту (аминокислота). На второй стадии появившаяся глутаминовая кислота подвергается дезаминированию, от нее отщепляется NH3 и снова образуется а-кетоглутаровая кислота.
Итоговое уравнение косвенного дезаминирования совпадает с уравнением прямого дезаминирования. Однако у косвенного дезаминирования скорость значительно выше прямого, что обусловлено высокой активностью ферментов, катализирующих обе стадии этого процесса.
Отсюда следует, что реакцией, с которой начинается распад аминокислот, является трансаминирование.
Образовавшиеся а-кетокислоты далее подвергаются глубокому распаду и превращаются в конечные продукты С02 и Н20. Для каждой из 20 кетокислот (их образуется столько же, сколько имеется видов аминокислот) имеются свои специфические пути распада. Однако при распаде некоторых аминокислот в качестве промежуточного продукта образуется пировиноградная кислота, из которой возможен синтез глюкозы. Поэтому аминокислоты, из которых возникают такие кетокислоты, получили название глюкогенные. Другие же кетокислоты при своем распаде не образуют пирувата. Промежуточным продуктом у них является ацетилкофермент А, из которого невозможно получить глюкозу, но зато могут синтезироваться кетоновые тела. Аминокислоты, соответствующие таким кетокислотам, называются кетогенные.
Второй продукт косвенного дезаминирования аминокислот — аммиак. Для организма аммиак является высокотоксичным. Поэтому в организме имеются молекулярные механизмы его обезвреживания.
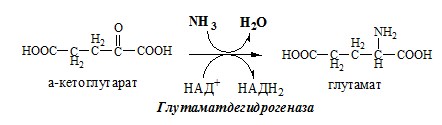
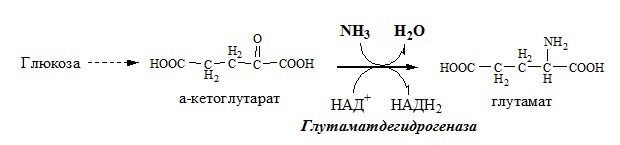
Вопрос49. Обезвреживание аммиака. синтез глутаминовой кислоты (восстановительное аминирование) – взаимодействие α-кетоглутарата с аммиаком. Реакция по сути обратна реакции окислительного дезаминирования, однако в качестве кофермента используется НАДФН. Происходит практически во всех тканях, кроме мышечной, но имеет небольшое значение, т.к. для глутаматдегидрогеназы предпочтительным субстратом является глутаминовая кислота и равновесие реакции сдвинуто в сторону α-кетоглутарата,
Реакция синтеза глутаминовой кислоты
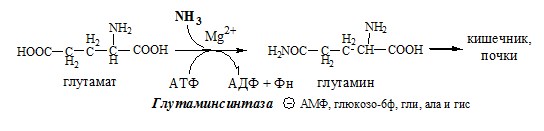
синтез глутамина – взаимодействие глутамата с аммиаком. Является главным способом уборки аммиака, наиболее активно происходит в нервной и мышечной тканях, в почках, сетчатке глаза, печени. Реакция протекает в митохондриях.
Реакция синтеза глутамина
Образование большого количества глутамина обеспечивает высокие концентрации его в крови (0,5-0,7 ммоль/л).
Так как глутамин проникает через клеточные мембраны путем облегченной диффузии, то он легко попадает не только в гепатоциты, но и в другие клетки, где есть потребность в аминогруппах. Азот, переносимый глутамином, используется клетками для синтеза пуринового и пиримидинового колец, гуанозинмонофосфата (ГМФ), аспарагина, глюкозамино-6-фосфата (предшественник всех остальных аминосахаров).
синтез аспарагина – взаимодействие аспартата с аммиаком. Является второстепенным способом уборки аммиака, энергетически невыгоден, т.к. при этом тратятся 2 макроэргические связи,
Реакция синтеза аспарагина
синтез карбамоилфосфата в митохондриях печени – реакция является первой в процессе синтеза мочевины, средства для удаления аммиака из организма.
Вопрос: 49 Обезвреживание аммиака.
Высокая интенсивность процессов дезаминирования аминокислот в тканях и очень низкий уровень аммиака в крови свидетельствуют о том, что в клетках активно происходит связывание аммиака с образованием нетоксичных соединений, которые выводятся из организма с мочой. Эти реакции можно считать реакциями обезвреживания аммиака. В разных тканях и органах обнаружено несколько типов таких реакций.
Основной реакцией связывания аммиака, протекающей во всех тканях организма, является
синтез глутамина под действием глутамин-синтетазы:
Глутаминсинтетаза локализована в митохондриях клеток, для работы фермента необходим кофактор — ионы Mg 2+ . Глутаминсинтетаза — один из основных регуляторных ферментов обмена аминокислот и аллостерически ингибируется АМФ, глюкозо-6-фосфатом, а также Гли, Ала и Гис.
Глутамин легко транспортируется через клеточные мембраны путём облегчённой диффузии (для глутамата возможен только активный транспорт) и поступает из тканей в кровь. Основными тканями-поставщикам:и глутамина служат мышцы, мозг и печень. С током крови глутамин транспортируется в кишечник и почки.
В клетках кишечникапод действием фермента глутаминазы происходит гидролитическое освобождение амидного азота в виде аммиака:
Образовавшийся в реакции глутамат подвергается трансаминированию с пируватом. ос-Аминогруппа глутаминовой кислоты переносится в состав аланина (рис. 9-10). Большие количества аланина поступают из кишечника в кровь воротной вены и поглощаются печенью. Около 5% образовавшегося аммиака удаляется в составе фекалий, небольшая часть через воротную вену попадает в печень, остальные
90% выводятся почками.
Рис. 9-10. Метаболизм азота глутамина в кишечнике.
В почкахтакже происходит гидролиз глутамина под действием глутаминазы с образованием аммиака. Этот процесс является одним из механизмов регуляции кислотно щелочного равновесия в организме и сохранения важнейших катионов для поддержания осмотического давления. Глутаминаза почек значительно индуцируется при ацидозе, образующийся аммиак нейтрализует кислые продукты обмена и в виде аммонийных солей экскретируется с мочой (рис. 9-11). Эта реакция защищает организм от излишней потери ионов Na + и К + , которые также могут использоваться для выведения анионов и утрачиваться. При алкалозе количество глутаминазы в почках снижается.
В почках образуется и выводится около 0,5 г солей аммония в сутки.
Высокий уровень глутамина в крови и лёгкость его поступления в клетки обусловливают использование глутамина во многих анаболических процессах. Глутамин — основной донор азота в организме.Амидный азот глутамина используется для синтеза пуриновых и пиримидиновых
Рис. 9-11. Метаболизм амидного азота глутамина в почках.
нуклеотидов, аспарагина, аминосахаров и других соединений (рис. 9-12).
Рис. 9-12. Пути использования глутамина в организме.
Ещё одной реакцией обезвреживания аммиака в тканях можно считать синтез аспарагинапод действием аспарагинсинтетазы.
Существуют 2 изоформы этого фермента — глутаминзависимая и аммиакзависимая, которые используют разные доноры амидных групп. Первая функционирует в животных клетках, вторая преобладает в бактериальных клетках, но присутствует и у животных. Однако такой путь обезвреживания аммиака в клетках человека используется редко и к тому же требует больших энергетических затрат (энергию двух макроэргических связей), чем синтез глутамина.
Наиболее значительные количества аммиака обезвреживаются в печени путём синтеза мочевины.В первой реакции процесса аммиак связывается с диоксидом углерода с образованием карбамоилфосфата, при этом затрачиваются 2 молекулы АТФ. Реакция происходит в митохондриях гепатоцитов под действием фермента карбамоилфос-фатсинтетазы I. Карбамоилфосфатсинтетаза II локализована в цитозоле клеток всех тканей и участвует в синтезе гшримидиновых нуклеотидов (см. раздел 10). Карбамоилфосфат затем включается в орнитиновый цикл и используется для синтеза мочевины.
В мозге и некоторых других органах может протекать восстановительное аминирование α-кетоглутаратапод действием глутаматдегидрогеназы, катализирующей обратимую реакцию. Однако этот путь обезвреживания аммиака в тканях используется слабо, так как глутаматдегидрогеназа катализирует преимущественно реакцию дезаминирования глутамата. Хотя, если учитывать последующее образование глутамина, реакция выгодна для клеток, так как способствует связыванию сразу 2 молекул NH3.
Из мышц и кишечника избыток аммиака выводится преимущественно в виде аланина. Этот механизм необходим, так как активность глутаматдегидрогеназы в мышцах невелика и непрямое дезаминирование аминокислот малоэффективно. Поэтому в мышцах существует ещё один путь выведения азота. Образование аланина в этих органах можно представить следующей схемой (см. схему ниже).
Аминогруппы разных аминокислот посредством реакций трансаминирования переносятся на пируват, основным источником которого служит процесс окисления глюкозы.
Мышцы выделяют особенно много аланина в силу их большой массы, активного потребления
Схема
глюкозы при физической работе, а также потому, что часть энергии они получают за счёт распада аминокислот. Образовавшийся аланин поступает в печень, где подвергается непрямому дезаминированию. Выделившийся аммиак обезвреживается, а пируват включается в глюконеогенез. Глюкоза из печени поступает в ткани и там, в процессе гликолиза, опять окисляется до пирувата (рис. 9-13).
Образование аланина в мышцах, его перенос в печень и перенос глюкозы, синтезированной в печени, обратно в мышцы составляют глюкозо-аланиновый цикл,работа которого сопряжена с работой глюкозо-лактатного цикла (см. раздел 7).
Совокупность основных процессов обмена аммиака в организме представлена на рис. 9-14. Доминирующими ферментами в обмене аммиака служат глутаматдегидрогеиаза и глутаминсинтетаза.
Вопрос 50. Биологическая роль витаминов. Основные причины гиповитаминозов.Биологическая роль- они входят в состав коферментов и простетических групп ферментов, и следовательно используются организмом как строительный материал при синтезе соответствующих небелковых частей ферментов.Гиповитаминоз- специфическое заболевание протекающие в более легкой форме по сравнению в авитаминозами, вызываемым недостаточным содержанием отдельных витаминов в организме .Причины: Экзогенные(связанные с питанием)неправильное приготовление пищи, приготовление пищи с малым кол-вом витаминов, однообразное питание. Эндогенные (связанные с состоянием организма)заболевание ЖКТ и печени, угнетение микрофлоры кишечника, повышенная потребность в витаминах( напр: беременность)
50. Биологическая роль витаминов, основные причины гиповитаминоза.
Биологическая роль витаминов.
Витамины – это органические соединения с низкомолекулярной структурой. Поступают в организм, в основном, с пищей, так как организм их синтезирует в крайне ограниченных количествах.
· Водорастворимые витамины (витамины группы В: В1, В2 ,В6, В12, ВС; С; РР; Р; Н). Эти витамины участвуют в образовании различных коферментов.
· Жирорастворимые витамины (A1, D2, D3,К и Е) участвуют в определении и поддержании функциональности субклеточных структур и клеточных мембран.
При значительном дефиците витаминов все процессы в организме не могут протекать в нормальном режиме, что вызывает нарушения в деятельности органов и их систем.
Витамин А (ретинол) нужен для поддержания красивой кожи, волос и всех слизистых, нормальной работы зрительной системы. Без него невозможно гармоничное формирование организма в период отрочества.
· Витамин В1 (тиамин) координирует углеводный обмен, поставляющий в организм энергию, поддерживает работу нервной, пищеварительной, дыхательной системы.
· Витамин В2 (рибофлавин) отвечает за способность клеток к восстановлению, поэтому при его недостатке даже маленькие кожные трещинки заживают с трудом. Незаменима его функция в процессах окисления и синтеза в организме, а также в поддержании функциональности вегетативного отдела нервной системы.
· Витамин В6 (пиридоксин) – участник обмена белков и жиров, стимулирующий использование организмом природных антиоксидантов в виде ненасыщенных жирных кислот. Определенная доля этого витамина образуется микрофлорой кишечника.
· Витамин В12 (цианокобаламин) принимает важное участие в процессах кроветворения и белковом обмене. Благодаря этому витамину каротин усваивается организмом, переходя в витамин А. Образуется в толстом кишечнике.
· Витамины группы D участвуют в кальциево-фосфорном обмене, поддержке здоровья эндокринных желез. При недостатке — происходит нарушение образования зубов и костей, поражаются мышцы, ухудшается работа пищеварительной, ССС и НС.
· Витамин С является важным компонентом окислительно-восстановительных процессов, препятствующим образованию опухолей. Без него не обходятся процессы кроветворения, усвоения железа. Он нужен для поддержки иммунитета.
· Витамин Е (токоферола ацетат) – природный антиоксидант, поддерживающий репродуктивные функции.
· Витамин РР – один из основных регуляторов обмена веществ, при недостатке которого большинство тканей и органов подвергаются патологическим изменениям.
· Нехватка витамина в рационе, несбалансированное питание
· Разрушение питательных веществ в содержащей их пище вследствие нарушений условий хранения или в результате температурной или иной кулинарной обработки
· Действие веществ-антагонистов, которые содержатся в тех или иных продуктах и приводят к разрушению витаминов, нарушению их усвоения (в частности, белок яйца затрудняет усвоение биотина).
Гиповитаминоз также может быть обусловлен эндогенными (внутренними причинами):
— расстройства работы желудочно-кишечного тракта, приводящие к нарушению процесса всасывания и усвоения витаминов. Часто недостаточное усвоение витаминов бывает вызвано дисбактериозом — нарушением микрофлоры кишечника, которое часто сопровождает длительный прием антибиотиков, прохождение химиотерапии при туберкулезе, онкологических болезнях. Микрофлора участвует в процессе синтеза некоторых витаминов, который происходит внутри организма; ухудшение ее состояния, наличие в ней патогенных микроорганизмов, а также глистные и другие паразитарные инвазии приводят к резкому сокращению запасов витамина в организме.
— генетически обусловленные дефекты ферментных систем, транспортных функций, обеспечивающих всасывание и распределение витаминов.
— прием некоторых лекарственных препаратов также может вызвать гиповитаминоз.
— увеличение потребности человека в витаминах(беременность и кормление, периоды повышенной физической и психической нагрузки, интенсивный рост в подростковом и детском возрасте).
51. В1, В2, В6, РР. Витамин В1.(Тиамин). Используется для синтеза кофермента тиаминдифосфата, необходимого для аэробного распада углеродов. Суточная потребность 2-3мг.Витамин В2.(Рибофлавин). Используется для синтеза коферментов тканевого дыхания-ФАД и ФМН, участвующих в переносе атомов водорода в дыхательной цепи митохондрий. ФАД (флавинадениндинуклеотид) — кофермент, состоящий из двух нуклеотидов соединенных между собой остатками фосфорной кислоты. В состав одного из нуклеотидов входит витамин В2. Совместно в флавиновыми ферментами участвует в переносе атомов водорода в дыхательной цепи митохондрий. ФМН (флавинмононуклеотид) — кофермент, являющийся по строению нуклеотидом, содержащим витамин В2. Совместно с флавиновыми ферментами участвует в переносе атомов водорода в дыхательной цепи митохондрий. Витамин В6. (Пиридоксин). Используется для синтеза кофермента фосфопиридоксаля , участвующего в трансаминировании аминокислот. Суточная потребность 2-3мг. Витамин РР. (Никотинамид). Используется для синтеза коферментов НАД (Никотинамидадениндинуклеотид): необходимого для переноса атомов водорода в дыхательной цепи митохондрий , и НАДФ участвующего в пентозном цикле. Суточная потребность 15-25мг.
Витамины С и Р.
Витамин С (Аскорбиновая кислота).
Биологическая роль. Участвует в окислительно-восстановительных реакциях. Особенно велика роль витамина С в гидроксировании аминокислот пролина и лизина соответственно в оксипролин и оксилизин при синтезе белка коллагена, а также в синтезе гармона надпочечников.
Проявление авитаминоза или гиповитаминоза-цинга.
Пищевые источники—Цитрусовые, красный перец, смородина, рябина клюква, квашенная капуста, хвоя.
Суточная потребность—50-100 мг.
Витамин проницаемости (рутин)
Биологическая роль. Совместно в витамином С учувствует в окислительно-восстановительных реакциях, снижает проницаемость стенок кровеносных сосудов, обладает антиоксидантными свойствами.
Проявление авитаминоза или гиповитаминоза-кровоизлияния
Пищевые источники- Цитрусовые, гречиха, красный перец, черноплодная рябина, черная смородина
Суточная потребность—Не установлена.
Витамины В12 и В6.
Витамин В12 (Цианокобаламин).
Биологическая роль-используется для синтеза коферментов ,участвующих в переносе метильной группы(-СН3),с последующим включением ее в синтезируемые вещества.
Проявление авитаминоза или гиповитаминоза—Анемия
Пищевые источники—Печень, почки, мясо, яйца ,сыр. Синтезируется микрофлорой кишечника при условии поступления с пищей кобальта.
Суточная потребность —2-3 мкг.
Биологическая рольиспользуется для синтеза кофермента фосфопиридоксаля, участвующего в трансаминировании аминокислот.
Проявление авитаминоза или гиповитаминоза —Дерматид
Пищевые источники—печень, почки, мясо, яичный желток. Синтезируется микрофлорой кишечника.
Суточная потребность—2-3 мг.
Жирорастворимые витамины.
Биологическая роль–участвует в восприятии света сетчаткой глаза. Оказывает влияние на барьерную функцию кожи, слизистых оболочек и на проницаемость клеточных мембран.
Проявление авитаминоза или гиповитаминоза- Ксерофтальмия (сухость роговой оболочки глаза), кератомаляция (разрушение роговой оболочки),сумеречная или «куриная слепота»
Пищевые источники-Жир печени морских рыб, говяжья и свиная печень, яичный желток, морковь.
Суточная потребность -2-3 мг.
Витамин D (Кальциферол)
Биологическая роль — участвует во всасывании в кишечнике ионов Са, их транспорте кровью и во включении их в состав костной ткани и в процессе окостенения
Проявление авитаминоза или гиповитаминоза — рахит.
Пищевые источники: Жир печени морских рыб, сливочное масло, растительные масла ,яйца, молоко.
Суточная потребность — 13-25 мкг для детей и для беременных, 7-12 мкг для взрослых.
Биологическая роль-является главным антиоксидантом организма, предохраняющим от окисления полиненасыщенные жирные кислоты, входящие в биологические мембраны.
Проявление авитаминоза или гиповитаминоза: У экспериментальных животных- бесплодие, мышечная дистрофия.
Пищевые источники- злаки, растительные масла, мясо сливочное масло.
Витамин К (Филлюхинон).
Биологическая роль — участвует в синтезе некоторых факторов свертывания крови(в том числе протромбина)
Проявление авитаминоза или гиповитаминоза — повышенная кровоточивость
Пищевые источники- Печень, шпинат, морковь, капуста. Синтезируется микрофлорой кишечника
Суточная потребность -100 мкг.
55. Общие механизмы действия гормонов.
Гормоны – органические вещества, вырабатываются в железах внутренней секреции, поступают с кровью в различные органы и оказывают в них регулирующие влияние на метаболизм и физиологические функции. Синтезируются гормоны в ничтожно малых концентрациях.
В клетках гормонов, в которых реализуется действия гормонов (органы – мишени), имеются особые белки, называемые рецепторами гормонов. Эти белки обладают способностью специфические связывается только с определёнными гормонами, и поэтому органы – мишени избирательно извлекают из протекающей крови лишь те гормоны, которые необходимы данному органу. Такой механизм позволяет гормонам строго избирательно воздействовать на определённые органы. Рецепторные белки находится либо внутри клеток, либо встроены в клеточную мембрану.
Для некоторых гормонов (например, для адреналина и глюкагона) таким рецепторам является мембраносвязанный (встроенные в клеточную мембрану) фермент аденилатциклаза. Присоединение гормона к этому ферменту приводит к повышению его каталитической активности. Под действием активированной аденилатциклазы внутри клеток имеющиеся там АТФ превращается циклическую форму АМФ (цАМФ). Образовавшиеся цАМФ непосредственно участвует в регуляция клеточного метаболизма.
В клетках органов – мишеней содержится ферменты, разрушающие поступающие в них гормоны, а также цАМФ, что ограничивает действие гормонов во времени и предупреждает их накопление.
Чувствительность рецепторов и активность ферментов, расщепляющих гормоны, может меняться при нарушение метаболизма, изменениях физико-химических параметров организма (температура, кислотность, осмотическое давление) и концентрации важнейших субстратов, возникающих при заболеваниях, а также при выполнение мышечной работы. Следствием этого является усиление или ослабления влияние гормонов на соответствующие органы.
Внутриклеточные механизмы действия гормонов разнообразны. Но все же можно выделить три главных механизма, присущих большинству гормонов:
1. Влияют на скорость синтеза ферментов, ускоряя или замедляя его. В результате такого воздействия в органах – мишенях повышается или снижается концентрация определённых ферментов (изменение скорости ферментативных реакций).
2. Влияют на активность ферментов в органах: в одних случаях они являются активаторами ферментов и повышают скорость ферментативных реакций, в других оказывают ингибирующее свойство и снижают скорость ферментативного процесса.
3. Влияют на проницаемость клеточных мембран по отношению к определенным химическим соединениям. В результате этого в клетки поступает больше или меньше субстратов для ферментативных реакций, что сказывается на скорости химических процессов.
По химическому строению делятся на:
1. Гормоны белковой природы (белки и полипептиды): гормоны гипоталамуса, гормоны гипофиза, кальцитонин щитовидной железы, гормон паращитовидных желез, гормоны поджелудочной железы;
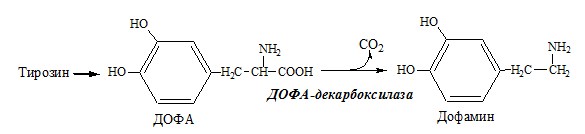
2. Гормоны — производные аминокислоты тирозина: йодсодержащие гормоны щитовидной железы, гормоны мозгового слоя надпочечников;
3. Гормоны стероидного строения: гормоны коры надпочечников, гормоны половых желез.
Синтез и выделение гормонов в кровь находится под контролем НС. При воздействии на организм каких-либо внешних факторов или при возникновении изменений в крови и в различных органах соответствующая информация передаётся по афферентным (чувствительным) нервам в ЦНС. В ответ на полученную информацию в гипоталамусе вырабатываются биологически активные вещества (гормоны гипоталамуса), которые затем поступают в гипофиз и стимулируют или тормозят в нём секрецию так называемых тропных гормонов (гормоны передней доли). Тропные гормоны выделяются из гипофиза в кровь, переносится в железы внутренней секреции и вызывают в них синтез и секрецию соответствующих гормонов, которые далее воздействуют на органы-мишени. Таким образом, в организме имеется единая нервно-гуморальная регуляция.
Все железы внутренней секреции оказывают друг на друга взаимное влияние. Введение в организм гормонов не только сказывается на функции железы, вырабатывающий вводимый гормон, ну и может оказать негативное воздействие на состояние всей нервной регуляция в целом.
56. Гормоны гипоталамуса и гипофиза.
Гипоталамус.
Либерины (рилизинг факторы)– Химическая природа гормона — белок
Стимулирует выделение в кровь гормонов передней доли гипофиза.
Статины (ингибирующие факторы)– Химическая природа гормона- белок
Тормозят выделения в кровь гормонов передней доли гипофиза.
Аминокислоты. Общие пути обмена аминокислот. Синтез мочевины.
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
Аминокислоты. Общие пути обмена аминокислот. Биосинтез мочевины.
Аминокислоты – органические соединения, содержащие –СООН и -NH2 в α-положении. Почти все аминокислоты имеют хиральный атом и обладают оптической изомерией. У человека присутствуют L-аминокислоты
Всего известно около 300 видов аминокислот, у человека в организме – 70, а в составе белков – 20.
Аминокислоты. Физико-химические свойства
Аминокислоты белые кристаллические вещества, хорошо растворимые в воде. Имеют высокую температуру плавления, в твердом состоянии находятся в виде внутренней соли. Многие сладкие на вкус (гли).
Аминокислоты амфотерные вещества – проявляют свойства кислот и оснований.
К наиболее важным общим реакциям аминокислот относятся реакции:
- 1. декарбоксилирования,
- 2. переаминирования,
- 3. дезаминирования,
- 4. образование пептидных связей
- 5. образование оснований Шиффа (при гликозилировании белков).
Специфические реакции аминокислот связаны с наличием функциональных групп в радикале (окислительно-восстановительные реакции цис).
Аминокислоты. Классификация.
Классификация аминокислот по природе радикала:
- 1). алифатические (гли, ала, вал, лей, иле и.т.д.);
- 2). ароматические (фен, тир, три, гис);
- 3). гетероциклические (про, оксипро).
Классификация аминокислот по количеству карбоксильных и аминогрупп:
- 1). нейтральные;
- 2). кислые (глу, асп);
- 3) основные (арг, лиз).
Классификация аминокислот по функциональным группам в радикале:
- 1). содержащие –ОН (сер, тре);
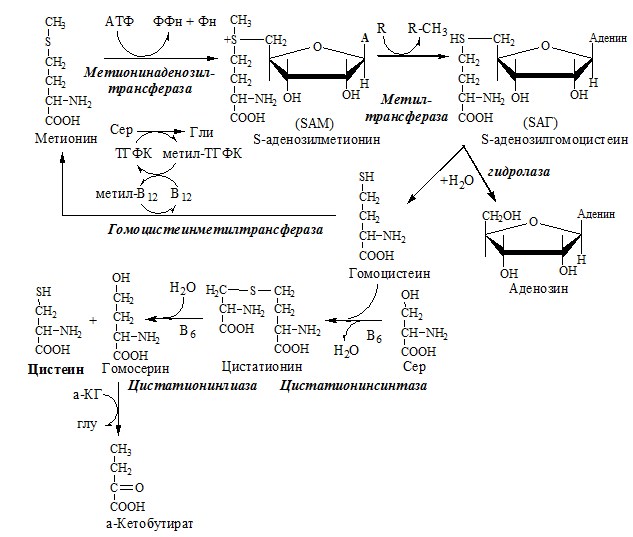
- 2). содержащие –SH (цис, мет);
- 3). содержащие –СОNH2 (глн, асн);
Классификация аминокислот по способности к синтезу:
- 1. Аминокислоты, которые синтезируются в организме, называют заменимыми (глицин, аспарагиновая кислота, аспарагин, глутаминовая кислота, глутамин, серии, пролин, аланин).
- 2. Аминокислоты, которые не синтезируются в организме, но для него необходимы, называются незаменимыми (фенилаланин, метионин, треонин, триптофан, валин, лизин, лейцин, изолейцин).
- 3. Аргинин и гистидин – частично заменимые аминокислоты , у взрослых они образуются в достаточных количествах, а у детей – нет. Поэтому, необходимо дополнительное поступление этих АК с пищей.
- 4. Тирозин и цистеин — условно заменимые, так как для их синтеза необходимы незаменимые аминокислоты (фенилаланин и метионин).
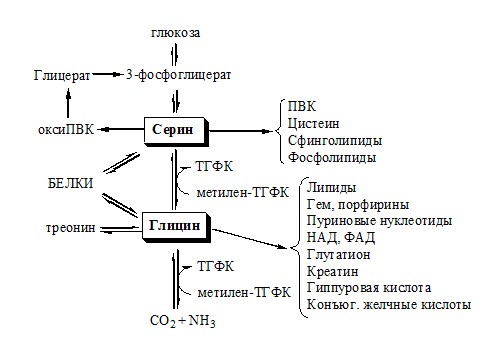
Аминокислоты. Функции
- Используются для синтеза белков, углеводов, липидов, нуклеиновых кислот, биогенных аминов (гормонов, нейромедиаторов), других аминокислот
- Служат источником азота при синтезе всех азотсодержащих небелковых соединений (нуклеотиды, гем, креатин, холин и др);
- Выполняют регуляторную функцию (гли, глу – нейромедиаторы);
- служат источником энергии для синтеза АТФ.
ПУТИ ОБРАЗОВАНИЯ ПУЛА АМИНОКИСЛОТ В КРОВИ
И ЕГО ИСПОЛЬЗОВАНИЕ В ОРГАНИЗМЕ
Большая часть аминокислот организма человека, примерно 15кг, входит в состав белков. Фонд свободных аминокислот организма составляет примерно 35г.
Источниками аминокислот в организме являются белки пищи, белки тканей и синтез АК из углеводов. В сутки у человека распадается на аминокислоты около 400г белков, примерно такое же количество синтезируется. Специальной формы депонирования аминокислот, подобно глюкозе (в виде гликогена) или жирных кислот (в виде ТГ), не существует (исключение – казеин молока). Поэтому резервом аминокислот служат все белки тканей, но преимущественно белки мышц (т.к. их много).
ОБЩИЕ РЕАКЦИИ ОБМЕНА АМИНОКИСЛОТ
Аминокислоты, появившиеся в организме, включаются в общие и специфические реакции обмена.
К общим реакциям обмена аминокислот относят реакции трансаминирования, дезаминирования и декарбоксилирования, биосинтеза белков и рацемизации (L переходы D).
ТРАНСАМИНИРОВАНИЕ (ПЕРЕАМИНИРОВАНИЕ) АМИНОКИСЛОТ
Трансаминирование — реакция переноса α-аминогруппы с аминокислоты на α-кетокислоту, в результате чего образуются новая α-кетокислота и новая аминокислота. Процесс трансаминирования легко обратим, при нем общее количество аминокислот в клетке не меняется.
Реакции катализируют аминотрансферазы, коферментом которых служит пиридоксальфосфат (ПФ) — производное витамина В6 (пиридоксина).
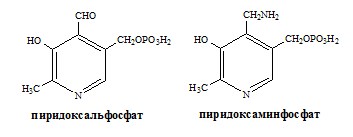
У человека найдено более 10 аминотрансфераз, которые локализуются в цитоплазме и митохондриях клеток. В реакции трансаминирования вступают почти все аминокислоты, за исключением лизина, треонина и пролина.
Механизм переаминирования
Вначале, аминоксилота передает свою аминогруппу на пиродоксальфосфат. Аминокислота при этом превращается в кетокислоту, а пиродоксальфосфат – в пиридоксаминфосфат.
Затем, реакции идут в обратную сторону: но уже другая кетокислота, принимает аминогруппу от пиридоксаминфосфата и превращается в новую АК, а пиридоксаминфосфат в пиродоксальфосфат.
Органоспецифичные аминотрансферазы АЛТ и АСТ
Чаще всего в трансаминировании участвуют аминокислоты и кетокислоты, которых много в организме — глу, ала, асп, α-КГ, ПВК и ЩУК. Основным донором аминогруппы служит глу, а кетогруппы – α-КГ.
Наиболее распространёнными аминотрансферазами в большинстве тканей млекопитающих являются аланинаминотрансфераза (АЛТ) и аспартатаминотрансфераза (ACT).
АЛТ катализирует реакцию трансаминирования между ала и α-КГ: ала+α-КГ↔ПВК+глу АЛТ локализуется в цитозоле клеток многих органов, больше всего ее в клетках печени и миокарде.
ACT катализирует реакцию трансаминирования между асп и α-КГ: асп+α-КГ↔ЩУК+глу
ACT имеет как цитоплазматическую, так и митохондриальную формы. Наибольшее ее количество обнаружено в миокарде и печени.
АСТ и АЛТ являются органоспецифичными ферментами, их определяют в крови для диагностики заболеваний печени, сердца и, в меньшей степени, скелетных мышц. Соотношение активностей АСТ/АЛТ называют «коэффициент де Ритиса». В норме он равен 1,33±0,42.
При инфаркте миокарда активность ACT в крови увеличивается в 8—10 раз, а АЛТ — в 1,5—2,0 раза, коэффициент де Ритиса резко возрастает.
При гепатитах активность АЛТ в сыворотке крови увеличивается в – 8—10 раз по сравнению с нормой, a ACT — в 2—4 раза. Коэффициент де Ритиса снижается до 0,6.
Биологическое значение трансаминирования
Реакции трансаминирования обеспечивают синтез и распад амино- и кетокислот, перераспределение аминного азота в тканях организма.
ДЕЗАМИНИРОВАНИЕ АМИНОКИСЛОТ
Дезаминирование аминокислот — реакция отщепления α-аминогруппы от аминокислоты, в результате чего образуется соответствующая α-кетокислота и выделяется молекула аммиака.
Дезаминирование бывает прямым и непрямым.
Прямое дезаминирование аминокислоты
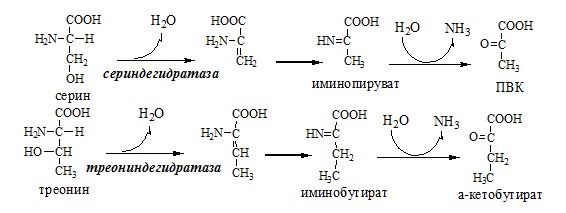
Прямое дезаминирование – это дезаминирование, которое происходит в 1 стадию с участием одного фермента. Прямому дезаминированию повергаются глу, гис, сер, тре, цис.
Существует 5 видов прямого дезаминирования аминокислот:
- 1. окислительное;
- 2. неокислительное;
- 3. внутримолекулярное;
- 4. восстановительное;
- 5. гидролитическое.
Окислительное дезаминирование – самый активный вид прямого дезаминирования аминокислот.
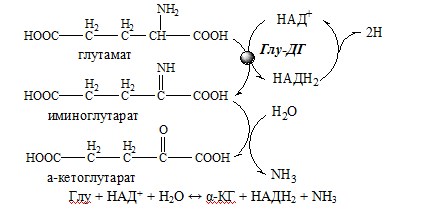
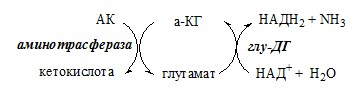
1. Глутаматдегидрогеназа (глу-ДГ) – олигомер, состоящий из 6 субъединиц (молекулярная масса 312 кД), содержит кофермент НАД+. Глу-ДГ катализирует обратимое дезаминирование глу, очень активна в митохондриях клеток практически всех органов, кроме мышц. Глу-ДГ аллостерически ингибируют АТФ, ГТФ, НАДH2, активирует избыток АДФ. Индуцируется Глу-ДГ стероидными гормонами (кортизолом).
Реакция идёт в 2 этапа. Вначале происходит ферментативное дегидрирование глутамата и образование α-иминоглутарата, затем — неферментативное гидролитическое отщепление иминогруппы в виде аммиака, в результате чего образуется α-кетоглутарат. При избытке аммиака реакция протекает в обратном направлении (как восстановительное аминирование α-кетоглутарата).
Глу + НАД+ + Н2О ↔ α-КГ + НАДН2 + NH3
2. Оксидаза L-аминокислот
В печени и почках есть оксидаза L-АК, способная дезаминировать некоторые L-аминокислоты:
Оксидаза L-АК имеет кофермент ФМН. Т.к. оптимум рН оксидазы L-АК равен 10,0, активность фермента очень низка и вклад ее в дезаминирование незначителен.
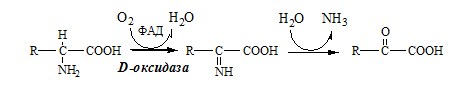
3. Оксидаза D-аминокислот
Оксидаза D-аминокислот также обнаружена в почках и печени. Это ФАД-зависимый фермент, с оптимумом рН в нейтральной среде. Оксидаза D-аминокислот превращает, спонтанно образующиеся из L-аминокислот, D-аминокислоты в кетокислоты.
Неокислительное дезаминирование
В печени человека присутствуют специфические пиридоксальфосфатзависимые ферменты сериндегидратаза, треониндегидратаза, катализирующие реакции неокислительного дезаминирования аминокислот серина и треонина.
Внутримолекулярное дезаминирование
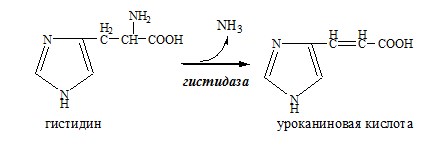
Внутримолекулярное дезаминирование характерно для гистидина. Реакцию катализирует гистидаза (гистидин-аммиаклиаза). Эта реакция происходит только в печени и коже.
Непрямое дезаминирование (трансдезаминирование) аминокислот
Непрямое дезаминирование – это дезаминирование, которое происходит в 2 стадий с участием нескольких ферментов. Оно характерно для большинства аминокислот, так как они не способны к прямому дезаминированию (нет ферментов).
На первой стадии происходит одна и несколько реакций переаминирования с участием аминотрансфераз, в результате аминогруппа аминокислоты переходит на кетосоединение (α-КГ, ИМФ).
На второй стадии происходит реакция дезаминирования аминосоединения (глу, АМФ), в результате чего образуется аммиак.
Последовательность реакций непрямого дезаминирования зависит от набора ферментов в тканях.
Непрямое дезаминирование в печени
Непрямое дезаминирование аминокислоты происходит при участии 2 ферментов: аминотрансферазы и глу-ДГ. Аминогруппы аминокислоты в результате трансаминирования переносятся на α-КГ с образованием глутамата, который затем подвергается прямому окислительному дезаминированию.
Обе стадии непрямого дезаминирования обратимы, что обеспечивает как катаболизм аминокислот, так и возможность образования практически любой АК из соответствующей α-кетокислоты.
При энергодефиците АДФ активирует Глу-ДГ, что усиливает катаболизм аминокислот и образование а-кетоглутарата, поступающего в ЦТК как энергетический субстрат.
Таким образом, Глу-ДГ играет ключевую роль в регуляции обмена аминокислот и энергии.
Непрямое дезаминирование в мышцах (и нервной ткани)
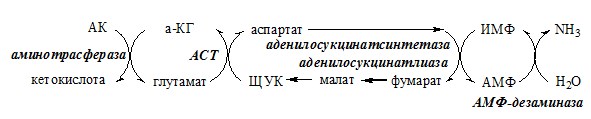
В мышечной ткани активность глу-ДГ низка, поэтому при интенсивной физической нагрузке функционирует ещё один путь непрямого дезаминирования с участием цикла ИМФ-АМФ.
Можно выделить 4 стадии этого процесса:
- 1. трансаминирование с а-кетоглутаратом, образование глутамата (аминотрансфераза);
- 2. трансаминирование глутамата с ЩУК, образование аспартата (АСТ);
- 3. реакция переноса аминогруппы от аспартата на ИМФ (инозинмонофосфат), образование АМФ и фумарата (аденилосукцинасинтаза и аденилосукцинатлиаза);
- 4. гидролитическое дезаминирование АМФ (АМФ-дезаминаза).
Этот путь дезаминирования преобладает в мышцах при интенсивной работе, в результате которой накапливается молочная кислота. Выделяющийся аммиак предотвращает закисление среды в клетках, вызванное образованием лактата.
Пути обмена безазотистого остатка аминокислот
За сутки у человека распадаются примерно 100г АК. Катаболизм всех АК сводится к образованию шести веществ, вступающих в общий путь катаболизма: ПВК, ацетил-КоА, α-кетоглутарат, сукцинил-КоА, фумарат и ЩУК. Эти вещества окисляются в ЦТК для образования АТФ или используются для синтеза глюкозы и кетоновых тел.
Гликогенные аминокислоты – АК, которые превращаются в ПВК и промежуточные продукты ЦТК (а-КГ, сукцинил-КоА, фумарат, ЩУК). Они через ЩУК, используются в глюконеогенезе (ала, асн, асп, гли, глу, глн, про, сер, цис, арг, гис, вал, мет, тре).
Кетогенные аминокислоты – АК, которые в процессе катаболизма превращаются в ацетоацетат (Лиз, Лей) или ацетил-КоА (Лей) и могут использоваться в синтезе кетоновых тел.
Смешанные (глико-кетогенными) аминокислоты – АК, при катаболизме которых образуются метаболит цитратного цикла и ацетоацетат (Три, Фен, Тир) или ацетил-КоА (Иле). Эти АК используются для синтеза глюкозы и кетоновых тел.
ОБМЕН АММИАКА
Аммиак в организме образуется:
- при дезаминировании аминокислоты во всех тканях (много);
- при дезаминировании биогенных аминов и нуклеотидов во всех тканях (мало);
- при дезаминировании АМФ в интенсивно работающей мышце;
- при гниении белков в кишечнике.
Концентрация аммиака
Концентрация аммиака в сыворотке крови в норме 11—35 мкмоль/л. В крови и цитозоле клеток при физиологических значениях рН аммиак переходит в ион аммония — NH4+, количество неионизированного NH3 невелико (
Токсичность аммиака
Аммиак — токсичное соединение. Даже небольшое повышение его концентрации оказывает неблагоприятное действие на организм, и, прежде всего на ЦНС.
Механизм токсического действия аммиака:
- 1. Аммиак легко проникает через мембраны в клетки и в митохондриях сдвигает реакцию, катализируемую глу-ДГ, в сторону образования глу:
α-Кетоглутарат + НАДH2 + NH3 → глу + НАД+.
Уменьшение концентрации α-кетоглутарата вызывает:
угнетение реакции трансаминирования АК и снижение синтеза из них нейромедиаторов (ацетилхолина, дофамина и др.);
снижения скорости ЦТК и развитие энергодефицита.
Недостаточность α-кетоглутарата ускоряет реакции синтеза ЩУК из ПВК, сопровождающейся интенсивным потреблением СО2 (особенно характерны для клеток головного мозга). - 2. Повышение концентрации аммиака в крови сдвигает рН в щелочную сторону, вызывает алкалоз. Алкалоз увеличивает сродство гемоглобина к кислороду, что препятствует отдачи им кислорода. В результате развивается гипоксия тканей, энергодефицит, от которого главным образом страдает головной мозг.
- 3. Высокие концентрации аммиака, при участии глутаминсинтетазы, стимулируют синтез глутамина из глутамата в нервной ткани:
- 4. Глу + NH3 + АТФ → Глн + АДФ + Н3РО4. Накопление глн в клетках нейроглии приводит к повышению в них осмотического давления, набуханию астроцитов и в больших концентрациях вызвает отёк мозга. Снижение концентрации глу нарушает обмен АК и нейромедиаторов, в частности синтез γ-аминомасляной кислоты (ГАМК), основного тормозного медиатора. При недостатке ГАМК и других медиаторов нарушается проведение нервного импульса, возникают судороги.
- 5. Ион NH4+ практически не проникает через цитоплазматические и митохондриальные мембраны. Избыток NH4+ в крови нарушает трансмембранный перенос одновалентных катионов Na+ и К+, конкурируя с ними за ионные каналы, что также влияет на проведение нервных импульсов.
- 6. Низкие концентрации аммиака стимулируют дыхательный центр, а высокие – угнетают.
Связывание (обезвреживание) аммиака
В связи с токсичностью аммиака в тканях происходит его связывание с образованием нетоксичных соединений – АК и мочевины. Процесс образования и обезвреживания аммиака регулируют в основном ферменты глутаматдегидрогеназа и глутаминсинтетаза.
Обмен глутамата
В мозге и некоторых других органах может протекать восстановительное аминирование α-кетоглутарата под действием глутаматдегидрогеназы, катализирующей обратимую реакцию.
Однако этот путь обезвреживания аммиака в тканях используется слабо, так как глутаматдегидрогеназа катализирует преимущественно реакцию дезаминирования глутамата. Хотя, если учитывать последующее образование глутамина, реакция выгодна для клеток, так как способствует связыванию сразу 2 молекул NH3.
Обмен глутамина
Основной реакцией связывания аммиака, протекающей во всех тканях организма (основные поставщики мышцы, мозг и печень), является синтез глутамина под действием глутаминсинтетазы:
Глутаминсинтетаза находиться в митохондриях клеток, содержит кофактор — ионы Mg2+, является одним из основных регуляторных ферментов обмена АК. Она аллостерически ингибируется АМФ, глюкозо-6ф, гли, ала и гис.
Глутамин, путём облегчённой диффузии, легко проходит клеточные мембраны (для глутамата возможен только активный транспорт), поступает из тканей в кровь и транспортируется в кишечник и почки.
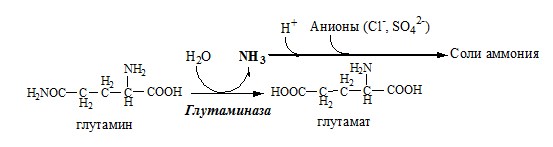
В почках происходит гидролиз глутамина под действием глутаминазы с образованием аммиака:
Аммиак с протонами и анионами образует соли аммония (0,5 г/сут), которые выделяются с мочой. Этот процесс используется для регуляции КОС и сохранения в организме важнейших катионов Na+ и К+. Глутаминаза почек значительно индуцируется при ацидозе, ингибируется при алкалозе.
В клетках кишечника также под действием глутаминазы происходит гидролитическое освобождение амидного азота в виде аммиака:
Образовавшийся аммиак поступает через воротную вену в печень или удаляется из организма с фекалиями.
Высокий уровень глутамина в крови и лёгкость его поступления в клетки обусловливают использование глутамина во многих анаболических процессах. Глутамин — основной донор азота в организме. Амидный азот глутамина используется для синтеза пуриновых и пиримидиновых нуклеотидов, аспарагина, аминосахаров и других соединений.
Обмен аспарагина
Обезвреживание аммиака в тканях происходит незначительно при синтезе аспарагина под действием глутаминзависимой и аммиакзависимой аспарагинсинтетазы.
Первая функционирует в животных клетках, вторая преобладает в бактериальных клетках, но присутствует и у животных.
Обмен аланина
Из мышц и кишечника избыток аминого азота выводится преимущественно в виде аланина.
В кишечнике:
Глутамат подвергается трансаминированию с ПВК с образованием аланина и α-кетоглутарата. Аланин поступает из кишечника в кровь воротной вены и поглощается печенью.
В мышцах:
Образование аланина в мышцах, его перенос в печень связан с обратным переносом в мышцы синтезированной в печени глюкозы.
Этот процесс называется глюкозо-аланиновый цикл:
Он необходим, так как активность глу-ДГ в мышцах невелика и непрямое дезаминирование АК малоэффективно.
Мышцы выделяют особенно много аланина в силу их большой массы, активного потребления глюкозы при физической работе, а также потому, что часть энергии они получают за счёт распада АК. Образовавшийся аланин поступает в печень, где подвергается непрямому дезаминированию. Выделившийся аммиак идет на синтез мочевины, а ПВК включается в глюконеогенез. Глюкоза из печени поступает в ткани и там, в процессе гликолиза, опять окисляется до ПВК.
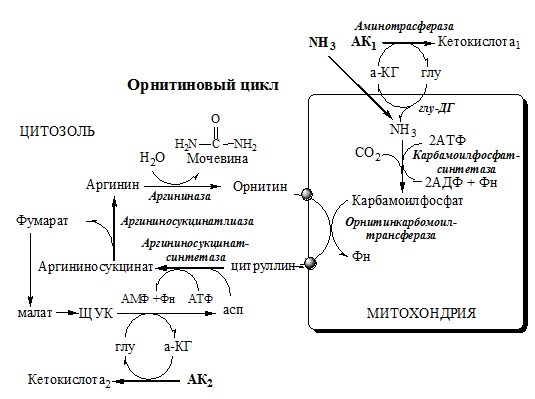
ОРНИТИНОВЫЙ ЦИКЛ
Большая часть свободного аммиака, а также аминного азота в составе (в основном глутамин, аланин) поступают в печень, где из них синтезируется нетоксичное и хорошо растворимое в воде соединение — мочевина. Мочевина является основной формой выведения азота из организма человека.
Синтез мочевины происходит в цикле, который замыкается орнитином. Цикл открыли в 40-х годах XX века немецкие биохимики Г. Кребс и К. Гензелейт.
Мочевина (карбамид) — полный амид угольной кислоты — содержит 2 атома азота, один из аммиака, другой – из асп.
Реакции орнитинового цикла
Предварительно в митохондриях под действием карбамоилфосфатсинтетазы I с затратой 2 АТФ аммиак связывается с СО2 с образованием карбамоилфосфата:
(Карбамоилфосфатсинтетаза II локализована в цитозоле клеток всех тканей и участвует в синтезе пиримидиновых нуклеотидов).
1. В митохондриях орнитинкарбамоилтрансфераза переносит карбамоильную группу карбамоилфосфата на орнитин и образуется — цитруллин:
2. В цитозоле аргининосукцинатсинтетаза с затратой 1 АТФ (двух макроэргических связей) связывает цитруллин с аспартатом и образует аргининосукцинат (аргининоянтарная кислота). Фермент нуждается в Mg2+. Аспартат — источник второго атома азота мочевины.
3. В цитозоле аргининосукцинатлиаза (аргининсукциназа) расщепляет аргининосукцинат на аргинин и фумарат (аминогруппа аспартата оказывается в аргинине).
4. В цитозоле аргиназа гидролизует аргинин на орнитин и мочевину. У аргиназы кофакторы ионы Са2+ или Мn2+, ингибиторы – высокие концентрации орнитина и лизина.
Образующийся орнитин взаимодействует с новой молекулой карбамоилфосфата, и цикл замыкается.
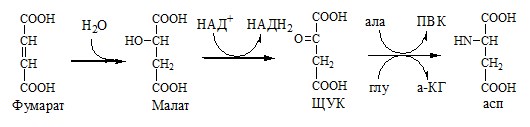
Регенерация аспартата из фумарата
Фумарат, образующийся в орнитиновом цикле, в цитозоле превращается в ЩУК, который переаминируется с аланином или глутаматом с образованием аспартата. Аланин поступает главным образом из мышц и клеток кишечника:
Малат может направиться в митохондрии и включиться в ЦТК.
Пируват, образующийся в этих реакциях из аланина, используется для глюконеогенеза.
Общее уравнение синтеза мочевины:
CO2 + NH3 + асп + 3 АТФ + 2 Н2О → мочевина + фумарат + 2АДФ + АМФ + 2Фн + ФФн
Энергетический баланс орнитинового цикла
На синтез 1 мочевины расходуются 4 макроэргических связи 3 АТФ. Дополнительные затраты энергии связаны с трансмембранным переносом веществ и экскрецией мочевины.
Энергозатраты при этом частично компенсируются:
- при окислительном дезаминировании глутамата образуется 1 молекула НАДН2, которая обеспечивает синтез 3 АТФ;
- в ЦТК, при превращении малата в ЩУК образуется еще 1 молекула НАДН2, которая также обеспечивает синтез 3 АТФ;
Орнитиновый цикл в печени выполняет 2 функции:
- 1. превращение азота АК в мочевину, которая экскретируется и предотвращает накопление токсичных продуктов, главным образом аммиака;
- 2. синтез аргинина и пополнение его фонда в организме.
Полный набор ферментов орнитинового цикла есть только в гепатоцитах. Отдельные же ферменты орнитинового цикла обнаруживаются в разных тканях. В энтероцитах, есть карбамоилфосфатсинтетаза I и орнитинкарбамоилтрансфераза, следовательно, может синтезироваться цитруллин. В почках есть аргининосукцинатсинтетаза и аргининосукцинатлиаза. Цитруллин, образовавшийся в энтероцитах, может поступать в почки и превращаться там в аргинин, который переносится в печень и гидролизуется аргиназой. Активность этих рассеянных по разным органам ферментов значительно ниже, чем в печени.
Выделение азота из организма
Азот выводиться из организма с мочой, калом, потом и с выдыхаемым воздухом в виде различных соединений. Основная масса азота выделяется из организма с мочой в виде мочевины (до 90%). В норме соотношение азотсодержащих веществ в моче составляет: мочевина 86%, креатинин 5%, аммиак 3%, мочевая кислота 1,5% и другие вещества 4,5%. Экскреция мочевины в норме составляет 25 г/сут, солей аммония 0,5 г/сут.
ГИПЕРАММОНИЕМИЯ
Нарушение реакций обезвреживания аммиака может вызвать повышение содержания аммиака в крови — гипераммониемию, что оказывает токсическое действие на организм.
Причинами гипераммониемии могут быть:
1. генетические дефекты ферментов орнитинового цикла в печени;
2. вторичное поражение печени в результате цирроза, гепатита или других заболеваний.
Известны пять наследственных заболеваний, обусловленные дефектом пяти ферментов орнитинового цикла.
Наследственные нарушения орнитинового цикла и их основные проявления
Гиперам-мониемия, тип I
В течение 24-48 ч после рождения кома, смерть
Гиперам-мониемия, тип II
Сцепленный с Х-хромосомой
Гипотония, снижение толерантности к белкам
Гипераммониемия тяжёлая у новорождённых. У взрослых — после белковой нагрузки
Гипераммониемия, атаксия, судороги, выпадение волос
Аргини-носукцинат NH 3
Аргини-носукци-нат, Глн, Ала, Лиз
Apг
Лиз Орнитин
Снижение активности какого-либо фермента синтеза мочевины приводит к накоплению в крови субстрата данного фермента и его предшественников.
При гипераммониемиях I и II типа происходит накопление карбамоилфосфата в митохондриях и выход его в цитозоль. Это вызывает увеличение скорости синтеза пиримидиновых нуклеотидов (вследствие активации карбамоилфосфатсинтетазы II), что приводит к накоплению оротата, уридина и урацила и выведению их с мочой.
Тяжесть течения заболевания зависит также от степени снижения активности ферментов.
Все нарушения орнитинового цикла приводят к значительному повышению в крови концентрации аммиака (до 6000 мкмоль/л), глутамина и аланина.
Гипераммониемия сопровождается появлением следующих симптомов:
- тошнота, повторяющаяся рвота;
- головокружение, тремор, судорожные припадки;
- нечленораздельная речь;
- потеря сознания, отёк мозга (в тяжёлых случаях);
- отставание умственного развития (при хронической врождённой форме).
В тяжёлых случаях развивается кома с летальным исходом.
Все симптомы гипераммониемии — проявление действия аммиака на ЦНС.
Для диагностики различных типов гипераммониемии производят определение содержания аммиака в крови, метаболитов орнитинового цикла в крови и моче, активности фермента в биоптатах печени.
Лечение больных с различными дефектами орнитинового цикла в основном направлено на снижение концентрации аммиака в крови за счёт малобелковой диеты, введения кетоаналогов АК в рацион и стимуляцию выведения аммиака в обход нарушенных реакций:
- путём связывания и выведения NH3 в составе фенилацетилглутамина и гиппуровой кислоты. Пищевой фенилацетат при конъюгации с глутамином образует фенилацетилглутамин, а пищевой бензоат при конъюгации с глицином образует гиппуровую кислоту, которые потом выводится с мочой;
- повышением концентрации промежуточных метаболитов цикла (аргинина, цитруллина, глутамата), образующихся вне блокируемых реакций. Введение больших доз цитруллина стимулирует синтез мочевины из аспартата. Большие дозы аргинина стимулируют регенерацию орнитина и выведение азота в составе цитруллина и аргининосукцината.
Обмен аминокислот и аммиака между тканями
Печень
В печень азот поступает в основном в виде аммиака, глутамина, аланина, а меньше в виде других аминокислот в основном из мышц и кишечника. Поглощает аминокислоты с разветвленной цепью (вал, лей, иле). Синтезирует глюкозу в основном из аланина и серина.
Мышцы
Поглощают аминокислоты с разветвленной цепью (вал, лей, иле). Выделяют много аланина и глутамина меньше других аминокислот.
Кишечник
Поглощает глутамин. Выделяет много аланина. С пищей из кишечника поступают все аминокислоты.
Мозг
Поглощает много аминокислот с разветвленной цепью (вал, лей, иле). Выделяет много глутамина.
Почки
Поглощают глутамин. Выделяют много серина и немного аланина.
ДЕКАРБОКСИЛИРОВАНИЕ АМИНОКИСЛОТ И ИХ ПРОИЗВОДНЫХ
Некоторые аминокислоты и их производные могут подвергаться декарбоксилированию – отщеплению α-карбоксильной группы. У млекопитающих декарбоксилируются: три, тир, вал, гис, глу, цис, арг, орнитин, SAM, ДОФА, 5-окситриптофан и т.д. Реакцию необратимо катализируют декарбоксилазы, которые содержат в активном центре пиридоксальфосфат. Механизм реакции похож на реакцию переаминирования.
Продуктами реакции являются СО2 и биогенные амины, выполняющие регуляторные функции (гормоны, тканевые гормоны, нейромедиаторы).
Серотонин
Серотонин образуется из триптофана в надпочечниках, ЦНС и тучных клетках.
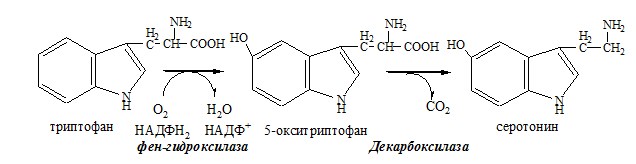
Серотонин – возбуждающий нейромедиатор средних отделов мозга (проводящих путей) и гормон. Стимулирует сокращение гладкой мускулатуры, вазоконстриктор, регулирует АД, температуру тела, дыхание, антидепрессант.
ГАМК
ГАМК образуется и разрушается в ГАМК-шунте ЦТК в высших отдела мозга. Он имеет очень высокую концентрацию.
ГАМК – тормозной нейромедиатор (повышает проницаемость постсинаптических мембран для К+), повышает дыхательную активность нервной ткани, улучшает кровоснабжение головного мозга.
Гистамин
Гистамин образуется в тучных клетках. Секретируется в кровь при повреждении ткани, развитии иммунных и аллергических реакций.
Гистамин – медиатор воспаления, аллергических реакций, пищеварительный гормон:
- 1. стимулирует секрецию желудочного сока, слюны;
- 2. повышает проницаемость капилляров, расширение сосудов, покраснение кожи, вызывает отеки, снижает АД (но увеличивает внутричерепное давление, вызывает головную боль);
- 3. сокращает гладкую мускулатуру легких, вызывает удушье;
- 4. вызывает аллергическую реакцию;
- 5. нейромедиатор;
- 6. медиатор боли.
Дофамин
Дофамин образуется (фен → тир → ДОФА → дофамин) в мозге и мозговом веществе надпочечников.
Дофамин – нейромедиатор среднего отдела мозга.
Аминокислоты. Специфические пути обмена аминокислот
ФОЛИЕВАЯ КИСЛОТА
Значительную роль в обмене ряда АК, синтезе некоторых сложных липидов, нейромедиаторов, гормонов и ряда других веществ играют производные фолиевой кислоты.
Фолиевая кислота широко распространёна в продуктах животного и растительного происхождения, синтезируется микрофлорой кишечника.
Активная форма фолиевой кислоты – ТГФК. Она образуется в печени при восстановлении фолиевой кислоты с участием фолатредуктазы и дигидрофолатредуктазы, коферментом которых служит НАДФН2.
Образование одноуглеродных фрагментов, их взаимопревращения
ТГФК принимает от АК одноуглеродные фрагменты: серин и глицин дают метиленовый фрагмент (-СН2-), гистидин – формимино- и формильный фрагменты.
В составе ТГФК одноуглеродные фрагменты могут подвергаться взаимопревращениям: метиленовая группа превращаться в метенильную (-СН=), формильную (-НС=О), метильную (-СН3) и формиминогруппу (-CH=NH).
Затем ТГФК отдает одноуглеродные фрагменты на:
- синтез пуриновых оснований
- синтез тимидиловой кислоты
- регенерацию метионина
- превращение дУМФ в дТМФ;
- превращение глицина в серина и т.д.
Недостаточность фолиевой кислоты
Гиповитаминоз фолиевой кислоты возникает редко, его вызывает использование сульфаниламидных препаратов. Сульфаниламиды — структурные аналоги парааминобензойной кислоты, они ингибируют синтез фолиевой кислоты у микроорганизмов, вызывая их гибель. Некоторые производные птеридина (аминоптерин и метотрексат) тормозят рост почти всех организмов, нуждающихся в фолиевой кислоте, их используют для подавления опухолевого роста у онкологических больных.
Гиповитаминоз фолиевой кислоты приводит к:
- 1. мегалобластической (макроцитарной) анемии. Она характеризуется уменьшением количества эритроцитов, снижением содержания в них гемоглобина, что вызывает увеличение размера эритроцитов. Причина — нарушение синтеза ДНК и РНК из-за недостатка тимидиловой кислоты и пуриновых нуклеотидов.
- 2. лейкопении;
- 3. задержке роста.
- 4. нарушению регенерации эпителия, особенно в ЖКТ (связано с недостатком нуклеотидов для синтеза ДНК в постоянно делящихся клетках слизистой оболочки).
КОБАЛАМИН (В12)
В12 синтезируется только микроорганизмами, им богаты печень, почки. Активные формы кобаламина – метилкобаламин (цитоплазма) и дезоксиаденозилкобаламин (митохондрии).
Кобаламин участвует:
1. в передачи метила с метил-ТГФК на гомоцистеин при регенерации метионина.
2. в превращениях одноуглеродных фрагментов в составе ТГФК.
3. в метаболизме жирных кислот с нечетным числом атомов С и аминокислот с разветвленной цепью. Перенос протонов в реакциях изомеризации.
Недостаточность В12
Гиповитаминоз возникает при нарушении всасывании В12 (дефицит фактора Касла при пониженной кислотности желудочного сока).
Гиповитаминоз В12 сопровождается:
1. макроцитарной (мегалобластической) анемией: снижение числа эритроцитов, гемоглобина, увеличение размера эритроцитов. Причина — нарушение синтеза ДНК.
2. расстройствами деятельности нервной системы. При распаде жирных кислот с нечетным количеством атомов С и разветвленных АК из-за дефицита В12 накапливается нейротоксичная метилмалоновая кислота.
ОБМЕН СЕРИНА И ГЛИЦИНА
Серин и глицин – заменимые аминокислоты.
Синтез серина и глицина. Основной путь катаболизма глицина.
Схема путей обмена серина и глицина
Серии и глицин выполняют в организме человека разнообразные и очень важные функции.
Глицин — важнейший (после ГАМК) тормозной нейромедиатор в спинном мозге, промежуточном мозге и некоторых отделах головного мозга.
Наследственные нарушения обмена глицина
Известно несколько заболеваний, связанных с нарушениями обмена глицина. В их основе лежит недостаточность ферментов или дефект системы транспорта этой АК.
Гиперглицинемия возникает при дефекте глицинрасщепляющей системы. Проявляется повреждением мозга, судорогами, гипотонией, нарушением дыхания.
Глицинурия характеризуется повышенным выделением глицина с мочой (до 1 г/сут) при нормальном содержании его в крови. Причиной является нарушение реабсорбции глицина в почках.
Первичная гипероксалатурия характеризуется постоянно высоким выделением оксалата с мочой, независимо от поступления его с пищей. Дефект глицинаминотрансферазы блокирует превращение глиоксилата снова в глицин. Глицин → глиоксилат → оксалат
Прогрессирует двустороннее образование оксалатных камней в мочевыводящих путях, развиваются нефрокальциноз и инфекция мочевыводящих путей. Больные погибают в детском возрасте от почечной недостаточности или гипертонии.
В состав белков человека входят 2 АК, содержащие серу, — метионин и цистеин. Эти аминокислоты метаболически тесно связаны между собой.
МЕТИОНИН
Метионин — незаменимая аминокислота, может регенерировать из гомоцистеина с участием серина и глицина. Метионин:
1. участвует в синтезе белков организма;
2. является источником метильной группы, используемой в реакциях трансметилирования;
3. является источником атома серы, необходимого для синтеза цистеина;
4. участвует в реакциях дезаминирования;
5. Метионил-тРНК участвует в инициации процесса трансляции.
Образование S-аденозилметионина
Метильная группа в метионине прочно связана с серой, поэтому донором этого одноуглеродного фрагмента служит активная форма метионина – S-аденозилметионин (SAM). (SAM — нестабилен т.к. сера при валентности 2 имеет 3 связи). SAM образуется при присоединении метионина к аденозину с участием метионинаденозилтрансферазы (есть во всех типах клеток). Аденозин образуется при гидролизе АТФ.
Ресинтез метионина, роль ТГФК и витамина В12.
Связь обменов метионина и цистеина
Реакции трансметилирования с участием S-аденозилметионина
Отщепление метильной группы от SAM и перенос её на соединение-акцептор катализируют ферменты метилтрансферазы. SAM в ходе реакции превращается в S-аденозилгомоцистеин (SAT).
Синтез холина и синтез лецитина
Аналогично синтезируются:
1. из ГАМК → карнитин;
2. из гуанидинацетата → креатин;
3. из норадреналина → адреналин;
4. из карнозина → анзерин;
5. Реакции трансметилирования используются также в синтезе азотистых оснований, инактивации гормонов, нейромедиаторов и обезвреживании ксенобиотиков.
ЦИСТЕИН
Цистеин – серосодержащая условнозаменимая АК. Синтезируется из незаменимого метионина и заменимого серина.
Нарушение синтеза цистеина возникает при гиповитаминозе фолиевой кислоты, В6, В12 или наследственных дефектах цистатионинсинтазы и цистатионинлиазы. Гомоцистеин превращается в гомоцистин, который накапливается в крови, тканях и выделяется с мочой.
Обмен цистеина: схема путей, их значение.
Цистеин:
- 1. используется в белках для формирования третичной структуры (дисульфидные мостики);
- 2. SH группы цистеина формируют активный центр многих ферментов;
- 3. идет на синтез глутатиона, таурина (парные желчные кислоты), НS-КоА, ПВК (глюкоза);
- 4. Является источником сульфатов, которые идут на синтез ФАФС или выделяются с мочой.
Образование сульфат-иона, его утилизация (образование ФАФС).
ФАФС используется:
1. В обезвреживании ксенобиотиков:
2. В синтезе гликозаминогликанов (сульфирование ОН групп производных глюкозы, галактозы сульфотрансферазой).
ФЕНИЛАЛАНИН
Фенилаланин — незаменимая АК, которая содержится в достаточных количествах в пищевых продуктах. Фенилаланин идет в основном на синтез белков и тирозина.
Превращение фенилаланина в тирозин необратимо катализирует фенилаланингидроксилаза (монооксигеназа), коферментом которой служит тетрагидробиоптерин (Н4БП), кофактором – Fe2+. Н4БП в результате реакции окисляется в дигидробиоптерин (Н2БП). Регенерация последнего происходит при участии дигидроптеридинредуктазы с использованием НАДФH2.
Реакция необходима для удаления избытка фенилаланина, так как высокие концентрации его токсичны для клеток. Образование тирозина не имеет большого значения, так как недостатка этой аминокислоты в клетках практически не бывает.
Фенилкетонурия
В печени здоровых людей небольшая часть фенилаланина (10%) превращается в фениллактат и фенилацетилглутамин. При дефекте фенилаланингидроксилазы этот путь катаболизма фенилаланина становится главным, что способствует развитию фенилкетонурии (ФКУ).
Классическая фенилкетонурия— наследственное заболевание, связанное с мутациями в гене фенилаланингидроксилазы (частота 1:10000 новорождённых), которые приводят к снижению активности фермента или полной его инактивации.
При ФКУ концентрация фен повышается в крови в 20—30 раз, в моче — в 100—300 раз по сравнению с нормой. В крови и моче повышается содержание метаболитов альтернативного пути: фенилпирувата, фенилацетата, фениллактата и фенилацетилглутамина.
Проявления фенилкетонурии:
1. нарушение умственного и физического развития;
2. судорожный синдром;
3. нарушение пигментации.
Проявления фенилкетонурии связаны с токсическим действием на клетки мозга высоких концентраций фенилаланина, фенилпирувата, фениллактата. Большие концентрации фенилаланина ограничивают транспорт тирозина и триптофана через гематоэнцефалический барьер и тормозят синтез нейромедиаторов (дофамина, норадреналина, серотонина).
Прогрессирующее нарушение умственного и физического развития у детей, больных ФКУ, можно предотвратить диетой с очень низким содержанием или полным исключением фенилаланина. Если такое лечение начато сразу после рождения ребёнка, то повреждение мозга предотвращается. Считается, что ограничения в питании могут быть ослаблены после 10-летнего возраста (окончание процессов миелинизации мозга), однако в настоящее время многие педиатры склоняются в сторону «пожизненной диеты». При отсутствии лечения больные не доживают до 30 лет.
Для диагностики фенилкетонурии используют качественные и количественные методы обнаружения патологических метаболитов в моче, определение концентрации фенилаланина в крови и моче.
Дефектный ген, ответственный за фенилкетонурию, можно обнаружить у фенотипически нормальных гетерозиготных носителей с помощью теста толерантности к фенилаланину.
ТИРОЗИН
Тирозин — условно заменимая АК, образуется из незаменимого фенилаланина. Содержание тир в пищевых белках достаточно велико.
Тирозин используется в синтезе белков, катехоламинов, тиреоидных гормонов и меланинов.
Обмен тирозина зависит от типа тканей.
1. Обмен тирозина в надпочечниках и нервной ткани
В мозговом веществе надпочечников и нервной ткани тирозин метаболизирует по катехоламиновому пути с образованием дофамина, норадреналина и адреналина (только в надпочечниках).
Тирозингидроксилаза (тирозинмонооксигеназа) Fe2+ -зависимый фермент, в качестве кофермента использующий Н4БП. Ее ингибирует норадреналин.
Дофамин и норадреналин служат медиаторами в синаптической передаче нервных импульсов, а адреналин — гормон широкого спектра действия, регулирующий энергетический обмен. Одна из функций катехоламинов — регуляция деятельности ССС.
Нарушение синтеза катехоламинов может вызывать различные нервно-психические заболевания, причём патологические отклонения наблюдаются как при снижении, так и при увеличении их количества. Снижение в нервных клетках содержания дофамина и норадреналина часто приводит к депрессивным состояниям. При шизофрении в височной доле мозга наблюдается гиперсекреция дофамина.
Болезнь Паркинсона
Болезнь Паркинсона развивается при снижении активности тирозинмонооксигеназы и ДОФА-декарбоксилазы, что приводит к недостаточности дофамина в чёрной субстанции мозга. Это одно из самых распространённых неврологических заболеваний (частота 1:200 среди людей старше 60 лет). Заболевание сопровождается акинезией (скованность движений), ригидностью (напряжение мышц) и тремором (непроизвольное дрожание).
Дофамин не проникает через гематоэнцефалический барьер и как лекарственный препарат не используется. Для лечения паркинсонизма используют заместительную терапию препаратами-предшественниками дофамина (производными ДОФА) — леводопа, мадопар, наком и др. Также подавляют инактивацию дофамина ингибиторами МАО (депренил, ниаламид, пиразидол и др.).
2. Обмен тирозина в меланоцитах
В пигментных клетках (меланоцитах) обмен тирозин идет по меланиновому пути. Из тирозина синтезируются пигменты — меланины 2 типов: эумеланины и феомеланины. Эумеланины (чёрного и коричневого цвета) — нерастворимые высокомолекулярные полимеры 5,6-дигидроксииндола. Феомеланины — жёлтые или красновато-коричневые полимеры, растворимые в разбавленных щелочах.
Меланины присутствуют в сетчатке глаз, в составе волос, в коже. Цвет кожи зависит от распределения меланоцитов и количества в них разных типов меланинов.
Альбинизм
При наследственном дефекте тирозиназы (1:20000) в меланоцитах нарушается синтез меланинов и развивается альбинизм.
Клиническое проявление альбинизма (от лат. albus — белый) — отсутствие пигментации кожи, сетчатки глаз и волос. У больных часто снижена острота зрения, возникает светобоязнь. Длительное пребывание таких больных под открытым солнцем приводит к раку кожи.
3. Превращение тирозина в щитовидной железе
В щитовидной железе из тирозина синтезируются и выделяются гормоны йодтиронины: тироксин (тетрайодтиронин) и трийодтиронин.
4. Катаболизм тирозина в печени
Катаболизм тирозина происходит в печени по гомогентизиновому пути (схема).
Фумарат может окисляться до СО2 и Н2О или использоваться для глюконеогенеза. Ацетоацетат — кетоновое тело, окисляемое до СО2 и Н2О с выделением энергии.
Алкаптонурия («чёрная моча»)
При наследственном дефекте диоксигеназы гомогентизиновой кислоты (2—5 случаев на 1 млн новорождённых) развивается алкаптонурия. При алкаптонурии происходит накопление в организме гомогентизиновой кислоты, избытки которой выделяются с мочой. На воздухе гомогентизиновая кислота окисляется с образованием тёмных пигментов – алкаптонов.
Клиническими проявлениями болезни, кроме потемнения мочи на воздухе, являются пигментация соединительной ткани (охроноз) и артрит.
Тирозинемии
Некоторые нарушения катаболизма тирозина в печени приводят к тирозинемии и тирозинурии.
Различают 3 типа тирозинемии.
- 1. Тирозинемия типа 1 (тирозиноз). Причиной заболевания является дефект фумарилацетоацетатгидролазы. Накапливающиеся метаболиты снижают активность некоторых ферментов и транспортных систем аминокислот. Патофизиология этого нарушения достаточно сложна. Острая форма тирозиноза характерна для новорождённых. Клинические проявления — диарея, рвота, задержка в развитии. Без лечения дети погибают в возрасте 6—8 мес из-за развивающейся недостаточности печени. Хроническая форма характеризуется сходными, но менее выраженными симптомами. Гибель наступает в возрасте 10 лет. Содержание тирозина в крови у больных в несколько раз превышает норму. Для лечения используют диету с пониженным содержанием тирозина и фенилаланина.
- 2. Тирозинемия типа II (синдром Рихнера—Ханхорта). Причина — дефект тирозинаминотрансферазы. Концентрация тирозина в крови больных повышена. Для заболевания характерны поражения глаз и кожи, умеренная умственная отсталость, нарушение координации движений.
- 3. Тирозинемия новорождённых (кратковременная). Заболевание возникает в результате снижения активности фермента п-гидроксифенилпируватдиоксигеназы. В результате в крови больных повышается концентрация п-гидроксифенилацетата, тирозина и фенилаланина. При лечении назначают бедную белком диету и витамин С.
ТРИПТОФАН
Триптофан – незаменимая АК. В физиологических условиях >95% триптофана метаболизирует по кинурениновому пути и 1% по серотониновому пути.
Схема кинуренинового пути
Серотонин образуется в надпочечниках, ЦНС и тучных клетках.
Серотонин – возбуждающий нейромедиатор средних отделов мозга (проводящих путей) и гормон. Стимулирует сокращение гладкой мускулатуры, вазоконстриктор, регулирует АД, температуру тела, дыхание, антидепрессант.
Образование и использование в организме ГАМК и ГОМК. Антиоксидантные, антигипоксические и адаптогенные свойства Глу, Асп, их клиническое применение.
ГЛУТАМАТ
Синтез глутамата
Глутамат образуется:
1). при восстановительном аминировании α-кетоглутарата глутаматдегидрогеназой:
2). В реакция переаминирования с участием аминотрансфераз:
Использование глутамата
- 1. Используется в синтезе белков, липидов, углеводов;
- 2. Ведущая роль в интеграции азотистого обмена. Обеспечивает реакции переаминирования АК: глутамат универсальный донор аминогруппы для синтеза заменимых АК (Ала, Асп, Асн, Сер, Гли, Глн, Про). Обеспечивает непрямое дезаминирование большинства АК. Участвует в обезвреживании аммиака с образованием глутамина;
- 3. Является источником α-КГ, необходимого для ЦТК и синтеза АТФ;
- 4. Входит в состав глутатиона;
Глутамат содержится в больших количествах в головном мозге, где выполняет разнообразные функции:
- 1. один из основных возбуждающих нейромедиаторов в коре, гиппокампе, полосатом теле и гипоталамусе;
- 2. используется для синтеза тормозного нейромедиатора ГАМК;
- 3. В виде пироглутамата (циклическая форма) входит в состав нейропептидов — люлиберина, тиролиберина, нейротензина, бомбезина и др.;
- 4. участвует в регуляции процессов памяти;
- 5. глутамат служит источником янтарной кислоты (сукцинат), которая может окисляться при гипоксии, давая АТФ (антигипоксант);
- 6. участвует в обезвреживании аммиака с образованием глутамина
Нарушение обмена глутамата приводит к целому ряду патологических нарушений ЦНС: эпилепсии, расстройствах вестибулярной системы, ишемии и др. Глутамат и его аналоги используют как лекарственные средства при хронической недостаточности аминокислотного обмена, вегетососудистой дистонии, эпилепсии (в качестве предшественника ГАМК — тормозного медиатора).
ГЛУТАМИН
Синтез глутамина
Использование глутамина
1. Используется в синтезе белков, углеводов;
2. Источник азота в синтезе пуриновых и пиримидиновых оснований, аспарагина, аминосахаров;
3. Обеспечивает транспорт азота из тканей;
АСПАРТАТ
Синтез аспартата
Использование аспартата
1. Используется в синтезе белков, липидов, углеводов;
2. Участвует в орнитиновом цикле при синтезе мочевины;
3. Участвует в синтезе карнозина, анзерина, пуриновых и пиримидиновых нуклеотидов, N-ацетиласпарагиновой кислоты.
АСПАРАГИН
Синтез аспарагина
Использование аспарагина
1. Используется в синтезе белков, липидов, углеводов;
http://zdamsam.ru/a16213.html
http://farmf.ru/lekcii/aminokisloty-obshhie-puti-obmena-aminokislot-sintez-mocheviny/