Гидрокарбонат натрия
| Гидрокарбонат натрия | |
|---|---|
 | |
 | |
| Систематическое наименование | гидрокарбонат натрия |
| Традиционные названия | пищевая (питьевая) сода, сода двууглекислая, двууглекислый натрий, бикарбонат натрия, кислый углекислый натрий |
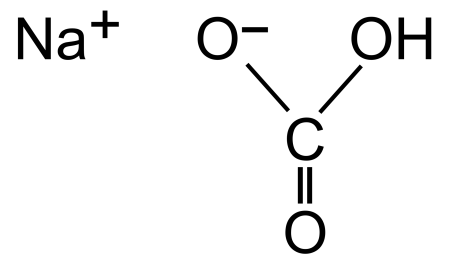
| Хим. формула | CHNaO₃ |
| Рац. формула | NaHCO3 |
| Состояние | твёрдое |
| Молярная масса | 84,0066 г/моль |
| Плотность | 2,159 г/см³ |
| Т. разл. | 60—200 °C |
| Растворимость в воде | 9,59 г/100 мл |
| ГОСТ | ГОСТ 2156-76 ГОСТ 4201-79 ГОСТ 32802-2014 |
| Рег. номер CAS | 144-55-8 |
| PubChem | 516892 |
| Рег. номер EINECS | 205-633-8 |
| SMILES | |
| Рег. номер EC | 205-633-8 |
| Кодекс Алиментариус | E500(ii) |
| RTECS | VZ0950000 |
| ChEBI | 32139 |
| ChemSpider | 8609 |
| ЛД50 | 4220 мг/кг |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Гидрокарбонат натрия (лат. Natrii hydrocarbonas ), другие названия: бикарбонат натрия, чайная сада, питьевая или пищевая сода, двууглекислый натрий — неорганическое соединение, натриевая кислая соль угольной кислоты с химической формулой NaHCO3.
В обычном виде — мелкокристаллический порошок белого цвета.
Используется в промышленности, пищевой промышленности, в кулинарии, в медицине как нейтрализатор химических ожогов кожи и слизистых оболочек концентрированными кислотами и для снижения кислотности желудочного сока. Также применяется в буферных растворах.
Содержание
- 1 Химические свойства
- 1.1 Реакция с кислотами
- 2 Термическое разложение
- 3 Получение
- 4 Применение
- 4.1 В химической промышленности
- 4.2 В кулинарии
- 4.3 В медицине
- 4.3.1 Противопоказания к применению в медицинских целях
- 4.4 Пожаротушение
- 4.5 В быту
- 4.6 В транспорте
- 5 Производство
- 6 Хранение
- 7 Безопасность
Химические свойства
Гидрокарбонат натрия — кислая натриевая соль угольной кислоты. Проявляет все свойства соли сильного основания и слабой кислоты. В водных растворах имеет слабощелочную реакцию. В широком диапазоне концентраций в водном растворе pH раствора изменяется незначительно, на этом основано применение раствора вещества в качестве буферного раствора.
Реакция с кислотами
Гидрокарбонат натрия реагирует с кислотами с образованием соответствующей кислоте соли, например, хлорида натрия, сульфата натрия и угольной кислоты, которая в процессе реакции распадается на углекислый газ и воду, при этом углекислый газ выделяется из раствора в виде пузырьков:
В быту обычно применяется реакция «гашения соды» уксусной кислотой, с образованием ацетата натрия или гашение лимонной кислотой с образование цитрата натрия, реакция с уксусной кислотой:
Термическое разложение
При температуре выше 60 °C гидрокарбонат натрия начинает распадаться на карбонат натрия, углекислый газ и воду (процесс разложения наиболее эффективен при 200 °C, при более высоких температурах карбонат натрия начинает распадаться на оксид натрия и углекислый газ):
При этом процессе выделения воды в виде водяного пара и углекислого газa масса исходного продукта уменьшается примерно на 37 %.
Получение
В промышленности гидрокарбонат натрия получают аммиачно-хлоридным способом. В концентрированный раствор хлорида натрия, насыщенный аммиаком, под давлением пропускают углекислый газ. В процессе синтеза происходят две реакции:
В холодной воде гидрокарбонат натрия мало растворим, и его отделяют от охлаждённого раствора фильтрованием, а из полученного после фильтрования раствора хлорида аммония снова получают аммиак, возвращаемый в производство вновь:
Применение
Двууглекислый натрий (бикарбонат) применяется в химической, пищевой, лёгкой, медицинской, фармацевтической промышленности, цветной металлургии, в быту. Зарегистрирован в качестве пищевой добавки E500 (ii), входит в состав пищевой добавки E500.
В химической промышленности
Применяется для производства красителей, пенопластов и других органических продуктов, фторорганических соединений, продуктов бытовой химии, наполнителей в огнетушителях, Реагент для отделения диоксида углерода, сероводорода из газовых смесей, например, отходящих газов топливосжигающих установок. В этом процессе углекислый газ поглощается раствором гидрокарбоната натрия при повышенном давлении и пониженной температуре, далее поглощённый углекислый газ выделяется из раствора при подогреве и снижении давления;
В лёгкой промышленности — в производстве резины для подошв обуви и в производстве искусственных кож, кожевенном производстве при дублении и нейтрализации кожи после кислого дубления, текстильной промышленности при отделке шёлковых и хлопчатобумажных тканей;
В пищевой промышленности — в хлебопечении, производстве кондитерских изделий, приготовлении газированных напитков.
В кулинарии
Основное применение пищевой соды в пищевой промышленности и в быту — кулинария, где применяется, преимущественно, в качестве основного или дополнительного разрыхлителя в составе кислого и пресного теста. При добавлении питьевой соды в кислое тесто происходит реакция с молочной кислотой, продуцированной при заквашивании дрожжевыми микроорганизмами, при этой реакции выделяется углекислый газ, вспучивающий тесто.
При добавлении в пресное тесто углекислый газ выделяется при выпечке из-за термического разложения.
При применении соды в чистом виде важно соблюсти правильную дозировку, так как она оставляет в продукте карбонат натрия, дающий определённый привкус. Порядок замешивания для теста: соду — в муку, кислые компоненты (уксус, кефир и пр.) — в жидкость.
В медицине
Традиционно раствор питьевой соды используется для дезинфекции зубов и дёсен при зубных болях и полости рта и горла, при сильном кашле, ангине, фарингите, а также как общепринятое средство от изжоги и болей в желудке.
Применяется при заболеваниях, сопровождающиеся выраженным ацидозом (при диабете, инфекциях и др), для борьбы с ацидозом при хирургических вмешательствах (назначается 3-5 г. внутрь).
Применяется в качестве антиаритмического средства.
Как антацидное средство (как и все другие щелочи) применяется при язвенной болезни желудка, и двенадцатиперстной кишки, при повышенной кислотности желудочного сока.
Имеются так же данные о применении препарата (в виде капельных и внутривенных вливаний) при гипертонической болезни, симптоматической почечной гипертонии, и хронической почечной недостаточности. Эффект связан с увеличением выделения ионов натрия и хлора и возрастанием осмотического диуреза.
В виде свечей применяется против укачивания при морской и воздушной болезнях
Применяется в качестве отхаркивающего средства, т.к. повышая щелочные резервы крови, сдвигает в щелочную сторону реакцию бронхиальной слизи, делая мокроту менее вязкой.
При ринитах, конъюнктивитах, стоматитах, ларингитах и т.п. применяют для полосканий, промываний, ингаляций 0,5 — 2% р-ры гидрокарбоната натрия.
Применяется внутривенно с целью быстрого устранения метаболического ацидоза во время реанимационных мероприятий, заболеваниях почек.
Нужно иметь ввиду, что в результате применения может возникнуть т.н. кислотный рикошет (при реакции содой с соляной кислотой происходит выделение CO2, который оказывает раздражающее действие на стенку желудка, усиливая выделение гастрина).
В альтернативной медицине питьевая сода иногда заявляется как «лекарство» от рака, однако, никакой экспериментально подтверждённой эффективности применения такого «лечения» не существует.
Противопоказания к применению в медицинских целях
Индивидуальная гиперчувствительность; состояния, сопровождающиеся развитием алкалоза; гипокальциемия, при приеме внутрь усиливает алкалоз и повышает риск развития тетанических судорог, гипохлоремия — снижение концентрации в крови ионов Cl — , в том числе вызванная рвотой, или снижением всасывания в желудочно-кишечном тракте, может привести к тяжёлому алкалозу.
Является источником натрия, тем самым увеличивая объём циркулирующей крови, усугубляя отёки и повышая артериальное давление. Применение при сниженной скорости клубочковой фильтрации может привести к метаболическому алкалозу.
Пожаротушение
Гидрокарбонат натрия вместе с карбонатом аммония используется в качестве наполнителя в огнетушителях с сухим наполнением и в стационарных системах сухого пожаротушения. Это применение обусловлено тем, что от воздействия высокой температуры в очаге горения вещество выделяет углекислый газ, атмосфера которого затрудняет доступ кислорода воздуха в очаг горения.
В быту
Применяется как безопасное для здоровья средство для чистки поверхностей столовой и кухонной посуды, поверхностей кухонных столов, иных поверхностей, соприкасающихся с пищей, путем протирки их с помощью влажной тряпки с сухим порошком питьевой соды.
В транспорте
Применяется для нейтрализации следов электролита — серной кислоты на поверхности пластмассовых корпусов свинцовых аккумуляторов насыщенным водным раствором питьевой соды.
Производство
В Российской Федерации двууглекислый натрий выпускается в соответствии с требованиями и техническими условиями, выпускается на предприятиях АО «Башкирская содовая компания» в г. Стерлитамак, Республика Башкортостан, а также на Крымском содовом заводе в г. Красноперекопск, Крымский полуостров.
Хранение
Гидрокарбонат натрия хранят в закрытых упаковках, в сухом месте вдали от источников огня. Гарантийный срок хранения натрия двууглекислого — 12 месяцев со дня изготовления. Срок годности не ограничен.
Безопасность
Вещество нетоксично, пожаро- и взрывобезопасно.
Имеет солоноватый, мыльный вкус. При попадании пыли вещества на слизистые оболочки глаз и носа вызывает лёгкое раздражение. При частой работе в атмосфере, загрязнённой пылью двууглекислого натрия, может возникнуть раздражение верхних дыхательных путей. Предельно допустимая концентрация пыли бикарбоната натрия в воздухе производственных помещений 5 мг/м 3 .
- ГОСТ 2156-76. Натрий двууглекислый. Технические условия (с Изменениями № 1, 2, 3, 4).
- ГОСТ 32802-2014. Добавки пищевые. Натрия карбонаты E500. Общие технические условия.
Без усилий отмыть даже многолетний нагар быстро и просто. Рабочий рецепт
Со временем на посуде, особенно дачной, может появиться вот такой сильный нагар, отмыть который, казалось бы, можно только титаническими усилиями.
Однако есть очень простой, но рабочий способ отмыть любую посуду без изнурительного оттирания, даже если она имеет многолетний нагар.
Вам потребуются:
- вода;
- пищевая сода;
- хозяйственное мыло;
- лимонная кислота
Для этой процедуры лучше всего использовать достаточно большую емкость или по крайней мере ту, в которую без труда поместится отмываемая посуда. Кроме того желательно, чтобы у вас была возможность поставить выбранную емкость на плиту.
Итак в выбранной емкости подогреваем воду, после чего в теплую воду добавляем 2 ст. л. соды, 2 ст. л. хозяйственного мыла, жидкого или натертого на терке, а также 1 ст. л. лимонной кислоты. После добавления лимонной кислоты произойдет реакция, поэтому необходимо проследить за тем, чтобы получившийся раствор «не убежал».
Опускаем посуду, которую вы хотите отмыть, в рабочий состав и ставим на плиту на медленный огонь. Кипятим посуду не более 7 минут.
Вот и все, теперь весь нагар без труда отстает от поверхности, он буквально снимается слоями. Небольшие частички также легко отмываются губкой.
Кроме того получившийся чистящий раствор можно использовать повторно и одной кастрюлей перемыть гору посуды.
А ниже вы можете посмотреть видео об этом простом и эффективном способе отмыть даже многолетний нагар.
Эффективные способы гашения соды лимонной кислотой
7 мин на чтение
Пищевая сода – один из наиболее широко используемых разрыхлителей в выпечке, однако до сих пор некоторые хозяйку задаются вопросом — как погасить соду лимонной кислотой. Рассмотрим эту пищевую добавку более подробно, а так же научимся использовать в кулинарии.
Также известное как бикарбонат натрия, это химическое соединение встречается в природе в кристаллическом виде, а для последующего использования в кулинарии или быту его измельчают до мелкого порошка.
Принцип работы пищевой соды в выпечке
Пищевая сода известна любой хорошей домохозяйке и пекарю. Это щелочное соединение выделяет углекислый газ, маленькие пузырьки которого начинают активно работать над тестом, заставляя его подняться быстрее. Также благодаря возникающим процессам формируется структура теста, что делает его воздушным и «пушистым».
Для ускорения процесса выделения углекислого газа можно воздействовать на пищевую соду тремя способами:
Смешивание с кислотными соединениями
Наилучшим способом, гарантирующим отличный результат, является добавление на стадии замешивания теста кислотных соединений. Это может быть уксус, йогурт, кефир или лимонная кислота. Так что, если в рецептуре выпечки присутствует кисломолочный продукт, то переживать о дополнительном добавлении кислот не нужно. Добавленные в выпечку мелиса или мед, хотя это и кажется невероятным, также активируют реакцию пищевой соды.
Реакция с теплом
Пищевая сода будет производить углекислый газ при воздействии тепла даже без добавления кислот. Минимальная температура для начала этого процесса – 80 С. Данный способ хоть и быстрый, но не гарантирует получение воздушной структуры теста.
Использование кислот и тепла
Самые опытные домохозяйки объединяют два варианта в один. Тесто, в которое добавили пищевую соду и кислоту, накрывается полотенцем и ставиться на 1 час в теплое место (достаточно поместить его на включенную батарею). Под воздействием тепла тесто начинает медленно подниматься и становиться легким и, как может показаться, пушистым. Максимальный подъем теста будет происходить уже в духовке, где воздействие температур более сильное — это завершающий аккорд действия углекислого газа.
Пищевая сода часто работает настолько быстро, что этот процесс можно буквально наблюдать в режиме реального времени. А готовая сдоба может поразить любого своей нежной и пористой структурой, полученной благодаря разложению соды в процессе выпечки.
Отличия между пищевой содой и разрыхлителем
При попытке заменить в рецептуре выпечки разрыхлитель на пищевую соду, можно потерпеть фиаско, поскольку два эти вещества, несмотря на колоссальное сходство, работают по-разному. Пищевая сода — это “чистый” бикарбонат натрия, без добавления каких-либо веществ. Разрыхлитель — это та же пищевая сода со “встроенной” кислотой. В разрыхлителе кислота находится в виде солей, поэтому она не реагирует с основным компонентом (пищевой содой). Для начала реакции необходимо только добавить жидкость. Поэтому недостаточно просто заменить разрыхлитель на соду. Необходимо учитывать добавление к последней кислотного компонента, например, лимонной кислоты.
Как проверить свежесть соды
Многие утверждают, что у пищевой соды нет срока годности. Она стоит на полке у каждого уважающего себя человека и, ввиду использования в небольших дозировках (в выпечке необходима всего 1 ч. ложка), может простоять в шкафу годы. Поэтому стоит отметить, что сода имеет свойство разлагаться со временем. И чтобы не разочароваться в ней в случае неудач в хлебопекарном деле, стоит проверить её эффективность заранее.
Для этого не нужно отправлять щелочь в лабораторию. Достаточно провести простой эксперимент в домашних условиях. Просто добавьте щепотку пищевой соды к небольшому количеству лимонной кислоты (уксуса) в миске. Появление пены является подтверждением того, что сода всё ещё активна и будет работать.
Правила гашения пищевой соды
Рассмотрим, как гасится сода лимонной кислотой.
Для достижения сильного эффекта, к пищевой соде необходимо добавить кислоту, которая подействует как катализатор и запустит реакцию быстрее. Этот процесс называется гашение соды. При соблюдении необходимых условий, кислотно-щелочная реакция будет сильной и устойчивой на протяжении всего процесса выпечки.
Очень важно, чтобы процесс выделения углекислого газа происходил непосредственно в тесте. В противном случае, он будет расходоваться зря, и желаемый эффект не будет достигнут. Более того, при гашении соды «на стороне», есть риск вместо пористой структуры получить лишь мыльный привкус. Поэтому опытные пекари советуют смешать отдельно все сухие и жидкие (в том числе и кислоты для гашения) компоненты рецептуры по отдельности, а потом объединить их в ёмкость, где будет готовиться тесто.
Если при замешивании теста будет допущена ошибка, то выделение газа будет минимальным и, вполне возможно, тесто не поднимется вовсе.
Использование лимонной кислоты для гашения: пропорции
Самый распространенный способ гашения пищевой соды – добавление к ней лимонной кислоты. Начинающим стоит обратить своё внимание на неё, поскольку при использовании этого компонента можно не бояться испортить вкус выпечки при ошибках в пропорциях. Можно использовать как порошок лимонной кислоты, так и сок лимона.
При использовании сока лимона не требуется никаких подготовительных операций. На 1 ч. ложку соды требуется всего 10 ч. ложек лимонного сока. Необходимо только помнить, что компоненты добавляются по правилам “правильного гашения”.
Лимонную кислоту необходимо перед добавлением в замес заранее развести с водой. Для этого потребуется треть стакана воды. Такое же количество понадобится и для соды. Жидкие компоненты смешиваются в отдельной ёмкости, после чего добавляются к муке и соде.
Как сделать разрыхлитель в домашних условиях
Приготовление домашнего разрыхлителя очень простое, с ним справится даже новичок. Более того, это сократит затраты во времени в будущем — не придется каждый раз производить подготовку кислоты и соды.
Для приготовления разрыхлителя понадобится:
- Мука пшеничная — 12 ч.л.
- Пищевая сода — 5 ч.л.
- Лимонная кислота — 3 ч.л.
Смешайте все компоненты и тщательно встряхните ёмкость для их равномерного распределения по всему объему тары. Полученный разрыхлитель добавляется сразу в муку при приготовлении замеса.
Хранить его стоит в сухом темном месте. Срок хранения не отличается от срока годности обычной пищевой соды.
Альтернативные способы гашения соды
Определенно бывают случаи, когда дома не оказалось лимонной кислоты или лимона. Поэтому важно рассмотреть использование других кислот для гашения пищевой соды.
Гашение соды уксусом столовым 9%
Использование этой кислоты также распространено, как и лимонной. Единственная опасность таится в том, что при случайной ошибке в дозе в большую сторону можно получить на выходе выпечку с горьковатым привкусом. Поэтому методика смешивания жидких и сухих компонентов по отдельности для начинающего не подойдет.
При использовании уксуса гашение соды лучше проводить отдельно от всех компонентов. Наберите необходимое количество соды (обычно, это не больше 1 ч. ложки) и добавьте к ней несколько капель уксуса. Как только смесь начнет пузыриться и шипеть (это значит, что кислоты достаточно), добавьте ее в замес.
Гашение соды яблочным уксусом
Технология использования этой кислоты аналогична с технологией при гашении соды столовым уксусом. Единственная разница лишь в том, что яблочный уксус даёт меньше горечи.
Гашение соды кисломолочными продуктами
При использовании кефира или сметаны, так же как и с лимонной кислотой, можно не бояться совершить промах в дозировке. Они никак не испортят вкусовые качества готового продукта. Соотношение гашения соды составляет 1:1, то есть на 1 ч.ложку щелочи понадобится всего 1 ч.ложка кислоты.
Если же рецептура предполагает использование в ней кисломолочным продуктов, то просто добавьте соду в тесто. Дополнительное добавление кислот уже не потребуется.
Рецепты
Рецепт бананового пирога с черникой
Этот пирог прост в приготовлении, и не требует особых знаний. Для пирога понадобятся следующие ингредиенты:
- мука – 1 стакана;
- пищевая сода – 1 ч.л.;
- лимонная кислота – 1 ч.л.;
- сливочное масло – 80 г;
- соль – 1 ч.л.;
- сахар – стакана;
- яйца куриные – 3 шт.;
- бананы – 4 шт. (можно переспелые);
- черника – стакана.
- Смешайте муку, соду и соль.
- В отдельной миске смешайте масло и сахар. Хорошо перемешайте, после чего добавьте яйца, ванилин и заранее разведенную лимонную кислоту.
- Бананы нарежьте небольшими кусочками и равномерно распределите их вместе с черникой на дно формы для выпечки.
- Смешайте жидкую смесь с сухими компонентами и тщательно перемешайте – тесто должно получиться жидким.
- Вылейте жидкое тесто в форму для выпечки, равномерно покрывая выложенные в ней фрукты и ягоды.
- Поставьте будущий пирог в заранее разогретую до 80С духовку и выпекайте пирог в течение 50 минут.
Готовность пирога можно проверить спичкой. После её погружения в пирог спичка должна остаться сухой, без остатков теста.
Оладьи без дрожжей с использованием соды и лимонной кислоты
Понадобятся следующие ингредиенты:
- мука – 2 стакана;
- пищевая сода – ч.л.;
- лимонная кислота – ч.л.;
- вода питьевая – 250 мл;
- сахар – стакана;
- яйцо куриное – 1 шт.;
- масло подсолнечное — 2 ст.л.
- Взбейте яйца с сахаром до получения пышной плотной пены.
- Влейте в полученную смесь воду, лимонную кислоту и подсолнечное масло.
- Муку необходимо просеять (для лучшего поступления в тесто кислорода), после чего добавьте к ней пищевую соду.
- Смешайте сухие и жидкие компоненты в одной ёмкости и хорошо перемешайте.
Обжаривайте оладьи на хорошо нагретой сковороде до готовности.
http://cpykami.ru/bez-usilij-otmyt-dazhe-mnogoletnij-nagar/
http://povkusu.guru/kak-pogasit-sodu-limonnoj-kislotoj-dejstvennye-sposoby/







