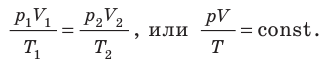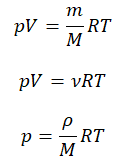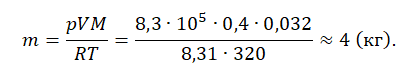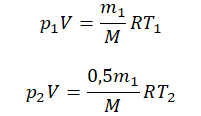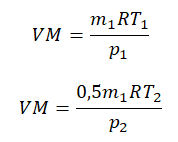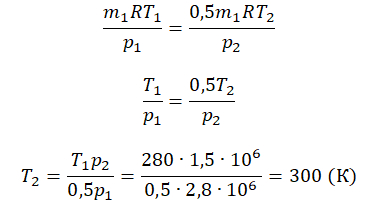Итоговое задание по физике.
тест (физика, 11 класс) по теме
Данное задание я предлагаю обучающимся по завершению изучения учебной дисциплины «Физика». Предложенные вопросы различного уровня сложности имеют отношение к каждому основному разделу физики.
Скачать:
| Вложение | Размер |
|---|---|
| itogovoe_zadanie_po_fizike.doc | 243.5 КБ |
Предварительный просмотр:
Итоговое задание по физике. Вариант 1.
При выполнении заданий части 1 в бланке ответов №1 под номером выполняемого вами задания (А1-А25)поставьте знак «+» в клеточке, номер которой соответствует номеру выбранного вами ответа.
Скорость тела за 3 с увеличилась от 2 м/с до 8 м/с. Выберите правильное утверждение.
- Ускорение тела 2 м/с 2
- Ускорение тела 3,3 м/с 2
- Ускорение тела 6 м/с 2
Тело массой 200 г движется с ускорением 0,5 м/с 2 . Выберите правильное утверждение.
- Равнодействующая всех приложенных к телу сил равна 0,1 Н.
- Равнодействующая всех приложенных к телу сил равна 100 Н.
- Равнодействующая всех приложенных к телу сил равна 0.
Снаряд, летевший горизонтально со скоростью 20 м/с, разорвался на два осколка массами 2 кг и 3 кг. Выберите правильное утверждение. Сопротивлением воздуха можно пренебречь.
- Импульс снаряда до взрыва был равен 100 кг м/с.
- После взрыва импульс снаряда стал равным нулю.
- Импульсы осколков снаряда при движении после взрыва не изменяются .
Сосулька падает с крыши дома. Считая, что сопротивлением воздуха можно пренебречь, выберите правильное утверждение.
- Потенциальная энергия сосульки в конце падения максимальна.
- Кинетическая энергия сосульки при падении не изменяется.
- Полная механическая энергия сосульки сохраняется.
Что является наиболее наглядным опытным подтверждением движения молекул? Выберите правильное утверждение.
- Броуновское движение.
- Наблюдение с помощью оптического микроскопа.
- Существование твёрдых тел.
Как нужно изменить объём данной массы газа для того, чтобы при постоянной температуре его давление уменьшилось в 4 раза? Выберите правильное утверждение.
- Увеличить в 2 раза.
- Увеличить в 4 раза.
- Уменьшить в 4 раза.
За 5 с маятник совершил 20 колебаний. Выберите правильное утверждение.
- Период колебаний 0, 25 с.
- Частота колебаний 100 Гц.
- Период колебаний 4 с.
Уравнение состояния газа устанавливает связь между …..(выберите правильное утверждение)
1….объёмом и количеством молекул.
2….температурой, объёмом и давлением газа.
3….средней кинетической энергией молекул и температурой газа.
С газом выполняют указанные ниже процессы. При каком процессе работа газа равна нулю? Выберите правильный ответ.
- При изотермическом сжатии.
- При изобарном охлаждении.
- При изохорном нагревании.
Как изменится сила кулоновского взаимодействия при увеличении каждого заряда в три раза, если расстояние между ними уменьшить в два раза? Выберите правильный ответ.
- Увеличится в 6 раз.
- Уменьшится в 2 раза.
- Увеличится в 36 раз.
Точечные заряды расположили в вершинах квадрата (смотри рисунок). Как они взаимодействуют? Выберите правильный ответ.
- Стягиваются к центру.
- Расходятся от центра.
- Остаются в равновесии .
Как изменятся показания вольтметра и амперметра, если ползунок реостата перемещать вправо? (смотри рисунок). Выберите правильный ответ.
- Показания амперметра увеличатся, вольтметра уменьшатся.
- Показания амперметра уменьшатся, вольтметра увеличатся.
- Показания амперметра возрастают, вольтметра не меняются.
Что возникает в контуре при изменении в нём магнитного потока? Выберите правильный ответ.
- ЭДС индукции и ток индукции.
- ЭДС индукции.
- Ничего не возникает .
Выберите из предложенных вариантов определение правила Ленца.
- Индукционный ток имеет такое направление, что препятствует изменению магнитного поля.
- Индукционный ток имеет такое направление, что его магнитное поле способствует изменению магнитного поля, его вызвавшего.
- Индукционный ток всегда имеет такое направление, что своим магнитным полем препятствует изменению поля, его вызвавшего .
От чего зависит ЭДС индукции, возникающая в катушке? Выберите правильный ответ.
- От числа витков и скорости изменения магнитного потока.
- От числа витков.
- От скорости изменения магнитного потока .
За счёт чего поддерживается ток в колебательном контуре, когда появляющаяся на конденсаторе разность потенциалов препятствует его протеканию? Выберите правильный ответ.
- За счёт увеличения энергии магнитного поля катушки.
- За счёт увеличения заряда на конденсаторе.
- За счёт уменьшения энергии магнитного поля катушки
В колебательном контуре ёмкость увеличена в 4 раза. Что нужно сделать, чтобы период колебаний остался прежний? Выберите правильный ответ.
- Уменьшить индуктивность в 4 раза.
- Увеличить индуктивность в 4 раза.
- Уменьшить индуктивность в 2 раза.
В качестве ротора часто используют многополюсный магнит для… Выберите правильный ответ.
- Увеличения ЭДС генератора.
- Получения тока высокой частоты (50Гц) при малых оборотах ротора.
- Уменьшения частоты тока при больших оборотах ротора .
От каких величин зависит частота генерируемого тока? Выберите правильный ответ.
- Только от числа оборотов в единицу времени.
- Только от числа пар магнитных полюсов.
- От числа оборотов в единицу времени и пар магнитных полюсов.
Какие из указанных на рисунке поверхностей зеркальные? Выберите правильный ответ.
- 1 и 3
- 2 и 4
- 2 и 3
Угол падения луча на зеркальную поверхность равен 15 о . Чему равен угол отражения? Выберите правильный ответ.
- 30 о
- 40 о
- 15 о
Луч света падает на поверхность воды. На каком из рисунков правильно показан ход преломленного луча?
Как называется явление испускания электронов веществом под действием электромагнитных излучений? Выберите правильный ответ.
- Электролиз.
- Ударная ионизация.
- Фотоэффект.
Из атомного ядра в результате самопроизвольного превращения вылетело ядро атома гелия. Какой это вид радиоактивного распада? Выберите правильный ответ.
- α– распад.
- β– распад.
- γ– излучение .
Атомное ядро висмута в результате ряда радиоактивных превращений превратилось в ядро свинца . Какие виды радиоактивных превращений оно испытало? Выберите правильный ответ.
- β-распад.
- Два α-распада.
- β- распад и α-распад.
Ответом к каждому из заданий В1 – В2 будет некоторая последовательность цифр. Эту последовательность надо записать в бланк ответов справа от номера соответствующего задания без пробелов и каких – либо символов, начиная с наименьшей цифры.
В сосуде неизменного объёма находилась при комнатной температуре смесь двух идеальных газов, по 1 моль каждого. Половину содержимого сосуда выпустили, а затем добавили в сосуд 1 моль первого газа. Температура газов в сосуде поддерживалась неизменной. Как изменились в результате парциальные давления газов и их суммарное давление?
Для каждой величины определите соответствующий характер изменения:
- увеличилось
- уменьшилось
- не изменилось
Запишите в таблицу выбранные цифры для каждой физической величины. Цифры в ответе могут повторяться.
Парциальное давление первого газа
Парциальное давление второго газа
Давление смеси газов в сосуде
Установите соответствие между физическими явлениями и приборами, в которых используются или наблюдаются эти явления.
ФИЗИЧЕСКИЕ ЯВЛЕНИЯ ПРИБОР
А) Ионизация газа 1) Дифракционная решётка
Б) Линейчатый спектр 2) Просветлённый объектив
3) Счётчик Гейгера
4) Призменный спектроскоп
Ответом к заданиям В3-В4 будет некоторое число. Это число надо записать в бланк ответов справа от номера соответствующего задания. Единицы физических величин писать не нужно.
Лыжник массой 60 кг, имеющий в конце спуска с горы скорость 10 м/с, остановился через 40 с после окончания спуска. Определите модуль силы сопротивления движению.
Какова индукция магнитного поля, в котором на проводник с длиной активной части 5 см действует сила 50 мН? Сила тока в проводнике 25 А. Проводник расположен перпендикулярно вектору индукции магнитного поля.
Решение задания С1 части 3 должно быть представлено с развёрнутым ответом.
Человек в очках вошёл с улицы в тёплую комнату и обнаружил, что его очки запотели. Какой должна быть температура на улице, чтобы наблюдалось это явление? В комнате температура воздуха 22 о С, а относительная влажность воздуха 50%. Поясните, как вы получили ответ.
(При ответе на этот вопрос воспользуйтесь таблицей для давления насыщенных паров воды).
Давление насыщенных паров воды при различных температурах.
Уравнение состояния идеального газа — основные понятия, формулы и определение с примерами
Содержание:
Уравнение состояния идеального газа:
Уравнения Клапейрона и Менделеева — клапейрона; законы Шарля, Гей-Люссака, Бойля — Мариотта, Авогадро, Дальтона, — пожалуй, такого количества «именных» законов нет ни в одном разделе физики. за каждым из них — кропотливая работа в лабораториях, тщательные измерения, длительные аналитические размышления и точные расчеты. нам намного проще. Мы уже знаем основные положения теории, и «открыть» все вышеупомянутые законы нам не составит труда.
Уравнение состояния идеального газа
Давление газа полностью определяется его температурой и концентрацией молекул: p=nkT. Запишем данное уравнение в виде: pV = NkT. Если состав и масса газа известны, число молекул газа можно найти из соотношения
Произведение числа Авогадро 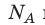
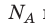
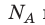
Обратите внимание! Состояние данного газа некоторой массы однозначно определяется двумя его макроскопическими параметрами; третий параметр можно найти из уравнения Менделеева — Клапейрона.
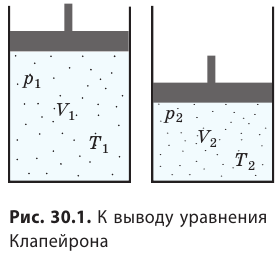
Уравнение Клапейрона
С помощью уравнения Менделеева — Клапейрона можно установить связь между макроскопическими параметрами газа при его переходе из одного состояния в другое. Пусть газ, имеющий массу m и молярную массу М, переходит из состояния (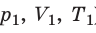
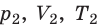
Для каждого состояния запишем уравнение Менделеева — Клапейрона: 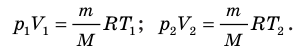
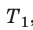
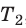
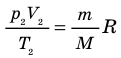
Для данного газа некоторой массы отношение произведения давления на объем к температуре газа является неизменным.
Изопроцессы
Процесс, при котором один из макроскопических параметров данного газа некоторой массы остается неизменным, называют изопроцессом. Поскольку состояние газа характеризуется тремя макроскопическими параметрами, возможных изопроцессов тоже три: происходящий при неизменной температуре; происходящий при неизменном давлении; происходящий при неизменном объеме. Рассмотрим их.
Какой процесс называют изотермическим. Закон Бойля — Мариотта
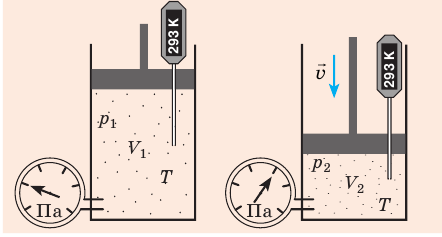
Пузырек воздуха, поднимаясь со дна глубокого водоема, может увеличиться в объеме в несколько раз, при этом давление внутри пузырька падает, поскольку вследствие дополнительного гидростатического давления воды (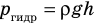
Рис. 30.2. Изотермическое сжатие газа. Если медленно опускать поршень, температура газа под поршнем будет оставаться неизменной и равной температуре окружающей среды. Давление газа при этом будет увеличиваться
Изотермический процесс — процесс изменения состояния данного газа некоторой массы, протекающий при неизменной температуре.
Пусть некий газ переходит из состояния (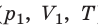
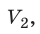
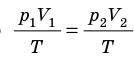
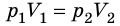
Закон Бойля — Мариотта:
Для данного газа некоторой массы произведение давления газа на его объем остается постоянным, если температура газа не изменяется:
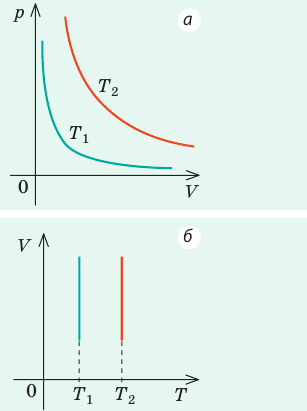
Графики изотермических процессов называют изотермами. Как следует из закона Бойля — Мариотта, при неизменной температуре давление газа данной массы обратно пропорционально его объему: 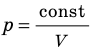
Какой процесс называют изобарным. Закон Гей-Люссака
Изобарный процесс — процесс изменения состояния данного газа некоторой массы, протекающий при неизменном давлении.
Пусть некий газ переходит из состояния (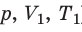
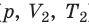
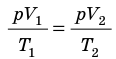
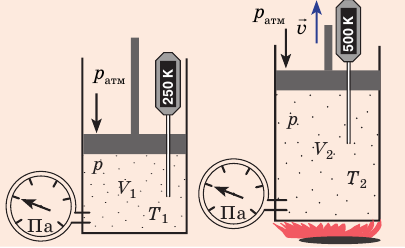
Рис. 30.4. Изобарное расширение газа. Если газ находится под тяжелым поршнем массой M и площадью S, который может перемещаться практически без трения, то при увеличении температуры объем газа будет увеличиваться, а давление газа будет оставаться неизменным и равным p
Закон Гей-Люссака
Для данного газа некоторой массы отношение объема газа к температуре остается постоянным, если давление газа не изменяется:
Графики изобарных процессов называют изобарами. Как следует из закона Гей-Люссака, при неизменном давлении объем газа данной массы прямо пропорционален его температуре: V = const⋅T. График данной зависимости — прямая, проходящая через начало координат (рис. 30.5, а). По графику видно, что с приближением к абсолютному нулю объем идеального газа должен уменьшиться до нуля. Понятно, что это невозможно, поскольку реальные газы при низких температурах превращаются в жидкости. В координатах p, V и p, T изобары перпендикулярны оси давления (рис. 30.5, б, в).
Изохорный процесс. Закон Шарля
Если газовый баллон сильно нагреется на солнце, давление в нем повысится настолько, что баллон может взорваться. В данном случае имеем дело с изохорным нагреванием.
Изохорный процесс — процесс изменения состояния данного газа некоторой массы, протекающий при неизменном объеме.
Пусть некий газ переходит из состояния (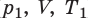
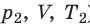
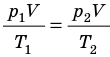
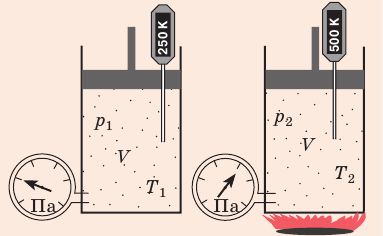
Рис. 30.6. Изохорное нагревание газа. Если газ находится в цилиндре под закрепленным поршнем, то с увеличением температуры давление газа тоже будет увеличиваться. Опыт показывает, что в любой момент времени отношение давления газа к его температуре неизменно:
Закон Шарля
Для данного газа некоторой массы отношение давления газа к его температуре остается постоянным, если объем газа не изменяется:
Графики изохорных процессов называют изохорами. Из закона Шарля следует, что при неизменном объеме давление газа данной массы прямо пропорционально его температуре: p T = ⋅ const . График этой зависимости — прямая, проходящая через начало координат (рис. 30.7, а). В координатах p, V и V, T изохоры перпендикулярны оси объема (рис. 30.7, б, в).
Пример №1
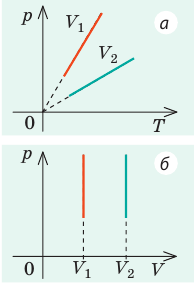
В вертикальной цилиндрической емкости под легкоподвижным поршнем находится 2 моль гелия и 1 моль молекулярного водорода. Температуру смеси увеличили в 2 раза, и весь водород распался на атомы. Во сколько раз увеличился объем смеси газов?
Анализ физической проблемы. Смесь газов находится под легкоподвижным поршнем, поэтому давление смеси не изменяется:
Решение:
Воспользуемся уравнением состояния идеального газа: pV = νRT. Запишем это уравнение для состояний смеси газов до и после распада: 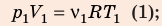
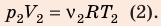

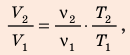
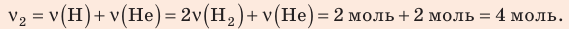
Ответ: примерно в 2,7 раза.
Пример №2
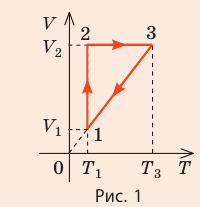
На рис. 1 представлен график изменения состояния идеального газа неизменной массы в координатах V, T. Представьте график данного процесса в координатах p, V и p, T.
Решение:
1. Выясним, какой изопроцесс соответствует каждому участку графика (рис. 1).
Зная законы, которым подчиняются эти изопроцессы, определим, как изменяются макроскопические параметры газа. Участок 1–2: изотермическое расширение; T = const, V ↑, следовательно, по закону Бойля — Мариотта p ↓. Участок 2–3: изохорное нагревание; V = const, T ↑, следовательно, по закону Шарля p ↑ . Участок 3–1: изобарное охлаждение; p = const , T ↓, следовательно, по закону Гей-Люссака V ↓ .
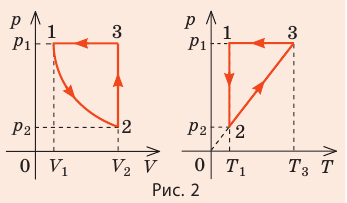
2. Учитывая, что точки 1 и 2 лежат на одной изотерме, точки 1 и 3 — на одной изобаре, а точки 2 и 3 на одной изохоре, и используя результаты анализа, построим график процесса в координатах p, V и p, T (рис. 2)
- Из соотношения p=nkT можно получить ряд важных законов, большинство из которых установлены экспериментально.
- Уравнение состояния идеального газа (уравнение Менделеева — Клапейрона):
— универсальная газовая постоянная.
- Уравнение Клапейрона:
- Законы, которым подчиняются изопроцессы, то есть процессы, при которых один из макроскопических параметров данного газа некоторой массы остается неизменным:
| Рекомендую подробно изучить предметы: |
|
| Ещё лекции с примерами решения и объяснением: |
- Температура в физике
- Парообразование и конденсация
- Тепловое равновесие в физике
- Изопроцессы в физике
- Абсолютно упругие и неупругие столкновения тел
- Механизмы, работающие на основе правила моментов
- Идеальный газ в физике
- Уравнение МКТ идеального газа
При копировании любых материалов с сайта evkova.org обязательна активная ссылка на сайт www.evkova.org
Сайт создан коллективом преподавателей на некоммерческой основе для дополнительного образования молодежи
Сайт пишется, поддерживается и управляется коллективом преподавателей
Whatsapp и логотип whatsapp являются товарными знаками корпорации WhatsApp LLC.
Cайт носит информационный характер и ни при каких условиях не является публичной офертой, которая определяется положениями статьи 437 Гражданского кодекса РФ. Анна Евкова не оказывает никаких услуг.
Уравнение состояния идеального газа
теория по физике 🧲 молекулярная физика, МКТ, газовые законы
Уравнение состояния идеального газа было открыто экспериментально. Оно носит название уравнения Клапейрона — Менделеева. Это уравнение устанавливает математическую зависимость между параметрами идеального газа, находящегося в одном состоянии. Математически его можно записать следующими способами:
Уравнение состояния идеального газа
Внимание! При решении задач важно все единицы измерения переводить в СИ.
Пример №1. Кислород находится в сосуде вместимостью 0,4 м 3 под давлением 8,3∙10 5 Па и при температуре 320 К. Чему равна масса кислорода? Молярная масса кислорода равна 0,032 кг/моль.
Из основного уравнения состояния идеального газа выразим массу:
Уравнение состояния идеального газа следует использовать, если газ переходит из одного состояния в другое и при этом изменяется его масса (количество вещества, число молекул) или молярная масса. В этом случае необходимо составить уравнение Клапейрона — Менделеева отдельно для каждого состояния. Решая систему уравнений, легко найти недостающий параметр.
Подсказки к задачам
| Давление возросло на 15% | p2 = 1,15p1 |
| Объем увеличился на 2% | V2 = 1,02V1 |
| Масса увеличилась в 3 раза | m2 = 3m1 |
| Газ нагрелся до 25 о С | T2 = 25 + 273 = 298 (К) |
| Температура уменьшилась на 15 К (15 о С) | T2 = T1 – 15 |
| Температура уменьшилась в 2 раза | 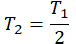 |
| Масса уменьшилась на 20% | m2 = 0,8m1 |
| Выпущено 0,7 начальной массы | |
| Какую массу следует удалить из баллона? | Нужно найти разность начальной и конечной массы: |
| Газ потерял половину молекул | 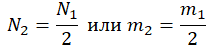 |
| Молекулы двухатомного газа (например, водорода), диссоциируют на атомы | 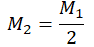 |
| Озон (трехатомный кислород) при нагревании превращается в кислород (двухатомный газ) | M (O3) = 3Ar (O)∙10 –3 кг/моль M (O2) = 2Ar (O)∙10 –3 кг/моль |
| Открытый сосуд | Объем V и атмосферное давление pатм остаются постоянными |
| Закрытый сосуд | Масса m, молярная масса M, количество вещества ν, объем V, число N и концентрация n частиц, плотность ρ— постоянные величины |
| Нормальные условия | Температура T0 = 273 К Давление p0 = 10 5 Па |
| Единицы измерения давления | 1 атм = 10 5 Па |
Пример №2. В баллоне содержится газ под давлением 2,8 МПа при температуре 280 К. Удалив половину молекул, баллон перенесли в помещение с другой температурой. Определите конечную температуру газа, если давление уменьшилось до 1,5 МПа.
2,8 МПа = 2,8∙10 6 Па
1,5 МПа = 1,5∙10 6 Па
Так как половина молекул была выпущена, m2 = 0,5m1. Объем остается постоянным, как и молярная масса. Учитывая это, запишем уравнение состояния идеального газа для начального и конечного случая:
Преобразим уравнения и получим:
Приравняем правые части и выразим искомую величину:

Алгоритм решения
Решение
График построен в координатах (V;Ek). Процесс 1–2 представляет собой прямую линию, исходящую из начала координат. Это значит, что при увеличении объема растет средняя кинетическая энергия молекул. Но из основного уравнения МКТ идеального газа следует, что мерой кинетической энергии молекул является температура:
Следовательно, когда кинетическая энергия молекул растет, температура тоже растет.
Запишем уравнение Менделеева — Клапейрона:
Так как количество вещества одинаковое для обоих состояния 1 и 2, запишем:
ν R = p 1 V 1 T 1 . . = p 2 V 2 T 2 . .
Мы уже выяснили, что объем и температура увеличиваются пропорционально. Следовательно, давление в состояниях 1 и 2 равны. Поэтому процесс 1–2 является изобарным, давление во время него не меняется.
Процесс 2–3 имеет график в виде прямой линии, перпендикулярной кинетической энергии. Так как температуры прямо пропорциональна кинетической энергии, она остается постоянной вместе с этой энергией. Следовательно, процесс 2–3 является изотермическим, температура во время него не меняется. Мы видим, что объем при этом процессе уменьшается. Но так как объем и давление — обратно пропорциональные величины, то давление на участке 2–3 увеличивается.
pазбирался: Алиса Никитина | обсудить разбор | оценить
На высоте 200 км давление воздуха составляет примерно 10 –9 от нормального атмосферного давления, а температура воздуха Т – примерно 1200 К. Оцените плотность воздуха на этой высоте.
http://www.evkova.org/uravnenie-sostoyaniya-idealnogo-gaza
http://spadilo.ru/uravnenie-sostoyaniya-idealnogo-gaza/

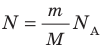
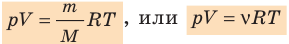
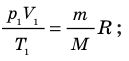
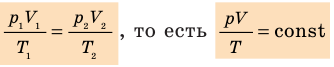
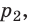
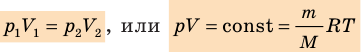

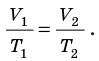
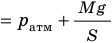
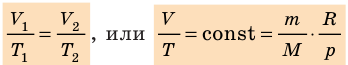
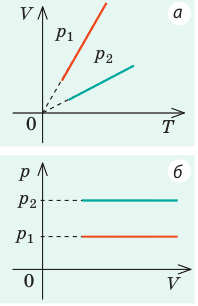

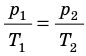
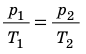
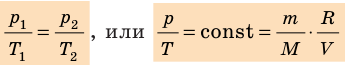

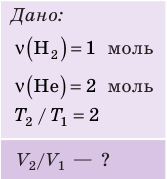
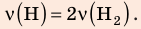

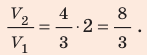
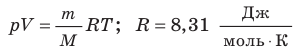 — универсальная газовая постоянная.
— универсальная газовая постоянная.